紫外法测定重组人红细胞生成素(Fc)融合蛋白的含量
2015-10-22张桂涛李庆昌韩为跃
张桂涛 阳 勇 李庆昌 何 凯 韩为跃
(广东联康生物与医药研究院,广东 东莞 523581)
紫外法测定重组人红细胞生成素(Fc)融合蛋白的含量
张桂涛阳勇李庆昌何凯韩为跃
(广东联康生物与医药研究院,广东 东莞 523581)
目的 建立紫外法测定重组人红细胞生成素(Fc)融合蛋白(rhEPO-Fc)含量的方法。方法 利用Edelhoch法测定rhEPO-Fc的摩尔消光系数,计算得到其溶液百分比消光系数,并测定rhEPO-Fc溶液A280值,依据公式c=A/ε计算rhEPO-Fc的含量。结果 rhEPO-Fc溶液百分比消光系数为1.3,在0.02~1.28 mg/mL浓度范围内,测定含量结果偏差<4%。结论 该方法操作简便、专属性强、结果准确可靠,可用于rhEPO-Fc含量测定。
消光系数;红细胞生成素;融合蛋白
蛋白质定量是重组蛋白药物研究开发中最基本的实验内容,常用的定量方法包括Bradford、Lowry和HPLC法等,这些方法需要对应的标准品,而重组蛋白的标准品一般情况下无法获取,以前多采用牛血清白蛋白或者人血清白蛋白作为替代标准品用于重组蛋白的含量测定,但不同蛋白质的氨基酸组成不同,其理化性质不同,因此用非同质标准品测定蛋白含量偏差比较大,不能准确反映待测蛋白的真实含量。近年来,紫外吸光法已成为FDA、EMA推荐的重组蛋白药物含量测定方法之一。在摩尔消光系数及相对分子质量已知的情况下,仅需要测定样品的光吸收值,即可计算出蛋白浓度,而不需要蛋白标准品。
目前已知的摩尔消光系数的测定有几种方法,包括dry weight[1]、nitrogen determination[2]和spectral method[3],这几种方法都存在蛋白质用量大、过程繁琐等缺点,限制了它们在实验室的使用。
rhEPO-Fc为创新蛋白质药物,拟用于肾性贫血治疗,该药物制剂在临床预试验中表现出长效化特征,该蛋白利用EPO融合Fc片段后以同源二聚体形式存在,理论上其半胱氨酸都以二硫键形成胱氨酸,因此其变性状态下的摩尔消光系数为111280;而二聚体的氨基酸相对分子质量为88629.2。
本研究中,笔者采用Edelhoch法测定rhEPO-Fc的摩尔消光系数,计算得到其溶液百分比消光系数,从而依据公式(1)测定其蛋白质含量;本法具有的优点:在确定溶液百分比消光系数后,不需要任何反应,可直接测定该蛋白溶液的吸收值,从而计算出蛋白质的含量,操作简便、可重复性良好且专属性强。
1 材料与仪器
rhEPO-Fc原液(纯度>95%,自制),脱盐柱为Amersham Biosciences产品(货号:52-13080-00)。紫外分光光度计(Beckman DU730)。盐酸胍、氯化钠等均为国产分析纯。
2 方法与结果
2.1rhEPO-Fc消光系数的测定:将经脱盐得到的rhEPO-Fc水溶液用超纯水稀释3、6、12、24、48倍,分别测定A280。由于在蛋白溶液中蛋白颗粒会出现光散射现象,因此必须对A280进行校正,即扣除光散射值A光散射。A光散射的测定方法是测定溶液在320、325、330、335、340、345、350 nm波长处的吸光度,用线性回归法,以吸光度的对数值与其相对应波长的对数值绘图,获得最适标准曲线,将此标准曲线外推至280 nm波长,从而确定A280光散射。同样,将EPO-Fc蛋白水溶液用相同的稀释倍数溶解在6mol/L盐酸胍溶液中,分别测定其A280和A280光散射。计算同一浓度的rhEPO-Fc在水溶液和6mol/L盐酸胍溶液中紫外吸收值的比值,并利用公式(3)(4)(5)计算rhEPO-Fc水溶液中的溶液百分比消光系数。结果:rhEPO-Fc的消光系数为1.3,RSD=0.41%,见表1。

表1 溶液百分比消光系数测定结果
2.2溶液百分比消光系数测定干扰性试验
2.2.1糖基化对rhEPO-Fc溶液百分比消光系数的影响:对于糖蛋白,虽然单糖分子在280 nm处没有紫外吸收值,但是其糖链组成可能会影响到蛋白质的构象,从而影响糖蛋白的紫外吸收值。为了研究糖基化是否对rhEPO-Fc的消光系数存在影响,取rhEPO-Fc蛋白原液,用肽N-糖苷酶F酶切N-糖链,酶切完成后,蛋白质用Protein A柱进行纯化,去除肽N-糖苷酶F和反应缓冲液,用上述方法测定无糖基化的rhEPO-Fc的溶液百分比消光系数,结果为1.2,去除糖基后的rhEPO-Fc消光系数下降了约7%,这说明糖基化会影响糖蛋白的消光系数,但是并不显著,可能是由于蛋白糖基化后构象发生改变引起。
2.2.2离子强度对rhEPO-Fc溶液百分比消光系数的影响:取适量的rhEPO-Fc蛋白水溶液,调整A280在0.6~1.4,用不同浓度的氯化钠分别进行倍比稀释,使rhEPO-Fc蛋白溶液中氯化钠的浓度分别为0、0.25、0.5、1.00、1.50、2.00mol/L,混合静置2~3min后用分光光度计分别测定其A280和A280光散射,校正A280,结果见表2,rhEPO-Fc蛋白在0.25~2.00mol/L的氯化钠溶液中A280值变化不大,而且与在0mol/L氯化钠溶液中相当,说明2mol/L以下的氯化钠不影响蛋白质的光吸收值,即不影响其溶液百分比消光系数。见表2。

表2 rhEPO-Fc在不同浓度氯化钠中的吸光值
2.3浓度测定范围确定:取适量rhEPO-Fc蛋白原液,用超纯水稀释成浓度为1.28、0.64、0.32、0.16、0.08、0.04、0.02、0.01 mg/mL,分别测定其A280和A280光散射。同时,利用rhEPO-Fc溶液百分比消光系数计算理论吸收值,并比较由计算得到的吸收值相对于测定校正吸收值的偏差,结果见表3,rhEPO-Fc浓度在0.02~1.28 mg/mL范围检测紫外吸收值与计算吸收值的相对偏差<4%,因此,在该浓度范围内,紫外法测定该rhEPO-Fc含量是可信的。见表3。
2.4重复性试验:分别取同批rhEPO-Fc原液5份,分别测定A280和A280光散射,校正A280,利用公式(1)计算得到原液含量为0.97 mg/mL,RSD=0.65%(n=5),重复性良好。
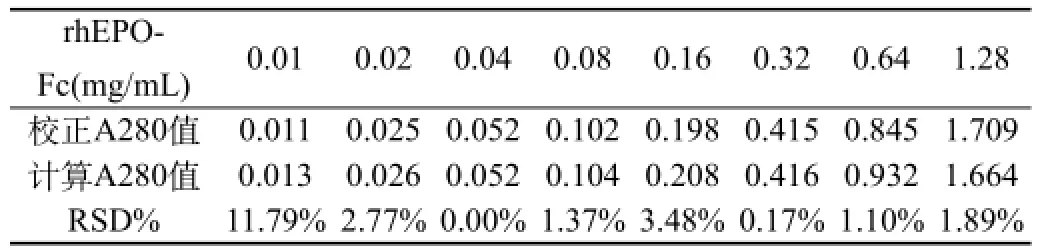
表3 相同浓度rhEPO-Fc测定校正后A280与c=A/εAbs0.1%计算A280比较
3 讨 论
利用Edelhoch法测定rhEPO-Fc蛋白的摩尔消光系数,操作简便,可用于rhEPO-Fc含量的测定。但考虑到消光系数的专属性,为保证结果的准确,待检样品的纯度应不低于95%,即所含的目标蛋白几乎为rhEPO-Fc的情况下,计算的rhEPO-Fc原液含量才更准确。笔者研究了数十种蛋白质消光系数发现,利用Edelhoch法测定的摩尔消光系数和直接经公式ε=(Trp数量)×5500+(Tyr数量)×1490+(cystine数量)×125计算的摩尔消光系数比较,大部分蛋白的偏差都5%左右,少数蛋白的偏差超过10%,如Rituximab。重组糖蛋白的糖基化程度、糖基化位点及糖基化的类型对其消光系数的影响也不尽相同,如rhEPO-Fc脱糖后的消光系数,相对于脱糖前下降约7%左右,而Rituximab脱糖前后几乎无差异。该方法专属性强、准确度高,可用于纯度高rhEPO-Fc原液或制剂的定量。
[1] Hunter MJ.A method for the determination of protein partial secific volum[J].J Phys Chem,1996,70(10):3285-3292.
[2] Jaenicke L.A rapid micromethod for the determination of nitrogen and phosphate in biological material[J].Anal Biochemis ty,1974,61(4):623-627.
[3] Whitaker JR, Granum PE.An absolute method for protein determination based on difference in absorbance at 235 and 280 nm[J] .Anal Biochem,1980,109(1):156-159.
R-3
B
1671-8194(2015)10-0065-02
广东省重大科技专项(重大新药创制)课题(编号:2011A080502001)
