木质素衍生物的吸附特性及三次采油牺牲效果*
2015-10-21邱学青张志鸣杨东杰黄恺周明松
邱学青 张志鸣 杨东杰 黄恺 周明松
(华南理工大学 化学与化工学院∥广东省绿色化学产品技术重点实验室,广东 广州510640)
逐渐枯竭的石油资源使人类正面临严重的能源危机,如何提高原油的采油率受到科学界的广泛关注.在三次采油过程中,传统表面活性剂的驱油效果虽好,但因容易吸附在岩石表面和缝隙中而损失严重,导致驱油成本提高.解决驱油表面活性剂吸附损失问题的一个有效方法就是在驱油表面活性剂中加入牺牲剂,这些廉价的牺牲剂优先吸附在岩石表面和缝隙中,占据吸附位点,并降低界面张力,从而降低驱油表面活性剂的损失[1-3]. 木质素衍生物具有来源广泛、价格低廉的特点,作为三次采油牺牲剂已有多年历史. 美国Texaco 公司分别将木质素磺酸盐、氧化木质素磺酸盐、木质素磺酸盐-甲醛缩合物、磺甲基化木质素磺酸盐等木质素衍生物用作三次采油牺牲剂,取得了一定的成果[4-7]. 张树彪、赵颖华等[8-9]的研究表明,改性木质素磺酸盐与石油磺酸盐具有较好的协同效应,复配体系中木质素磺酸盐的含量越高,达到最低界面张力所需的时间越短.徐广宇、伍伟青等[10-11]的研究表明,改性木质素磺酸盐与石油磺酸盐以1∶1 复配后可以减少石油磺酸盐的吸附损失达50%以上. 韦汉道等[12]用大庆油田的地层砂作吸附剂,发现添加木质素磺酸盐可以使仲烷基磺酸钠在地层砂上的吸附量由2.57 mg/g减少到0.46 mg/g.
虽然关于木质素衍生物用作三次采油牺牲剂的研究较多,但是牺牲效果不突出,添加量大,因此未能实现在三次采油领域的广泛应用. 而且以往的研究多采用磺酸盐型木质素衍生物作为牺牲剂,改性方法多集中于在木质素大分子中引入磺酸亲水基和长链疏水基,而忽视了羧酸基对牺牲效果的影响.而羧基作为一种络合型亲水基,对金属离子的络合性远超磺酸基,在金属矿物质表面具有强烈的络合吸附作用[13-15],可以引入到木质素分子中以制备高效能的木质素基牺牲剂.
文中采用高纯度碳酸钙作为岩石矿物的模型物吸附剂,研究木质素磺酸钠(SL)在碳酸钙表面的吸附驱动力,分别探讨了静电、氢键、络合吸附作用力对SL 在碳酸钙表面吸附的贡献大小,揭示SL 的牺牲机理;针对SL 在矿物质表面吸附能力不足的缺点,将羧基引入到碱木质素分子中制备木质素羧酸钠(CAL),得到新型的木质素羧酸盐三次采油牺牲剂,同时对比研究了SL 与CAL 的牺牲性能.
1 实验部分
1.1 主要试剂与仪器
SL 由吉林石岘造纸有限公司提供,来自于杨木亚硫酸盐法制浆废液,经过超滤[16]纯化而得,超滤的截留相对分子质量分别为1000 和50000;麦草碱木质素由山东泉林纸业有限责任公司提供,为麦草碱法制浆黑液经酸析提纯得到的产品;碳酸钙由上海国药集团化学试剂有限公司提供,分析纯,含量≥99%;驱油表面活性剂十二烷基苯磺酸钠(LAS)由上海国药集团化学试剂有限公司提供,分析纯,含量≥99%.
SCF-106 型激光粒度分析仪,珠海欧美克公司生产;D8 Advance 型X 射线衍射仪,德国Bruker 公司生产;ZetaPALS 型 Zeta 电位分析仪,美国Brookhaven 公司生产;809 Titrando 型自动电位滴定仪,瑞士Metrohm 公司生产;UV-2450 型紫外分光光度计,日本岛津公司生产;THZ-C-1 型台式冷冻恒温振荡器,常州澳华仪器有限公司生产;AnkeTGL-16C型高速离心机,上海安亭科学仪器厂生产;DCAT12型表面/界面张力仪,德国Dataphysic 公司生产.
1.2 碱木质素羧酸盐的合成
[17]合成碱木质素羧酸盐:将一定质量浓度的麦草碱木质素溶液的pH 值调至10 ~12,加入到500mL 四口烧瓶中,边搅拌边升温至40℃使碱木质素完全溶解,调节反应液的pH 值至11 ~12,然后在搅拌下滴加一定质量浓度的一氯乙酸溶液,滴加完毕后,升温至70 ~80℃反应1 ~3h,即可制得液体碱木质素羧酸盐.
1.3 测试与表征
1.3.1 CaCO3的物化性质表征
CaCO3样品的平均粒径由激光粒度分析仪测定,3 次平行实验的平均测定结果为4.92 μm.
X 射线衍射光谱(XRD)实验运用X 射线衍射仪测定,实验条件为:铜靶,LynxExe 阵列探测器,40 kV,40 mA,扫描步长0.02°,扫描速度17. 7 s/步.结果如图1 所示,运用Jade 软件扣背底校正后与CaCO3标准谱图高度吻合,说明样品中CaCO3纯度很高.

图1 CaCO3 样品的XRD 图谱Fig.1 XRD spectra of CaCO3 samples
1.3.2 碳酸钙等电点的测定
取0.1 g 固体加入100 mL 浓度为10 mmol/L 的KCl 溶液中,用盐酸和氢氧化钠溶液调节溶液pH值.测量时摇匀,静置2 min,取上层悬浮液用Zeta 电位分析仪测定Zeta 电位,保持残差值在0.05 以下,测定5 次,取平均值.然后根据不同pH 下的Zeta 电位找出等电点[18].
1.3.3 SL 和CAL 羧基含量的测定
采用自动电位滴定仪测定样品SL 和CAL 的羧基含量[16],测得SL 和CAL 的羧基含量分别为1.49和2.59 mmol/g.
1.3.4 SL 在CaCO3表面吸附量的测定
用残余质量分数法[19]测量不同浓度SL 在Ca-CO3表面的吸附量.
1.3.5 表面张力的测定
采用表面/界面张力仪测定LAS 及其复配物溶液的表面张力,测量范围为1 ~1000 mN/m,测量误差为±0.001mN/m,待测样品溶液质量为0.01mg ~210g.
1.3.6 SL 和CAL 牺牲效果的测定
表面活性剂牺牲效果是指在添加不同浓度的表面活性剂后,质量浓度为1 000 mg/L 的LAS 溶液在CaCO3表面的吸附量的相对减少量. 根据紫外分光光度计多组分定量方法[20],可分别测定吸附过程溶液中SL、CAL 和LAS 的浓度,为避免偏离Lambert-Beer 定律,配制溶液的浓度均小于0.01 mol/L.
2 结果与分析
2.1 碳酸钙的等电点分析
固体颗粒表面所带电荷随着悬浮液pH 值的变化而变化,固体颗粒的等电点指颗粒表面呈电中性时溶液的pH 值. 颗粒的带电性对其吸附性能的影响很大,实验测定了不同pH 值条件下CaCO3表面的Zeta 电位,结果如图2 所示.

图2 CaCO3 样品的Zeta 电位Fig.2 Zeta potentials of CaCO3 sample
由图2 可见,碳酸钙的等电点为8.1,与文献[18]中的8.2 接近,即当pH <8.1 时,碳酸钙表面带正电荷,且随着pH 值的减小,正电性增强;当pH >8.1 时,碳酸钙表面带负电荷,且随着pH 值的增加,负电性增强.
2.2 pH 对SL 在碳酸钙表面吸附等温线的影响
CaCO3表面所带电荷随着SL 溶液pH 值的变化而变化,因此可以通过改变SL 溶液的pH 值来研究静电作用对SL 在CaCO3表面吸附特性的影响.实验分别建立了溶液pH 值分别为7、9、11 时SL 在CaCO3表面的吸附等温线,结果如图3 所示. 其中,平衡浓度是指吸附剂在碳酸钙表面吸附时的初始浓度.

图3 不同pH 值下SL 在CaCO3 表面的吸附等温线Fig.3 Adsorption isotherms of SL on CaCO3 at different pH values
由图3 可见,pH 值为7 和9 时,SL 在CaCO3表面的吸附量差别不大,而pH 值增加到11 时,SL 的吸附量有所减少,最大减少量约为1 mg/g,说明pH值的增大不利于SL 在CaCO3表面的吸附. 分析认为,SL 属于阴离子型聚合物,表面带有负电荷;当溶液pH 值为7 时,CaCO3表面带一定量的正电荷,与SL 间具有静电吸引力;当pH 值大于8.1 时,CaCO3表面开始带有负电荷,静电作用变弱,当pH 值为11时,CaCO3表面带有大量负电荷,导致SL 的吸附量减少.但pH 值为9 时吸附量几乎不变,而pH 值为11 时吸附量减少量较小,说明静电作用对SL 在Ca-CO3表面的吸附特性的影响有限,不是其在CaCO3表面上的主要吸附驱动力.
2.3 尿素对SL 在碳酸钙表面吸附等温线的影响
尿素能优先和水、聚合物等之间形成氢键,从而有效地阻止聚合物与固体之间形成氢键[21].杨东杰等[22]指出,在中性条件下,SL 主要通过疏水作用和氢键作用吸附在活性炭/水界面,为了研究氢键作用对SL 在CaCO3表面吸附特性的影响,在pH 值为7、9 的吸附体系中加入0.1 mol/L 的尿素[22],以破坏体系中的氢键,然后分别测定尿素对SL 在CaCO3表面吸附等温线的影响,结果如图4 所示.

图4 添加尿素后不同pH 值下SL 在CaCO3 表面的吸附等温线Fig.4 Adsorption isotherms of SL on CaCO3 at different pH values after adding urea
由图4 可见,在pH 值为7、9 的溶液中加入尿素后,当平衡浓度较低时,SL 在CaCO3表面的吸附量不变,当平衡浓度较高时才稍有不同,说明尿素对SL 在CaCO3表面吸附特性的影响很小.分析认为,氢键对SL 在CaCO3表面吸附力的贡献很小,即使加入尿素破坏了体系中的氢键,各吸附量也变化很小,可知氢键不是SL 在CaCO3表面吸附的主要作用力.
2.4 硫酸盐、亚硫酸盐和羧酸盐对SL 在CaCO3表面吸附等温线的影响
木质素磺酸盐主要含有磺酸基和羧基等亲水基,能以静电吸附的方式吸附在固体颗粒表面.但是在磺酸基和羧基中,究竟哪一种基团的吸附作用力占主导,在以往文献中没有细化研究. 为了揭示SL的磺酸基和羧基对其在CaCO3表面的吸附作用力的贡献,实验分别选取含有硫酸基的硫酸钠、含亚硫酸基的亚硫酸钠和含羧酸基的柠檬酸钠加入到吸附溶液中,通过研究其对SL 在CaCO3表面吸附量的影响来分析不同的亲水基对SL 在CaCO3表面吸附性能的影响规律. 由于3 种盐的水溶液pH 值各不相同,因此在配制吸附溶液时,pH 值统一调整为7,其对SL 在CaCO3表面吸附等温线的影响如图5 所示.

图5 添加硫酸钠、亚硫酸钠、柠檬酸钠后SL 在碳酸钙表面的吸附等温线Fig.5 Adsorption isotherms of SL on CaCO3 after adding sodium sulfate,sodium sulfite and sodium citrate
由图5 可见,0.1 mol/L 硫酸钠、亚硫酸钠、柠檬酸钠的加入对SL 在CaCO3表面吸附等温线的影响具有很大差异:硫酸钠的加入使700 mg/L 的SL 在CaCO3表面的吸附量比空白样稍有增多,且吸附量随着SL 浓度的增加而增加;亚硫酸钠的加入使SL在CaCO3表面的吸附量显著降低,降低幅度在30%以上;柠檬酸钠的加入使SL 在CaCO3表面的吸附量几乎减少为0.分析认为,3 种盐对SL 在CaCO3表面吸附性能影响的显著差异主要是由其结构导致的. 硫酸钠中的硫元素没有多余的孤对电子,因此没有络合能力,与CaCO3之间的相互作用很弱,与SL 在CaCO3表面基本不产生竞争吸附,但其提高了溶液的离子强度,对SL 的吸附有所促进,所以SL 在CaCO3表面的饱和吸附量有少量提高;亚硫酸钠中的硫元素有一对孤对电子,因此对钙、镁、铁等高价金属离子具有一定的络合能力,可与CaCO3之间形成较强的相互作用,与SL 产生了较强的竞争吸附,且大于溶液离子强度的提高对SL 吸附的影响,所以亚硫酸钠使SL 在CaCO3表面的吸附量显著降低;柠檬酸钠是多羧基化合物,对钙、镁、铁等具有强烈的络合能力,因此与CaCO3之间能形成很强的相互作用,与SL 在CaCO3表面的竞争吸附中处于绝对优势,完全占据了SL 的吸附位点,导致SL 的吸附量几乎减少为0.以上结果表明,盐或者酸根对金属离子的络合能力越强,其与SL 在CaCO3表面的竞争吸附能力也越强,对SL 在CaCO3表面吸附的影响越大.
SL 含有较多的磺酸基和羧基亲水基,其中磺酸基与硫酸钠相似,硫元素没有多余的孤对电子,对金属离子的络合作用很弱;但是SL 分子中的多个羧基对金属离子具有较强的络合作用,可以通过络合吸附作用与CaCO3表面发生多点吸附,类似于柠檬酸钠.在SL 与CaCO3表面的吸附驱动力中,磺酸基和羧基都能提供静电作用力,但是只有羧基可以提供络合吸附作用力. 图5 表明,溶液的离子强度对SL的吸附有所影响[23],说明疏水范德华力对SL 在CaCO3表面的吸附具有一定的影响,SL 分子中的磺酸基和羧基与CaCO3之间的静电吸附作用力对吸附的影响很小,SL 分子中的羧基与CaCO3之间的络合吸附作用力才是主要的吸附驱动力.
2.5 氯化锂和氯化钠对SL 在CaCO3 表面吸附等温线的影响
为了证明SL 分子中的羧基是其在CaCO3表面吸附的主要吸附基团,实验用锂盐封闭SL 的部分羧基,然后进行吸附研究. 锂离子原子半径小,可以与羰基氧之间形成紧密键合[24],且Li—COO 键的极性强于H—COO 键和Na—COO 键[25],由于Li—COO 络合物比H—COO 和Na—COO 稳定,因此可以用锂盐封闭SL 分子中的大部分羧基[26]. 本实验在SL 溶液中分别加入0.01 和0.10mol/L 氯化锂预先屏蔽SL 分子中的羧基,同时加入氯化钠对离子强度的变化进行对比,各吸附等温线如图6 所示.
由图6(a)可见,加入0.01、0.10 mol/L 氯化钠后,SL 在CaCO3表面的吸附量比空白样明显增大,而且氯化钠浓度越高,吸附量越大. 图6(b)情况则不同,加入0.01、0.10 mol/L 氯化锂后,吸附量均比空白样低,加入0.10 mol/L 氯化锂的吸附量稍大于加入0.01mol/L 氯化锂时的吸附量.因此可以看出,虽然氯化钠和氯化锂结构相似,但是其对SL 在CaCO3表面吸附的影响是不同的.
分析认为,氯化钠的加入主要加强了SL 与CaCO3之间的疏水范德华作用力,对SL 分子中的羧基与CaCO3之间的络合吸附作用力没有影响,因此SL 的吸附量随着氯化钠浓度的增加而增加,这与文献报道的规律相符[23]. 氯化锂对SL 在CaCO3表面吸附的影响有两方面:一是氯化锂中的锂与SL 中的羧基结合,屏蔽了SL 的大部分羧基,减弱了SL 分子中的羧基与CaCO3之间的络合吸附作用力,因此氯化锂的加入使SL 在CaCO3表面的吸附量均比空白样低;二是氯化锂的加入增大了溶液的离子强度.当加入的氯化锂浓度过高,如加入0.10 mol/L 氯化锂时,屏蔽了SL 的部分羧基,但同时也显著增大了溶液的离子强度,故SL 在CaCO3表面的吸附量稍大于加入0.01 mol/L 氯化锂时的吸附量,但仍少于空白样的吸附量.
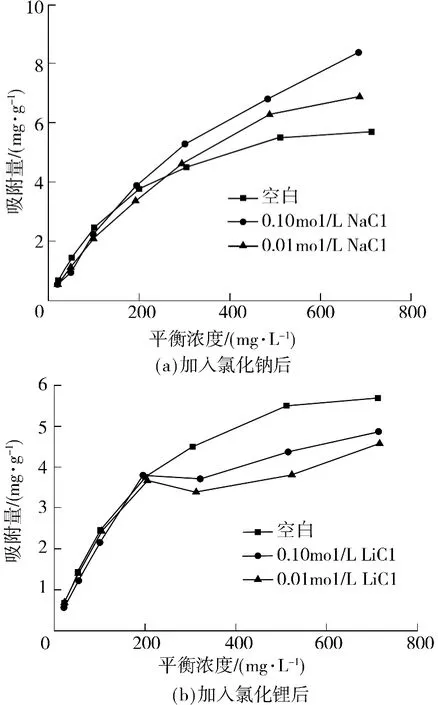
图6 加入氯化锂和氯化钠后SL 在CaCO3 表面的吸附等温线Fig.6 Adsorption isotherms of SL on CaCO3 after adding LiCl and NaCl
分析结果表明,SL 的羧基与CaCO3的络合作用是其在CaCO3表面吸附的主要驱动力,SL 的羧基是其在CaCO3上的主要吸附基团.
2.6 SL、CAL 和LAS 在碳酸钙表面的吸附等温线
为了考察不同羧基含量的木质素衍生物作为三次采油牺牲剂的牺牲能力,文中分别研究了SL、CAL 和LAS 在CaCO3上的吸附特性,在pH =9 时分别测定了SL、CAL 和LAS 在CaCO3表面的吸附等温线,结果如图7 所示.

图7 SL、CAL 和LAS 在CaCO3 表面的吸附等温线Fig.7 Adsorption isotherms of SL,CAL and LAS on CaCO3
由图7 可见,SL、CAL 和LAS 的吸附量都随着样品浓度的增加而增加,超过一定的浓度后出现了吸附平台.CAL 达到饱和吸附的速率最快,在质量浓度为200 mg/L 时就达到了饱和吸附;其次是SL在质量浓度超过700 mg/L 时基本达到饱和吸附;LAS 达到饱和吸附的速率最慢,在质量浓度超过1000 mg/L 时才基本达到饱和吸附,但是饱和吸附量远超CAL 和SL,达到8.98 mg/g. 从结果可以看出,CAL 在CaCO3上的吸附速率快于SL,这是因为CAL 的羧基含量较高,达到2.59 mmol/g,在络合吸附驱动力的作用下很快在CaCO3上达到饱和吸附;而SL 的羧基含量为1.49 mmol/g,络合吸附作用力相对较弱,因此达到饱和吸附的速率较慢.另外可以看出,LAS 在CaCO3上的吸附量很大,这导致在实际的三次采油中由于吸附而造成的浪费很大,因此与牺牲剂的配伍非常必要.
2.7 SL 和CAL 对LAS 在CaCO3 表面吸附量的影响
为了研究SL 和CAL 用作牺牲剂时对LAS 在CaCO3表面吸附量的影响,向1 000 mg/L 的LAS 中加入不同浓度的SL 和CAL,然后在CaCO3上进行吸附,得到LAS 的吸附量随着SL 和CAL 浓度的变化,如图8 所示.

图8 SL 和CAL 对LAS 在CaCO3 表面的吸附量的影响Fig.8 Effects of SL and CAL on LAS adsorption amount on CaCO3
由图8 可见,LAS 在CaCO3表面的吸附量随着SL 质量浓度的增加而减少,当SL 质量浓度低于40 mg/L时,LAS 的吸附量比空白样高,超过40 mg/L后,开始低于空白样的饱和吸附量,到100 mg/L 时LAS 的吸附量几乎不变.而LAS 在CaCO3表面的吸附量随着CAL 质量浓度的增加先减少后升高,超过30 mg/L 后趋于稳定,且当CAL 添加量低于10 mg/L时,LAS 的吸附量比空白样还高,20 mg/L 时,LAS 的吸附量最低.
分析认为,在较低的SL 和CAL 添加量下,LAS不仅在CaCO3表面吸附,而且与SL 和CAL 吸附单体之间发生二次吸附,形成混合表面胶团,导致吸附量比空白样大,没有起到牺牲效果.随着SL 和CAL添加量的增加,其在CaCO3表面的吸附量逐渐增多,减少了CaCO3表面的吸附位点,与LAS 产生竞争吸附,减少了LAS 在CaCO3表面的吸附量,从而减少了驱油表面活性剂的损失;当SL 添加量达到100 mg/L 时,其在CaCO3表面达到饱和吸附,不再占用吸附位点,LAS 的吸附量也不再减少而趋于稳定.当CAL 添加量为20 mg/L 时,其在CaCO3表面达到饱和吸附,使得LAS 的吸附量达到最低;但随着CAL添加量继续增大,过量的CAL 会作为聚电解质引起LAS 的沉淀,因而导致测得的吸附量有所增加[27].
不同添加量SL 和CAL 的牺牲效果如表1 所示,其中负值代表没有起到牺牲效果,反而使LAS吸附损失增加.
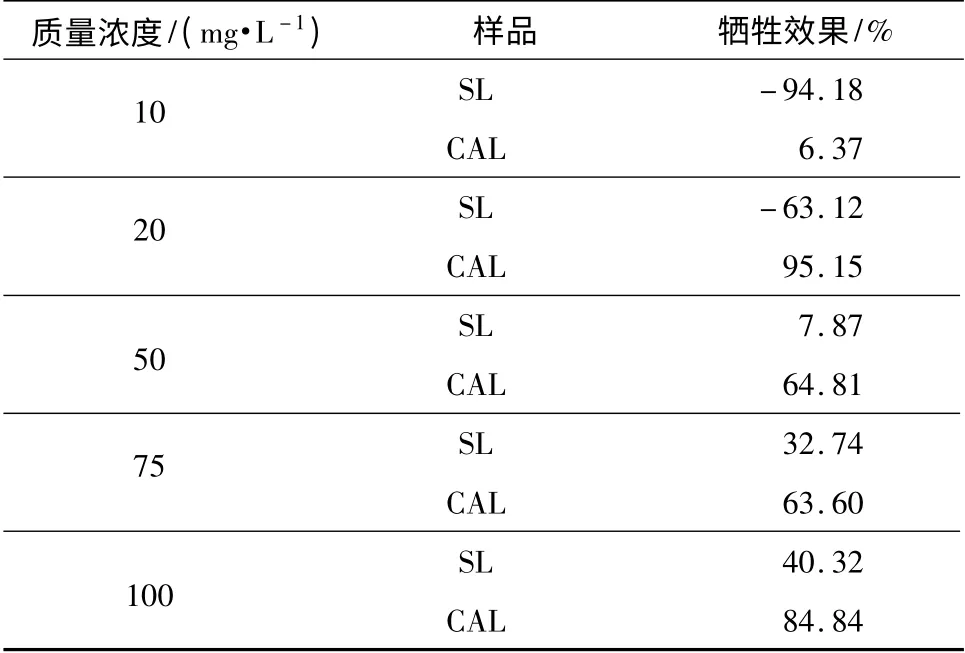
表1 不同浓度SL 和CAL 的牺牲效果Table 1 Sacrificial effects of SL and CAL with different concentrations
由表1 可见,SL 的最大牺牲效果达40.32%,CAL 的最大牺牲效果达95.15%,比SL 的大很多,且达到最大牺牲效果时的用量少80%. 分析认为,CAL 分子中羧基含量较多,约为SL 的1.74 倍,由于CAL 和SL 主要靠羧基与CaCO3之间的络合作用先吸附在CaCO3表面,减少了CaCO3表面的吸附位点,从而降低LAS 的吸附量,起到牺牲效果,所以CAL 在CaCO3表面的吸附能力更强,牺牲效果更好,且达到最大牺牲效果时的用量更少,这也与前面SL 和CAL在CaCO3表面的吸附特性相符.
2.8 SL 和CAL 对LAS 在水溶液中表面张力的影响
在单独使用时,表面活性剂的许多特性和作用往往得不到充分发挥,两种或几种表面活性剂通过复配能更好地满足应用的要求.其中,研究复配后的表面活性剂表面张力的变化是确定其之间是否存在协同效应的手段之一[28].为了研究SL、CAL 和LAS之间是否存在协同增效效应,在LAS 中分别加入100 mg/L的SL 和CAL,同时加入相同浓度的硫酸钠做对比,分析其对LAS 表面张力及临界胶束浓度(CMC)的影响,结果如图9 所示.

图9 SL、CAL 和Na2SO4 对LAS 的表面张力的影响Fig.9 Influences of SL,CAL and Na2SO4 on the surface tension of LAS
由图9 可见,加入相同质量浓度的SL、CAL 和硫酸钠后,LAS 的表面张力都有所降低,CMC 几乎不变.当LAS 质量浓度低于700 mg/L 时,加入SL 与CAL 后,LAS 的表面张力比加入硫酸钠的小,SL 降低LAS 表面张力的能力较强,当其质量浓度在60 mg/L左右时,最大降低约5 mN/m,复配效果最好.LAS 质量浓度高于700 mg/L 时,加入SL 和CAL后,LAS 表面张力比加入硫酸钠的大,降低了约3 mN/m.结果表明,在低质量浓度下,SL 和CAL 与LAS 复配能产生更好的协同作用.
分析认为,加入硫酸钠后,Na+所带的正电荷能够屏蔽LAS 分子的负电荷,减小分子之间的静电排斥力,使分子之间排列更密集,易吸附于气液界面,从而降低了LAS 的表面张力. SL 与CAL 属于阴离子表面活性剂,既含有磺酸基、羧基、羟基等亲水性官能团,又含有苯丙烷组成的疏络合水性骨架,具有表面活性,与LAS 复配后可产生一定的协同效应,使LAS 的表面张力降低.
3 结论
文中研究了pH、尿素和无机盐对SL 在CaCO3表面吸附特性的影响,还制备了高羧基含量的CAL,并对比研究了其与SL 用作三次采油牺牲剂的牺牲效果,得到以下结论:
(1)调节pH 值和加入尿素后,SL 在CaCO3表面的吸附量变化不大,说明静电作用和氢键不是SL 在CaCO3表面吸附过程中的主要吸附驱动力;分别加入具有不同络合能力的硫酸钠、亚硫酸钠和柠檬酸钠,发现没有络合能力的硫酸钠使SL 的吸附量稍有增加,而具有较强络合能力的亚硫酸钠使SL 的吸附量减少30%以上,具有强络合能力的柠檬酸钠使SL 的吸附量几乎减少为0;加入氯化锂封闭SL 的羧基后,SL 的吸附量也下降,表明SL 分子中羧基与CaCO3表面钙离子的络合作用是支配吸附的主要驱动力.
(2)向1000 mg/L 的LAS 中加入不同浓度的SL和CAL,羧基含量较高的CAL 的牺牲效果比SL 好;CAL 质量浓度为20 mg/L 时,其牺牲效果最好,达到95.15%;SL 质量浓度为100mg/L 时,其牺牲效果最好,为40.32%.
(3)SL 和CAL 与LAS 具有较好的协同作用,能使LAS 表面张力最大降低约5 mN/m,尤其是在低质量浓度下,协同效果更明显.
参考文献:
[1]Howard J,Stirling M. Sacrificial agents for enhanced oil recovery:US,4713185[P].1987-12-15.
[2]Li D,Lu S,Liu Y,et al.The effect of biosurfactant on the interfacial tension and adsorption loss of surfactant in ASP flooding[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects,2004,244(1):53-60.
[3]Zhang S,Yan J,Qi H.Interfacial tensions of phenyl tetradecane sulfonates for enhanced oil recovery upon the addition of fatty acids[J]. Journal of Petroleum Science and Engineering,2005,47(3):117-122.
[4]Kalfoglou G. Oxidized lignosulfonates as additives in oil recovery processes involving chemical recovery agents:US,4133385[P].1979-01-09.
[5]Kalfoglou G.Lignosulfonates carboxylated with chloroacetic acid as additives in oil recovery processes involving chemical recovery agents:US,4172497[P].1979-10-30.
[6]Kalfoglou G. Sulfomethylated lignosulfonates as additives in oil recovery processes involving chemical recovery agents:US,4172498[P].1979-10-30.
[7]Kalfoglou G.Lignosulfonate-formaldehyde condensation products as additives in oil recovery processes involving chemical recovery agents:US,4219082[P].1980-08-26.
[8]张树彪,乔卫红,王绍辉,等. 改性木质素磺酸盐与石油磺酸盐的复配研究[J]. 大连理工大学学报,2000,40(3):297-300.Zhang Shu-biao,Qiao Wei-hong,Wang Shao-hui,et al.Interfacial tension behavior characteristics of modified lignosulfonate-petroleum sulfonate mixtures [J]. Journal of Dalian University of Technology,2000,40(3):297-300.
[9]赵颖华,徐艳妹,王海峰,等. 木质素磺酸盐的改性及其在三次采油中的应用[J]. 大庆石油地质与开发,2005,24(4):90-91.Zhao Ying-hua,Xu Yan-mei,Wang Hai-feng,et al.Modification and application of lignosulfonate for enhanced oil recovery[J].Petroleum Geology & Oilfield Development in Daqing,2005,24(4):90-91.
[10]徐广宇,周宇鹏.改性碱木质素产品在三次采油中的应用研究[J].精细与专用化学品,2001,9(17):11-12,14.Xu Guang-yu,Zhou Yu-peng.The application of modified alkali lignin in tertiary oil recovery fine and specialty chemicals[J]. Fine and Specialty Chemicals,2001,9(17):11-12,14.
[11]伍伟青,徐广宇,周宇鹏. 改性碱木质素产品作为牺牲剂在三次采油中的应用研究[J].湖南大学学报:自然科学版,2001,28(2):21-26.Wu Wei-qing,Xu Guang-yu,Zhou Yu-peng. The application of modified alkali lignin as sacrificial agent in tertiary oil recovery[J].Journal of Hunan University:Natural Sciences Edition,2001,28(2):21-26.
[12]韦汉道,黄焕琼,刘石,等.改性木质素磺酸盐减少驱油过程中石油磺酸盐损失的研究[J]. 油田化学,1991,8(4):325-329.Wei Han-dao,Huang Huan-qiong,Liu Shi,et al.Laboratory study on modified lignosulfonates as sacrificial adsorbate in surfactant flooding [J]. Oilfield Chemistry,1991,8(4):325-329.
[13]Guo X,Zhang S,Shan X.Adsorption of metal ions on lignin[J].Journal of Hazardous Materials,2008,151(1):134-142.
[14]Demirbas A. Adsorption of lead and cadmium ions in aqueous solutions onto modified lignin from alkali glycerol delignication[J].Journal of Hazardous Materials,2004,109(1):221-226.
[15]Yang L,Li Y,Jin X,et al.Synthesis and characterization of a series of chelating resins containing amino/imino-carboxyl groups and their adsorption behavior for lead in aqueous phase[J].Chemical Engineering Journal,2011,168(1):115-124.
[16]周明松,黄恺,邱学青,等.水相电位滴定法测定木质素的酚羟基和羧酸基含量[J]. 化工学报,2012,63(1):258-265.Zhou Ming-song,Huang Kai,Qiu Xue-qing,et al. Content determination of phenolic hydroxyl and carboxyl in lignin by aqueous phase potentiometric titration [J].Journal of Chemical Industry and Engineering,2012,63(1):258-265.
[17]邱学青,周明松,杨东杰,等.一种水溶性碱木质素羧酸盐及其制备方法:中国,201110065840. 2 [P].2011-09-07.
[18]Somasundaran P,Agar G E.The zero point of charge of calcite[J]. Journal of Colloid and Interface Science,1967,24:433-440.
[19]Yang D J,Qiu X Q,Zhou M S,et al.Properties of sodium lignosulfonate as dispersant of coal water slurry[J].Energy Conversion and Management,2007,48(9):2433-2438.
[20]叶宪曾,张新祥.仪器分析教程[M].北京:北京大学出版社,2007:44-45.
[21]Zou Q,Habermann-Rottinghaus S M,Murphy K P. Urea effect on protein stability:hydrogen bonding and hydrophobic effect[J]. Proteins:Structure,Function,and Bioinformatics,1998,31(2):107-115.
[22]杨东杰,白孟仙,胡文莉,等.木质素磺酸钠在活性炭/水界面的吸附机理[J].高校化学工程学报,2012,26(5):748-754.Yang Dong-jie,Bai Meng-xian,Hu Wen-li,et al.Adsorption mechanism of sodium lignosulfonate on the activated/water interface[J].Journal of Chemical Engineering of Chinese Universities,2012,26(5):748-754.
[23]Ouyang X P,Deng Y H,Qian Y,et al. Adsorption characteristics of lignosulfonates in salt-free and salt-added aqueous solutions [J]. Biomacromolecules,2011,12:3313-3320.
[24]姚立丹,杨海宁,孙洪伟,等.复合锂基润滑脂和脲基润滑脂成脂机理的差异[J]. 石油学报:石油加工,2010,26(5):747-754.Yao Li-dan,Yang Hai-ning,Sun Hong-wei,et al. Difference between the formation mechanism of lithium complex grease and urea grease[J]. Acta Petrolei Sinica:Petroleum Processing Section,2010,26(5):747-754.
[25]杨大荣. 锂键与氢键的比较[J]. 大学化学,1993,8(6):29-32.Yang Da-rong.Comparison of hydrogen bonding and lithium bonding[J].University Chemistry,1993,8(6):29-32.
[26]周明松,王文利,杨东杰,等.木质素磺酸钠在氧化铁表面的吸附驱动力[J].高等学校化学学报,2014,35(8):1828-1834.Zhou Ming-song,Wang Wen-li,Yang Dong-jie,et al.Adsorption driving force of sodium lignosulphonate on Fe2O3surface[J].Chemical Journal of Chinese Universities,2014,35(8):1828-1834.
[27]韦汉道,黄焕琼,刘石,等.木素磺酸盐用作表面活性剂驱油牺牲剂的研究[J].广州化学,1990(2):37-44.Wei Han-dao,Huang Huan-qiong,Liu Shi,et al.A study of lignosulfonate as a sacrificial adsorbate in surfactant flooding[J].Guangzhou Chemistry,1990(2):37-44.
[28]焦艳华.改性木质素磺酸盐的合成及其在三次采油中的应用研究[D]. 大连:大连理工大学化工学院,2005.
