聚丙烯酸/萘酰亚胺纳米粒荧光增强法测定蛋白质
2015-10-17李杰鹏梁淑彩刘衍斌鄢国平
李杰鹏, 梁淑彩, 余 慧, 刘衍斌, 鄢国平
(1.武汉工程大学材料科学与工程学院,湖北武汉 430074;2.武汉大学药学院,湖北武汉 430072)
蛋白质定量检测在生命科学、临床、医疗及卫生等领域具有重要意义。采用荧光探针的荧光分析法因操作简单、灵敏度高、选择性好等特点在蛋白质定量分析中有着举足轻重的地位[1]。传统的蛋白质荧光探针有稀土离子[2]、金属配合物[3],及有机小分子化合物如荧光素类、花菁类和芳酸类染料[4-6]等。近年来,随着纳米技术的发展,荧光纳米粒作为新兴荧光探针引起了科研工作者的关注,基于无机材料的半导体纳米晶[7,8]、金纳米粒[9]和复合SiO2纳米粒[10]等已用于蛋白质的荧光分析测定。相比于无机纳米荧光材料,聚合物荧光纳米粒具有结构可控,功能可设计及良好的生物相容性等显著优势,在生物分析方面具有广阔的应用前景,但目前用于蛋白质测定的报道[11,12]不多。
聚丙烯酸(PAA)水溶性好且无毒性,在水处理、生物医药及石油化工等方面有较多应用[13]。1,8-萘酰亚胺荧光团光稳定性好,Stokes位移大,对其进行结构修饰可获得具有高灵敏度和选择性的荧光探针,在荧光分析测定方面的潜力已得到普遍认可[14,15]。本文以萘酰亚胺荧光化合物为交联剂对PAA进行交联,得到了水溶性的聚合物荧光纳米粒。以444 nm为激发波长,该纳米粒在544 nm处发射荧光,而牛血清白蛋白(BSA)能使其发射波长蓝移至535 nm,且荧光显著增强。据此,建立了一种快速、简便和灵敏地测定蛋白质的新方法。用该方法成功测定了BSA合成样品及牛奶样品中的蛋白质含量。
1 实验部分
1.1 仪器及试剂
LS55型荧光分光光度计(美国,Perkin Elmer公司);UV-2550型紫外分光光度计(日本,岛津公司);Delta 320-S pH计(梅特勒-托利多(上海)仪器有限公司);JEM-100CXII型透射电镜(日本,电子株式会社)。
N-羟乙基-4-羟乙基-1,8-萘酰亚胺(AN)按文献方法[16]制备。聚丙烯酸(PAA,分子量为2.6万)购于河南省凯特化学实业总公司。BSA购于Sigma公司,溶于水中配制成浓度为1.5×10-5mol·L-1的标准溶液,于冰箱中4 ℃保存。其他试剂均为分析纯。实验用水为超纯水。
1.2 实验方法
1.2.1纳米粒的合成[16]4.0 mL氯化亚砜缓慢滴入溶有0.5 g聚丙烯酸的N,N-二甲基甲酰胺(DMF)溶液中,混合物在35±2 ℃下反应2 h后,减压抽至无气泡产生,得到聚丙烯酰氯溶液。1.0 g AN溶于DMF中,缓慢滴入上述溶液中,然后室温搅拌反应5 h。将反应液转移至透析袋(截留分子量3 500 Da)于水中透析,每4 h换水一次,同时监测透析液荧光强度(激发和发射波长分别为444 nm和544 nm),透析液荧光强度为零时停止透析。将透析袋内溶液减压蒸发除去溶剂,干燥后即得目标纳米粒(AN/PAA-NP)。
1.2.2纳米粒的表征用水将纳米粒溶解并稀释至适当浓度测定其紫外光谱;用乙醇溶解AN配制1.0 mg·mL-1的储备溶液,再用水稀释至不同浓度,在444 nm下测定吸光度并绘制标准曲线。根据纳米粒在444 nm处的吸光度和AN的标准曲线,利用文献方法[17]计算荧光团的摩尔取代度。将待测液滴在表面喷涂碳膜的铜网上并进行负染,用透射电镜(TEM)观察形态和粒径。
1.2.3蛋白质检测方法在10.0 mL比色管中,加入1.0 mL浓度为10.0 μg·mL-1的AN/PAA-NP溶液,1.0 mL 20.0 mmoL·L-1磷酸盐缓冲溶液(PBS,pH=3.0)及不同量的BSA标准溶液,用水定容后摇匀。室温放置10 min,然后以444 nm为激发波长,在535 nm处测定试剂空白和反应体系的荧光强度F0和F,计算相对荧光强度△F(△F=F-F0)。
2 结果与讨论
2.1 纳米粒的表征
PAA的羧基经过酰氯化后与AN的羟基反应,形成PAA交联的荧光纳米粒,通过透析对其进行纯化。紫外光谱测定结果(图1)显示,AN和AN/PAA-NP在444 nm处均有特征吸收,而PAA在可见光区没有吸收峰,表明萘酰亚胺荧光团已经固定于交联PAA中,经测定其摩尔取代度为1.38%。透射电镜(TEM)结果(图2)表明纳米粒呈球状,粒径为10±5 nm。
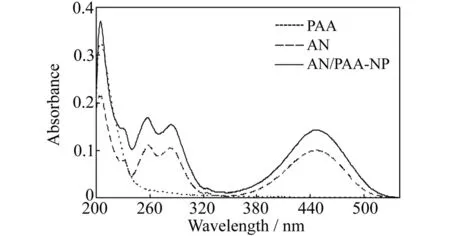
图1 PAA、AN和AN/PAA-NP的吸收光谱Fig.1 Absorption spectra of PAA,AN and AN/PAA-NP cPAA=0.2 mg·mL-1,cAN=2.5 mg·L-1,cAN/PAA-NP=0.1 mg·mL-1.

图2 TEM测定AN/PAA-NP的形态和粒径Fig.2 The morphology and size of AN/PAA-NP measured by TEM

图3 AN/PAA-NP及AN/PAA-NP/BSA体系的激发与发射光谱Fig.3 Excitation and emission spectra of AN/PAA-NP and AN/PAA-NP/BSA system 1 and 1’ are excitation and emission spectra of AN/PAA-NP,respectively;2 and 2′ are excitation and emission spectra of AN/PAA-NP/BSA system,respectively.cAN/PAA-NP=2.0 μg·mL-1,cBSA=7.5 μmol·L-1.
2.2 AN/PAA-NP及AN/PAA-NP/BSA的荧光光谱
对AN/PAA-NP及AN/PAA-NP/BSA体系进行荧光光谱扫描,见图3。可以看出,AN/PAA-NP的荧光激发和发射波长分别为444 nm和544 nm,加入BSA后,激发波长没有变化,发射波长蓝移至535 nm,同时荧光强度显著增大,表明AN/PAA-NP可用于荧光增强法测定蛋白质。
2.3 测定条件的优化
2.3.1缓冲溶液pH值及用量的影响研究发现,酸性条件有助于AN/PAA-NP/BSA体系的荧光增强,而碱性条件下△F较小,当pH=3.0时△F最大(图4)。另外,考察了pH=3.0的PBS(20.0 mmol·L-1)用量为0.5、1.0、1.5、2.0、2.5和3.0 mL时,体系荧光强度的变化。结果表明当缓冲溶液用量大于1.0 mL时,△F趋于稳定。本研究选择加入pH=3.0的PBS 1.0 mL。
2.3.2AN/PAA-NP浓度的影响固定BSA的浓度,△F随AN/PAA-NP浓度的变化见图5。当AN/PAA-NP的浓度为1.0 μg·mL-1时,△F最大;提高纳米粒浓度△F略有下降,且会增大背景荧光。实验选择1.0 μg·mL-1的AN/PAA-NP。

图4 pH值对△F的影响Fig.4 Effect of pH values on △F cAN/PAA-NP=1.0 μg·mL-1,cBSA=3.0 μmol·L-1.
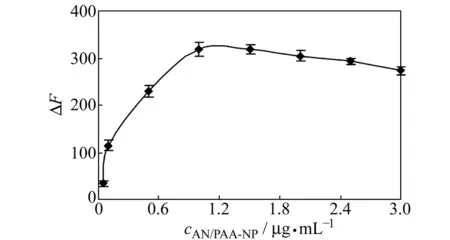
图5 AN/PAA-NP浓度对△F的影响Fig.5 Effect of AN/PAA-NP concentrations on △F cBSA=3.0 μmol·L-1.
2.3.3反应时间的影响纳米粒与BSA的结合反应进行很快,在室温下5 min内即完成,且体系荧光至少稳定2 h。为了确保反应充分完全,在加入BSA溶液且定容后,放置10 min后再进行测定。
2.4 线性范围、检测限和精密度
在最佳测定条件下,以体系的△F对BSA浓度绘制标准曲线。结果表明,BSA浓度在0.15~7.5 μmol·L-1范围内与△F呈良好线性关系,线性回归方程为:△F=84.288cBSA+21.206,相关系数为0.9973(n=7)。对空白溶液平行10次测定,以3倍标准偏差计算得检测限为0.095 μmol·L-1。按上述方法对浓度为1.5 μmol·L-1和4.5 μmol·L-1的BSA各进行10次测量,其相对标准偏差(RSD)分别为3.68% 和2.52%。
2.5 共存物质的影响
固定BSA浓度为3.75 μmol·L-1,控制相对误差在±5%范围内,考察常见物质对测定的影响。结果表明, 50.0 μmol·L-1的Fe3+、Ni2+、Co2+、Li+、Ba2+、Mg2+、Mn2+,15.0 μmol·L-1的Hg2+、Cu2+、Zn2+对测定结果没有影响。共存氨基酸(Arg、Ala、Leu、Gly、Trp、Phe、Thr、Tyr)的浓度为0.5 mmol·L-1时对测定也没有影响。
2.6 样品的测定
2.6.1人工合成样品取浓度为50.0 μmol·L-1的Mg2+、Fe3+和Li+,20.0 μmol·L-1的Cu2+和Zn2+,100.0 μmol·L-1的Arg、Phe、Gly和Leu各0.5 mL,及一定量的BSA标准溶液混合后定容至10 mL得到合成样品。取4.0 mL合成样品按照实验方法对BSA进行测定。测定结果见表1。
2.6.2牛奶样品市售纯牛奶稀释100倍,取4.0 mL用标准加入法进行回收率实验。测定结果如表1所示。
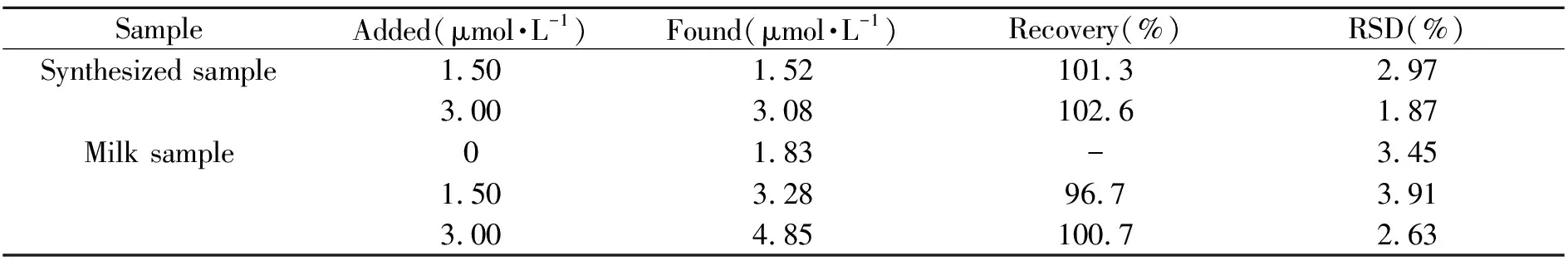
表1 样品分析结果(n=5)
3 结论
发展了一种以水溶性聚合物纳米粒为荧光探针,荧光增强法测定蛋白质的新方法。该纳米粒由双羟基萘酰亚胺化合物与PAA交联而成,具有较长的荧光发射波长(>500 nm)和大的Stokes位移(~100 nm),BSA能使其荧光显著增加。在选定的实验条件下,纳米粒与BSA的反应5 min内即完成,测定BSA的线性范围为0.15~7.5 μmol·L-1,检测限为0.095 μmol·L-1。该方法具有简单、快速、灵敏度高、重现性好的优点,已成功用于 BSA合成样品及牛奶样品中蛋白质的测定。
