恩替卡韦在肝硬化临床治疗中应用价值观察
2015-10-17刘秀鹏舒晴谭永港刘俊
刘秀鹏 舒晴 谭永港 刘俊
(广东省深圳市第二人民医院消化内科深圳518035)
恩替卡韦在肝硬化临床治疗中应用价值观察
刘秀鹏舒晴谭永港刘俊#
(广东省深圳市第二人民医院消化内科深圳518035)
目的:研究恩替卡韦治疗肝硬化的临床效果。方法:选取2013年1月~2014年6月我院接诊的肝硬化患者76例,随机分为对照组与观察组各38例,对照组采用常规药物治疗,观察组在对照组的基础上加用恩替卡韦治疗。比较两组的临床疗效。结果:治疗后观察组Child-Pugh评分、HBV-DNA定量分别为(8.53±1.48)分、(932.47±178.49)copies/ml,均显著低于对照组,差异具有统计学意义(t=8.51、9.32;P均<0.05);且观察组ALT复常率、HBeAg阴转率分别为86.84%、71.05%,均显著高于对照组,差异具有统计学意义(X2=8.53、9.36;P均<0.05);观察组HBeAg血清学转换率与对照组比较差异无统计学意义(X2=0.87;P>0.05)。结论:恩替卡韦辅助治疗肝硬化的效果确切,可改善患者预后,促进HBeAg阴转,具有较高的临床推广价值。
肝硬化;恩替卡韦;临床疗效
慢性肝炎进展为肝硬化的几率较大,此类患者的预后较差,可出现肝肾器官衰竭等严重并发症而导致死亡。抗病毒治疗是目前控制肝硬化病情进展的主要手段,部分临床研究显示肝硬化患者在接受抗病毒治疗后有很大几率维持病情稳定,延缓病情进展与恶化。目前应用核苷酸类似物对肝硬化患者进行抗病毒治疗已成为临床共识,恩替卡韦治疗慢性肝炎的效果已在多项临床研究中得到证实,但其对于肝硬化的临床疗效研究相对短缺。鉴于此,本研究通过随机对照试验,分析恩替卡韦在肝硬化临床治疗中的应用效果,旨在为临床工作提供参考。现报告如下:
1 资料与方法
1.1一般资料选取2013年1月~2014年6月在我院接受治疗的肝硬化患者76例,作为本研究的观察对象,均符合《病毒性肝炎防治方案》中的肝硬化诊断标准[1],无误诊病例。排除标准[2]:合并酒精肝或药物性肝炎等其他肝脏器质性病变患者;合并肝癌、心脏、肝肾等重要脏器功能衰竭患者;入组前2周内有抗病毒治疗史者。按照完全随机数字表法,将入选对象分为观察组与对照组各38例,观察组中男21例,女17例,年龄56~73岁,平均年龄(62.39± 4.08)岁,HBeAg阴性9例,HBeAg阳性29例;对照组中男23例,女15例,年龄54~70岁,平均年龄(61.33±4.57)岁,HBeAg阴性8例,HBeAg阳性30例。两组一般资料比较均无明显差异(P>0.05),具有可比性。所有患者均对本研究内容充分知情,且均自愿签署知情同意书后入组,符合伦理学要求。
1.2治疗方法对照组采用保肝、降门脉压、退黄等常规药物治疗。观察组在对照组基础上加用恩替卡韦片(国药准字H20052237,规格:0.5 mg)治疗,即口服恩替卡韦0.5 mg/次,1次/d。治疗1年后评定疗效。
1.3观察指标[3~4]使用荧光定量聚合酶链反应(PCR)测定血清中HBV-DNA含量,试剂盒检测下限为1.0×103copies/ml,若检测结果无法显示则记为0。记录两组ALT复常率、HBeAg阴转率与HBeAg血清学转换率。HBV标志物采用电化学发光法检测,并采用自动生化分析仪对ALT进行检测。同时使用Child-Pugh评分对两组治疗前后的肝功能分级进行评分,分数越高表示肝功能越差。
1.4统计学方法所有数据采用SPSS17.0软件分析,计数资料采用构成比(%)表示,行卡方检验,计量资料以均数±标准差(±s)表示,行t检验,P<0.05为差异具有统计学意义。
2 结果
两组患者在治疗后均未出现肝性脑病或肝功能衰竭等严重并发症,无死亡病例,所有患者均完成整个治疗过程。
2.1两组治疗前后Child-Pugh评分和HBV-DNA定量比较两组治疗前Child-Pugh评分、HBV-DNA定量比较均无显著差异(P均>0.05);治疗后观察组Child-Pugh评分、HBV-DNA定量均显著低于对照组,差异具有统计学意义(P<0.05)。见表1。
表1 两组治疗前后Child-Pugh评分和HBV-DNA定量比较(±s)

表1 两组治疗前后Child-Pugh评分和HBV-DNA定量比较(±s)
组别nChild-Pugh评分(分)治疗前治疗后HBV-DNA定量(copies/ml)治疗前治疗后观察组对照组tP 38 38 11.27±3.10 11.86±4.32 0.78>0.05 8.53±1.48 10.15±2.33 8.51<0.05 1 534.29±274.30 1 621.83±231.58 0.47>0.05 932.47±178.491 279.50±205.44 9.32<0.05
2.2两组ALT复常率、HBeAg阴转率及HBeAg血清学转换率比较观察组ALT复常率、HBeAg阴转率均显著高于对照组,差异具有统计学意义(P均<0.05);观察组HBeAg血清学转换率与对照组比较差异无统计学意义(P>0.05)。见表2。
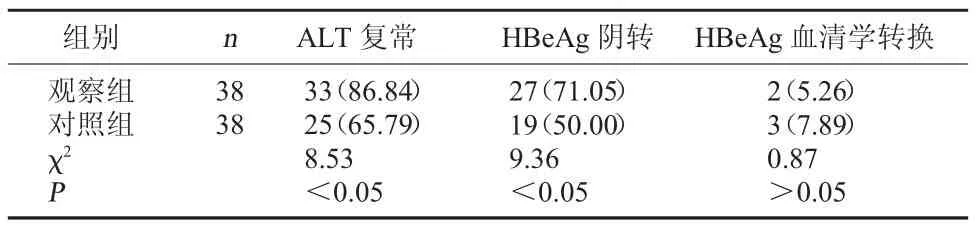
表2 两组ALT复常率、HBeAg阴转率及HBeAg血清学转换率比较[例(%)]
3 讨论
到目前为止,已有多位学者在临床研究中指出,肝硬化的病情进展及预后与患者血清中的HBV-DNA载量密切相关[5]。由于病毒的持续性复制,将会进一步加重肝脏炎症,使肝纤维化加重而导致肝硬化,故而临床上始终将抗炎治疗以及抑制病毒复制作为控制肝炎病情进展的重点,对于肝硬化的预后改善也有积极意义。肝硬化的长期治疗目标是尽可能地抑制HBV-DNA的复制或消除病毒基因,使肝细胞的纤维化进程得到控制,以便将肝癌的发生风险控制在最低水平,为患者的预后改善创造有利条件。恩替卡韦属于鸟嘌呤核苷类似物,其抑制肝炎病毒的作用已得到证实,传统药物拉米夫定虽说与恩替卡韦均为核苷类似物,但若长时间治疗则会引起耐药性,甚至可能出现反弹或复发现象,不利于患者恢复正常生活。而大量的动物模型与临床研究证实恩替卡韦在治疗过程中出现耐药性的几率低[6]。恩替卡韦在进入机体后可发生磷酸化反应生成活性物质三磷酸盐,具有活性的三磷酸盐可与HBV多聚酶的天然底物三磷酸脱氧鸟嘌呤核苷发生竞争性作用,抑制HBV病毒逆转录酶的所有活性,从而达到治疗目的。另外,药代动力学显示恩替卡韦的血药有效时间为15~17 h,给药1次/d即可,很好地避免了多次用药所带来的不良反应风险,安全性高,应用价值高。本研究发现观察组在接受恩替卡韦辅助治疗后,其Child-Pugh评分、HBV-DNA定量均显著低于对照组,而ALT复常率、HBeAg阴转率均显著高于对照组,差异均具有统计学意义(P均<0.05);两组HBeAg血清学转换率比较无明显差异(P>0.05)。与冯继红[7]的研究结论具有一致性,表明恩替卡韦辅助治疗肝硬化效果确切,可抑制病毒复制,延缓病情进展,还具有良好的肝功能保护作用,且不会加大引起HBeAg血清学转换风险,安全可靠。
[1]尤红,吴晓宁,王倩怡,等.恩替卡韦对慢性乙型肝炎、肝硬化代偿期和失代偿期的2年抗病毒疗效比较[J].首都医科大学学报,2010,31(5):563-565
[2]徐严,王江滨,徐杰,等.恩替卡韦治疗104例乙型肝炎肝硬化患者96周的疗效观察[J].中华肝脏病杂志,2010,18(2):109-112
[3]叶素素,张新雷,徐伟.替比夫定、阿德福韦酯联用与恩替卡韦单药治疗失代偿期乙肝肝硬化疗效对比观察[J].山东医药,2015,55(2): 65-67
[4]朱刚剑,苏传真,王健,等.恩替卡韦治疗代偿期乙肝肝硬化患者过程中血清甲状腺激素的变化[J].实用医学杂志,2013,29(3):461-463
[5]吴刚,何鸿雁,李烨,等.复方鳖甲软肝片联合恩替卡韦对HBV相关肝硬化患者的临床疗效观察[J].中华肝脏病杂志,2014,22(8): 604-608
[6]杨兆辉,刘丽萍,于建武,等.恩替卡韦治疗失代偿期乙型肝炎肝硬化短期疗效观察[J].哈尔滨医科大学学报,2010,44(6):583-586
[7]冯继红.恩替卡韦治疗失代偿期乙肝肝硬化临床疗效观察[J].医学与哲学(临床决策论坛),2011,32(4):29-30
R575.2
B
10.13638/j.issn.1671-4040.2015.12.014
2015-08-20)
刘俊,E-mail:liujunwenwen@163.com
