超声辅助萃取-分散液液微萃取/气相色谱法测定环境水样中六氯苯、林丹及硫丹
2015-10-16侯德坤呼日乐达瓦张福金张婷瑜张欣昕姚一萍
侯德坤, 何 江, 呼日乐达瓦, 张福金, 张 敏, 张婷瑜, 张欣昕, 姚一萍
(1.内蒙古大学生命科学院,内蒙古呼和浩特 010021; 2.内蒙古大学环境与资源学院,内蒙古呼和浩特 010021; 3.内蒙古农牧业科学院,资源环境与检测技术研究所,内蒙古呼和浩特 010031; 4.内蒙古大学环境地质研究所,内蒙古呼和浩特 010021)
六氯苯(Hexachlorobenzene)、林丹(Lindane)和硫丹(Endosulfan)都属于典型的持久性有机污染物(Persistent Organic Pollutants,POPs),对皮肤[1]、肝脏[2]、新陈代谢[3]和中枢及周围神经系统都有较大的影响。我国自1983年就开始禁用六氯苯和林丹,但由于其化学性质稳定、难以降解及“三致”毒性效应的特点,在各种环境介质如江河、湖泊、海洋、土壤、底泥等中至今仍有残留。2012年,硫丹也被列入《斯德哥尔摩公约》的黑名单,并在全球范围内开展消减与控制[4]。环境介质中六氯苯、林丹及硫丹主要来源于除草剂和杀菌剂的生产过程及农业生产中的应用[5,6],且可在环境及生物中累积并严重危害人类健康。因此,监控此类污染物在环境中的残留具有重要意义。
目前,环境水样中氯苯类、有机氯类化合物的检测以气相色谱-电子捕获检测法(GC-μECD)为主。富集手段主要有溶剂法、顶空法、吹扫捕集、膜萃取技术、固相萃取法、液相萃取法等[7]。然而这些技术操作繁琐耗时,需要使用大量有毒、有害溶剂,对人体及环境有不利影响。分散液液微萃取技术(Dispersive Liquid-liquid Microextraction,DLLME)是近年来兴起的样品前处理方法,该方法将样品采集、萃取和浓缩于一体,兼具液液萃取和固相萃取的特点,具有操作简单、快速、成本低、富集效率高等优点[8]。
超声辅助萃取-分散液液微萃取(UAE-DLLME)是在分散液液微萃取的基础上辅以超声技术,利用超声过程中产生的空化、振动、粉碎、搅拌等综合效应,来加速不互溶两相之间的质量传递,从而提高萃取效率[9,10]。本文以三氯乙烯为萃取剂,甲醇为分散剂,建立了UAE-DLLME/GC-μECD法测定环境水样中六氯苯、林丹和硫丹含量的新方法,并对影响萃取效率的因素进行了优化,确定了最佳条件,最后将优化后的方法用于实际水样中六氯苯、林丹和硫丹的分析检测。
1 实验部分
1.1 仪器与试剂
Agilent 7890A型气相色谱仪(美国,安捷伦公司),配有电子捕获检测器(μECD);S7500型超声波清洗仪(上海必能信超声有限公司);CR22GIII型离心机(日本,日立公司);BT125D型电子天平(赛多利斯科学仪器(北京)有限公司);pHS-3C型pH计(上海精密科学仪器有限公司);Milli-Q超纯水系统(美国,Millipore公司)。
六氯苯(美国Chem Service公司);林丹(纯度为99.8%,德国有机工业所);α-硫丹(纯度大于99.6%,美国Sigma公司),β-硫丹(纯度大于99.0%,美国Sigma公司)。甲醇、正己烷、丙酮、乙腈(色谱纯,美国Tedia公司);无水乙醇(分析纯,天津市四通化工厂);二氯甲烷(分析纯,成都化学试剂厂);二氯乙烷、四氯化碳、三氯乙烯(分析纯,北京化工厂);氯苯(分析纯,上海中秦化学试剂有限公司);NaCl和NaOH(分析纯,国药集团化学试剂有限公司);HCl(优级纯,成都科龙化学试剂厂);实验用水为Milli-Q水。所有溶剂与实验用水均经过0.45 μm滤膜过滤后使用。
1.2 实验方法
1.2.1标准溶液的配制与实际水样的处理精密称取六氯苯、林丹、α-硫丹和β-硫丹标准品0.100 mg置于4个10 mL的容量瓶中,用正己烷溶解并定容,配成10 mg/L的储备液。准确移取4种储备液各1.00 mL,置于10 mL的容量瓶中,用正己烷定容,配成1.0 mg/L的混合标准溶液,于4 ℃冰箱中保存备用。将1.0 mg/L的混合标准液用正己烷逐级稀释至所需浓度得到工作液。
实验采集的灌溉水(内蒙古农牧业科学研究院,呼和浩特市)、自来水(内蒙古农牧业科学研究院,呼和浩特市)、湖水1(乌梁素海,乌拉特前旗)、湖水2(岱海,凉城市)均经过0.22 μm滤膜过滤,4 ℃保存。
1.2.2分散液-液微萃取步骤准确移取5.0 mL待测水样于10 mL带旋冒的锥形离心管中,用稀HCl调节溶液pH=4.0,用气密型注射器快速注入1.0 mL甲醇(分散剂)和100 μL三氯乙烯(萃取剂)的混合液,形成乳浊液(水/三氯乙烯/甲醇乳浊体系),超声萃取5 min后,冰水浴中静置20 min。然后以10 000 r/min离心5 min,弃掉上层液体,用微量进样器抽取一定体积沉淀相,用适量的正己烷溶解后,定容至0.5 mL,吸取1.0 μL进行GC分析。
1.2.3色谱条件色谱柱:HP-5毛细管柱(30 m×0.25 mm×0.25 μm);进样口温度250 ℃;检测器温度280 ℃;柱温升温程序:初始温度100 ℃,保持1 min,以10 ℃/min升至240 ℃保持5 min,以5 ℃/min升至260 ℃,保持2 min;载气:高纯氮气(纯度大于99.99%),流速1.0 mL/min,尾吹气25 mL/min;进样模式:不分流;进样量:1.0 μL。
2 结果与讨论
2.1 DLLME萃取条件的优化
2.1.1萃取剂及其体积的选择在DLLME中,选择合适的萃取剂是提高萃取效率的重要因素,通常要考虑萃取剂的密度及挥发性、对目标物质的萃取能力、能否形成稳定悬浊液以及对待测物后续色谱分离分析的影响[11 - 13]。实验考察了二氯甲烷、二氯乙烷、四氯化碳、三氯乙烯及氯代苯5种有机溶剂作为萃取剂时对六氯苯、林丹和硫丹萃取效率的影响。结果表明:二氯甲烷在水中的溶解度较大,离心后无沉淀相;1,2-二氯乙烷萃取效果差;氯代苯的杂质峰较多,干扰目标物的测定;三氯乙烯的萃取效率比四氯化碳略有提高,因此本研究选用三氯乙烯作为萃取剂。实验对比了10~200 μL三氯乙烯与1.0 mL甲醇混合时对六氯苯、林丹和硫丹的萃取效率的影响。结果表明,萃取剂体积在40 μL以下时,离心后沉淀相稳定性较差,且体积较小难以移取、定量;当三氯乙烯加入量为100 μL时,所得目标物的萃取效果最佳,实验选择其加入量为100 μL。
2.1.2分散剂及其用量的选择在DLLME中对分散剂的要求有3个主要方面,一是与萃取溶剂及水有良好的混溶性,而在分相时又要能形成两相;二是对目标化合物的分析测定不形成干扰;三是毒性低和价廉[14]。本研究选择符合上述条件的甲醇、无水乙醇、乙腈和丙酮4种分散剂进行实验。结果表明在相同的实验条件下,4种分散剂均对三氯乙烯有良好的分散悬浮作用,其中以甲醇效果最好,因此实验选择甲醇作为分散剂。萃取剂三氯乙烯用量固定为100 μL的情况下,考察了不同分散剂用量对于六氯苯、林丹及硫丹萃取效率的影响,分散剂体积选择为0.5~2.0 mL,实验表明各待测物的峰面积在甲醇体积为1.0 mL时最大,而后随分散剂用量增加而减小。因此,实验选用分散剂体积为1.0 mL。
2.1.3溶液pH及盐效应的影响在DLLME中,体系的pH值对萃取过程中的传质起着至关重要的作用。通过控制溶液的pH可改变溶液中某些分析物的存在形式,使分析物呈分子状态而降低其水溶性,增大在有机相中的分配[14]。本实验考察了pH值分别为3.0、4.0、5.0、7.0、9.0及10.0时,样品溶液的pH值对萃取效率的影响(用稀HCl和NaOH溶液调节pH值)。结果表明,当pH值为4.0时,各目标物的峰面积最大;当pH>4.0时,萃取效率开始下降;当pH>7.0时,萃取效率急剧下降。这可能与三种农药理化性质有关:在弱酸性环境下较为稳定,碱性时发生缓慢水解。因此在后续的实验中调节溶液的pH值为4.0。一般来讲,离子强度的增加,分析物和有机萃取剂在水相中的溶解度会减小,有利于回收率的提高[15]。本实验中,在同一浓度的样品溶液中,通过添加0.5%~10%(m/V)的NaCl改变样品溶液的离子强度,得到峰面积随离子强度变化的曲线。随盐浓度的增加,峰面积变化不大,但沉淀相的体积增大,使得富集倍数降低,故在后续实验中不加入盐。
2.1.4冰浴时间及离心时间对萃取效率的影响本实验选取冰浴时间为0~20 min,获得不同冰浴时间下的峰面积值。结果显示,硫丹的萃取效率在20 min冰浴时间内变化不大,六氯苯及林丹在10~20 min内萃取效率迅速增加。因此本实验选取冰浴的时间为20 min。对于离心时间,本实验选择了 10 000 r/min离心2、3、5、10 min进行比较,结果发现离心 5 min 后,萃取效率已达最高值,故离心时间选择5 min。
2.2 超声功率及超声时间对萃取效率的影响
利用超声技术对DLLME进行辅助萃取,通常情况下低功率超声可使萃取时间延长且萃取不完全;而超声功率过高又会造成六氯苯、林丹及硫丹的降解率升高。因此比较了不同超声功率对3种有机物回收率的影响。结果表明,随超声功率的增大,3种有机物的回收率都在增加,至超声功率为80 W时,回收率最大,100 W时回收率有小幅下降,因此本实验确定最佳超声功率为80 W。
在萃取过程中超声起到分散剂的作用,超声时间的长短对萃取效率也产生一定的影响。实验考察了超声时间1~20 min内对水样中六氯苯、林丹及硫丹的提取效率的影响。实验结果表明:随着超声提取时间的延长,水样中3种有机物的提取效率增加,超声时间从1 min 增加到5 min,萃取效率也随之增加,当超声时间达到5 min时,萃取效率保持稳定。继续增加超声的时间,萃取效率变化不大。因此本实验选取超声时间为5 min.
2.3 方法的线性关系、检出限和精密度
在优化条件下,考察了所建立方法的线性范围、线性相关系数(r2)、相对标准偏差(RSD),检出限(LOD,信噪比S/N=3)和定量限(LOQ,信噪比S/N=10),结果见表1。
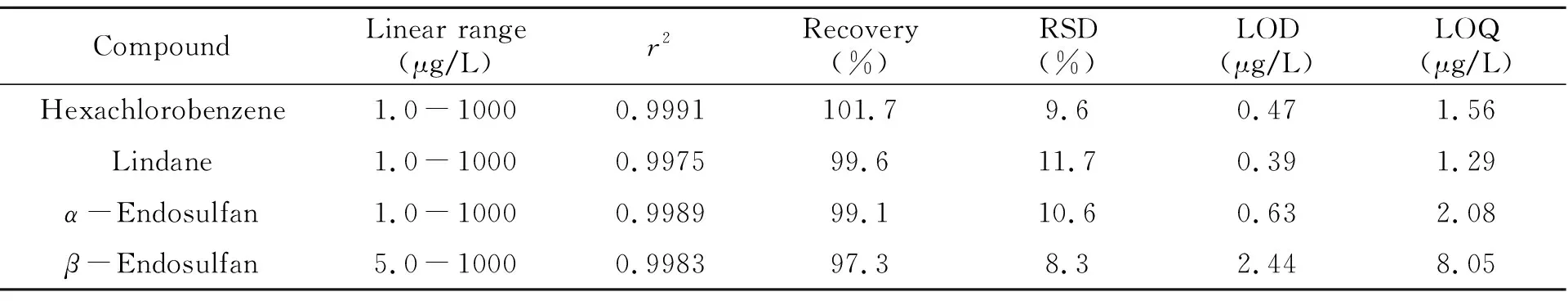
表1 方法的线性范围、相关系数、回收率、相对标准偏差及检出限、定量限(n=7)
2.4 实际样品分析
为考察此方法对实际样品的分析能力,对实际水样自来水、灌溉水及湖水进行了测定。在自来水中未检测到3类农药的残留,但是在灌溉水及部分湖水中检测到了六氯苯和林丹的存在,灌溉水:六氯苯1.42 μg/L,林丹1.64 μg/L;湖水1:六氯苯1.71 μg/L,林丹1.63 μg/L;湖水2:六氯苯9.52 μg/L;林丹4.37 μg/L。在湖水2和湖水3中检测到了硫丹的存在,但是其浓度值在检出限以下(表2)。

表2 自来水、灌溉水及湖水中六氯苯、林丹和硫丹的萃取回收率(n=3)
* not detected;** detected but below the LODs.
3 结论
本研究建立了一种适用于快速测定环境水样中六氯苯、林丹和硫丹的UAE-DLLME-GC分析方法。实验结果表明,该方法简便、快速、灵敏、准确,可用于环境水样中六氯苯、林丹和硫丹的检测。
