聚合物整体柱毛细管微萃取-电感耦合等离子体质谱分析生物样品中的痕量重金属离子
2015-10-16尤国颖陈贝贝
尤国颖, 陈贝贝, 何 蔓*, 胡 斌
(武汉大学化学与分子科学学院,生物医学分析化学教育部重点实验室,湖北武汉 430072)
随着冶金、采矿、电镀工业的发展和城市化进程的加剧,大量金属离子被排放到环境中,不仅对水体中的植物、动物和微生物具有潜在的威胁,而且还可以通过食物链进入人体并在各器官中累积,对人类的健康造成危害。因此,建立生物样品中痕量金属离子的分析检测方法具有重要的现实意义。常见的痕量金属离子检测方法有电感耦合等离子体光谱(ICP-OES)、电感耦合等离子体质谱(ICP-MS)、原子吸收光谱(AAS)、原子荧光光谱(AFS)等。其中,ICP-MS法灵敏度高、线性范围宽、检出限低、分析速度快,可以获得同位素信息,且易于联用并实现自动化。但将其用于生物样品分析时,通常需要进行样品前处理,使其适于ICP-MS进样及分析,同时达到去除复杂基体、富集目标分析物的目的。
毛细管微萃取(CME)是一种新型的微型化样品前处理技术,具有操作简单、成本低廉、样品消耗量少、易于实现在线联用、可以避免引入污染等优点。在各种CME萃取材料中,有机聚合物整体柱萃取材料因具有通透性高、孔结构多和比表面积大、吸附容量大、耐酸性强以及制备简单等优点,克服了传统填充柱制备方法复杂的缺点,避免了开管柱涂层相比小、柱容量低等问题。目前,聚合物整体柱CME与高效液相色谱、毛细管电泳、毛细管电色谱等方法联用已广泛应用于痕量有机物分析,但在无机痕量元素分析中应用较少。Yin等[1]制备了聚(丙烯酰胺-乙烯基吡啶-N,N-亚甲基双丙烯酰胺)整体柱,并将其成功用于人发和尿样中Cd2+、Tl2+、Pb2+的富集和分析。Zheng等[2]制备了聚甲基丙烯酰胺涂层纤维,并将其插入毛细管中,基于此建立了CME-ICP-MS分析人尿和血清中痕量金属离子的新方法。相对而言,纤维填充式毛细管的制备操作繁琐,因此,探索制备简单、对金属离子选择性好的整体柱萃取材料具有重要的应用价值。本文采用聚合法制备了聚(丙烯酰胺-乙二醇二甲基丙烯酸酯)整体柱(Poly(AA-EGDMA)),在碱性条件下,该整体柱所含的官能团酰胺(CO-NH2)具有裸露的孤对电子;基于酰胺的孤对电子与金属离子之间的络合作用,建立了Poly(AA-EGDMA)整体柱CME-ICP-MS联用检测重金属离子的分析方法,并将其用于生物样品中痕量重金属离子Cd2+与Pb2+的测定。
1 实验部分
1.1 仪器装置及工作条件
Quanta 200扫描电子显微镜(FEI,Holand)和170SX FT-IR红外光谱仪(NICOL ET,USA)用于整体柱的表征;HH-6数显恒温水浴锅(常州澳华仪器有限公司)用于温度控制;FIA-3110流动注射分析仪(北京吉天仪器有限公司)用于将溶液引入毛细管管路;Mettler Toledo 320-S pH计(Mettler Toledo(上海)仪器有限公司)用于调节溶液的pH值;WX-4000微波消解仪(上海屹尧仪器科技发展有限公司)用于样品消解;XH-B型涡旋混合器(江苏康健医疗用品有限公司)用于快速混匀混合溶剂。玻璃毛细管规格为:内径0.9~1.1 mm,管长100 mm(华西医科大学仪器厂)。Agilent 7500a ICP-MS仪的工作参数如表1所示。

表1 ICP-MS的操作参数Table 1 Operating parameters of ICP-MS
1.2 试剂和标准溶液
Cd2+和Pb2+的标准储备液(1.000 mg·mL-1)分别由CdO(光谱纯,上海第一试剂厂)和Pb(NO3)2(优级纯,上海第一试剂厂)溶解于2%HNO3溶液中配制;混合金属离子和标准溶液系列均由储备液逐级稀释而成。其它无机离子的标准储备液按照常规方法配制;丙烯酰胺(AA)(化学纯,国药集团化学试剂有限公司);聚乙烯醇(PEG 4000)(化学纯,国药集团化学试剂有限公司);乙二醇二甲基丙烯酸酯(EGDMA,阿拉丁);偶氮二异丁基腈(AIBN)(化学纯,上海试四赫维化工有限公司);其他试剂均为分析纯或分析纯以上级别。实验用水为Milli-Q超纯水(18.2 MΩ·cm,Millipore,Molsheim,France)。
所用容器均在10%HNO3溶液中浸泡24 h,用超纯水充分洗涤后,烘干备用。
1.3 聚合物整体柱的制备
将内径1 mm的玻璃毛细管依次用水、甲醇清洗,用1 mol·L-1NaOH溶液浸泡12 h后用水冲洗至中性,再用1 mol·L-1HCl浸泡3 h并用水洗至中性,甲醇冲洗后用Ar气吹干。将玻璃毛细管浸入到WD -70∶甲醇=1∶1(V/V)的混合溶剂中,在60 ℃下反应12 h,反应完毕用甲醇清洗并用Ar气吹干。
将40 mg PEG加入1 200 μL甲醇中,涡旋后得到均一透明溶液,然后加入240 μL EGDMA,超声混匀后加入90 mg AA和3 mg AIBN,超声脱气5 min后,将混合溶液毛吸入玻璃毛细管中;用硅橡胶将毛细管两端封口,在60 ℃水浴锅中放置12 h后,即制得Poly(AA-EGDMA)整体柱。
1.4 样品处理
取5 mL人体尿样,加入5 mL浓HNO3并在电热板上进行预消解,然后进行微波消解,程序为:150 ℃,15 atm,1 000 W,5 min;180 ℃,20 atm,1 000 W,5 min;200 ℃,25 atm,1 000 W,5 min。将得到透明澄清的液体加热蒸发至近干,溶解残渣,调节pH值为7.5,并转移定容至5 mL。以5 mL浓HNO3作为空白样品,消解制备方法同上。
1.5 毛细管微萃取过程
调节样品溶液pH值为7.5,移取1.5 mL样品溶液并将其以100 μL·min-1的流速通过毛细管整体柱进行预富集,再将150 μL 1 mol·L-1HNO3洗脱剂以75 μL·min-1的流速进行洗脱后,洗脱液引入ICP-MS进行检测。用0.5 mL 1 mol·L-1HNO3以50 μL·min-1的流速缓慢通过毛细管整体柱使涂层得到再生,再用0.5 mL 0.1 mol·L-1的NH4Ac平衡柱子至中性。
2 结果与讨论
2.1 聚(丙烯酰胺-乙二醇二甲基丙烯酸脂)整体柱的表征

图2是自制Poly(AA-EGDMA)整体柱的扫描电镜(SEM)图。可以看出,Poly(AA-EGDMA)整体柱与玻璃表面键合很牢固,没有脱壁现象;Poly(AA-EGDMA)整体柱的骨架是由纳米级微球颗粒相互连接而成,骨架之间具有相互交联的微米级大孔结构,纳米级微球可以提高萃取容量,微米级大孔可以提高目标金属离子的传质速率。
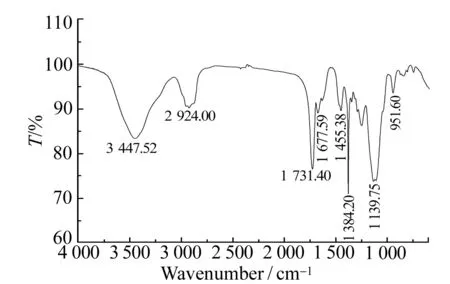
图1 Poly(AA-EGDMA)的红外光谱图Fig.1 Infrared spectra of Poly(AA-EGDMA)

图2 Poly(AA-EGDMA)整体柱的扫描电镜(SEM)图Fig.2 SEM image of Poly(AA-EGDMA) monolithic column(×80(A) and×1200(B))
2.2 毛细管微萃取参数的优化
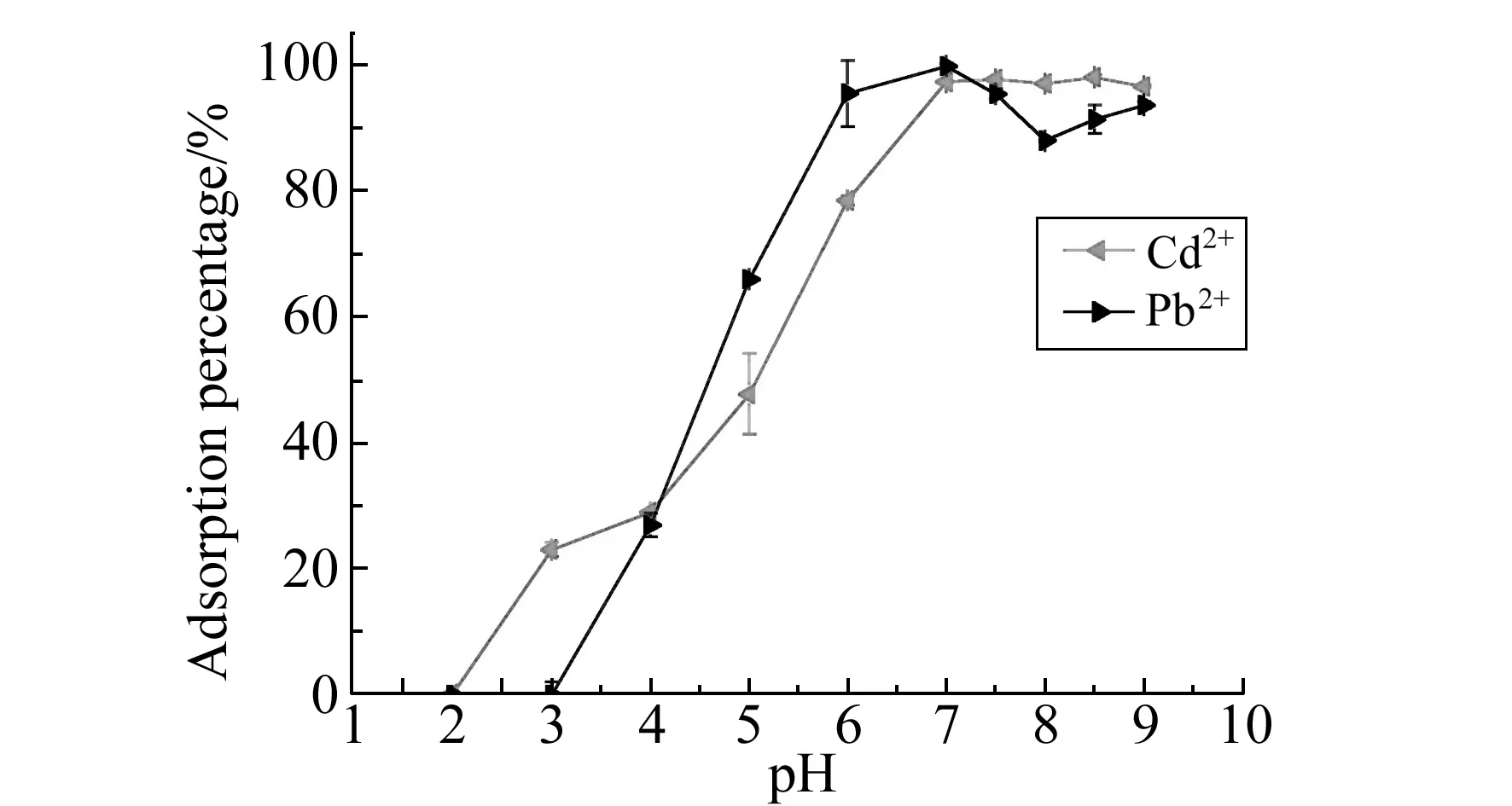
图3 pH对Cd2+和Pb2+在Poly(AA-EGDMA)整体柱上吸附率的影响Fig.3 Effect of pH on the adsorption percentage of Cd2+ and Pb2+ on Poly(AA-EGDMA) monolithic column sample concentration and volume:1 mL,20 μg·L-1;sample flow rate:50 μL·min-1.
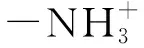
2.2.2上样流速及样品体积的优化控制进样体积为1 mL,考察了上样流速在50~200 μL·min-1范围内,目标金属离子在整体柱上的吸附率。结果表明,在所考察的流速范围内,Cd2+和Pb2+均能定量吸附。在后续实验中选择上样流速为150 μL·min-1。
固定金属离子的绝对量为20 ng,改变样品体积,实验考察了样品体积分别为1、1.5、2、4、5 mL时,Poly(AA-EGDMA)整体柱对目标金属离子回收率的影响。结果表明,当样品体积为1、1.5、2 mL时,Cd2+和Pb2+均可定量回收。最终选择上样体积为1.5 mL。
2.2.3洗脱条件的优化由pH的影响可以看出,当pH小于3时,目标金属离子几乎不被Poly(AA-EGDMA)整体柱吸附,因此实验考察了HNO3在0.01~1.5 mol·L-1浓度范围对金属离子的洗脱效果,如图4所示。可以看出,当HNO3浓度大于或等于0.1 mol·L-1时,Cd2+和Pb2+均可定量回收(>85%),为了减小解吸剂的体积以及介质酸度对仪器的影响,后续实验采用1 mol·L-1HNO3作为洗脱剂。
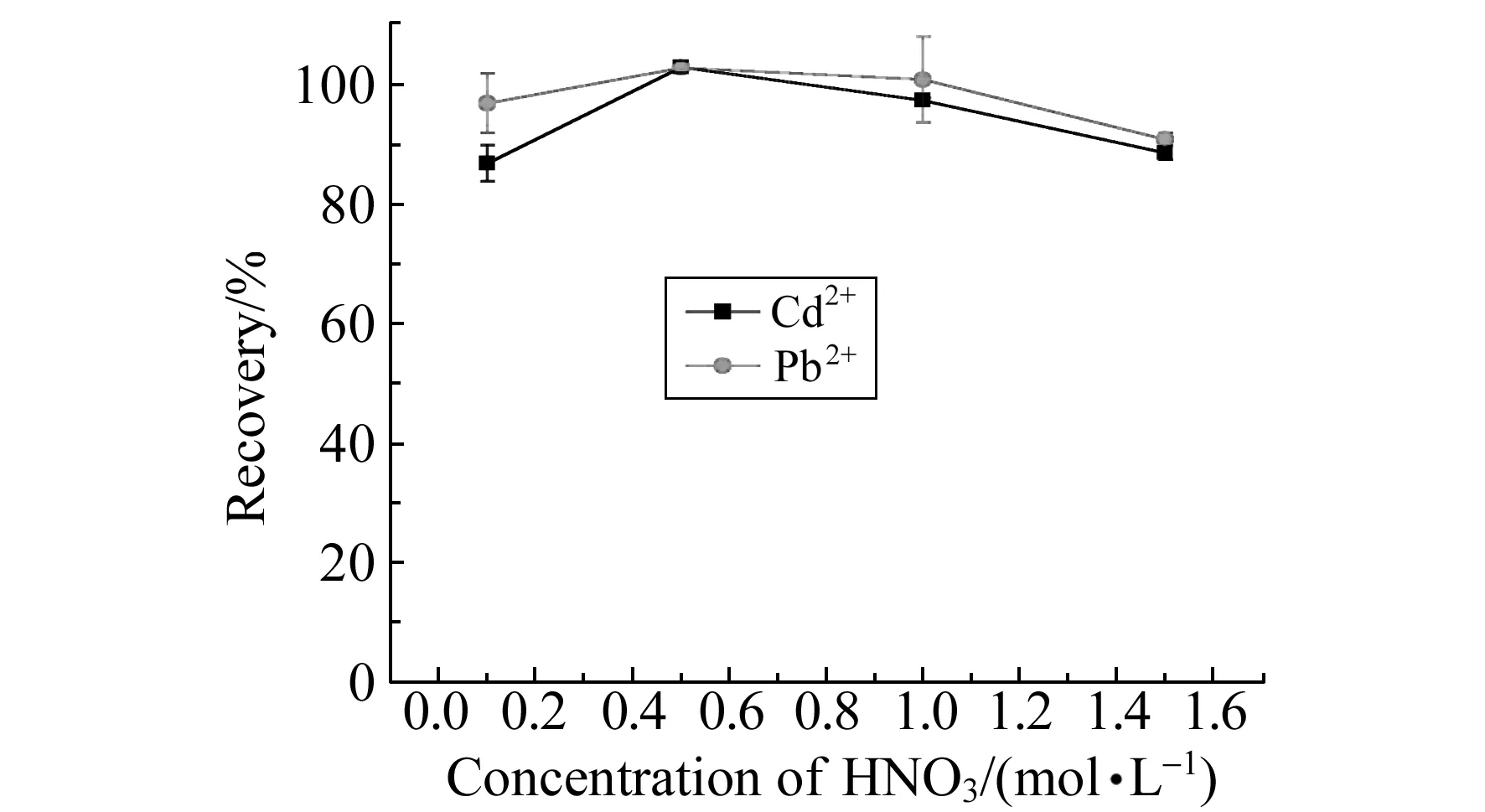
图4 HNO3浓度对Cd2+和Pb2+在Poly(AA-EGDMA)整体柱上回收率的影响Fig.4 Effect of concentration of HNO3 on the recoveries of Cd2+ and Pb2+ on Poly(AA-EGDMA) monolithic column pH=7.5,sample volume and concentration:1 mL 20 μg·L-1,sample flow rate:100 μL·min-1;elution volume:1 mL,elution flow rate:50 μL·min-1.
洗脱剂体积会影响洗脱效果及方法的富集倍数,洗脱剂体积过少时,目标金属离子不能被完全洗脱,洗脱剂体积过大时,会影响方法的富集倍数。为了考察洗脱剂体积对目标金属离子回收率的影响,将200 μL 1 mol·L-1HNO3洗脱液平均分成4份,依次用50 μL洗脱液进行连续洗脱,ICP-MS测定后计算回收率。结果表明,当洗脱剂体积为150 μL时,所考察的金属离子Cd2+和Pb2+的回收率均能达到85%以上,最终选择洗脱剂体积为150 μL。由于上样体积为1.5 mL,所以本方法对Cd2+和Pb2+的理论富集倍数为10倍。
固定洗脱剂HNO3体积为150 μL,考察了洗脱剂流速在50~150 μL·min-1范围内目标金属离子的回收率。结果表明,当洗脱剂流速小于100 μL·min-1时,Cd2+和Pb2+均能定量回收,后续实验选择洗脱剂流速为75 μL·min-1。
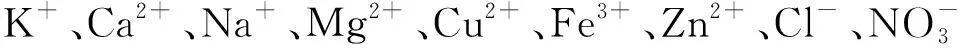
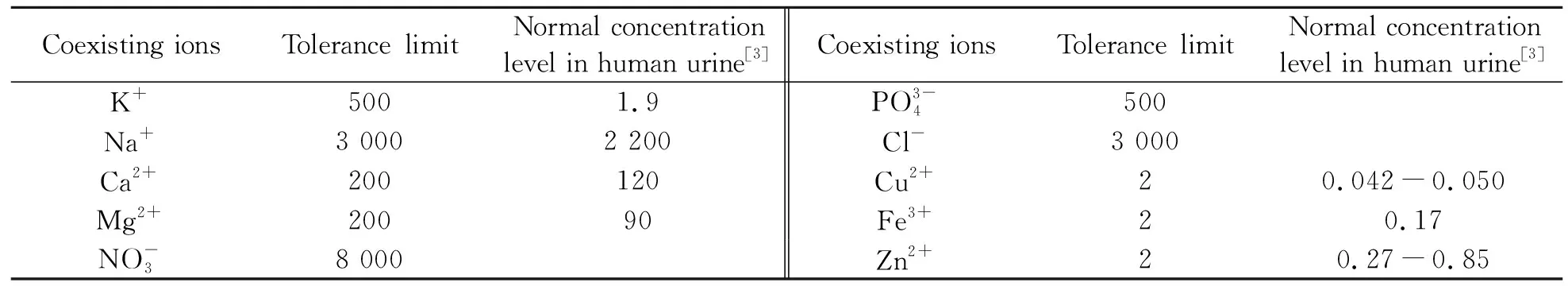
表2 Cd2+和Pb2+测定对共存离子的耐受量(μg·mL-1)Table 2 Tolerance limits of coexisting ions for the determination of Cd2+ and Pb2+(μg·mL-1)
2.3 毛细管整体柱性能评价
2.3.1毛细管整体柱制备的重现性实验考察了同一批(n=6)以及不同批次(n=6)制备的毛细管整体柱的重现性,结果如表3所示。可见,同批次和不同批次制备的整体柱对目标金属离子回收率的相对标准偏差(RSD)在1.6%~6.8%范围内,说明Poly(AA-EGDMA)整体柱具有良好的制备重现性。
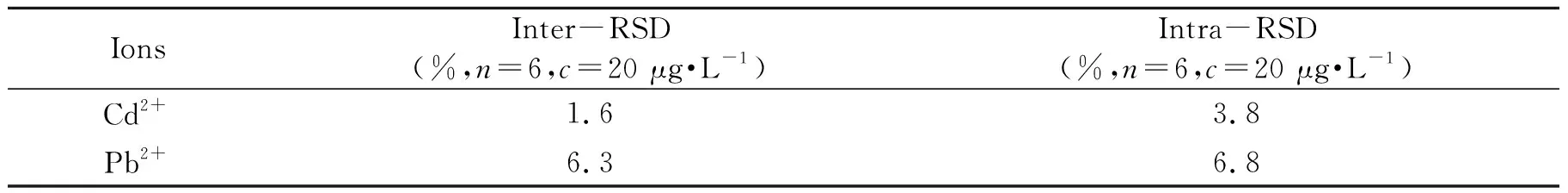
表3 Poly(AA-EGDMA)整体柱制备的重现性Table 3 Reproducibility of Poly(AA-EGDMA) monolith column
2.3.2毛细管整体柱的使用寿命实验结果表明,将0.5 mL 1 mol·L-1HNO3以50 μL·min-1的流速通过Poly(AA-EGDMA)整体柱,即可实现再生。同时,将Poly(AA-EGDMA)整体柱连续使用50次,其萃取性能没有明显变化,说明自制Poly(AA-EGDMA)整体柱可重复使用50次以上。
2.3.3毛细管整体的吸附容量分别将40 mL含有100 μg·L-1Cd2+和Pb2+的样品溶液以100 μL·min-1的流速连续通过一段6 cm Poly(AA-EGDMA)整体柱,流出液引入ICP-MS仪进行检测,若流出液中金属离子的浓度大于15 μg·L-1,说明该毛细管整体柱对金属离子的吸附量已达到饱和。实验结果表明,Poly(AA-EGDMA)整体柱对Cd2+和Pb2+的吸附容量分别为46.7 μg·m-1和130 μg·m-1。将该材料与其它吸附材料的吸附容量进行对比(表4),可以看出与填充柱材料和无机涂层相比,Poly(AA-EGDMA)整体柱具有较高的吸附容量,与APTES改性硅胶整体柱相比,吸附容量相当。

表4 吸附容量的比较(μg·m-1)Table 4 Comparison of adsorption capacity(μg·m-1)
2.4 分析性能
在优化实验条件下,对方法的分析性能进行了考察,结果列于表5。表6比较了本方法与其他方法的分析性能,可以看出,本方法检出限较低,重现性较好。
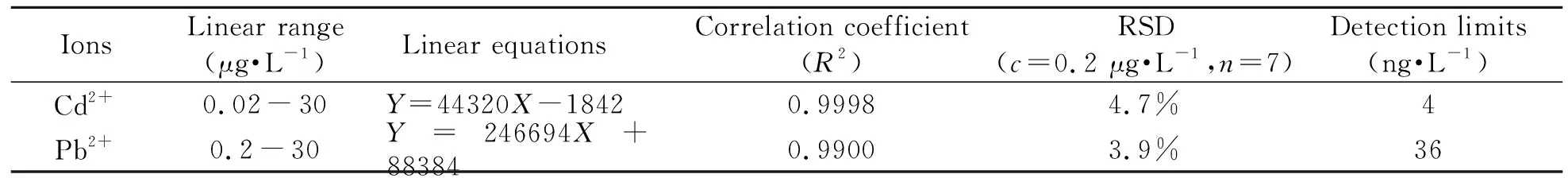
表5 本方法的分析性能Table 5 Analytical performance of the proposed method
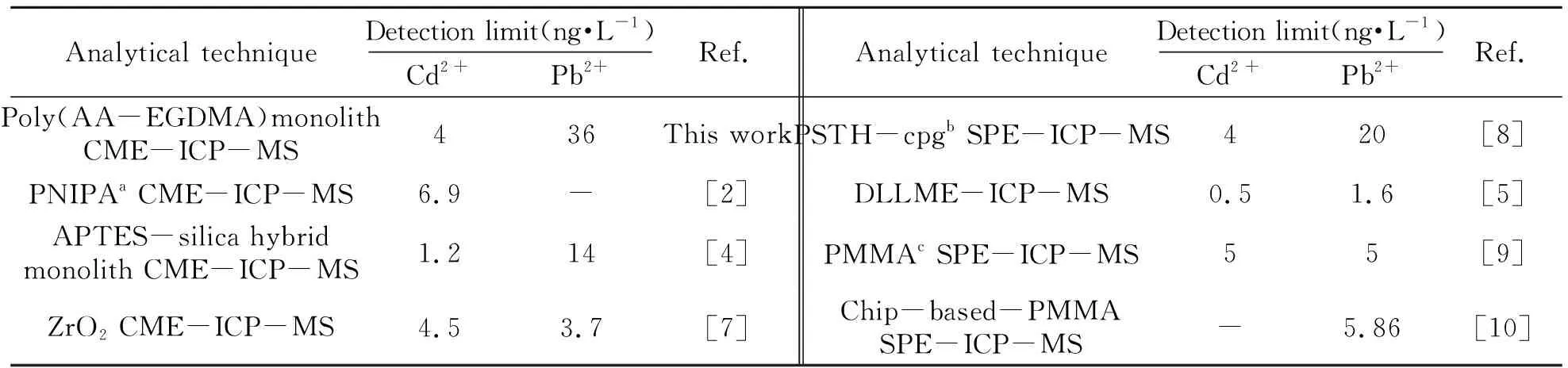
表6 Cd2+和Pb2+测定方法的性能比较Table 6 Comparison of analytical performance for the determination of Cd2+ and Pb2+
2.5 实际样品分析
在优化实验条件下,将所建立的方法用于人体尿样中痕量Cd2+和Pb2+的测定,结果列于表 7。可以看出,尿样中Cd2+和Pb2+的含量分别为0.4 μg·L-1和12.69 μg·L-1。有文献报道[3],健康人尿样中Cd2+含量在0.4~70 μg·L-1之间,Pb2+含量在12~30 μg·L-1之间,与本方法测定的结果相吻合。

表7 人体尿样中 Cd2+和Pb2+的分析结果Table 7 Analytical results of Cd2+ and Pb2+ in human urine sample(Mean±SD,n=3)
3 结论
本文采用原位聚合法制备了聚(丙烯酰胺-乙二醇二甲基丙烯酸酯)(Poly(AA-EGDMA))整体柱,表征结果说明该整体柱骨架是由纳米级微球颗粒相互连接而成,骨架之间具有相互交联的微米级大孔结构,具有传质速率快、吸附容量大且制备简单、易于再生、使用寿命长的特点。基于此,建立了整体柱CME-ICP-MS联用检测重金属离子的分析方法,并将其成功用于人体尿样中痕量Cd2+和Pb2+的测定。
