基于PB-CCD设计的固肠止泻丸HPLC-DAD指纹图谱研究△
2015-09-25刘妍如吕杨宋忠兴张岁玲唐志书刘力王兴海
刘妍如,吕杨,宋忠兴,张岁玲,唐志书,刘力*,王兴海
(1.陕西中医学院 陕西省中药资源产业化协同创新中心,陕西省中药基础与新药研究重点实验室,陕西 咸阳 712083;2.陕西中医学院制药厂,陕西 咸阳 712083)
·中药工业·
基于PB-CCD设计的固肠止泻丸HPLC-DAD指纹图谱研究△
刘妍如1,吕杨1,宋忠兴1,张岁玲1,唐志书1,刘力1*,王兴海2
(1.陕西中医学院 陕西省中药资源产业化协同创新中心,陕西省中药基础与新药研究重点实验室,陕西 咸阳 712083;2.陕西中医学院制药厂,陕西 咸阳 712083)
目的:以Plackett Burman-Central Composite Design(PB-CCD)设计为基础,通过分析固肠止泻丸的高效液相指纹图谱,完善其质量控制和评价方法。方法:基于试验优化设计(DOE,Design of Experiment)原则,采用PB-CCD方法优化液相分析中的多种因素。样品采用Agilent 5 TC-C18(2)色谱柱(250 mm×4.6 mm,5 μm),0.2%甲酸/水-乙腈溶液线性梯度洗脱,以280 nm作为检测波长,计算10批固肠止泻丸及中间体指纹图谱的相似度,评价各批样品质量。结果:建立了固肠止泻丸的高效液相色谱-二极管阵列检测器(HPLC-DAD)指纹图谱,确认了21个共有峰,其中8个为主要成分色谱峰(标定峰)。结论:基于PB-CCD设计建立的固肠止泻丸HPLC-DAD指纹图谱分析方法,标定峰分离度较好,可用于该复方制剂加工过程中的质量控制。
固肠止泻丸;试验设计;高效液相色谱法;指纹图谱
固肠止泻丸源自医圣张仲景经典名方“乌梅丸”,成方由乌梅、干姜、黄连、罂粟壳、木香、延胡索组成。具有调和肝脾,涩肠止痛,解痉,止泻的功能[1-2]。目前研究建立的固肠止泻丸HPLC定量分析方法大多只反映方剂中黄连的盐酸巴马汀、盐酸小檗碱、延胡索乙素等生物碱类成分,其他单味药材中的成分很少体现[3-6],也还没有基于试验优化设计(DOE,Design of Experiment)方法来研究固肠止泻丸指纹图谱的报道[7-8]。
本研究基于Plackett Burman-Central Composite Design(PB-CCD)设计,首先对影响指纹图谱质量的液相色谱关键因素进行优化,然后利用优化后的液相条件,建立反映固肠止泻丸中主要成分信息的高效液相色谱-二极管阵列检测器(HPLC-DAD)指纹图谱,为固肠止泻丸的质量控制提供参考。
1 仪器与材料
1.1 仪器
Agilent 1260 型高效液相仪(包括配脱气机、G1311C四元梯度泵、G1329B自动进样器、G1316A柱温箱、G1315D DAD检测器);佑科FA2704b型分析天平(上海佑科仪器仪表有限公司);KQ-300DE型数控超声波清洗器(昆山超声仪器有限公司)。
1.2 材料
乙腈为色谱纯(Honeywell公司,批号分别为DK268,DK364);甲酸为色谱纯(天津市科密欧化学试剂有限公司,批号:20140421);其余试剂均为分析纯;水为娃哈哈纯化水。
固肠止泻丸(陕西中医学院制药厂,批号分别为141201,141202,141204,141205,141206);中间体(陕西中医学院制药厂,批号分别为141201,141203,141204,141205,141206);对照品咖啡酸、盐酸罂粟碱、延胡索乙素、盐酸药根碱、盐酸巴马汀、盐酸小檗碱、6-姜辣素、异欧前胡素(中国食品药品检定研究院,批号分别为110885-200102,171214-201205,110726-201414,110733-201108,110732-201309,110713-201212,111833-201303,110827-201109)
2 方法
2.1 固肠止泻丸供试品溶液配制
根据《中华人民共和国卫生部药品标准·中药成方制剂》第二十册(WS3-B-3870-98)对固肠止泻丸样品的处理方法,取固肠止泻丸,研细,取粉末约0.5 g,精密称定,置25 mL具塞三角瓶中,加甲醇溶液20 mL,超声处理30 min,将提取液转移至蒸发皿中,待溶剂蒸干后,再用0.1%甲酸水-乙腈(90∶10)溶液边洗涤边转移至50 mL容量瓶中,直至将蒸发皿内残渣完全洗净,最后用0.1%甲酸水-乙腈(90∶10)溶液定容至刻度,摇匀,0.22 μm滤膜过滤,取续滤液,作为供试品溶液。
2.2 色谱条件
Agilent 5 TC-C18(2)色谱柱(250 mm×4.6 mm,5 μm);Agilent ZORBAX Eclipse plus C18色谱柱(100 mm×4.6 mm,3.5 μm);流动相:水(A)-乙腈溶液(B)。
2.3 影响因子设计
采用比例特定的乙腈-水混合洗脱系统,以不同比例甲酸调节流动相系统pH值。选用不同色谱柱类型、检测波长、柱温、线性梯度时间、流速、乙腈初始比例作为考察变量,以两峰分离度之和∑Rs、归一化分离因子r*(×10-10)、色谱信息量Ф和色谱分层响应效能HCRF作为响应因子,见表1[9]。
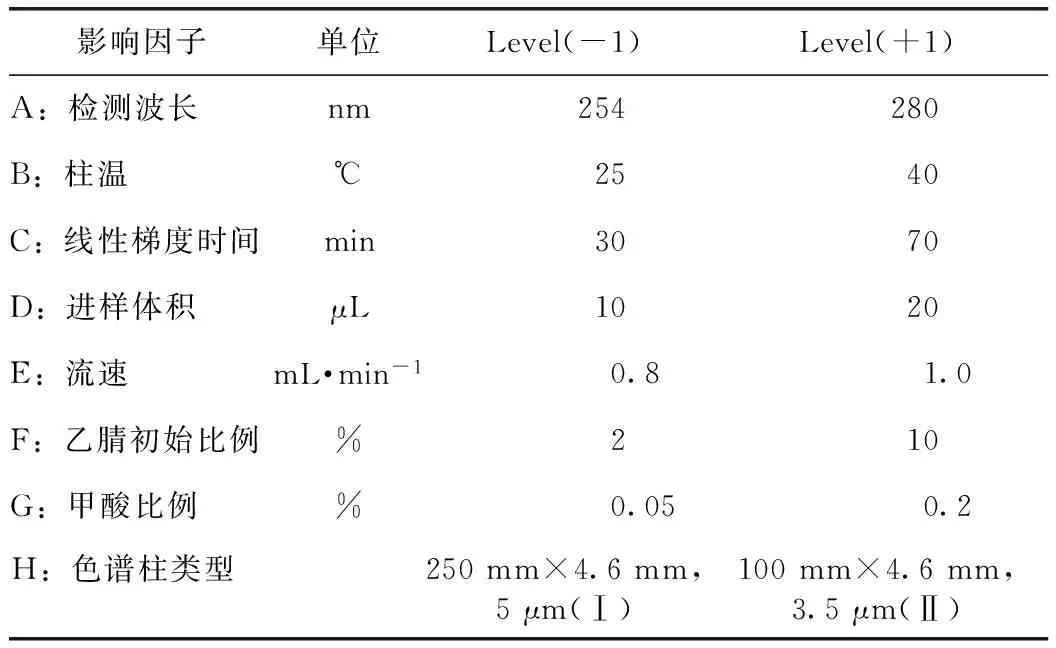
表1 影响因子及响应因子设计表(7因素2水平)
2.4 数据分析
以各因素无相互作用且对设计结果干扰少作为设计前提,采用Design-Expert Version 8.0.7统计软件,首先对检测波长、柱温、梯度时间、进样体积、流速、酸浓度、乙腈初始比例进行PB因子筛选;然后以CCD响应曲面法对重要因素进行寻优,以确定最优的参数设置,见表2。
2.5 方法学验证
按照《中华人民共和国药典》2010版一部对中药质量控制方法的规定,对优化结果进行精密度、重复性、稳定性等方法学验证。以咖啡酸、罂粟碱、延胡索乙素、盐酸巴马汀、盐酸药根碱、盐酸小檗碱、6-姜辣素和异欧前胡素为对照,鉴定指纹谱中主要成分。
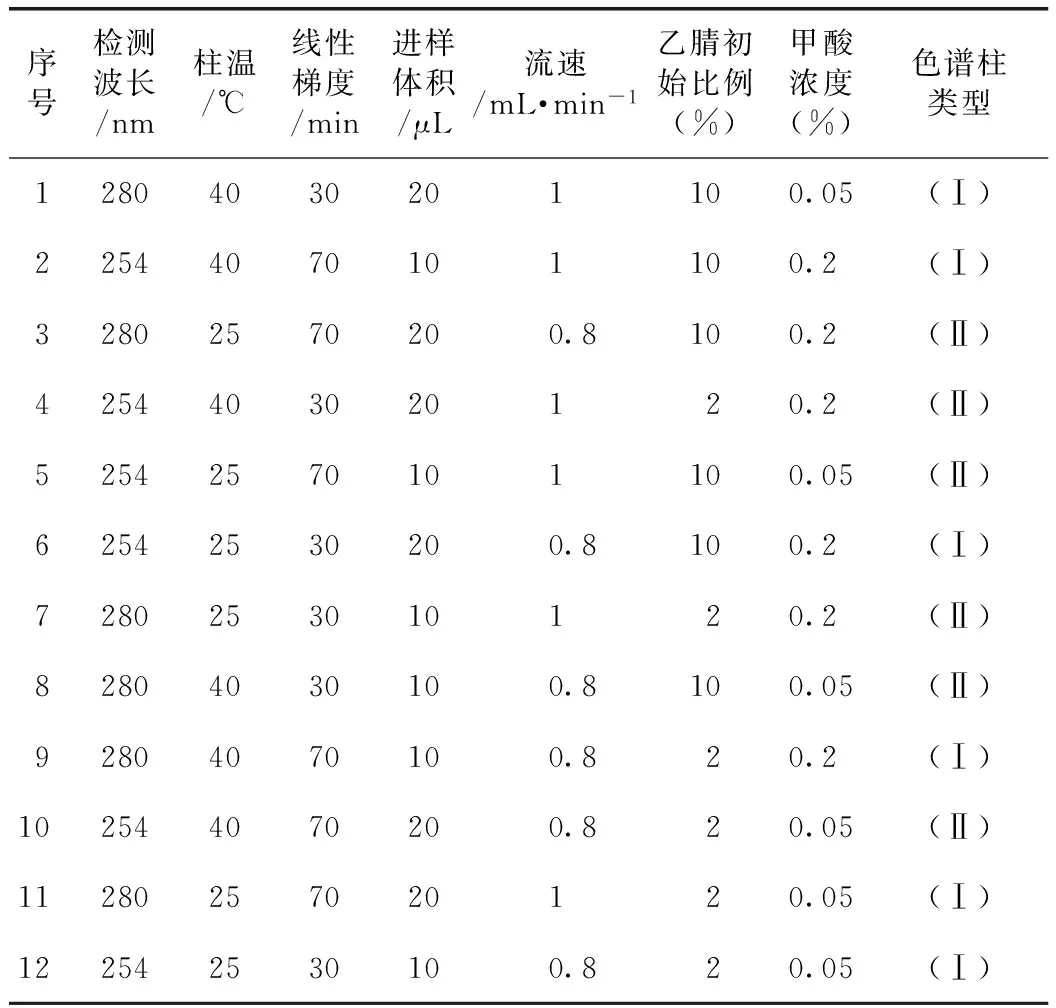
表2 PB设计试验方案(n=3)
3 结果与讨论
3.1 液相色谱优化因子选择
由于甲醇和分析物间氢键的相互作用,可能引入额外的共振结构并可能引起拖尾峰,因此选择乙腈作为有机相。另外,色谱柱温度也是影响极性化合物保留时间的重要参数,一般温度升高,扩散系数也升高,这样会导致更窄的峰和更高的分离效率。为了增加色谱柱使用寿命,将柱温优化范围设置为25~40 ℃。
3.2 PB试验设计
为了在最少的试验次数下获得最佳的参数设置,选择因子设计中的PB法作为筛选设计方法,以CCD响应曲面法对优化后的因素进行进一步优化,以∑Rs、r*(×10-10)、Ф、HCRF评价样品的分离效能,见公式1~3。结果见表3。
公式1
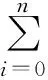
公式2
HCRF=1000000n+10000Rmin+(tm-t1)
公式3
其中,R表示两峰间分离度;n为理论塔板数;Rmin为最小分离度;tm-t1为最大与最小保留时间差;A为色谱峰面积。
∑Rs、r*(×10-10)是用于评价色谱分离质量的参数;Ф值指色谱信息量值,是用于评价色谱交互信息的参数;HCRF指分层色谱响应值,用于评价方法中分离峰个数、分离度和分析时间性能。
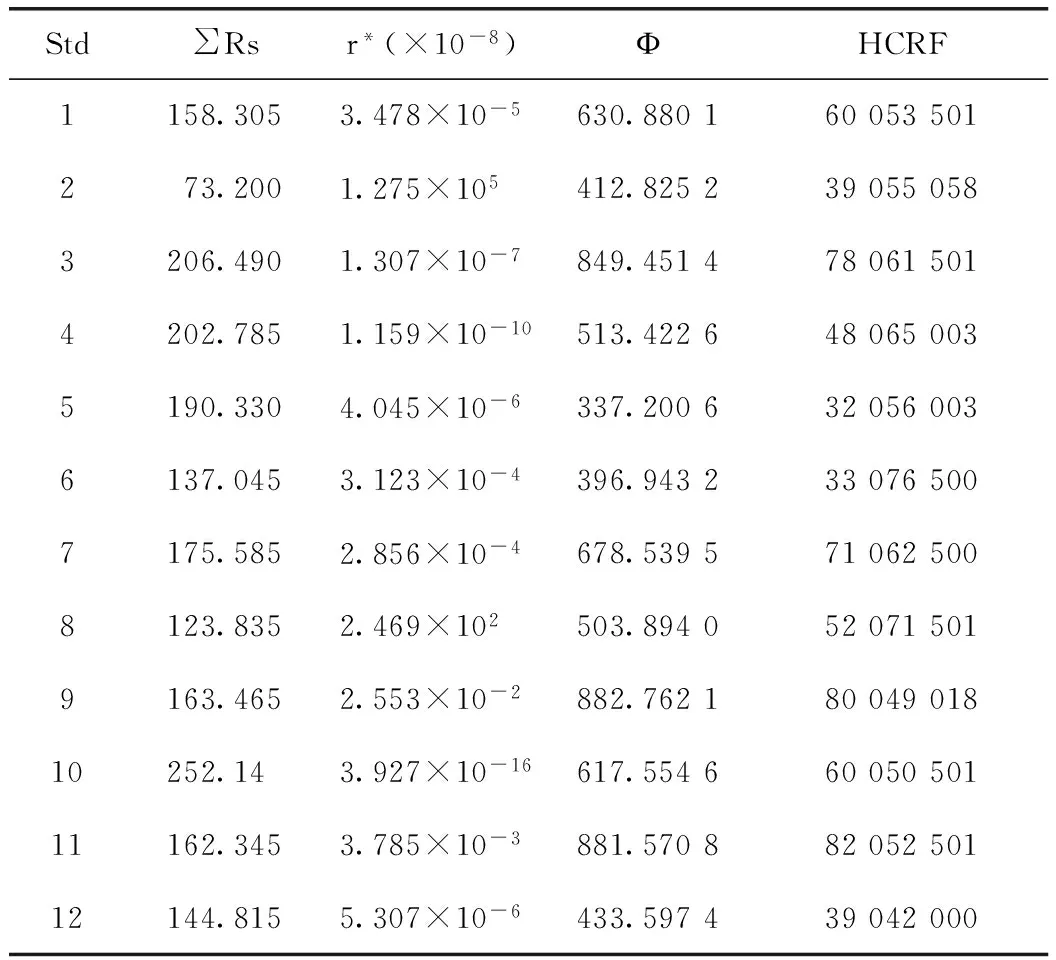
表3 PB响应因子结果
PB试验的ANOVA结果显示,Ф和HCRF项的p值分别为0.004 3和0.005 4,均小于0.01,说明各变量与HCRF回归方程的关系非常显著。拟合系数(R-Squared)分别为0.992 4和0.991 1,说明模型拟合度很好。
根据各影响因子对各响应因子的最大值运算结果,将影响不显著的影响因子进行最大值预测并作为固定条件:检测波长为280 nm;柱温为40 ℃;流速为1.0 mL·min-1;甲酸浓度为0.2%;色谱柱类型为250 mm×4.6 mm,5 μm。
3.3 CCD试验设计
在PB设计结果的基础上,对进样体积、线性梯度和乙腈初始比例因素进行寻优。试验采用通用旋转组合设计(Rotatable=6),以Ф和HCRF作为响应因子进行三水平CCD试验,结果见表4。
从Ф和HCRF项的ANOVA分析结果中可以看出,对Ф影响显著的因素为进样体积(p=0.000 3)和线性梯度时间(p=0.003 3),乙腈初始比例对Ф影响不具有统计学意义(p=0.305 9>0.05);对HCRF影响显著的因素为线性梯度时间(p=0.003 4)和进样体积(p=0.044 0),乙腈初始比例对HCRF影响不具有统计学意义(p=0.106 6>0.05)。从Ф和HCRF的主效应图可以看出,三因素交互作用显著,进样体积(A)越大,图谱Ф和HCRF越高;而线性梯度时间(B)越长,对谱图分析越不利。见图1。
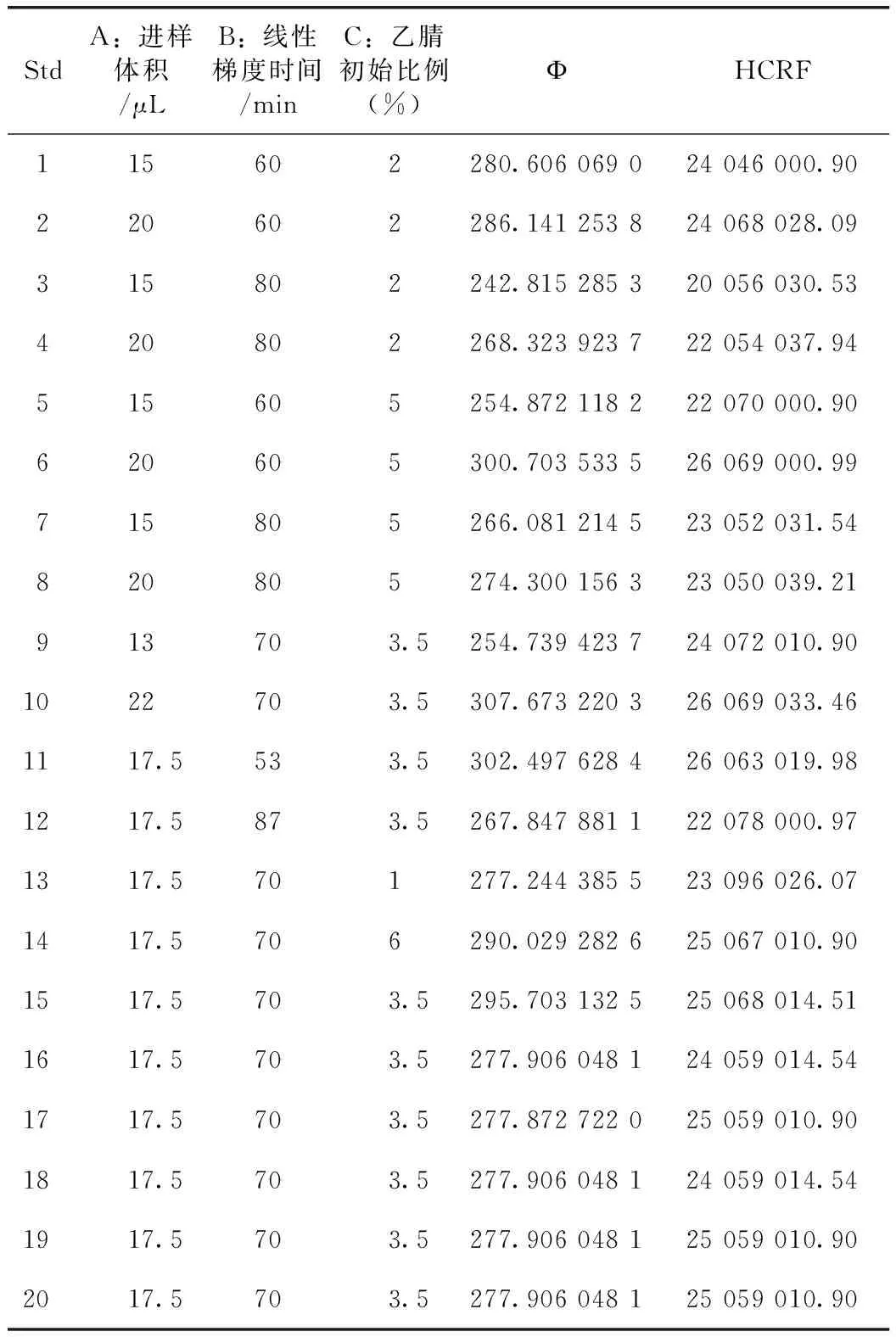
表4 Central Composite响应因子结果
根据方差分析响应曲面图所示,进样体积和线性梯度时间的交互影响是比较显著的。在进样体积不变的情况下,线性梯度时间越长,Ф和HCRF越小;而在线性梯度时间不变的情况下,随着进样体积的增加,Ф和HCRF增大。从HCRF响应曲面分析图可以看出,进样体积不变时,HCRF响应曲面曲率比Ф响应曲面曲率更大,说明线性梯度时间对HCRF(峰个数、分离度和性能)的影响更大。见图1。最后得到响应方程:
Ф=254.867+5.099×进样体积-0.945×线性梯度时间
HCRF=26 714 700+274 606×进样体积-107 952×线性梯度时间
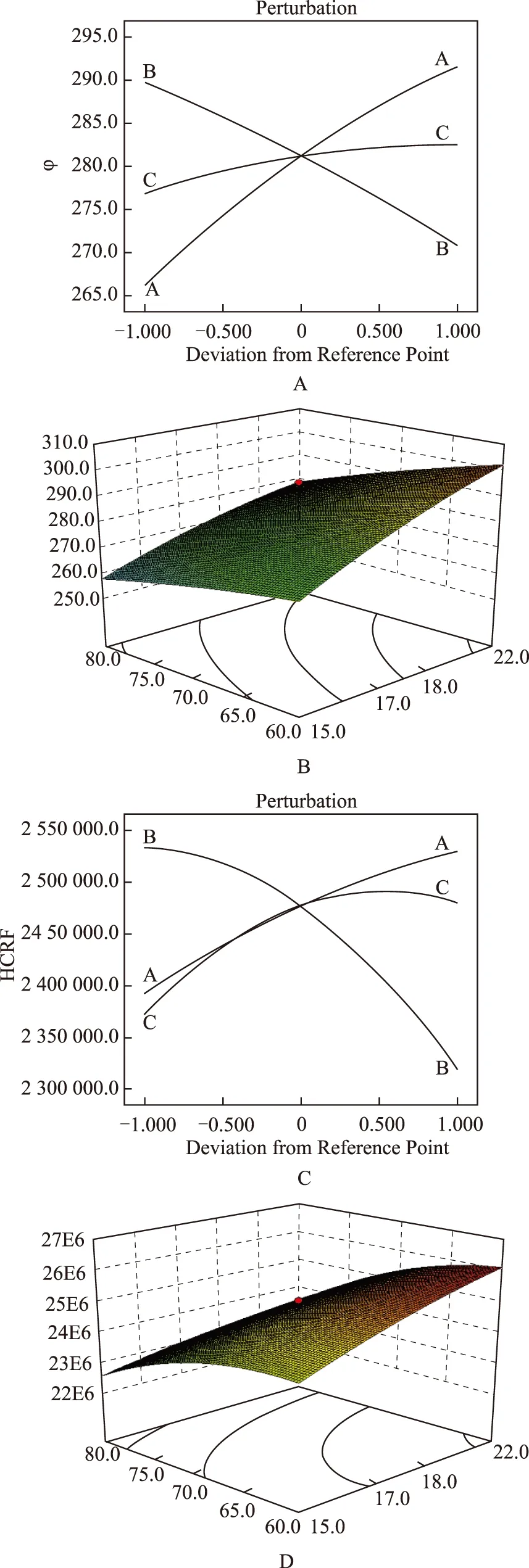
注:A.Ф分离效果影响因素主效应图;B.Ф响应曲面分析图;C.HCRF分离效果影响因素主效应图;D.HCRF响应曲面分析图图1 分离效果影响因素主效应及响应曲面分析图
根据上述筛选结果,在设计水平范围内对响应因子做最大值计算。以3次重复试验验证因子分析结果,最终得到的色谱分析条件:色谱柱为Agilent 5 TC-C18(2)色谱柱(250 mm×4.6 mm,5 μm);检测波长为280 nm;柱温为40 ℃;梯度时间为60 min;进样体积为20 μL;流速为1.0 mL·min-1;乙腈初始比例为3.5%;甲酸浓度为0.2%。
3.4 方法学验证
3.4.1 精密度试验 取同一批供试品溶液,连续进样6次,记录色谱图。对21个共有峰以均值法进行差异性评价,结果表明各共有峰保留时间RSD 为0.02%~0.24%,主要成分共有峰面积RSD 为0.72%~1.01%,符合指纹图谱的要求。
3.4.2 稳定性试验 取同一批供试品溶液,分别于制备后0、3、6、9、12、15、18、21、24 h进样,记录色谱图。共有峰以均值法进行评价,结果表明各共有峰保留时间RSD为0.02%~0.34%,主要成分共有峰面积RSD为 0.36%~1.52%,证明供试液在24 h内稳定。
3.4.3 重复性试验 取同一供试品5份,分别制备供试品溶液,进样,记录色谱图。结果表明,共有峰保留时间RSD为0.02%~0.33%,峰面积RSD为0.38%~2.91%,表明该方法重复性较好。
3.5 固肠止泻丸特征峰鉴定及不同批次制剂相似度评价
取10批固肠止泻丸及中间体,按2.1项下方法分别制备供试品溶液,进样,记录色谱图。通过与对照品混标图谱比较,确定8个特征峰,分别为咖啡酸、罂粟碱、延胡索乙素、盐酸巴马汀、盐酸药根碱、盐酸小檗碱、6-姜辣素和异欧前胡素,见图2。
将10批固肠止泻丸及中间体的色谱数据导入《中药色谱指纹图谱相似度评价系统》2004年A版,进行相似度评价。结果表明,除1个批次外,其他批次制剂及中间体的指纹图谱相似度均>0.98。10批制剂及中间体的HPLC指纹图谱相似度结果见表5。
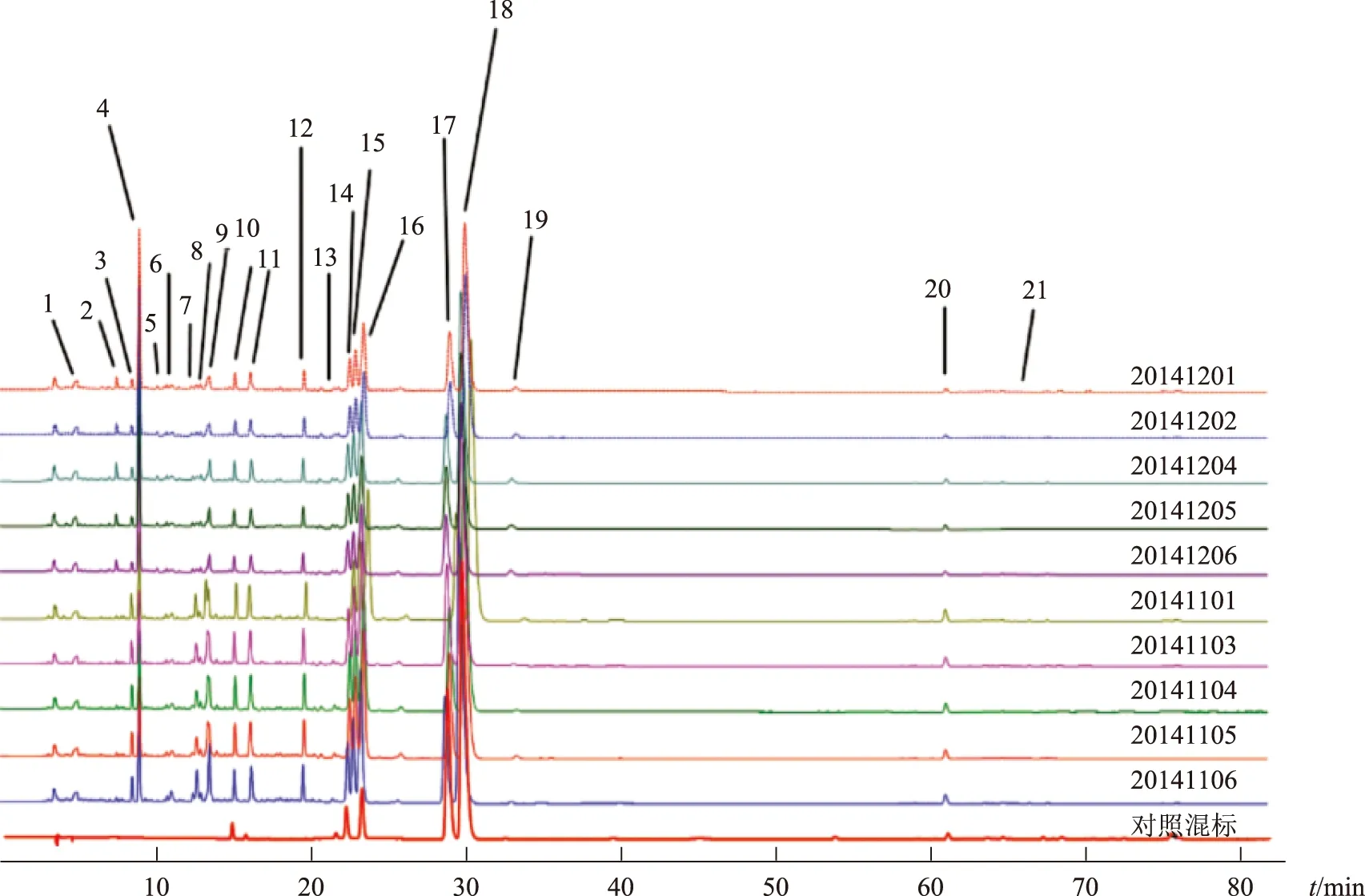
注:1.4.934 min;2.7.505 min;3.8.498 min;4.8.969 min;5.10.762 min;6.12.425 min;7.12.688 min;8.12.943 min;9.13.509 min;10.15.136 min,咖啡酸;11.16.150 min;12.19.559 min;13.21.751 min,盐酸罂粟碱;14.22.422 min,延胡索乙素;15.22.826 min;16.23.33 min,盐酸药根碱;17.28.858 min,盐酸巴马汀;18.29.768 min,盐酸小檗碱;19.33.207 min;20.61.028 min,6-姜辣素;21.64.607 min,异欧前胡素。图2 固肠止泻丸及中间体对照指纹图谱
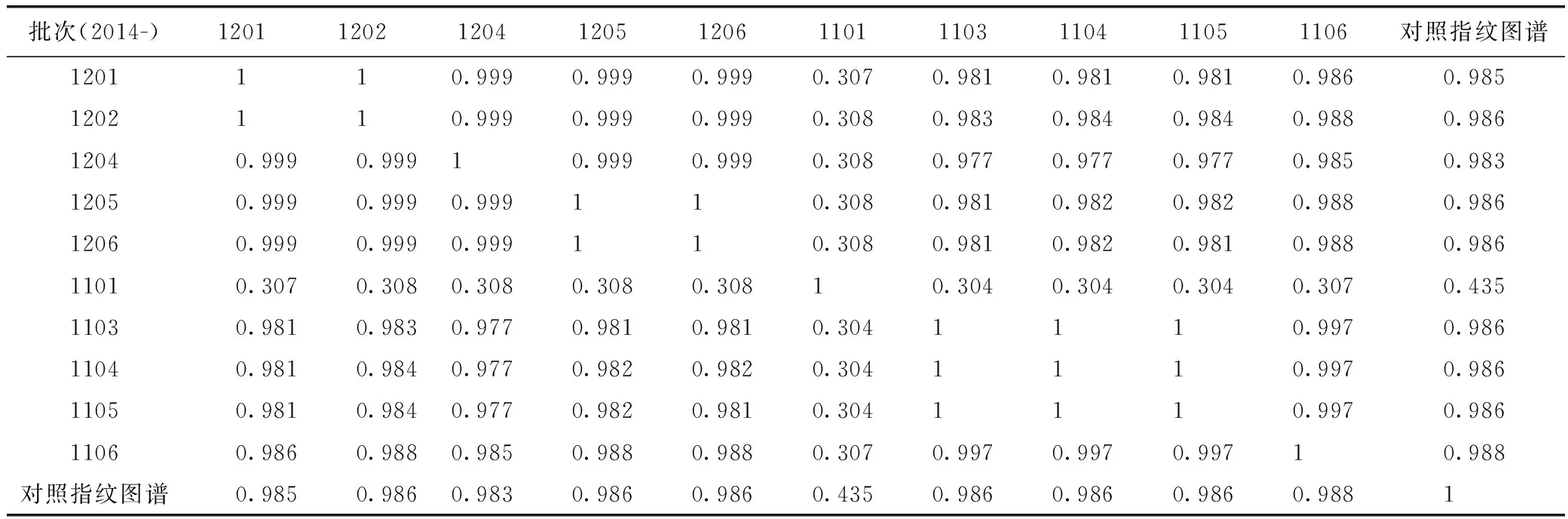
批次(2014-)1201120212041205120611011103110411051106对照指纹图谱1201110.9990.9990.9990.3070.9810.9810.9810.9860.9851202110.9990.9990.9990.3080.9830.9840.9840.9880.98612040.9990.99910.9990.9990.3080.9770.9770.9770.9850.98312050.9990.9990.999110.3080.9810.9820.9820.9880.98612060.9990.9990.999110.3080.9810.9820.9810.9880.98611010.3070.3080.3080.3080.30810.3040.3040.3040.3070.43511030.9810.9830.9770.9810.9810.3041110.9970.98611040.9810.9840.9770.9820.9820.3041110.9970.98611050.9810.9840.9770.9820.9810.3041110.9970.98611060.9860.9880.9850.9880.9880.3070.9970.9970.99710.988对照指纹图谱0.9850.9860.9830.9860.9860.4350.9860.9860.9860.9881
4 结论
近几十年来,现代中药复方制剂被广泛用于疾病的预防与治疗,但药材中的活性成分非常复杂,使其应用受到限制[10-13]。目前已有应用高效液相色谱、质谱、核磁共振等分析技术对中药活性成分进行的大量研究,但是这些研究还不足以全面反映中药多成分的特点[14-15]。由于中药的治疗作用是基于多种成分互相作用而产生的,因此,其指纹色谱被认为是中药质量控制最有利的方法,而这种技术也成功地应用于中药制剂的质量控制中。相比于超高效液相色谱,高效液相色谱虽然分离效率较低,但对于成分复杂的中药体系而言,分离可操作性更加理想,更适于大范围的中药指纹图谱的检测。
本研究设计了“三步”开发固肠止泻丸HPLC指纹图谱的方法,通过优化液相分析中的影响因素,确定可控参数,得到有效的线性梯度洗脱法,最后进行方法验证以及指纹图谱共有峰的比对。本研究为固肠止泻丸的鉴定及质量控制提供新的手段,为中药色谱指纹图谱的分析提供新的思路。
[1] 吴华君,陈哉考.固肠止泻丸联合维柳芬对溃疡性结肠炎患者血清IL-2、IL-8的影响及疗效观察[J].辽宁中医杂志,2014,41(03):462-464.
[2] 袁文泽.固肠止泻丸治疗腹泻型肠道易激综合症临床研究[J].中医临床研究,2013,5(17):62-63.
[3] 王卫锋,卫伟光.HPLC测定固肠止泻丸中吗啡及盐酸小檗碱的含量[J].中成药,2010,32(06):967-970.
[4] 吴凡.HPLC法测定固肠止泻胶囊中盐酸吗啡的含量[J].西北药学杂志,2009,24(06):462-463.
[5] 朱静毅,李倚云.RP-HPLC法同时测定固肠止泻丸中盐酸小檗碱和盐酸巴马汀的含量[J].中国医药导报,2007,4(35):118-119.
[6] 陈金文,曹林林,田玉先.HPLC法测定固肠止泻丸中盐酸小檗碱的含量[J].现代中医药,2003(05):79-80.
[7] 史亚军,陈金文.新固肠止泻丸质量标准研究[J].辽宁中医药大学学报,2009,11(07):169-170.
[8] 陈金文,王娟.固肠止泻丸质量标准的研究[J].陕西中医,2008,29(08):1070-1071.
[9] Gooding O W.Process optimization using combinatorial design principles:parallel synthesis and design of experiment methods[J].Curr Opin Chem Biol,2004,8(3):297-304.
[10] Tian T,Chen H,Zhao Y Y.Traditional uses,phytochemistry,pharmacology,toxicology and quality control of Alisma orientale(Sam.)Juzep:A review[J].J Ethnopharmacol,2014,158(PartA):373-387.
[11] Yang D,Li Y,Yang F,et al.High-performance liquid chromatographic column packings with different particle sizes:Chromatographic behavior for the quality analysis of HuanglianShangqing pill[J].J Se PSci,2014,38(3):381-389.
[12] Yang D Z,Yin X X,Ong C N,et al.Multidimensional information-based HPLC technologies to evaluate traditional chinese medicine[J].J Chromatogr Sci,2013,51(7):716-725.
[13] Che C T,Wang Z J,Chow M S,et al.Herb-herb combination for therapeutic enhancement and advancement:theory,practice and future perspectives[J].Molecules,2013,18(5):5125-5141.
[14] 孙国祥,邹跃,刘中博.中药指纹图谱数据库发展历程和建设中药定量云计算标准指纹规范数据库构想[J].中南药学,2014,12(04):289-294.
[15] 孙国祥,侯志飞,李文颖.中药多元多维指纹图谱特征与构成方式及评价方法研究[J].中南药学,2014,12(06):497-504.
ApplicationofPlackett-Burman-CentralCompositeDesignforFingerprintAnalysisofGu-Chang-Zhi-XiepillbyHPLC-DADapproach
LIUYanru1,LYUYang1,SONGZhongxing1,ZHANGSuiling1,TANGZhishu1,LIULi1*,WANGXinghai2
(1.ShaanxiUniversityofChineseMedicine/ShaanxiCollaborativeInnovationCenterofChineseMedicinalResourcesIndustrialization,ShaanxiprovincekeylaboratoryofnewdrugsandChinesemedicinefoundationresearch,Xianyang712083,Shaanxi,China;2.ShaanxiChineseTraditionalMedicineAcademyPharmaceuticalFactory,Xianyang712083,Shaanxi,China;)
Objective:To identify and evaluate quality of Gu-Chang-Zhi-Xie pill (GCZX),APlackett-Burman-Central Composite Design with response surface analysis method was implemented to optimize and validate the chromatographic system of GCZX fingerprint.Methods:Firstly,the controllable factors were selected,design of experiments (DOEs) were performed for further optimization.Then,injection precision,repeatability,and sample stability test were performed.Results:A feasible and reliable HPLC-DAD system was established by using a acetonitrile-0.2% formic acid linear gradient elution with a column temperature of 30 ℃ and a detection wavelength of 280 nm.21 common peaks were found and 8 characteristic peaks were identified referred to reference substances.Conclusion:The strategy of optimization method can be applied for the development of fingerprints in the quality control of Gu-Chang-Zhi-Xie pill.
Gu-Chang-Zhi-Xie pill;design of experiment;HPLC-DAD;fingerprint
10.13313/j.issn.1673-4890.2015.6.017
2015-02-10)
陕西省科技统筹创新工程计划项目(2011KTCG03-02)
*
刘力,硕士生导师,研究方向:溃疡性结肠炎的发病机制与中医药治疗研究、脾胃病诊疗技术的标准化与临床疗效评价方法研究;Tel:(029)38185009,Email:liuyan791@163.com
