心脏手术后低血容量患者早期目标导向液体治疗策略
2015-09-15韩宏光王辉山李晓密徐莉莹孟庆涛张晓慧张春振都业君
韩宏光 王辉山 李晓密 徐莉莹 孟庆涛 张晓慧 张春振 都业君
心脏手术后低血容量患者早期目标导向液体治疗策略
韩宏光 王辉山 李晓密 徐莉莹 孟庆涛 张晓慧 张春振 都业君
目的 探讨心脏手术后低血容量患者早期目标导向液体治疗(EGDT)的策略。方法 选取2013年6月至2014年6月在沈阳军区总医院心血管外科术后低血容量患者538例,随机分为治疗组和对照组,每组各269例。在综合治疗的基础上,对照组根据传统方法进行液体治疗,治疗组根据EGDT方案进行液体治疗,观察两组第8、24、48小时液体输入量、中心静脉压(CVP)、平均动脉压(MAP)、HR、中心静脉血氧饱和度(ScvO2)、血乳酸水平(Lac)、机械通气时间、ICU停留时间、血管活性药物使用时间、并发症发生率和病死率等情况。结果 两组患者术前基本情况未见统计学差异(P>0.05)。治疗组第8、24小时晶体、胶体用量,液体总量均显著多于对照组,CVP、ScvO2明显高于对照组(P<0.05);两组第 8、24、48 h MAP无明显差异(P>0.05);治疗组心率在同一时间均低于对照组,但未见统计学差异(P>0.05);治疗组术后第8、24小时Lac低于对照组,差异具有统计学意义(P<0.05),第48 h无明显差异(P>0.05),机械通气时间、ICU停留时间、血管活性药物使用时间、并发症发生率及死亡率均小于对照组,除多器官功能障碍综合征外,差异具有统计学意义(P<0.05)。结论 早期目标导向性液体治疗能动态反映心脏手术后低血容量患者的血流动力学状态,实时监测容量指标,个体化调整治疗方案,指导液体管理,对提高临床疗效、降低心脏手术并发症发生率和死亡率均具有重要的临床意义,值得推广应用。
早期目标导向治疗; 血流动力学; 低血容量; 心脏手术
早在1988年Shoemaker等学者就提出了通过液体复苏或血管活性药物维持正常或稍高的心排出量,优先将维持危重患者的循环和呼吸稳定作为治疗的主要目标。2001年Rivers等[1]根据其进行的一项涉及263例患者的随机对照试验结果提出了早期目标导向治疗(early goal-directed therapy,EGDT)的概念,证明EGDT对于脓毒症患者的液体复苏及预后具有重要意义。由于术前心脏功能障碍、手术创伤等诸多因素,传统方法常常采用以最小容量维持循环的原则,尽管可避免术后容量负荷过重,但却容易导致潜在的低血容量,影响循环稳定及组织愈合,增加各类并发症的罹患率,特别是肾前性的肾功能不全严重影响患者预后。同样,过重的容量负荷不但增加心衰的发生率,也增加急性肺水肿、低氧血症等并发症的发生率。
研究显示,心脏术后早期(<8 h)合理的液体复苏方案对改善患者循环状态、防治不良病生发展过程、减少术后并发症具有重要意义[2-4]。因此,如何优化心脏手术围术期液体治疗方案是围术期处理的一个重点研究方向。EGDT作为一种以达到一定的血流动力学指标为目标,以增加心排血量及组织氧供为目的个体化液体治疗方案,能够有效改善患者的微循环,减少心衰、肺水肿等并发症风险[5]。为此,我科对心脏手术后低血容量患者实施EGDT,取得了良好效果,现报道如下。
1 对象与方法
1.1 研究对象 选择2013年6月至2014年6月于沈阳军区总医院心血管外科术后低血容量患者538例作为研究对象,其中男性276例、女性262例,年龄 18~75(54.6±21.3)岁。病种类型:冠状动脉旁路移植术278例,瓣膜置换术212例(包括二尖瓣置换术79例、主动脉瓣置换术74例、二尖瓣+主动脉瓣置换术59例),先天性心脏病48例。入选标准:①年龄>18岁;②收缩压(SP)<90 mm Hg或较基础血压下降>40 mm Hg(1 mm Hg=0.133 kPa);③中心静脉压(CVP)<5 cm H2O(1 cm H2O=0.098 kPa);④心率>100 次/min,尿量<0.5 ml·kg-1·h-1;⑤既往无肝脏及肾脏疾病。所有患者均签署知情同意书。排除标准:①左心室舒张末期内径(LVEDD)>80 mm,心胸比>0.75,左心室射血分数(LVEF)<0.4;②重要脏器功能严重受损;③精神或法律上的残疾患者;④需大剂量血管活性药维持循环患者。
1.2 分组方法及观察指标 按照随机原则将入选患者分为治疗组和对照组各269例。在综合治疗的基础上,治疗组根据EGDT方案进行液体治疗;对照组根据传统方法进行液体治疗。记录两组年龄、性别、体重、病种,术前 LVEDD、LVEF、心胸比、肝肾功能等基本情况;分别记录两组患者术后第8、24、48小时平均动脉压(MAP)、中心静脉压(CVP)、中心静脉血氧饱和度(ScvO2)、血乳酸水平(Lac);记录两组患者机械通气时间、ICU停留时间、血管活性药物使用时间、液体用量、并发症及病死率等。
1.3 治疗方法
1.3.1 EGDT治疗组 治疗目标:①机械通气者:CVP维持在12~15 cm H2O,已脱机患者CVP维持在 8~12 cm H2O;②MAP>65 mm Hg;③ScvO2≥70%;④心率80~100次/min;⑤每小时尿量>0.5 ml/kg;⑥血乳酸清除率≥10%。优先达到次序为上述排列次序。EGDT实施方案:以30 min输注250 ml液体的速度进行液体复苏,术前LVEF<0.5者适当降低输液速度,按晶胶比例为1∶0.6~1.0选择输注液体,晶体液选用乳酸林格氏液,胶体液选130/0.4羟乙基淀粉氯化钠,也可根据ScvO2(<70%时)适当输注红细胞以维持HCT 30%以上。动态观察CVP上升程度,至CVP达到目标要求或上升幅度≥5 cm H2O;再根据目标血压适当调整血管活性药物,使MAP维持在65~90 mm Hg;应用β受体阻滞剂或起搏等控制心率在80~100次/min。若此时的ScvO2仍然<70%,则静脉泵入多巴酚丁胺,从2.5 μg·kg-1·min-1开始,每30 min增加2.5 μg·kg-1·min-1,至 20 μg·kg-1·min-1止,以达到前述目标值。
1.3.2 对照组 采用常规方法对患者进行循环与容量支持。根据患者前一天出量或术中失血、失液量及每日液体需要量进行容量治疗,计算所需总量,每小时匀速输注,晶胶比例仍为1∶0.6~1.0选择输注液体,晶体液选用乳酸林格氏液,胶体液选130/0.4羟乙基淀粉氯化钠。如血流动力学不稳定,适当加用多巴胺、肾上腺素等血管活性药物,使患者血液动力学指标基本正常,即血压至90/60 mm Hg以上,脉压差≥30 mm Hg,尿量达到 0.5 ml·kg-·1h-1。
1.4 统计学方法 采用SPSS 19.0统计学软件进行统计分析。计量资料以±s表示,组间比较采用成组t检验;计数资料用例数或百分比表示,组间比较采用 χ2检验。P<0.05为差异具有统计学意义。
2 结果
2.1 两组患者一般资料比较 两组患者年龄,性别,体重,病种,术前 LVEDD、LVEF,心胸比值,肝肾功能等基本情况比较未见统计学差异(P>0.05),见表1。
2.2 液体用量分析 治疗组第8、24小时晶体、胶体用量、液体总量均显著多于对照组(P<0.05);第48小时患者入量趋于稳定,治疗组略高于对照组,但未见统计学差异(P>0.05)。见表2。
2.3 复苏效率与效果比较
2.3.1 两组观察指标比较 治疗组术后第8、24小时CVP、ScvO2明显高于对照组,差异具有统计学意义(P<0.05),第 48 小时未见统计学差异(P>0.05)。两组第 8、24、48小时 MAP无明显差异(P>0.05),但观察得知对照组患者血压波动性明显大于治疗组。两组心率随液体治疗均呈下降趋势,治疗组心率在同一时间均低于对照组,但未见统计学差异(P>0.05)。治疗组术后第8、24小时 Lac低于对照组,差异具有统计学意义(P<0.05),第48小时未见统计学差异(P>0.05)。见表 3。
表2 两组患者第8、24、48小时液体用量比较(±s)
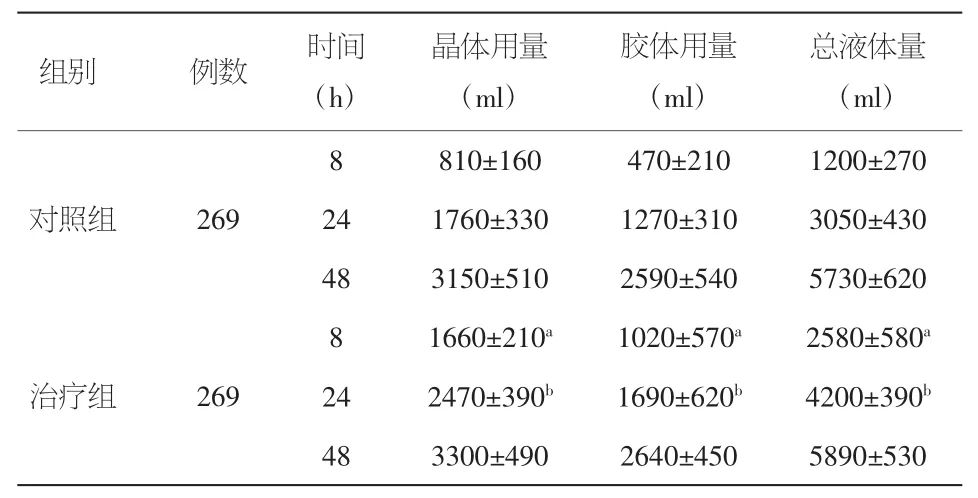
表2 两组患者第8、24、48小时液体用量比较(±s)
注:与对照组8 h比较,aP<0.05;与对照组24 h比较,bP<0.05
组别 例数 时间(h)晶体用量(m l)胶体用量(m l)总液体量(m l)对照组 2 6 9 8 8 1 0±1 6 0 4 7 0±2 1 0 1 2 0 0±2 7 0 2 4 1 7 6 0±3 3 0 1 2 7 0±3 1 0 3 0 5 0±4 3 0 4 8 3 1 5 0±5 1 0 2 5 9 0±5 4 0 5 7 3 0±6 2 0治疗组 2 6 9 8 1 6 6 0±2 1 0a 1 0 2 0±5 7 0a 2 5 8 0±5 8 0a2 4 2 4 7 0±3 9 0b 1 6 9 0±6 2 0b 4 2 0 0±3 9 0b4 8 3 3 0 0±4 9 0 2 6 4 0±4 5 0 5 8 9 0±5 3 0
2.3.2 两组患者机械通气时间、ICU停留时间、血管活性药物使用时间比较 治疗组患者机械通气时间、ICU停留时间和血管活性药物使用时间均少于对照组,差异具有统计学意义(P<0.05),见表4。
表4 两组患者机械通气时间、ICU停留时间、血管活性药物使用时间比较(±s)
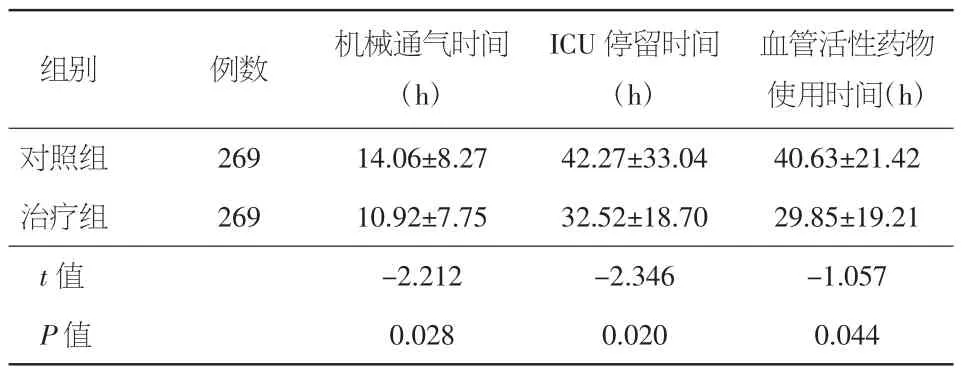
表4 两组患者机械通气时间、ICU停留时间、血管活性药物使用时间比较(±s)
血管活性药物使用时间(h)对照组 2 6 9 1 4.0 6±8.2 7 4 2.2 7±3 3.0 4 4 0.6 3±2 1.4 2治疗组 2 6 9 1 0.9 2±7.7 5 3 2.5 2±1 8.7 0 2 9.8 5±1 9.2 1 t值 -2.2 1 2 -2.3 4 6 -1.0 5 7 P值 0.0 2 8 0.0 2 0 0.0 4 4组别 例数 机械通气时间(h)I C U停留时间(h)
2.3.3 两组患者术后并发症及病死率比较 呼吸机相关性肺炎治疗组4例(1.49%),对照组12例(4.46%);低心排量综合征治疗组8例(2.97%),对照组26例(9.67%);急性肾功能衰竭治疗组0例(0%),对照组6例(2.23%);多器官功能障碍综合征治疗组1例(0.37%),对照组3例(1.12%)。两组患者除多器官功能障碍综合征外,各并发症发生率比较差异有统计学意义(P<0.01)。共死亡11例(1.86%),其中治疗组2例(0.74%),对照组 9例(3.35%),差异具有统计学意义(P<0.05)。见表5。
表1 两组患者基本情况比较(±s)
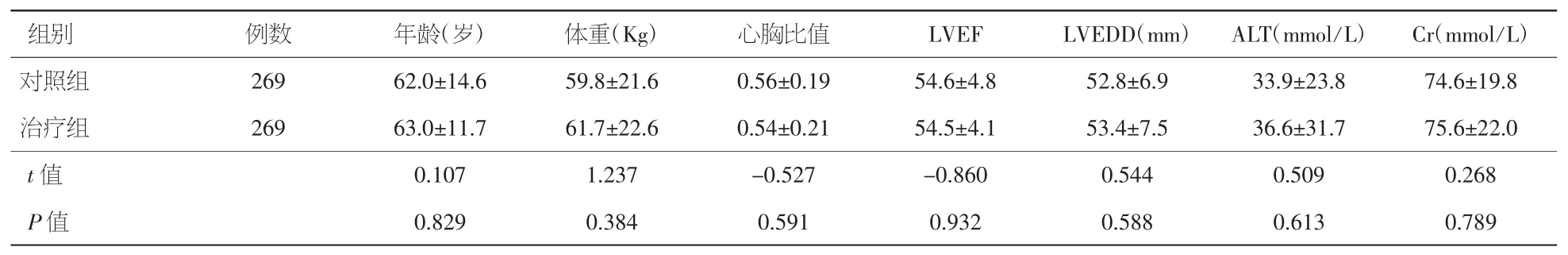
表1 两组患者基本情况比较(±s)
注:LVEF:左室射血分数;LVEDD:左心室舒张末期内径;ALT:丙氨酸转氨酶;Cr:肌酐
组别例数年龄(岁)体重(K g)心胸比值L V E F L V E D D(m m)A L T(m m o l/L)C r(m m o l/L)对照组 2 6 9 6 2.0±1 4.6 5 9.8±2 1.6 0.5 6±0.1 9 5 4.6±4.8 5 2.8±6.9 3 3.9±2 3.8 7 4.6±1 9.8治疗组 2 6 9 6 3.0±1 1.7 6 1.7±2 2.6 0.5 4±0.2 1 5 4.5±4.1 5 3.4±7.5 3 6.6±3 1.7 7 5.6±2 2.0 t值 0.1 0 7 1.2 3 7 -0.5 2 7 -0.8 6 0 0.5 4 4 0.5 0 9 0.2 6 8 P值0.8 2 9 0.3 8 4 0.5 9 1 0.9 3 2 0.5 8 8 0.6 1 3 0.7 8 9
表 3 两组患者第 8、24、48 小时 CVP、MAP、HR、ScvO2、Lac比较(±s)
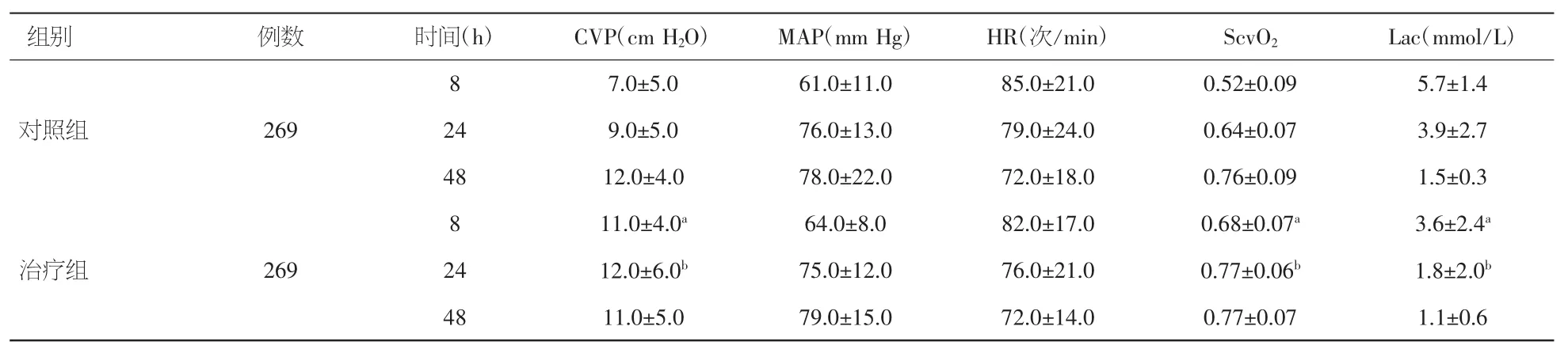
表 3 两组患者第 8、24、48 小时 CVP、MAP、HR、ScvO2、Lac比较(±s)
注:CVP:中心静脉压;MAP:平均动脉压;HR:心率;ScvO2:中心静脉血氧饱和度;Lac:血乳酸水平。与对照组8 h比较,aP<0.05;与对照组24 h比较,bP<0.05
组别 例数 时间(h) C V P(c m H2O) M A P(m m H g) H R(次/m i n) S c v O2 L a c(m m o l/L)对照组 2 6 9 7.0±5.0 6 1.0±1 1.0 8 5.0±2 1.0 0.5 2±0.0 9 5.7±1.4 2 4 9.0±5.0 7 6.0±1 3.0 7 9.0±2 4.0 0.6 4±0.0 7 3.9±2.7 4 8 1 2.0±4.0 7 8.0±2 2.0 7 2.0±1 8.0 0.7 6±0.0 9 1.5±0.3 8 8治疗组 2 6 9 1 1.0±4.0a 6 4.0±8.0 8 2.0±1 7.0 0.6 8±0.0 7a 3.6±2.4a2 4 1 2.0±6.0b 7 5.0±1 2.0 7 6.0±2 1.0 0.7 7±0.0 6b 1.8±2.0b4 8 1 1.0±5.0 7 9.0±1 5.0 7 2.0±1 4.0 0.7 7±0.0 7 1.1±0.6
3 讨论
随着近十年来对目标导向性液体治疗的诠释及临床推广应用,个体化的液体复苏治疗得到了越来越多临床医师的认可。与依赖于医师临床经验的传统液体输注方法相比较,EGDT既可有效防止围术期容量不足,又可防止容量超负荷,其通过容量复苏达到每搏量的最大化,以达到个体循环功能的最优状态[6]。EGDT快速的容量补充,迅速达到液体复苏的目标值,恢复循环血容量,以增加心排出量和氧输送,缩短各组织器官灌注不足时间,阻断缺氧过程,逆转器官功能衰竭的出现或进行性加重,改善循环,以期降低病死率[7]。
心血管外科患者术前均存在不同程度的心功能障碍,再加上全麻、手术创伤、体外循环等因素,其围术期的组织灌注常处于边缘状态,过高或不足的容量负荷均会对心、肺功能产生影响,造成第三间隙液体潴留或微循环灌注不足,增加并发症罹患率,影响其预后。因此,如何维持组织灌注及围术期液体负荷的平衡,在心脏外科围术期液体管理上尤为重要。传统方法主要根据患者的体重计算其生理需要量,在此基础上,参考24 h出入量进行液体管理,常常造成容量的不平衡。多者,容量负荷过重,增加充血性心力衰竭及肺水肿罹患率;少者,循环血量不足,组织灌注障碍,急性肾衰发生率较高。国内外多项研究均证实,输液量与术后并发症的发生率呈正相关,并且在一定程度上影响预后[8-10]。手术早期合理的液体复苏策略能够明显减低围术期并发症的发生率[11]。早期目标导向性液体治疗通过实时监测各项容量指标,量化液体治疗方案,动态反映复苏效果,将围术期的液体量维持在满足循环的最低血容量状态,保证最佳的复苏效果,对心脏术后患者的容量控制策略起到极为重要的作用。
相关研究显示,液体复苏时机的选择较复苏方法更为重要[12]。1 h内将MAP提升至65~75 mm Hg,能够更有效地改善感染性休克患者的血流动力学状态[13],达到更好的复苏效果;而术后6 h内成功达到复苏目标对疾病的发生发展具有良好的防治作用[11,13]。本组患者通过有效的血流动力学指标监测,对CVP、MAP、ScvO2、尿量等变化实施动态调整,对心脏术后低血容量患者进行EGDT治疗,并严格按照目标要求对补液的种类及用量进行调控,精确应用血管活性药物,力争在术后8 h内达到目标要求。此策略体现了液体复苏的个体化治疗思维,更为准确合理地实现容量控制,为心脏手术后容量管理提供了有效的实施方案。结果显示,治疗组术后第8、24小时CVP、ScvO2明显高于对照组,Lac低于对照组,差异具有统计学意义(P<0.05)。然而尽管两组患者第8、24、48小时MAP无明显差异,但对照组患者血压波动性明显大于治疗组。两组患者心率均随液体治疗呈下降趋势,治疗组在同一时间比较中均低于对照组。与传统治疗策略相比,治疗组更早达到治疗要求,在氧供及组织代谢方面取得了较好的复苏效果,与近年的研究结果一致[14-16]。而其在机械通气时间、ICU停留时间、血管活性药物使用时间上均小于对照组(P<0.05),标志着治疗组患者能够更早地脱离呼吸机辅助,减少胸腔正压通气对循环的影响及气管插管刺激,增加治疗舒适度,减少ICU停留时间,减轻患者经济负担。本研究中治疗组患者呼吸机相关性肺炎4例(1.49%),对照组12例(4.46%);低心排量综合征治疗组 8例(2.97%),对照组 26例(9.67%);急性肾功能衰竭治疗组 0例(0%),对照组 6例(2.23%);多器官功能障碍综合征治疗组1例(0.37%),对照组3例(1.12%)。两组患者除多器官功能障碍综合征外,各并发症发生率差异具有统计学意义(P<0.01)。共死亡 11例(1.86%),其中治疗组2例(0.74%),对照组9例(3.35%),差异具有统计学意义(P<0.05)。证明早期目标导向治疗不但能够改善液体复苏效果,也可有效降低术后并发症的发生率。
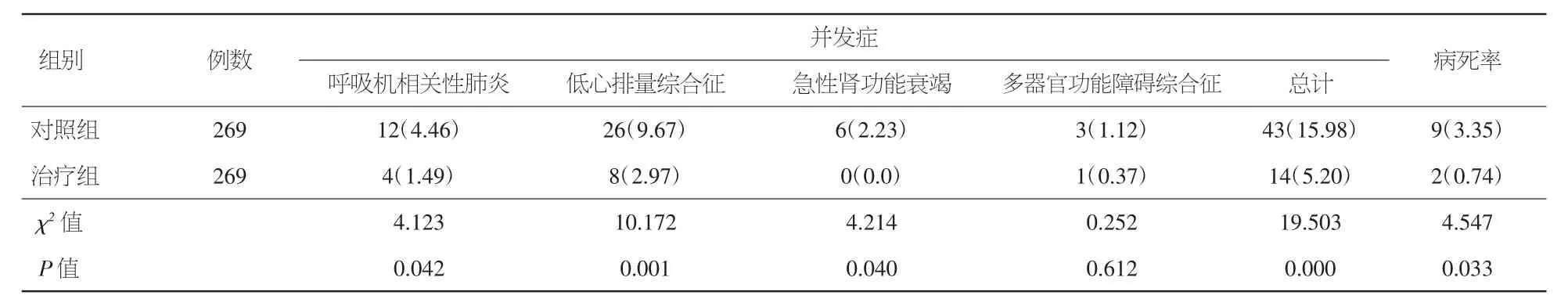
表5 两组患者术后并发症及病死率比较[例数及百分率(%)]
对心血管外科患者来说,过多过快地进行液体复苏,同样带来一定问题。主要表现在:①血液稀释及出血倾向。大量的非血液制品短时间扩容必会造成体内血液中红细胞、凝血因子、血小板等的稀释,再加上术后体外循环的抗凝需求,患者常处于低凝状态,造成凝血功能障碍,具有一定的出血倾向。本组5例患者术后引流液增多,ACT监测提示150~180 s。其中3例患者给予0.5 mg/kg鱼精蛋白静脉滴注后,引流液逐渐减少;1例患者给予输注冷沉淀10 U、血小板1.0治疗量后好转;1例患者急诊行开胸探查术。②复温困难。EGDT时由于输注液体均为常温保存,无加温措施,再加上心外科手术本身的低温状态,会造成患者的低体温,影响心脏功能,使外周血管收缩,增加体循环阻力,心排量减少。为此,我们积极给予保暖等措施,除2例患者出现体温不升、2例患者出现肌颤外,均平稳渡过复温期。③心律失常及ST段变化。EGDT造成的血液稀释、低温、钾离子浓度降低等均可使患者的心率、心律出现变化。临床上实施持续心电监测,及时给予预防心律失常治疗。而患者的低血容量及低心排可造成心肌缺血,应监测心电图ST段变化。本组有15例患者出现心律失常,其中快速房颤8例、室性期前收缩5例、窦性心动过速2例,经调整电解质,给予抗心律失常药物治疗后好转。
综上所述,EGDT作为一种液体治疗理念,早期目标导向性液体治疗能动态反映心脏手术后低血容量患者的血流动力学状态,实时监测容量指标,个体化调整治疗方案,指导液体管理,对提高临床疗效、降低心脏手术并发症发生率和死亡率均具有重要的临床意义,值得推广应用。
[1]Rivers E,Nguyen B,Havstad S,et al.Early goal-directed therapy in the treatment of severe sepsis and septic shock.N Engl Med,2001,345:1368-1377.
[2]李秀华,穆心苇,郑曙云,等.早期目标导向治疗对重症监护病房中感染性休克患者预后的影响.临床荟萃,2010,25:50-52.
[3]喻莉,龙鼎,许涛,等.严重感染和感染性休克早期集束化治疗,临床分析.中国现代医学杂志,2010,20:2632.
[4] Benes J,Chytra I,Altmann P, et al.Intraoperative fluid optimization using stroke volume variation in high risk surgical patients:resultsofprospectiverandomized study.CritCare,2010,14:R118.
[5]Blank RS,Hueklenbrueh C,Gurka KK,et al.Intraoperative factors and the risk of respiratory complications after pneumonectomy.Ann Thorac Surg,2011,92:1188-1194.
[6]O′Connor L,Mclntosh D.Management ofthe circulation on the intensive care unit.Surgery(Oxford),2012,30:543-551.
[7]Hamilton MA,Cecconi M,Rhodes A.A systematic review and meta-analysis on the use of preemptive hemodynamic intervention to improve postoperative outcomes in moderate and high-risk surgical patients.Anesth Analg,2011,112:1392-1402.
[8]Boyd JH,Forbes J,Nakada TA,et al.Fluid resuscitation in septic shock:a positive fluid balance and elevated cental venous pressure are associated with increased mortality.Crit Care Med,2011,39:259-265.
[9]Hohe K,Sharrrock NE,Kehlet H,et al.Pathophysiology and clinical implications of perioperative fluid excess.Br J Aneasth,2002,89:622-632.
[10]解雅英,于建设,吴莉.目标导向液体治疗临床新进展.中华临床医师杂志(电子版),2012,6:1828-1829.
[11] Dellinger RP,Levy MM,Cadet JM,et al.Surviving sepsis campaign:internat ional guidelines for management of severe sepsis and septic shock.Intensive Care Med,2008,34:17-60.
[12]何征宇,皋源,王祥瑞,等.早期目标导向治疗在感染性休克中应用的临床探讨.中国危重病急救医学,2007,19:14-16.
[13]Micek ST,Roubinian N,Heufing T,et al.Before-after study of a standardized hospital order set for the management of septic shock.Crit Care Med,2006,34:2707-2713.
[14]Jochen M,Joachim B,Andinet MM,et al.Goal-directed intraoperative therapy based on autocalibrated arterial pressure waveform analysis reduces hospital stay in high-risk surgical patients:a randomized,controlled trial.Crit Care,2010,14:R18.
[15]Van Beest PA,Spronk PE.Early hemodynamic resuscitation in septic shock:understanding and modifying oxygen delivery.Crit Care,2014,18:111.
[16]Cecconi M,Corredor C,Arulkumaran N,et al.Clinical review:goal-directed therapy-what is the evidence in surgical patients?The effect on different risk groups.Crit Care,2013,17:209.
The strategies of early goal-directed therapy hypovolemic patients after cardiac surgery
HAN Hong-guang,WANG Hui-shan,LI Xiao-mi,et al.Department of Cardiovascular Surgery,General Hospital of Shenyang Military Region,Shenyang 110016,China
WANG Hui-shan,E-mail:hanxiyao@163.com
ObjectiveTo explore the strategies of early goal-directed therapy hypovolemic patients after cardiac surgery.Methods538 hypovolemic patients after cardiac surgery in Department of Cardiovascular surgery,General Hospital of Shenyang Military Command from June 2013 to June 2014 were selected,and were divided into the treatment group and control group,269 cases per group.Patients in control group were given conventional fluid resuscitation on the basis of comprehensive treatment,and patients in treatment group were given EGDT.Liquid input,CVP,MAP,HR,ScvO2,Lac in 8 h,24 h,48 h,mechanical ventilation time,ICU stay time,vasoactive drugs use time,complication rate and mortality in 28 d and so on were observed in two groups.ResultsThere were no significant differences in between the two groups(P>0.05).The amount of crystalloid solution,colloid and the total liquid,CVP and ScvO2in the treatment group were significantly more and higher than that in control group postoperative 8,24 hours(P<0.05).There was no difference between two groups in MAP after 8,24,48 hours(P>0.05).The heart rate in the treatment group was lower than that in the control group at the same time,but no difference between two groups(P>0.05).Lac in the treatment group was less than that in control group postoperative 8,24 hours(P<0.05).There was no difference between two groups in Lac after 48 hours(P>0.05).Duration of mechanical ventilation,vasoactive drug use time,ICU stay time,complication rate and mortality in the treatment group were less than that in control group,except MODS(P<0.05).ConclusionIt can reflect hypovolemic patients after cardiac surgery hemodynamic status dynamically by EGDT,and it has important clinical significance on improving its clinical efficacy,adjusting regimens individual.It is helpful for hypovolemic patients after cardiac surgery to management fluid,enhance the operation successful rate and reduce complication and mortality rate.EGDT is worthy of clinical application.
Early goal-directed therapy; Haemodynamics; Hypovolemia; Cardiac surgery
110016 辽宁省沈阳市,沈阳军区总医院心外科
王辉山,E-mail:hanxiyao@163.com
10.3969/j.issn.1672-5301.2015.10.018
R654.2
A
1672-5301(2015)10-0935-05
2015-04-22)
