FPIA与CMIA测定环孢素A血药浓度的相关性
2015-09-06董玉波
贾 暖,董玉波
环孢素A(CsA)自1972年发现以来,被广泛地应用于器官移植术后的免疫排斥反应。由于CsA服用后个体差异大,患者术后需长期服用,治疗窗范围窄,低于有效浓度易引起排斥反应或诱发自身免疫性疾病,高于有效浓度则易引起感染或肝/肾及中枢神经系统损害,所以有必要对用药患者进行血药浓度监测,CsA全血的浓度测定已经成为临床医师监测或调整给药剂量的依据和常规。但是影响CsA血药浓度结果的因素有很多[1],其中检测方法的不同,也会影响到临床医师对监测结果评判,以致影响用药方案的调整。目前,临床对CsA的检测方法多为荧光免疫偏振法(FPIA),因其具备自动化程度高,样品需求量少、重现性好、检测速度快等优点,但此测定方法存在代谢物交叉反应,为了减少交叉反应对最终结果的影响,检测方法从FPIA发展到化学发光微粒子分析法 (CMIA)。本文对 FPIA的 AxSYM与 CMIA的Architect I1000中测定结果的相关性进行研究,为临床合理应用环孢素A提供理论依据。
1 材料与方法
1.1 仪器与试剂 荧光偏振免疫仪AxSYM (美国雅培公司);化学发光微粒子分析仪Architect I1000(美国雅培公司);Heraeus台式离心机(德国 Heraeus);XW-80A 旋涡混合器(上海医科大学仪器厂)。试剂为Architect环孢霉素全血试剂盒、单克隆抗体全血环孢霉素试剂盒,及两种仪器原配质量控制试剂盒、校准曲线试剂盒,以上试剂均为美国雅培(Abbott)制药有限公司提供的标准试剂。
1.2 方法
1.2.1 样本采集 肾移植术后2周至12年患者124例。男95例,女29例;年龄19~64岁,平均38.9岁。服用环孢素A作为免疫抑制药,于下次服药前30 min抽取空腹静脉血2~3ml,EDTA抗凝后进行全血CsA谷浓度检测。
1.2.2 实验室条件及血药浓度测定 CsA全血浓度测定在室温25℃标准化实验室中进行,每一例患者样本在同一天分别用AxSYM和Architect I1000两台仪器测定,测定方法按照美国Abbott公司提供的AxSYM全自动免疫生化分析仪和Architect I1000分析仪操作手册操作。①荧光偏振免疫法:样本取全血 150μl置1.5m l离心管中,加入 AxSYM标配50μl细胞溶解剂和300μl蛋白沉淀剂,涡旋混匀30 s,10000 r/min离心5min,取上清进行检测。②化学发光微粒子法:样本取全血200μl置1.5ml离心管中,加入 Architect I1000标配100μl细胞溶解剂和400μl蛋白沉淀剂,涡旋混匀30 s,10000 r/min离心4min,取上清液进行检测。
1.2.3 校准曲线及最低检测浓度 AxSYM标配校准曲线试剂盒浓度分别为 0、40、100、200、400、800 ng/ml CsA 的标准品溶液,按1.2.2项下操作进行校准,最低检测浓度为23.2 ng/m l;取Architect I1000标配校准曲线试剂盒浓度分别为0、40、150、400、800、1500 ng/mlCsA 的标准品溶液,按 2.2 项下操作进行校准,最低检测浓度为 25.0 ng/ml。
1.2.4 质量控制 AxSYM 标配低、中、高(70、300、600 ng/m l)3种不同浓度质量控制 (QC)样品,按2.2项下操作;Architect I1000 标配低、中、高(81.3、150、761 ng/ml)3 种不同浓度质量控制(QC)样品,按1.2.2项下操作。两种仪器分别于同一天内分别处理并测定5份,评价日内精密度;同一样品连续测定5 d,每天测定一份,评价日间精密度。
1.2.5 统计学方法 数据及结果以均数±标准差(x±s)表示,对两种方法的检测结果间进行相关分析,以r表示。两种方法结果的比较采用配对t检验,P<0.05则认为结果具有显著性差异。
2 结 果
2.1 质控样品的分析测定 质控样品的分析测定结果见表1。

表 1 两种方法的 QC及 CV 结果(ng/m l,n=5)
2.2 相关性分析 经两种仪器对124例患者CsA全血样本进行测试,将测试样品以CMIA法测定结果(X)为横坐标,FPIA法测定结果(Y)为纵坐标进行线性回归,得回归方程y=1.241x+8.8438,r=0.9502(n=124),曲线见图 1。 CMIA 法测定浓度范围 24.1~554.0 ng/m l,FPIA 法测定浓度范围 57.7~769.1 ng/ml,CMIA 法比 FPIA 法平均偏差低 35.69 ng/ml。 将两种方法的测定结果进行配对t检验,P<0.05提示结果具有显著性差异。
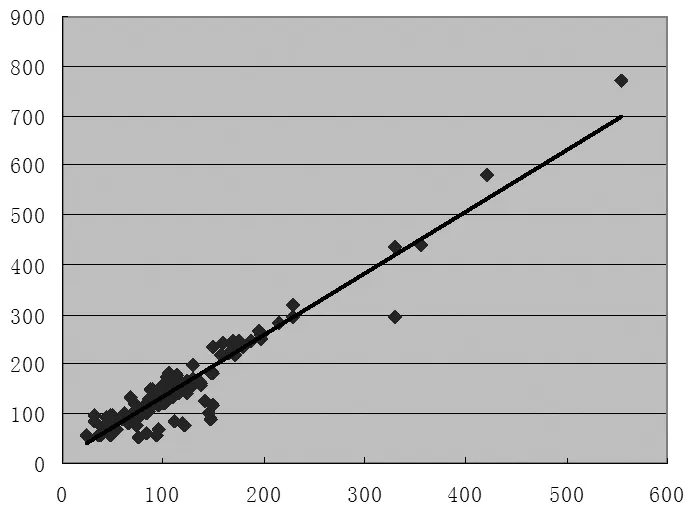
图 1 两种方法相关性分析
3 讨 论
目前临床上对CsA的测定HPLC和FPIA法较为成熟,而且两种方法对检测结果的比较也多受关注[2],由于HPLC测定周期长,批量检测时,FPIA法在临床应用中已成为测定的首选方法[3]。但是这种技术也存在一定的局限性,被测药物的多种内源性代谢物因为与其具有非常相似结构,易发生交叉反应而影响结果的准确性。CMIA与FPIA测定原理不同:FPIA法是根据抗原、抗体竞争结合法的原理,即利用被测物质中被测对象所有的偏振光性进行荧光免疫分析。CMIA采用两步双抗原夹心法,以顺磁性微珠包被CsA抗体后,与标本中的CsA抗原结合,加入吖啶酯标记的CsA抗原后,在特定的磁场区发生沉积,经反复洗涤使游离抗原或抗体与抗原抗体复合物分离,测定其激发光强度的方法。受测定原理的影响,同一份样品的结果也产生了偏倚,本试验研究中同一CsA全血样品分别采用两种方法测定,ARCHITECT测定结果较AxSYM测定结果低,平均浓度低35.69 ng/m l,也有文献报道 ARCHITECT 测定结果较 AxSYM平均浓度低 42.6 ng/ml[4]、76.5 ng/ml[5],可能与所测样品的浓度范围以及样本量、群体样本的来源等因素有关。CsA口服吸收后,经CYP3A4代谢后产生30多种代谢产物(AM1、AM9、AM1c、AM4n、AM19 等)[6], 而在达稳态后 AM1 能够占母药的40%[7],CMIA法能够减少代谢产物的交叉反应,尤其减少与AM1、AM9的交叉反应[8],说明CMIA法相比FPIA法特异性较高,两组数据之间的差异具有统计学意义。CMIA法的测定值更能够反应母药在体内的浓度,结果更准确。两方法相关系数为0.9502,表明两测量结果具有高度相关,与文献[9,10]报道一致。 另 CMIA 法的线性范围 0~1500 ng/m l,而FPIA法的线性范围0~800 ng/m l,若在临床上需要监测服药后 2 h的血药浓度 (C2) 或待测标本浓度超过 800 ng/m l,CMIA方法可以减少需要稀释而带来的误差。
CMIA法比FPIA法特异性和灵敏度高,CMIA法优于FPIA法。患者在进行环孢素血药浓度检测时,尽量选择同一医院同一种仪器进行测定,检测报告最好注明检测方法,以方便临床医师结合患者的个体情况给出准确的药物调整方案。
[1] 王 超.肾移植后环孢素A浓度监测及其影响因素[J].中国组织工程研究,2012,16(18):3387-3390.
[2] 刘 晓,张相林,张 镭,等.单克隆荧光偏振免疫法、多克隆荧光偏振免疫法和高效液相色谱法分别测定环孢素A血药浓度结果的相关性探讨[J].中国药学杂志,2009,44(10):46-48.[3]沈景芬.环孢素A血药浓度监测方法的研究进展[J].安徽医药,2009,13(1):83-86.
[4] 张培环.化学发光微粒子免疫分析与荧光偏振免疫分析检测环孢霉素血药浓度分析[J].实用医药杂志,2012,29(54):424-425.
[5] 谢服役,王 峰,吴巧萍.CMIA FPIA及MS在全血环孢素A浓度监测中的对比分析[J].医学研究杂志,2012,41(4):118-120.
[6] Christians U,Sewing KF.Cyclosporin metabolism in transplant patients[J].Pharmac Ther,1993,57(3):291-345.
[7] Suchy D,Dostalek M,Perinova I,et al.Single-dose and steady state pharmacokinetics of CSA and two main primary metabolites,AM1 and AM4n in patients with rheumatic/autoimmune diseases[J].Biomed Pap Med Fac Univ Palacky Olomouc Czech Repub,2011,155(3):269-274.
[8] Brate EM,Finley DM,Grote J,et al.Development of an Abbott ARCHITECT cyclosporine immunoassay without metabolite crossreactivity[J].Clin Biochem,2010,43(13-14):1152-1157.
[9] Nafija Serdarevic,Lejla Zunic C.Omparision of ARCHITECT i2000 for determination of cyclosporine assay[J].Acta Inform Med,2012,20(4):214-217.
[10] Wallemacq P,Maine GT,Berg K,et al.Multisite analytical evaluation of the Abbott ARCHITECT cyclosporine assay[J].Ther Drug Monit,2010,32(2):145-151.
