磷酸化壳聚糖/无定形磷酸钙复合物与多聚磷酸钠对脱矿牙本质仿生再矿化的影响
2015-08-24苗瑞婧张旭孙迎春高平
苗瑞婧,张旭,孙迎春,高平
应用研究
磷酸化壳聚糖/无定形磷酸钙复合物与多聚磷酸钠对脱矿牙本质仿生再矿化的影响
苗瑞婧,张旭,孙迎春,高平△
目的 探讨磷酸化壳聚糖/无定形磷酸钙(P-chi/ACP)与多聚磷酸钠(TPP)对脱矿牙本质体外仿生再矿化的影响,为深龋再矿化治疗提供思路。方法 将32颗中度磨耗的离体磨牙制成大小相同的完全脱矿牙本质片32个,其中2个样品用于透射电镜表征,另30个分成2组:P-chi/ACP+TPP组(n=15)经TPP预处理后,固定在放置有P-chi/ACP的体外模型上;P-chi/ACP组(n=15)不经过TPP处理。所有样品根据是否与P-chi/ACP接触分为实验侧与对照侧。处理1周后,进行显微计算机断层扫描定量分析密度变化、透射电子显微镜定性分析微观形态变化。结果 显微计算机断层扫描结果显示P-chi/ACP+TPP组的实验侧灰度值高于对照侧(125.42±12.16 vs 96.96±10.56,t= 7.124,P<0.01),P-chi/ACP组中的实验侧灰度值高于对照侧(119.39±8.64 vs 105.27±9.42,t=5.329,P<0.01)。透射电子显微镜显示P-chi/ACP+TPP组有纤维内横纹样结构出现,提示脱矿牙本质片实现了其主要成分Ⅰ型胶原的分级化纤维内矿化;P-chi/ACP组未见横纹样结构。结论 单独利用P-chi/ACP能够提高脱矿牙本质的密度,但共同利用TPP与P-chi/ACP复合物才能实现完全脱矿牙本质的仿生再矿化。
牙本质;仿生学;磷酸化壳聚糖;多聚磷酸钠;再矿化
微创牙科(minimally invasive dentistry,MID)在治疗深龋时往往进行间接盖髓以促进软化牙本质的再矿化[1]。传统的氟化物再矿化方法必须依赖残余晶体,因此对于脱矿程度较大的牙本质,再矿化效果不够理想[2]。研究表明,利用聚丙烯酸[3]和多聚磷酸钠(sodium tripolyphosphate,TPP)[4]能够使胶原纤维和部分脱矿牙本质再矿化,但目前尚少有研究利用仿生材料对完全脱矿的牙本质进行仿生再矿化。本研究利用具有良好生物相容性的磷酸化壳聚糖(phosphorylated chitosan,P-chi),研究新型仿生矿化材料对不含残余晶体的完全脱矿牙本质的再矿化效果,并利用体外模型模拟深龋结构,探索深龋底部软化牙本质的仿生再矿化治疗方法。
1 材料与方法
1.1 材料 因松动拔出的人中度磨耗离体磨牙共32颗(我院口腔颌面外科)。乙二胺四乙酸(EDTA)、壳聚糖、TPP、CaCl2·2H2O、Na2HPO4均购自上海生工生物工程股份有限公司。傅里叶变换红外光谱仪(MAGNA-560,Nicolet,美国)、显微计算机断层扫描仪(1174-v2,Skyscane,比利时)、透射电子显微镜(JEM-2100F,JEOL,日本)、蠕动泵(BT/101S,雷弗,中国)。
1.2 方法
1.2.1 脱矿牙本质片的制备 将32颗磨牙制成直径为1 cm、厚度为1 mm的牙本质片。在37℃恒温摇床中,用0.5 mol/L EDTA溶液处理2周做成脱矿牙本质片。选取其中2个样品进行透射电子显微镜(transmission electron microscopy,TEM)表征。
1.2.2 磷酸化壳聚糖/无定形磷酸钙复合物(P-chi/ACP)的制备 根据文献[5]中的方法制备P-chi,将2.0 g壳聚糖与适量P2O5粉末加入20 mL甲基磷酸中,在0~5℃恒温环境下搅拌3 h后,在-20℃冰箱中静置24 h,取出后用甲醇沉淀,并通过离心收集,丙醇洗净,离心3个循环后,通风橱下风干,得到1.0~1.3 g P-chi。按照60 mmol/L Na2HPO4、50 g/L P-chi、100 mmol/L CaCl2·2H2O的先后顺序和浓度配制溶液,搅拌至完全溶解。将孔径1 cm的多孔板切割为孔高1 mm的模具,利用冷冻干燥技术制备出直径1 cm,厚度1 mm的圆盘状P-chi/ACP复合物。衰减全反射傅里叶变换红外光谱仪(attenuated total internal reflectance,ATR-FTIR)、扫描电子显微镜及TEM对P-chi/ACP进行表征。
1.2.3 样品分组 将余下30个牙本质片均分为2组,A组:P-chi/ACP+TPP组;B组:P-chi/ACP组。A组样品在脱矿处理后,浸泡于25 g/L TPP(pH=9.7)溶液中24 h。B组样品不进行25 g/L TPP处理。ATR-FTIR分别对2组样品进行表征。
1.2.4 体外再矿化模型的构建 建立体外再矿化模型,模拟深龋垫底环境,用离心管和滴管顶部制成双层结构,分别模拟窝洞干燥的环境与牙髓腔的体液循环环境。采用蜡固定P-chi/ACP与牙本质片。塑料隔离帽中央制备1个直径为2 mm的圆孔,模拟牙本质小管结构,模拟体液通过蠕动泵以10 mL/min的速度在下层循环,上层干燥,见图1。采用刘燕等[3]的方法进行模拟体液配制。实验进行1周之后取出样品。
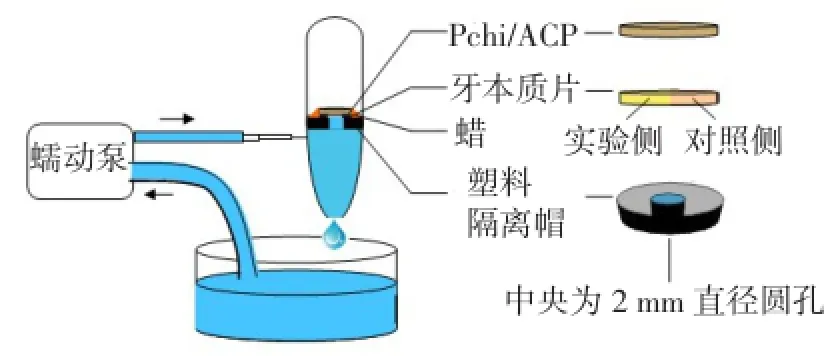
Fig.1 In vitro model of remineralization图1 体外深龋模型示意图
1.2.5 微型计算机断层扫描(Micro-computed tomography,μCT)检测 经过1周的实验处理后将样品取出,用μCT对样品进行非破坏性的三维扫描。利用CT-An软件(Skyscane)将牙本质片的扫描图像进行三维重建、叠加后,分别采集每个样品对照侧与实验侧的灰度平均值。
1.2.6 TEM检测 P-chi/ACP支架、2个脱矿牙本质片与实验处理后的30个牙本质片,经过固定、脱水、包埋和修块后,切出100 nm厚的透射电镜制件,于TEM下观察超微结构,以判断是否实现牙本质胶原纤维内分级再矿化。
1.3 统计学方法 数据以均数±标准差表示,采用SPSS17.0统计软件分析,对数据进行正态性检验与方差齐性检验,数据呈正态分布,方差齐性,比较采用配对t检验,以双侧P<0.01为差异有统计学意义。
2 结果
2.1 牙本质片的ATR-FTIR检测结果 ATR-FTIR检测EDTA脱矿后的牙本质片,出现Ⅰ型胶原的特征峰,且未出现磷酸钙晶体的特征峰,见图2。牙本质片经过25 g/L TPP预处理后,出现磷酸特征峰,见图3。提示牙本质片经过EDTA处理后为完全脱矿牙本质,经过25 g/L TPP处理后完全脱矿牙本质片被磷酸化。
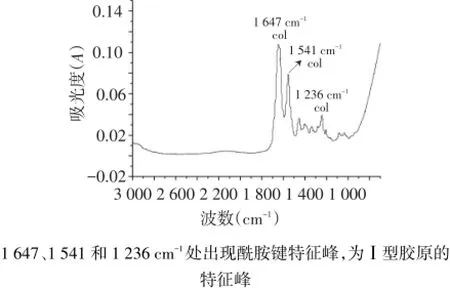
Fig.2 ATR-FTIR of dentin demineralized by EDTA图2 牙本质片经EDTA脱矿处理后的ATR-FTIR结果
2.2 P-chi/ACP的ATR-FTIR检测结果与TEM检测结果 ATR-FTIR显示P-chi/ACP具有PO的特征性波峰,且无磷酸钙晶体的尖锐峰,见图4,提示P-chi/ACP中无磷酸钙晶体。TEM图像显示P-chi/ ACP的超微结构为纳米球形颗粒,见图5,提示Ca2+与PO离子结合为非晶相的无定形磷酸钙颗粒。
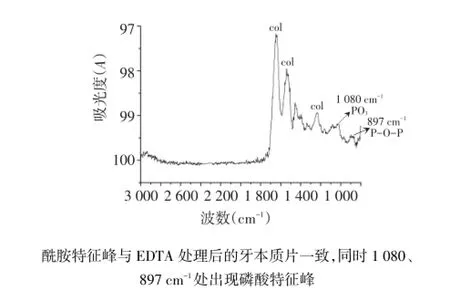
Fig.3 ATR-FTIR of demineralized dentin treated by 25g/L TPP图3 脱矿牙本质片经25g/L TPP处理后的ATR-FTIR结果
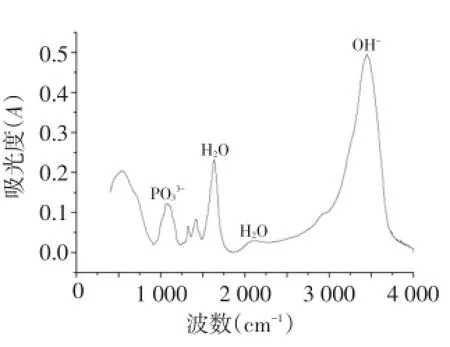
Fig.4 ATR-FTIR of P-chi/ACP图4 P-chi/ACP复合物的ATR-FTIR结果
2.3 牙本质片μCT检测结果 2组牙本质片实验侧的灰度值均高于对照侧,见表1。分别从2组中选出1张典型的三维重构图像,以分析灰度值增高的范围及分布特征,见图6。用Image J软件对图6中灰度值随深度的变化趋势进行绘图,结果示2组中实验侧的灰度值均高于对照侧,灰度值增高区域的深度达到距牙本质片上表面0.7 mm以上,且随着深度增加,灰度值有减小趋势,见图7。

Tab.1 Comparison of grey values of experimental and control sides between two groups表1 2组牙本质片实验侧与对照侧的灰度值比较
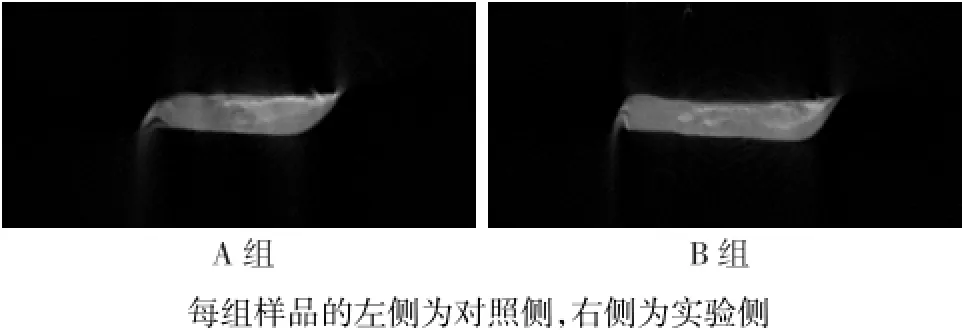
Fig.6 Three-dimension superimposed image of dentin disks图6 牙本质片纵截面三维重构叠加图像
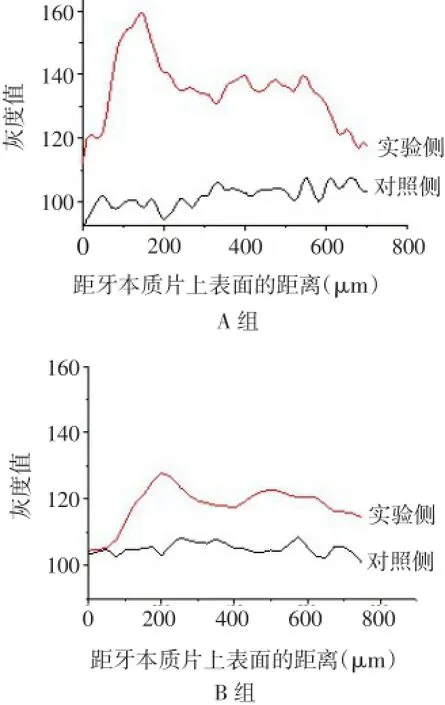
Fig.7 Image J analysis of reconstructed longitudinal sections of dentin disks图7 牙本质片纵截面三维重构图像Image J分析图
2.4 EDTA处理后的牙本质片TEM检测结果 EDTA处理后的牙本质片主要结构为膨松的胶原纤维,见图8。A组牙本质片经过1周再矿化处理后牙本质胶原纤维排列致密,胶原纤维内具有横纹样结构,提示牙本质片实现了其主要成分Ⅰ型胶原的分级化纤维内矿化,见图9。B组牙本质片经过1周再矿化处理后牙本质胶原纤维塌陷,条带不清晰,纤维内部仅观察到窄细条纹,未出现纤维内横纹样结构,提示未实现Ⅰ型胶原的分级化纤维内矿化,见图10。
3 讨论
本研究ATR-FTIR结果显示,经脱矿处理后牙本质的主要成分为Ⅰ型胶原,说明牙本质片已被完全脱矿,不含无机成分及残余晶体。在扫描参数一致的条件下,μCT扫描后的三维重建图像中,灰度值与实际矿物质密度为线性关系,灰度值越高代表矿物质密度越高[6]。本研究μCT扫描结果显示,2组实验侧灰度值均高于对照侧,提示利用P-chi/ACP可以实现脱矿牙本质片矿物质密度的增加。由典型的三维重建图像分析中可见,2组样品矿物质密度增高区域的深度可达到0.7 mm以上,说明材料可以透过表面渗入到牙本质片的深层,具有应用于深龋底部软化牙本质再矿化治疗的潜力。
TEM图像中显示P-chi/ACP微观结构为纳米球形颗粒。P-chi是一种多聚电解质,能够将Ca2+与PO离子包裹形成无定形的纳米磷酸钙亚稳定结构,成为矿化提供结晶来源。研究表明,牙本质胶原带正电荷,具有周期性的结构,有空隙区和重叠区,能通过静电作用吸引带负电的ACP纳米球,ACP进一步成核、生长,使牙本质胶原实现再矿化[7]。晶体结晶理论是指导胶原仿生矿化方法研究的重要基础理论之一[8],非经典的结晶理论中,多聚电解质将离子稳定为无定形的初始粒子。本研究中的P-chi材料具有将Ca2+与PO离子稳定为无定形磷酸钙的粒子,是牙本质基质蛋白 1(dentin matrix protein,DMP1)的仿生物,与Dai等[9]利用聚丙烯酸(PAA)将Ca2+与PO组装成了无定形纳米磷酸钙,从而矿化胶原组织的研究结果一致。
2 组样品经处理后的矿物质密度均有所增加,微观结构也有所差异。TEM图像中,A组出现纤维内横纹样结构,B组胶原纤维塌陷,说明A组样品的超微结构更接近于自然矿化组织,与Tay等[10]的研究结果一致。牙本质的再矿化不仅在于密度的增加,更重要的是要实现接近自然矿化组织的分级结构,从而提高其机械性能,因此A组较B组更好地实现了仿生再矿化。
推测在TPP的作用下,2组矿化的机制不同。A组样品在TPP碱性溶液处理的条件下,胶原表面的氨基酸缺乏正电荷,与带负电荷的ACP粒子不能主动相互吸引。A组中完全脱矿的牙本质片在经过TPP处理后,ATR-FTIR结果显示出现PO3/P-O-P的特征峰,说明牙本质胶原发生了磷酸化。研究表明,TPP能够与胶原分子中空隙区的氨基酸离子交联,有利于进一步螯合ACP纳米球中的钙离子,最终形成纤维内的分级再矿化[11]。未经TPP处理的胶原纤维中,随着ACP纳米球的不断沉积,静电势能逐渐缩小,在空隙区和重叠区的每个矿化带微晶分布逐渐均匀,形成的分级结构不明显[9]。
以往研究多采用部分脱矿的牙本质、Ⅰ型胶原冻干粉,本研究样品来自人离体磨牙,更接近于向临床医学的转化。深龋垫底再矿化的体外模型的建立,可应用于更多的牙本质再矿化体外研究与深龋治疗的实验研究。本研究中采用的P-chi生物相容性较好,已广泛使用于医药研究,较以往使用较多的PAA具有更良好的生物相容性。虽然P-chi/ACP复合物尚不能直接应用于临床,但本实验已经证实完全脱矿的牙本质胶原能够在P-chi/ACP支架的作用下实现矿物质含量的增加和纤维内的分级再矿化,但其缺点为不易保持形态稳定,今后的研究可以致力于提高材料的亲水性及耐久性,并能建立ACP纳米颗粒的缓释系统。
(图5、8~10见插页)
[1]Momoi Y,Hayashi M,Fujitani M,et al.Clinical guidelines for treating caries in adults following a minimal intervention policy—Evidence and consensus based report[J].J Dent,2012,40(2):95-105.doi:10.1016/j.jdent.2011.10.011.
[2]Ten Cate JM.Remineralization of deep enamel dentine caries lesions[J].Aust Dent J,2008,53(3):281-285.doi:10.1111/j.1834-7819.2008.00063.x.
[3]Liu Y,Mai S,Li N,et al.Differences between top-down and bottom-up approaches in mineralizing thick,partially demineralized collagen scaffolds[J].Acta Biomater,2011,7(4):1742-1751.doi: 10.1016/j.actbio.2010.11.028.
[4]Liu Y,Kim YK,Dai L,et al.Hierarchical and non-hierarchical mineralisation of collagen[J].Biomaterials,2011,32(5):1291-1300.doi: 10.1016/j.biomaterials.2010.10.018.
[5]Zhang X,Neoh KG,Lin CC,et al.Biomimetic deposition of calcium phosphate minerals on the surface of partially demineralized dentine modified with phosphorylated chitosan[J].J Biomed Mater Res B Appl Biomater,2011,98(1):150-159.doi:10.1002/jbm.b.31844
[6]Nazarian A,Snyder BD,Zurakowski,D,et al.Quantitative microcomputed tomography:a non-invasive method to assess equivalent bone mineral density[J].Bone,2008,43(2):302-311.doi:10.1016/j.bone.2008.04.009.
[7]Xie BQ,Halter TJ,Borah BM,et al.Tracking amorphous precursor formation and transformation during induction stages of nucleation[J].Cryst Growth Des,2014,14(4):1659-1665.doi:10.1021/cg401777x.
[8]Niederberger M,Cölfen H.Oriented attachment and mesocrystals:nonclassical crystallization mechanisms based on nanoparticle assembly[J].Phys Chem Chem Phys,2006,8(28):3271-3287.doi:10.1039/ B604589H.
[9]Dai L,Qi YP,Niu LN,et al.Inorganic-organic nanocomposite assembly using collagen as template and sodium tripolyphosphate as a biomimetic analog of matrix phosphoprotein[J].Cryst Growth Des,2011,11(8):3504-3511.doi:10.1021/cg200663v.
[10]Tay FR,Pashley DH.Guided tissue remineralisation of partially demineralised human dentine[J].Biomaterials,2008,29(8):1127-1137.doi:10.1016/j.biomaterials.2007.11.001.
[11]Niu LN,Zhang W,Pashley DH,et al.Biomimetic remineralization of dentin[J].Dent Mater,2014,30(1):77-96.doi:10.1016/j.dental.2013.07.013.
(2014-11-20收稿 2014-12-30修回)
(本文编辑 闫娟)
In vitro biomimetic remineralization of dentin collagen by phosphorylated chitosan/amorphous calcium phosphate compound and tripolyphosphate
MIAO Ruijing,ZHANG Xu,SUN Yingchun,GAO Ping△
Stomatological Hospital,Tianjin Medical University,Tianjin 300070,China
△Corresponding Author E-mail:Gaoping@tmu.edu.cn
Objective To investigate the remineralizing therapy of deep caries and in vitro biomimetic remineralization of demineralized dentin by phosphorylated chitosan/amorphous calcium phosphate compound(P-chi/ACP)and tripolyphosphate(TPP).Methods Thirty-two extracted human molars were cut and completely demineralized.Two samples were used to show the characteristics by transmission electron microscopy(TEM).The other 30 samples were divided into two groups: fifteen samples were treated by P-chi/ACP and TPP(P-chi/ACP+TPP group),the other fifteen samples were not treated by TPP(P-chi/ACP group).All of the samples were distinguished into experimental side and control side,and then they were set on the in vitro model for 1 week.Micro-computed tomography(μCT)and TEM were used to assess the effects of remineralization.Results μCT detection revealed that the mineral density were higher in the experimental sides(125.42±12.16 and 119.39±8.64)than that of control sides(96.96±10.56 and 105.27±9.42)in both groups(P<0.01).TEM figures showed that hierarchical intrafibrillar remineralization was realized in samples of P-chi/ACP+TPP group,while trace amounts of hierarchical remineralization was detected in P-chi/ACP group.Conclusion Fully demineralized dentin appears to have the potential to be remineralized with the application of P-chi/ACP.The ultrastructure of samples is better in P-chi/ACP+TPP group than that of P-chi/ACP group.
dentin;bionics;phosphorylated chitosan;sodium tripolyphosphate;remineralization
R781.1;R318.08
A DOI:10.11958/j.issn.0253-9896.2015.05.019
国家自然科学基金青年项目(81200817);天津市应用基础及前沿技术研究计划青年项目(12JCQNJC09200)
天津医科大学口腔医院(邮编300070)
苗瑞婧(1989),女,硕士在读,主要从事口腔材料研究
△E-mail:Gaoping@tmu.edu.cn
