三乙醇胺+哌嗪混合胺液的脱碳性能及配比优选
2015-08-19花亦怀唐建峰陈杰冯颉韩雅萍姜雪周凯杨帆黄彬
花亦怀,唐建峰,陈杰,冯颉,韩雅萍,姜雪,周凯,杨帆,黄彬
(1中海石油气电集团有限责任公司技术研发中心,北京 100029;2中国石油大学(华东)储运与建筑工程学院,山东 青岛 266580)
由气井井口采出或从矿场分离器分出的天然气除含有水蒸气外,往往还含有一些酸性组分。酸性组分含量超过管输气或商品气质量要求的天然气称为酸性天然气或含硫气[1]。天然气质量标准 GB 17820-1999《天然气》中要求CO2的体积分数不大于3%。CO2溶入水后对钢铁有极强的腐蚀性,在相同的pH值下,CO2的总酸度比盐酸高,对钢铁的腐蚀比盐酸严重[2]。化学吸收法具有脱除效果好、技术成熟等特点,是脱除、回收CO2的主要方法[3]。在使用的化学试剂中,MEA(一乙醇胺)和DEA(二乙醇胺)已得到广泛研究,而TEA(三乙醇胺)的研究报道则较少[4]。TEA是叔胺,其对CO2吸收容量与MEA和DEA相比较大,具有良好的应用前景[5]。PZ(哌嗪)是工业上应用较广泛的吸收剂,目前国内外对AMP-PZ和MDEA-PZ混合胺液的研究较多,对TEA-PZ的研究很少[6]。本文运用高压反应釜等小型实验装置研究TEA+PZ不同配比混合胺液对CO2的吸收与解吸性能,并针对2mol/L TEA+1mol/L PZ混合胺液研究其循环性能,旨在为实际天然气胺法脱碳工艺提供基础数据及理论依据。
1 吸收机理
TEA与CO2反应生成亚稳态的碳酸氢盐,普遍认同的反应机理是碱催化水合机理[6-7]。叔胺与CO2的反应如式(1)所示。CO2与水中OH-反应也生成碳酸氢根,抑制反应(1),故在与CO2反应时,叔胺与伯胺、仲胺相比虽吸收负荷有所提高,但吸收速率较慢。
TEA与PZ的混合溶液反应速率由以下5个可逆反应控制[7],如式(1)~式(5)。
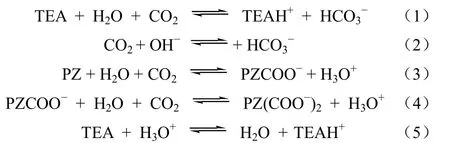
PZ与H2O、CO2反应生成PZCOO-和H3O+,生成的PZCOO-与H2O、CO2反应生成PZ(COO-)2和H3O+。TEA与H3O+反应生成H2O与TEAH+。TEA与CO2反应的化学计量数之比为1∶1,PZ与CO2反应的化学计量数之比为1∶2。两个反应都是二阶反应[8]。
2 实验部分
2.1 实验气体与试剂
TEA,西陇化工有限公司,分析纯,含量> 98.0%;PZ,成都格雷西亚化学技术有限公司,分析纯,含量为98%;CaCl2,国药集团化学试剂有限公司,分析纯,含量≥96.0;CuSO4,上海振欣试剂厂,分析纯,含量为99%;H2SO4,广东省精细化学品工程技术研究开发中心,分析纯,质量分数95%~98%;CH4,青岛天源特种气体厂,纯度99.999%;CO2,青岛天源特种气体厂,纯度99.999%;CH4+CO2,青岛天源特种气体厂,纯度约为93.51%+6.44%(体积分数)。
2.2 实验装置与流程
本课题研究所采用的吸收、解吸及酸解实验装置及流程参见文献[7]。
2.2.1 吸收实验
高压气瓶中原料气经减压阀调压后通入高压反应釜,与反应釜内预先充入的胺液进行吸收反应。磁力搅拌速率范围为150~1200r/min。反应釜外壳为循环夹套,恒温水浴可提供一定温度的导热液体,用于胺液反应过程中的温度控制,进行不同操作温度的实验。恒温水浴的温度控制范围为室温以上5~100℃,控制精度为±0.1℃。实验采用真空泵对反应釜及管线进行排空。计算机数据采集系统由数据变送器、数据采集卡和计算机构成,用于对实验数据进行采集记录[7]。
胺液吸收CO2性能实验具体操作步骤如下。
(1)预热恒温水浴 打开恒温水浴,将加热温度设定到要求值。
(2)配制胺液样本 使用电子天平按所需胺液组成配制一定浓度和体积的胺液,使用真空泵抽出反应釜内气体后,将预先配制的胺液充入釜中。
(3)反应釜抽真空 胺液充入反应釜后,持续抽真空一段时间,直至釜内压力不再降低为止,以消除胺液内溶解空气中CO2量及釜内气相空间残留CO2气体的影响。
(4)充入反应气体 打开CO2纯气体高压气瓶,通过减压阀控制充气压力,充气完毕10s左右,待釜内气体稳定,关闭进口阀与气瓶减压阀。
(5)开启数据采集 打开数据采集系统,进行数据记录。
(6)开启搅拌装置 打开磁力搅拌系统,将搅拌速率控制在设定值。
(7)进行吸收实验 观察反应釜内温度、压力变化数据,待釜内压力趋于稳定后,关闭数据采集系统及恒温水浴,吸收实验结束。
2.2.2 解吸实验
胺液在三口烧瓶内进行解吸反应,解吸出的酸气通过皂膜流量计记录瞬时流量,通过湿式气体流量计记录累计流量。需每隔1min记录一次胺液气相和液相温度、皂膜流量计读数、湿式气体流量计读数及压差,待湿式气体流量计读数连续5次不变时,停止实验[7,10]。
2.2.3 酸解实验
胺液吸收与解吸实验所得胺液样品中CO2含量使用酸解法测得,酸解法主要利用强酸置换弱酸的原理,使用强酸H2SO4将CO2从胺液中置换出来,通过测定放出的CO2气体体积计算溶液对CO2的吸收量。胺液吸收实验所取样品中CO2含量较高,称为富液;胺液解吸实验所取样品中CO2含量很低,称为贫液,分别采用不同的装置进行实验计量[7]。
测定胺液中CO2含量实验具体操作步骤如下。
(1)量取酸解胺液样品 用10mL的量筒量取一定量的胺液(富液5mL,贫液10mL),将实验编号和环境温度记录在实验表中。
(2)连接酸解实验装置 将胺液样品注入三口烧瓶中,连接各仪器,将稀硫酸注入滴液漏斗中,并封闭整个系统。
(3)检查系统气密性 将量筒(或滴定管)的位置抬高或放低,量筒(或滴定管)液位在1min内无降低则视为气密性良好,若降低则检查并旋转各密封部位,看乳胶管或容器有无损坏,重复检测,至液位不再降低为止。
(4)初始数据记录 将量筒(或滴定管)放回至液面与广口瓶(或锥形瓶)相平的位置,记录液位刻度。
(5)进行酸解实验 打开滴液漏斗,注入一部分硫酸(大约20mL)后关闭,待量筒内液面稳定后,再注入一定量硫酸,至注入硫酸后量筒(或滴定管)1min内液位不再变化。
(6)实验数据记录 调节量筒(或滴定管)和广口瓶(或锥形瓶)的高度,使量筒(或滴定管)中的液位稍低于广口瓶(或锥形瓶)中油层上表面,记录此时的刻度,并计算实验前后刻度差。
2.3 实验指标与参数
2.3.1 实验指标
对胺液吸收性能的评价指标包括吸收速率、吸收负荷、酸气负荷,对胺液解吸性能的评价指标包括解吸率、残余酸气负荷,各个指标的含义如下。
(1)吸收速率vab吸收速率指单位时间内单位体积的胺液吸收CO2的量,其表达式如式(6)所示,吸收速率越高,吸收性能越好。

式中,vab为胺液吸收速率,mol/(L·min);V为胺液量,L;Δτ为时间,min;Δn为Δτ时间内CO2物质的量的变化量,mol。
(2)吸收负荷L吸收负荷指单位体积的胺液吸收CO2的量,代表胺液对CO2的吸收能力,其表达式如(7)所示。

式中,L为胺液吸收负荷,mol/L。
(3)酸气负荷α酸气负荷指胺液中单位摩尔量的醇胺所含CO2的摩尔量,其表达式如式(8)所示。

式中,α为胺液酸气负荷,mol/mol;A为胺液中醇胺浓度,mol/L。
(4)解吸率rde解吸率指一定时间内胺液解吸出的CO2量与胺液解吸前所含CO2总量的比值,胺液解吸前所含CO2量使用酸解法测定,一段时间内解吸出的CO2量使用解吸实验装置中湿式气体流量计测定。解吸率能够表示出胺液的再生能力。
(5)残余酸气负荷αre残余酸气负荷指胺液进行解吸实验后单位摩尔量醇胺中残余的CO2摩尔量,其单位为mol/mol,可以表示胺液的再生效果。
2.3.2 实验参数
本课题研究所进行的实验中,设定统一的实验参数。吸收实验设定气体初始CO2分压为0.21MPa,吸收温度50℃,搅拌速率220r/min;解吸实验设定油浴温度为125℃。
3 实验结果及分析
3.1 TEA+PZ吸收性能分析
本节针对相同实验参数下,TEA+PZ混合胺液总浓度3.0mol/L,不同配比下混合胺液的吸收性能进行实验对比分析。TEA+PZ不同配比下混合胺液CO2吸收负荷随时间的变化曲线如图1所示,吸收速率随时间的变化曲线如图2所示。

图1 TEA+PZ不同配比胺液CO2吸收负荷变化曲线

图2 TEA+PZ不同配比胺液CO2吸收速率变化曲线
由图1可知,随吸收时间的增加不同配比胺液的吸收负荷均逐渐增大,并最终稳定至一定的负荷值。同一时间下不同TEA/PZ配比的混合胺液吸收负荷不同,从大到小依次为:2.4mol/L/0.6mol/L、2.0mol/L/1.0mol/L、2.8mol/L/0.2mol/L、3.0mol/L/ 0.0mol/L,且这4种TEA/PZ配比胺液吸收负荷变化趋势依次变缓,TEA/PZ配比值为2.4mol/L/ 0.6mol/L和2.0mol/L/1.0mol/L时,吸收负荷变化趋势相似且明显高于配比值为2.8mol/L/0.2mol/L的混合胺液。说明随着TEA中PZ添加量增加,即TEA/PZ配比减小,混合胺液吸收负荷逐渐增大,吸收酸气稳定时间明显缩短,吸收效率提高,胺液对CO2的吸收能力逐渐变强,但这一现象随着PZ添加量到达一定数值后而变得不明显。不同配比下胺液最终吸收负荷基本相同,说明改变配比对胺液的最终CO2负载能力影响较小。
从图2中可以看出,随吸收时间的增加,不同配比胺液的吸收速率均逐渐减小。不同配比TEA+PZ混合胺液单位时间内吸收的CO2含量不同,即吸收速率不同,在TEA中加入PZ后混合胺液对CO2的吸收速率明显高于单一TEA溶液对CO2的吸收速率,反应开始后前16min内,TEA/PZ混合胺液吸收速率按配比2.0mol/L/1.0mol/L、2.4mol/L /0.6mol/L、2.8mol/L/0.2mol/L、3.0mol/L/0.0mol/L依次减小,且配比为2.0mol/L/1.0mol/L和2.4mol/L /0.6mol/L的胺液CO2吸收速率变化规律接近一致,说明TEA中PZ的添加量明显影响胺液的吸收速率,添加量越大,吸收速率越高,但这一现象随着PZ添加量到达一定数值而变得不明显。
从图1、图2中还可以看出,TEA+PZ混合胺液吸收达到平衡的时间按配比2.0mol/L/1.0mol/L、2.4mol/L/0.6mol/L、2.8mol/L/0.2mol/L、3.0mol/L/ 0.0mol/L依次增大,TEA/PZ配比为2.0mol/L/ 1.0mol/L和2.4mol/L /0.6mol/L的混合胺液吸收反应最先达到平衡,说明随着TEA中PZ添加量的增加,吸收酸气稳定时间逐渐缩短,吸收效率提高。
3.2 TEA+PZ解吸性能分析
本节针对相同实验参数下,TEA+PZ混合胺液总浓度3.0mol/L,不同配比下混合胺液的解吸性能进行实验对比分析,不同配比TEA+PZ混合胺液的CO2解吸速率随时间的变化曲线如图3所示,解吸率随时间的变化曲线如图4所示,解吸率随温度的变化曲线如图5所示。

图3 不同TEA+PZ配比胺液解吸速率随时间变化曲线
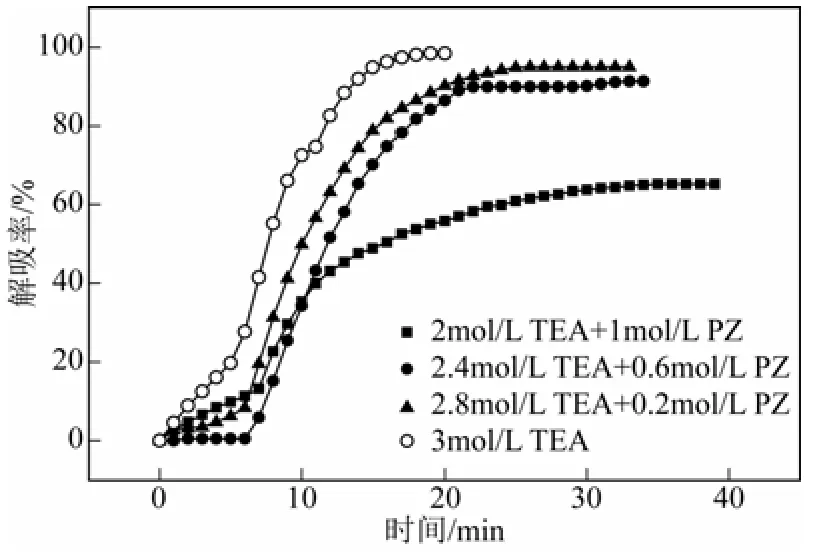
图4 不同TEA+PZ配比胺液解吸率随时间变化曲线

图5 不同TEA+PZ配比胺液解吸率随温度变化曲线
从图3可以看出,TEA/PZ配比为2.0mol/L/ 1.0mol/L与2.8mol/L/0.2mol/L的混合胺液较TEA单一胺液的解吸速率相比相差较小,2.4mol/L/ 0.6mol/L配比混合胺液解吸速率较低。如图4、图5所示,解吸初始阶段,前8min,同一解吸时间或解吸温度下,2.0mol/L/1.0mol/L配比的TEA+PZ混合胺液解吸率明显高于其他几种混合胺液,但混合胺液较单一TEA胺液解吸率并无提高,随着反应的 进行,2.8mol/L/0.2mol/L配比的混合胺液解吸率明显高于其他几种配比的混合胺液,解吸温度达到90℃后,解吸率略高于单一TEA胺液。由图4可以看出,TEA/PZ配比按最终解吸率由大到小为3.0mol/L/0.0mol/L > 2.8mol/L/0.2mol/L > 2.4mol/L/ 0.6mol/L>2.0mol/L/1.0mol/L,TEA/PZ配比按解吸反应达到平衡所需时间由低到高为3.0 mol/L/0.0mol/L>2.8mol/L/0.2mol/L>2.4mol/L/0.6mol/ L>2.0mol/L/1.0mol/L。由此可知,混合胺液的解吸性能与单一胺液相比较差。在相同条件下,TEA单一胺液达到解吸完全所需要的时间最少,所以其需要的解吸能耗最少。这是由于TEA与CO2反应不生成氨基甲酸盐,而PZ与CO2反应会生成氨基甲酸盐,故TEA+PZ混合胺液能耗高于TEA单一胺液,且混合胺液的解吸能耗随着PZ浓度的增加而增加。
综合分析TEA+PZ不同配比下混合胺液的吸收和解吸性能可以得出,随着TEA中PZ添加量增加,胺液对CO2的吸收能力逐渐变强。TEA/PZ配比为2.0mol/L/1.0mol/L的混合胺液吸收负荷及吸收速率均明显高于其他配比胺液,且吸收反应最先达到平衡,说明吸收性能良好。对于解吸反应,在TEA中添加PZ后对其解吸率并无明显改善。
3.3 循环性能分析
在实际天然气预处理工艺中,胺液在酸气脱除系统中进行吸收解吸循环利用,因此,在胺液性能评价时,需要考虑胺液的稳定性。本节基于3.1~3.2节中对不同配比混合胺液吸收及解吸性能的分析,选择2mol/L TEA+1mol/L PZ混合胺液配方,分别进行3次吸收-解吸循环实验,考察该胺液配方的循环利用效果,分析其循环稳定性能。
3.3.1 循环吸收性能
经过吸收-解吸循环实验后,根据吸收实验所得数据分析胺液的吸收效果。该胺液配方在3次循环实验中的吸收负荷随时间的变化曲线如图6所示,吸收速率随酸气负荷变化曲线如图7所示。
从图6中可以看出,随着实验中循环次数的增加,吸收负荷上升趋势略有变缓,达到平衡的时间有所增加,但胺液最终吸收负荷略有上升,说明混合胺液随着使用次数的增加,吸收能力有一定程度的上升。从图7中可以看出,该配方胺液在循环往复实验中吸收速率变化稍有差异,在相同的酸气负荷下,混合胺液2mol/L TEA+1mol/L PZ随着循环次数的增加吸收速率逐步降低,第二、第三次循环吸收的吸收速率差别不大。综合上述分析可知,在2mol/L TEA+1mol/L PZ溶液的循环吸收实验中,3次循环的胺液吸收负荷和吸收速率大致相当,无明显减弱现象,证明2mol/L TEA+1mol/L PZ溶液的循环吸收性能良好。
3.3.2 循环解吸性能

图6 2mol/L TEA+1mol/L PZ循环实验吸收负荷随时间 变化
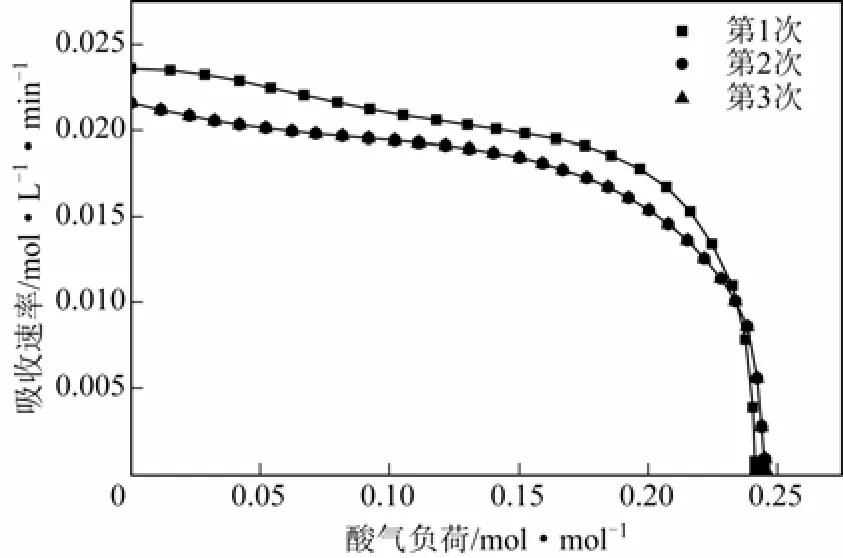
图7 2mol/L TEA+1mol/L PZ循环实验吸收速率随酸气负荷变化
经过吸收-解吸循环实验后,根据解吸与酸解实验所得数据分析胺液在循环过程中的解吸性能。该胺液配方在3次循环实验中的解吸率随时间的变化 曲线如图8,吸收率随温度的变化曲线如图9。从图8中可以看出,解吸率随时间的增长速度为第三次循环>第一次循环>第二次循环,最终解吸率的大小为第三次循环>第二次循环>第一次循环,达到平衡所需时间为第一次循环>第二次循环>第三次循环。说明循环使用次数对该配方混合胺液的解吸率影响较大,解吸后的贫液经过重复吸收后再次解吸时最终解吸效果变好。从图9中可以看出,该胺液配方在3次循环过程中,解吸率随着温度的变化曲线十分接近,均在100℃进入快速解吸阶段。说明循环使用时解吸温度对胺液的解吸率影响较小。综合上述分析可知,在2.0mol/L TEA+1.0mol/L PZ溶液的循环解吸实验中,3次循环的最终解吸率随循环次数的增加而逐步增大;相同温度下,3次循环的解吸率基本一致,证明2.0mol/L TEA+1.0mol/L PZ混合胺液的循环解吸性能良好。
综合本节分析,可以得出循环使用时2.0mol/L TEA+1.0mol/L PZ混合胺液的吸收解吸性能均有所改善,解吸效果改善明显,能够解决前述添加PZ后降低TEA解吸率的问题。TEA/PZ配比为2.0mol/L/1.0mol/L的混合胺液在循环实验中验证综合性能较好,适合在工业生产中应用。
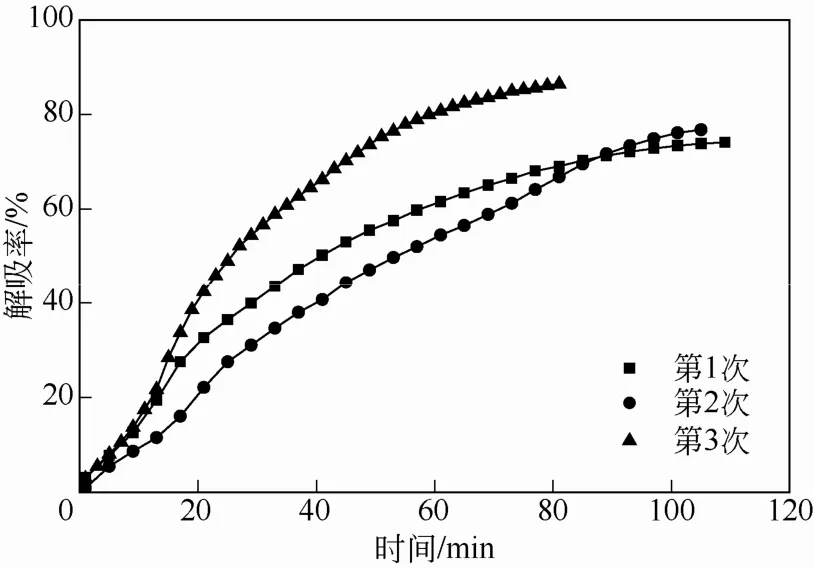
图8 2mol/L TEA+1mol/L PZ循环实验解吸率随时间变化
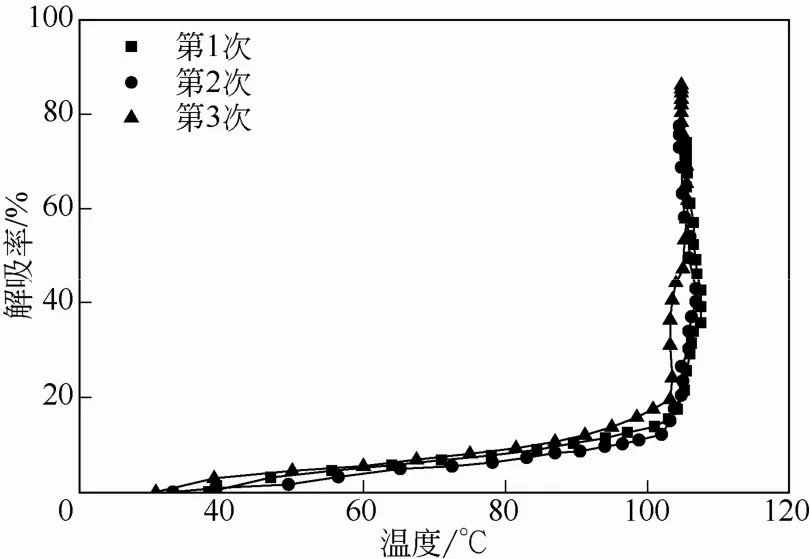
图9 2mol/L TEA+1mol/L PZ循环实验解吸率随温度变化
4 结 论
本文通过对TEA+PZ混合胺液进行不同配比下的吸收、解吸、酸解及实验,综合各指标对混合胺液的吸收解吸性能进行评价,针对的2mol/L TEA+1mol/L PZ胺液配比,最后加以循环实验进行验证。本课题研究所得数据及结论对于胺液配方筛选具有重要的指导意义。
(1)TEA+PZ混合胺液相比单一TEA溶液,吸收负荷及吸收速率均有显著提高,胺液对CO2的吸收能力变强,吸收性能得到明显改善,而解吸性能无明显改善。
(2)不同配比的TEA/PZ混合胺液吸收性能不同,TEA中PZ的添加量越大,混合胺液吸收负荷逐渐增大,吸收速率越高,吸收酸气稳定时间明显缩短,胺液对CO2的吸收能力逐渐变强,但这一现象随着PZ添加量到达一定数值而变得不明显。
(3)TEA/PZ配比2.0mol/L/1.0mol/L的混合胺液吸收负荷及吸收速率均明显高于其他配比胺液,且吸收反应最先达到平衡,吸收性能良好。在解吸性能方面与同浓度下单一胺液相比无明显优势。
(4)循环次数影响TEA+PZ混合胺液的吸收和解吸性能。2.0mol/L TEA+1.0mol/L PZ混合胺液随着循环使用次数的增加吸收能力有一定程度的上升,最终解吸率增大;相同温度下3次循环的解吸率基本一致,证明2.0mol/L TEA+1.0mol/L PZ溶液的循环性能良好。
[1] 刘火得. 天然气脱碳工艺现状与印尼SES天然气项目脱碳工艺[J]. 石油工程建设,2009,35(s1):130-135.
[2] 何龙. 天然气脱碳工艺选择[J]. 科学咨询,2012(4):49-50.
[3] 国立清华大学(台湾). 以吸收法回收二氧化碳之技术手册[R]. 台北:经济部工业局,2002.
[4] Gerald O. Carbon dioxide gets grounde[J].Chemical Engineering,2000,107(3):41-45.
[5] 李清方,陆诗建,张建,等. 搅拌法对TEA溶液吸收和解吸CO2的实验研究[J]. 陕西科技大学学报:自然科学版,2009,27(4):48-51.
[6] 王洪波. 有机胺法吸收二氧化碳的研究[D]. 上海:上海师范大学,2012.
[7] 周丹,陈杰,花亦怀,等. TEA与烯胺混合胺液脱碳性能及配比优选实验研究[J]. 化工进展,2015,34(1):95-101.
[8] 宿辉,崔琳. 二氧化碳的吸收方法及机理研究[J]. 环境科学与管理,2006(8):79-81.
[9] 刘今朝,王淑娟,赵博,等.N-甲基二乙醇胺/哌嗪溶液和氨水吸收二氧化碳的实验研究[J]. 环境科学学报,2012,32(10):2533-2539.
[10] 花亦怀,郭清,冯颉,等. 天然气脱碳单一胺液及混合胺液解吸性能研究[J]. 天然气化工:C1化学与化工,2014,01:47-51.
