锂离子电池磷酸铁锂正极材料的研究进展
2015-08-19张克宇姚耀春
张克宇,姚耀春
(昆明理工大学真空冶金国家工程实验室,云南省有色金属真空冶金重点实验室,省部共建有色金属资源清洁利用国家重点实验室,云南 昆明650093)
随着国民经济的快速发展,以石油、煤炭、天然气为代表的不可再生能源逐渐减少,大气污染、水污染、固体废弃物污染不断加剧,能源与环境问题逐渐成为可持续发展面临的挑战。基于这种背景,新能源的开发不断深入,但新能源的利用离不开储能电源,所以新能源产业的快速发展为锂离子电池在储能电池领域的应用提供了前所未有的机遇!
锂离子电池因其具有能量密度高、自放电流小、安全性高、可大电流充放电、循环次数多、寿命长等优点,越来越多地应用于手机、笔记本电脑、数码相机、电动汽车、航空航天、军事装备等多个领域。据统计,2011年中国锂电池行业市场达到了397亿元,同比增长43%,全年锂电池产量达到29.7亿颗,同比增长28.6%。锂电池产业已经成为国民经济发展的重要产业方向之一[1]。
目前,锂离子电池正极材料分为以下几类[1]:①具有层状结构的钴酸锂(LiCoO2)、镍酸锂(LiNiO2)正极材料;②具有尖晶石结构的锰酸锂(LiMn2O4)正极材料;③具有橄榄石结构的磷酸铁锂(LiFePO4)正极材料;此外还有三元材料。磷酸铁锂正极材料的理论比容量为170mA/g,电压平台为3.7V,在全充电状态下具有良好的热稳定性、较小的吸湿性和优良的充放电循环性能[2],因此成为现今动力、储能锂离子电池领域研究和生产开发的重点。但由于其本身结构的限制,导致以LiFePO4为正极材料的锂离子电池导电率差、锂离子扩散速率慢,在低温条件下放电性能较差[3],这些都制约了LiFePO4正极材料的大规模工业化生产。
1 LiFePO4基本性能
1.1 LiFePO4基本结构
磷酸铁锂正极材料具有正交的橄榄石结构,pnma空间群,如图1所示。在晶体结构中[1,4-6],氧原子以稍微扭曲的六方紧密堆积的方式排列。Fe与Li分别位于氧原子八面体中心4c和4a位置,形成了FeO6和LiO6八面体。P占据了氧原子四面体4c位置,形成了PO4四面体。LiFePO4结构在c轴方向上是链式的,1个PO4四面体与1个FeO6八面体、2个LiO6八面体共边,由此形成三维空间网状结构。从结构上看,PO4四面体位于FeO6层之间,这在一定程度上阻碍了锂离子的扩散运动。此外,相邻的FeO6八面体通过共顶点连接层状结构和尖晶石结构中存在共棱的MO6八面体连续结构不同,共顶点的八面体具有相对较低的电子传导率。这使得磷酸铁锂只能在小的放电倍率下充放电,而在大 倍率放电条件下,内部的锂离子来不及迁出,电化学极化就会很大。

图1 LiFePO4晶体结构示意
1.2 LiFePO4充放电原理
磷酸铁锂电池充放电的过程是在LiFePO4与FePO4两相之间进行的,如图2所示,其具体机理为[4,7-9]:在充放电过程中,Li+在两个电极之间往返嵌入和脱出。充电时,Li+从正极脱出,迁移到晶体表面,在电场力的作用下,经过电解液,然后穿过隔膜,经电解液迁移到负极晶体表面进而嵌入负极晶格,负极处于富锂状态。与此同时,电子经正极导电体流向正极电极,经外电路流向负极的集流体,再经负极导电体流到负极,使负极的电荷达到平衡。锂离子从正极脱出后,磷酸铁锂转化为磷酸铁;而放电过程则相反。
其充放电反应式可表示成[7]式(1)和式(2)。
充电时

放电时
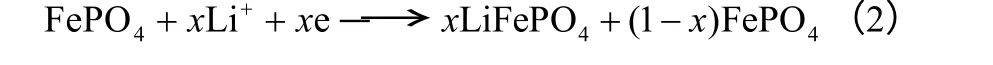
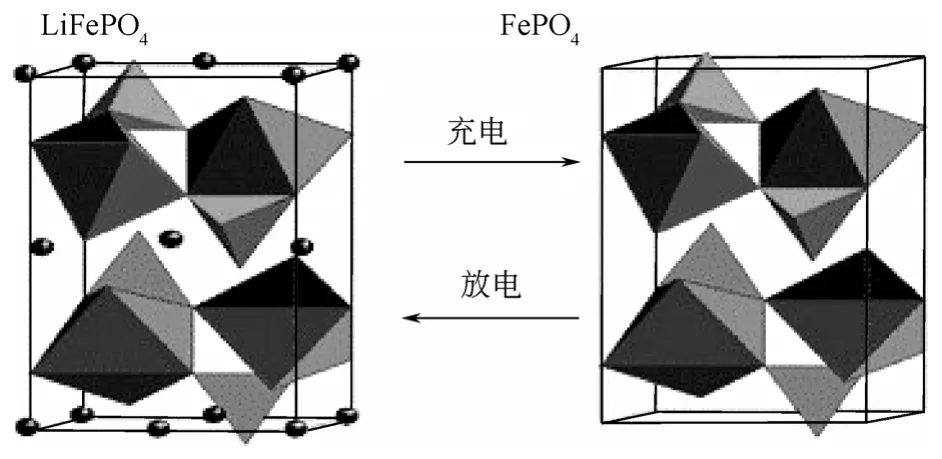
图2 磷酸铁锂电池充放电原理
1.3 LiFePO4电化学反应模型
对于磷酸铁锂正极材料的电化学反应过程,一般要经过液相传质、电极表面吸附、电极表面放电、电极附近转化、新相生成等步骤。研究正极材料的电化学反应一般是为了找出控制因素,从而有针对性地改善材料的性能,提高电池充放电的能力。
针对磷酸铁锂充放电过程中的电化学反应,经典的模型主要有3个:Padhi提出的界面迁移模型[4]、Andersson提出的径向模型(radial model)和马赛克模型(Mosaic model)[5,10-11]。其中,界面迁移模型如图3所示,Padhi等[4]认为脱嵌过程是从磷酸铁锂颗粒表面经过一个两相界面(FePO4/LiFePO4界面)进行的。充电时,随着锂离子的迁出而形成FePO4层逐渐向内核推进,则FePO4/LiFePO4界面不断减少。由于锂离子扩散速率在一定条件下为常 数,当FePO4/LiFePO4界面减少到一定程度时,位于核心部分的磷酸铁锂就不能利用,成为容量损失的来源。放电时,锂离子的嵌入模式与此相同。
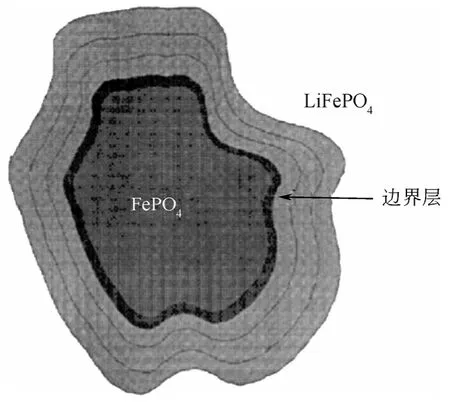
图3 磷酸铁锂充放电过程中界面变化示意图
Anderson等[5]利用中子粉末衍射研究磷酸铁锂材料的首次容量损失时,认为残存没有反应的LiFePO4和FePO4是造成容量损失的原因。由此,他提出了“径向模型”,如图4(a)所示,其实质与界面反应模型相似,都认为在充放电过程中,随着界面的推移,核心处未反应的磷酸铁锂是造成容量损失的原因。但由于很少有反应是均匀发生的,因此在此基础上又提出了“马赛克模型”,如图4(b)所示。这个模型认为锂离子的脱嵌过程发生在颗粒的任何一个位置。充电时,随着锂离子脱出量的增加,残留未反应的磷酸铁锂被充电过程中形成的无定形物质包覆,形成了容量损失。放电时,锂离子嵌入磷酸铁中,未嵌入锂离子的核心处则是未参加反应的磷酸铁。最后磷酸铁锂相连通,未参加反应的磷酸铁锂以及磷酸铁形成了容量损失的来源。根据其实验测算,有15%~20%(质量分数)未参加反应的LiFePO4和7%(质量分数)未参加反应的FePO4。
3种电化学模型解释了纯相磷酸铁锂材料无法耐受大电流的原因,也可以看出锂离子与电荷的迁移途径与扩散动力学是磷酸铁锂正极材料大功率应用的决定因素。
2 LiFePO4改性
由于磷酸铁锂正极材料本身较差的导电率和较低的锂离子扩散系数[12-13],国内外研究者在这些方面进行了大量的研究,也取得了一些很好的效果。其改性研究主要在3个方面:掺杂法、包覆法和材料纳米化。

图4 单个磷酸铁锂颗粒中锂离子脱/嵌的两种模型
2.1 掺杂法
掺杂法主要是指在磷酸铁锂晶格中的阳离子位置掺杂一些导电性好的金属离子,改变晶粒的大小,造成材料的晶格缺陷,从而提高晶粒内电子的导电率以及锂离子的扩散速率[14-17],进而达到提高LiFePO4材料性能的目的。目前,掺杂的金属离子主要有Ti4+、Co2+、Zn2+、Mn2+、La2+、V3+、 Mg2+等。
张俊喜等[18]在对钒掺杂改性研究分析时,得出钒离子在不同位掺杂均可以提高磷酸铁锂的性能,而铁位掺杂具有更好的效果。在0.1C放电时,放电比容量达到了145mA·h/g,放电比容量获得明显提升。通过对样品的交流阻抗谱图的分析研究,电荷转移阻抗由纯磷酸铁锂的110Ω降低到掺杂后的32Ω,电荷转移阻抗明显减小。
除了一元离子掺杂外,也可以进行多元离子同时掺杂。王震坡等[19]在氮气气氛下采用固相法,合成了Mg、Ti离子复合掺杂改性的正极材料(Li0.98Mg0.01)(Fe0.98Ti0.01)PO4/C。测试结果表明,复合离子掺杂可显著改善材料的电化学性能,模拟电池在0.2C和1C倍率下的放电比容量分别为154.7mA·h/g和146.9mA·h/g。以此复合掺杂样品为正极材料组装60A·h动力电池,其3C倍率放电容量仍保持为1C倍率放电容量的100%;低温0℃和-20℃测试条件下,动力电池放电容量分别保持为常温初始放电容量的89.7%和63.1%;在常温1C/1C充放电条件下,经过2000次循环后,电池容量依然保持为初始放电容量的89%,显示出优良的倍率放电性能和循环性能。
冯晓叁等[20]在对LiFePO4/C复合正极材料进行离子掺杂时,分别进行了单一Mn2+、Mg2+以及两种离子同时掺杂实验。结果表明,掺杂的LiMg0.1Fe0.9PO4/C、LiMn0.1Fe0.9PO4/C、LiFe0.8Mn0.1Mg0.1PO4/C在0.1C倍率下首次放电比容 量 分 别 为128.4mA·h/g、110.8mA·h/g、131.8mA·h/g。LiFe0.8Mn0.1Mg0.1PO4/C在10次循环后容量仍保持为96%,性能优于其他一元掺杂。说明在一定条件下,二元掺杂可以小幅度改善材料的性能。
针对离子掺杂来改变材料性能的研究,也有一些研究者认为掺杂效果与掺杂离子、掺杂浓度的关系不大。关于显著改善材料性能,倪江峰提出了怀疑,他认为用无机盐作前体,特别是用草酸亚铁作原料,难以区分残余热解碳与金属离子掺杂的效 果[21]。从众多研究成果来看,掺杂有可能改变材料的可逆循环特性,但至今还没有见到掺杂能改善磷酸铁锂材料本征导电率的严格实验证据。
2.2 包覆法
在LiFePO4材料表面包覆碳是提高电子电导率的一种有效方法,碳可以起到以下几个方面的作 用[7,22-25]:①抑制LiFePO4晶粒的长大,增大比表面积;②增强粒子间和表面电子的导电率,减少电池极化的发生;③起到还原剂的作用,避免Fe的生成,提高产品纯度;④充当成核剂,减小产物的粒径;⑤吸附并保持电解液的稳定。
近年来,针对碳包覆改进材料性能的研究一直都很活跃,新的方法也不断尝试,也取得了一定的成果。Hsieh等[26]在对碳含量对磷酸铁锂电化学性能的影响进行研究时,利用煅烧-热解法在650℃条件下合成有碳包覆的LiFePO4粉末,并通过控制葡萄糖的加入量来控制LiFePO4粉末中的含碳量。实验结果表明,适量的碳层在提高LiFePO4性能方面表现显著,但葡萄糖添加量太多,易于形成颗粒间的LiFePO4聚集,从而导致锂离子扩散速率的减慢和等效串联电阻的升高。通过测定,碳的最佳含量为2.55%(质量分数)。
黄远提等[27]采用改进的固相碳热还原法通过两步包碳法制备了双层碳包覆的LiFePO4正极材料。经分析表明,通过前体磷酸铁的碳包覆能有效控制产品双层碳包覆磷酸铁锂的颗粒大小,双层碳包覆不改变磷酸铁锂的晶体结构,0.1C倍率下首次放电比容量为150mA·h/g,循环50次后的比容量仅减少了3.9%。这表明制得的LiFePO4样品具有较好的电化学性能。
Dhindsa等[28]以CH3COOLi·2H2O、FeCl2、P2O5为前体与石墨烯的氧化物混合,使用溶胶-凝胶法合成LiFePO4/G复合材料。扫描电子显微镜和透射电子显微镜显示,LiFePO4颗粒被呈现三维导电网络的石墨烯片材料均匀覆盖着。通过对电导率的测定发现,复合材料的电导率为8.4×10-2S/cm而未加入石墨烯的磷酸铁锂电导率为5.0×10-8S/cm,其导电性有了大幅提升。在电化学性能方面,与未加入石墨烯的磷酸铁锂相比,也显示出了显著地大倍率(27C)充放电性能和优异的充放电循环(500次)稳定性。
碳包覆层的结构和形态对LiFePO4/C正极材料导电率影响很大,其结构决定了所加碳源的种类和处理方法。
Xing等[29]将FeCl3·6HO、(NH4)2HPO4、NH4OH混合,并加入一定量的溴化十六烷基三甲基铵(CATB)和淀粉作为碳源,制备出具有三维碳网结构的LiFePO4/C。通过对材料的电化学性能检测,其锂离子扩散系数D=1.00×10-10cm2/s,高于大多数使用CV数据计算的结果。在0.1C、10C与20C三种不同倍率放电条件下,其容量分别是166mA·h/g、110mA·h/g和95mA·h/g,且在20C倍率条件下完成1200次循环后,其容量仍然能达到74mA·h/g。通过对三维碳网的分析,其完整均匀的全碳涂层和连续的碳膜框架,构造出了电子的良好电导路径与有利的锂离子多孔扩散结构,从而提高了离子和电子的导电率。
Tang等[30]利用化学气相沉积法获得三维石墨烯,并利用制得的三维石墨烯高电导率、低电阻的三维电导网络引入LiFePO4,得到一种大容量、高传导率的磷酸铁锂/三维石墨烯(质量分数5%)的复合材料。在室温下,以0.2C倍率首次充放电,放电比容量可达158mA·h/g,循环35次后放电比容量仍然可达153mA·h/g;以10C倍率首次充放电,放电比容量可达109mA·h/g。通过对样品的交流阻抗谱图的分析研究,与纯LiFePO4相比,此复合材料的转移阻抗仅为90Ω,而纯LiFePO4为170Ω,充放电过程中电荷转移阻抗明显减小,从而有利于克服此过程中的动力学限制,使LiFePO4活性颗粒在高倍率充放电时嵌/脱锂深度得到提高,从而改善了电化学性能。
2.3 材料纳米化
相较在导电性方面的限制,锂离子在磷酸铁锂材料中的扩散是电池放电的最主要也是决定性的控制步骤。由于LiFePO4的橄榄石结构,决定了锂离子的扩散通道是一维的,因此可以减小颗粒的粒径来缩短锂离子扩散路径,从而达到改善锂离子扩散速率的问题。纳米材料的优点主要有[31-34]:①纳米材料具有高比表面积,增大了反应界面并可以提供更多的扩散通道;②材料的缺陷和微孔多,理论储锂容量高;③因纳米离子的小尺寸效应,减少了锂离子嵌入脱出深度和行程;④聚集的纳米粒子的间隙缓解了锂离子在脱嵌时的应力,提高了循环寿命;⑤纳米材料的超塑性和蠕变性,使其具有较强的体积变化承受能力,而且可以降低聚合物电解质的玻璃化转变温度。
Ren等[35]对纳米化的磷酸铁锂制备进行了详细的研究,他们利用亲水性的碳纳米颗粒作为模型制备出介孔磷酸铁锂正极材料。发现其具有亚微米大小的颗粒中心在2.9nm和30nm的双峰孔分布,介孔的引入也有利于电解质的流动和锂离子的扩散。在1C倍率下,放电比容量为137mA·h/g。在30C高倍率充放电后,材料的容量仍能恢复到160mA·h/g。可以看出纳米化的磷酸铁锂电化学性能得到了显著地提升。
除了单独对磷酸铁锂正极材料纳米化研究外,很多研究者也进行了材料纳米化与碳包覆、离子掺杂相结合的方法进行改性研究,也取得了很好的 成果。
从长杰等[36]利用液相沉淀法合成了纳米级磷酸铁,并以此为铁源,通过碳热还原技术制备了粒径均匀的纳米级球形LiFePO4/C正极材料。经分析检验结果表明,材料的首次放电比容量达161.8mA·h/g,库仑效率为98.3%,室温下在0.2C、0.5C、1C、2C及5C倍率充放电其首次放电比容量分别为156.5mA·h/g、144mA·h/g、138.9mA·h/g、125.6mA·h/g和105.7mA·h/g,材料具有较好的电化学性能。
Chen等[37]以偏磷酸亚铁和石墨的纳米层状模板,通过水热法制备出拥有纳米层状形态的LiFePO4颗粒。通过SEM分析,尽管原纳米层模板和LiFePO4纳米层模板之间存在差异,但最终得到的LiFePO4模板的纳米层状态保存完好。拉曼光谱表明,原纳米有机基团的分层模板成功地转换成细小的具有有序石墨结构的碳颗粒,并很好地分散在层状LiFePO4颗粒之间。经使用循环伏安法和电阻抗法评估,锂离子扩散系数分别是1.5×10-11cm2/s和3.1×10-13cm2/s,而电子电导率为3.28mS/cm,远远高于普通LiFePO4的电导率(<10-9S/cm)。纳米层状结构的LiFePO4颗粒表现出了显著的循环性能和可逆性。
Kuwahara等[38]利用水热合成法,将聚乙二烯乙二醇加入溶液中,获得了良好的磷酸铁锂颗粒,并向溶液中加入乙炔黑、等体积的表面活性剂以及等量的碳。将溶液搅拌24h,导入耐压容器,在150℃、N2保护下水热合成3h,获得的LiFePO4/C化合物在1%N2-99%Ar的气氛、500℃条件下煅烧1h后得到具有碳包覆的纳米级磷酸铁锂材料。经XRD和SEM分析,表明LiFePO4/C化合物存在微结构:每个尺寸接近50nm的碳颗粒的表面覆盖着一个磷酸铁锂薄层或埋在磷酸铁锂的集合体中。这使得LiFePO4/C表面相互接触,减小了锂离子的扩散距离,从而提高了材料的电化学性能。
Liu等[39]将CH3COOLi·2H2O、Fe2O3、Fe、NH4H2PO4以摩尔比3∶1∶1∶3和适量的柠檬酸混合,在氮气条件下通过传统的固相合成法制得纳米级LiFePO4/C复合材料。经TEM分析,所得LiFePO4/C复合材料颗粒大小在50~70nm,具有纳米结构。在电化学性能方面,其首次放电容量为162.4mA·h/g,在循环30次后,其容量仍达到166.6mA·h/g。分析其原因,初始放电容量可归因于纳米颗粒,其提供了更大的表面积和较短的扩散距离;而此后容量的增加可能是由式(3)的反应产生的Fe2P所引起的,而少量Fe2P可以提高材料的电化学性能。
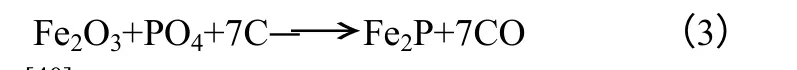
Yang等[40]以Fe(NO3)3·9H2O、LiH2PO4为原料,以具有超导电性炭黑科琴黑为碳源,采用液相沉积法制备出具有纳米结构的LiFePO4/KB复合材料。在-20℃条件下,分别以1C、5C、10C、20C倍率放电测试,其放电容量分别为120.2mA·h/g、100.1mA·h/g、85.5mA·h/g、64.5mA·h/g;此外,在循环200次之后,其容量仍保持在90%以上。经SEM分析,复合材料具有均匀的颗粒尺寸和三维网络结构,LiFePO4颗粒大约在10nm,嵌入在介孔颗粒科琴黑上。正是由于材料的这种纳米结构,使得LiFePO4与科琴黑之间存在一种“桥效应”,有利于锂离子和电子的传输,使得复合材料在低温条件下具有良好的充放电高倍率性和循环性能。
3 结 语
采用离子掺杂、包覆、材料纳米化3种改性方法对磷酸铁锂正极材料在电导率低、锂离子扩散速率慢、低温放电性能差等方面的不足有很大的改进。其中离子掺杂通过掺杂导电性好的离子,改变了颗粒大小,造成材料的晶格缺陷,从而提高了材料电子的电导率和锂离子的扩散率;包覆主要以碳包覆为主,抑制LiFePO4晶粒的长大,增大了比表面积,从而增强粒子间和表面电子的导电率;材料的纳米化一方面增大了材料的比表面积,为界面反应提供更多的扩散通道,另一方面,缩短了离子扩散的距离,减小了锂离子在脱嵌时的应力,提高循环寿命。
此外,磷酸铁锂正极材料改性方面仍存在一些不足,如离子掺杂改进材料的导电率和锂离子扩散速率方面仍存在分歧;纳米材料的制备工艺、生产成本要求较高;此外,除了考虑实验室条件下的可行性研究外,还要考虑大规模工业化的生产要求,这些都有待于进一步研究。因此,通过以上方法来全面提高磷酸铁锂的综合性能仍然是当前和今后该领域研究和应用的主要发展方向之一。
[1] 梁广川. 锂离子电池磷酸铁锂正极材[M]. 北京:科学出版社,2013.
[2] 唐致远,邱瑞玲,滕国鹏,等. 锂电池正极材料LiFePO4的研究进展[J]. 化工进展,2008,27(7):995-1000.
[3] 谢晓华,张建,李佳,等. 磷酸铁锂电池低温性能的研究[J]. 华南师范大学学报:自然科学版,2009(A02):113-114.
[4] Padhi A K,Nanjundaswamy K S,Goodenough J B. Phospho-olivines as positive electrode materials for rechargeable lithium batteries[J].Journal of the Electrochemical Society,1997,144(4):1188-1194.
[5] Andersson A S,Thomas J O. The source of first-cycle capacity loss in LiFeP4[J].Journal of Power Sources,2001,97:498-502.
[6] Xu Bo,Qian Danna,Wang Ziying,et al. Recent progress in cathode materials research for advanced lithium ion batteries[J].Materials Science and Engineering R,2012,73(1):57-60.
[7] 朱敏,盘毅,郑春满. 功率型LiFePO4锂离子电池正极材料的设计与制备研究进展[J].材料导报:综述篇,2012,26(9):143-149.
[8] 张嵩,丁广乾,胡铁军,等. 磷酸铁锂电池性能与应用研究[J]. 山东电力技术,2012,3:66 .
[9] 倪江峰,苏光耀,周恒辉,等. 锂离子电池正极材料LiMPO4的研究进展[J]. 化学进展,2003,4(16):554-559.
[10] 崔学军,李国军,卢俊峰,等. 正极材料LiFePO4充放电原理及改性研究[J]. 材料导报:综述篇,2010,24(6):53-54.
[11] Zhang S S,Allen J L,Xu K,et al. Optimization of reaction condition for solid state synthesis of LiFePO4-C composite cathodes[J].Power Sources,2005,147:234-240.
[12] Lee S B,Cho S H,Cho S J,et al. Synthesis of LiFePO4material with improved cycling performance under harsh conditions[J].Electrochemistry Communications,2008,10:1219-1221.
[13] Yu F,Zhang J,Yang Y,et al. Reaction mechanism and electrochemical performance of LiFePO4/C cathode materials synthesized by carbothermal method[J].Electrochimica Acta,2009,54(1):7389-7395.
[14] 窦俊青,康雪雅,吐尔迪·吾买尔,等. Mn掺杂LiFePO4的第一性原理研究[J]. 物理学报,2012,61(8):1-6.
[15] Shu Hongbo,Wang Xianyou,Wen Weicheng,et al. Effective enhancement of electrochemical properties for LiFePO4/C cathode material by Na and Tico-doping[J].Electrochimica Acta,2013,89:479-487.
[16] Baster Dominika,Zheng Kun,Zajac Wojciech,et al. Toward elucidation of delithiation mechanism of zinc-substituted[J].Electrochimica Acta,2013,92(1):79-86.
[17] 刘洪权,郑田田,郭倩颖,等. 锂离子电池正极材料磷酸铁锂研究进展[J]. 稀有金属材料与工程,2012,41(4):748-752.
[18] 张俊喜,许明玉,颜立成,等. 锂离子电池正极材料磷酸铁锂的钒掺杂改性研究[C]//第七届中国功能材料及其应用学术会议论文集,2010:172-175.
[19] 王震坡,刘文,王悦,等. Mg、Ti离子复合掺杂改性磷酸铁锂正极材料及其电池性能[J]. 物理化学学报,2012,28(9):2084-2090.
[20] 冯晓叁,莫祥银,俞琛捷,等. 锂离子电池LiFePO4/C复合正极材料掺杂金属离子的制备及改性研究[J]. 材料导报:研究篇,2012,26(10):33-37.
[21] 倪江峰,周恒辉,陈继涛,等. 金属氧化物掺杂改善LiFePO4电化学性能[J]. 无机化学学报,2005,21(4):472-476.
[22] 王文琴,郭志猛,姜冰,等. 碳热还原法制备LiFePO4/C锂电池正极材料的研究[J]. 稀有金属,2012,36(4):578-583.
[23] Liu H,Li C,Zhang H P,et al. Kinetic study on LiFePO4/C nanocamposites synthesized by solid state technique[J].Journal of Power Sources,2006,159(1):717-720.
[24] 蒋志君. 锂离子电池正极材料磷酸铁锂:进展与挑战[J]. 功能材料,2010,41(3):365-368.
[25] Zhang Yong,Huo Qingyuan,Du Peipei,et al. Advances in new cathode material LiFePO4for lithium-ion batteries[J].Synthetic Metals,2012,162(1):1319-1322.
[26] Hsieh C T,Pai C T,Chen Y F,et al. Preparation of lithium iron phosphate cathode materials with different carbon contents using glucose additive for Li-ion batteries[J].Journal of the Taiwan Institute of Chemical Engineers,2014,815(1):1-8.
[27] 黄远提,卢周广,郭忻,等. 双层碳包覆LiFePO4合成和电化学性能研究[J]. 电池工业,2012,17(1):20-27.
[28] Dhindsa K S,Mandal B P,Bazzi K,et al. Enhanced electrochemical performance of graphene modified LiFePO4cathode material for lithium ion batteries[J].Solid State Ionics,2013,253(1):94-100.
[29] Xing Yutao,He Yanbing,Li Baohua,et al. LiFePO4/C composite with 3D carbon conductive network for rechargeable lithium ion batteries[J].Electrochimica Acta,2013,109(1):512-518.
[30] Tang Yufeng,Huang Fuqiang,Bi Hui,et al. Highly conductive three-dimensional graphene for enhancing the rate performance of LiFePO4cathode[J].Journal of Power Sources,2012,203:130-134.
[31] Kim Haegyeom,Kim Hyungsub,Kim Sung Wook,et al. Nano-graphite platelet loaded with LiFePO4nano particles used as the cathode in a high performance Li-ion battery[J].Sciverse Science Direct,2012,50(1):1966-1971.
[32] 梁风. 孔状纳米级锂离子电池正极材料磷酸铁锂的制备与研究[D]. 昆明:昆明理工大学,2009.
[33] 倪聪,莫祥银,俞琛捷,等. 纳米磷酸铁锂的研究进展[J]. 化工新型材料,2010,38(5):1-4.
[34] Song M K,Park S,Alamgir F M,et al. Nanostructured electrodes for lithium ion and lithium-air batteries the latest developments,challenges,and perspectives[J].Materials Science and Engineering R,2011,72(1):220-224.
[35] Ren Yu,Bruce Peter G. Mesoporous LiFePO4as a cathode material for rechargeable lithium ion batteries[J].Electrochemistry Communications,2012,17(1):60-62.
[36] 从长杰,张向军,卢世刚,等. 纳米磷酸铁锂的制备及电化学性能研究[J]. 无机化学学报,2011,27(7):1319-1323.
[37] Chen Jin,Yan Liuming,Yue Baohua. Nano-layered LiFePO4particles converted from nano-layered ferrous phenylphosphonate templates[J].Journal of Power Sources,2012,209(1):7-14.
[38] Kuwahara A,Suzuki S,Miyayama M,et al. High-rate properties of LiFePO4/carbon composites as cathode materials for lithium-ion batteries[J].Ceramics International,2008,34:863-866.
[39] Liu Haowen,Tang Dingguo. The low cost synthesis of nanoparticles LiFePO4/C composite for lithium rechargeable batteries[J].Solid State Ionics,2008,179(1):1897-1901.
[40] Yang Xu,Xu Yunlong,Zhang Huang,et al. Enhanced high rate and low-temperature performances of mesoporous LiFePO4/Ketjen Black nanocomposite cathode material[J].Electrochimica Acta,2013,114(1):259-264.
