柱后碘衍生—高效液相色谱法测定脂必妥片中黄曲霉毒素B1的含量
2015-08-01罗霄,代琪,曾桢,汪丹
罗 霄,代 琪,曾 桢,汪 丹
(1.成都市食品药品检验研究院,四川 成都 6101061;2.成都大学 基础医学与护理学院,四川 成都 610106;3.四川大学 华西药学院,四川 成都 610041)
0 引 言
脂必妥片收载于国家食品药品监督管理局国家药品标准WS-11524(ZD-1524)-2002-2013Z,由红曲单味药制备而成,具有健脾消食、除湿祛痰、活血化瘀的功效,常用于脾瘀阻滞、症见气短及高血脂症等疾病的辅助治疗.由于红曲制备过程中易产生黄曲霉毒素(Aflatoxin,AFT),该毒素是黄曲霉和寄生曲霉中产毒菌株的代谢产物,普遍存在于霉变的粮食及粮食制品中,长期摄入对人体会造成极大伤害[1-2].黄曲霉毒素主要有4 种,G1、G2、B1、B2,其中B1 被认为是主要的有毒物质[3].研究发现,黄曲霉毒素B1(AFT B1)含有一个双呋喃环和一个氧杂萘邻酮(香豆素),前者为基本毒性结构,后者与致癌有关[4].鉴于AFT B1 对人体的危害,建立AFT B1 高效定量的检测方法已成为研究重点.对此,本研究采用有机溶剂提取、免疫亲和柱(IAC)净化分离和柱后碘衍生—高效液相色谱法,建立了AFT B1 的含量测定方法,拟为该制剂的安全保证提高提供科学依据.
1 仪器与试药
1.1 仪 器
实验所用仪器包括:Waters2998 高效液相色谱仪,荧光检测器,AE-240 电子天平(德国赛多利斯公司),AUX-220 电子天平(日本岛津仪器公司),SK250H 超声仪(上海科导超声仪器有限公司),TGL-16G 离心机(上海安亭科学仪器厂).
1.2 试药与试剂
实验所用试药与试剂包括:AFT B1(批号,Pribolab STD#1041 1200823,25 μg/mL);玻璃滤纸为WhatmanTM(Diameter 110 mm);流动相中的甲醇和乙腈为色谱纯(德国LiChrosolv);水为超纯水,其余试剂均为分析纯;脂必妥片(批号,S120904、S120905、S120906)由成都地奥九鸿制药厂提供.
2 方法与结果
2.1 色谱条件
实验的色谱条件:十八烷基硅烷键合硅胶为填充剂;以甲醇—乙腈—水(40∶ 18∶ 42)为流动相,流速为0.8 mL/min;采用柱后衍生法检测,衍生溶液为0.05%的碘溶液(取碘0.5 g,加入甲醇100 mL 使溶解,用水稀释至1 000 mL 制成),衍生化泵流速为0.3 mL/min,衍生化温度70 ℃;以荧光检测器检测,激发波长λex 为360 nm,发射波长λem 为450 nm.
2.2 对照品溶液的制备
精密量取AFT B1 对照品(25 μg/mL)0.4 mL,置100 mL 量瓶中,用甲醇稀释至刻度,摇匀,作为储备液.精密量取储备液1 mL,置500 mL 量瓶中,加70%甲醇稀释至刻度,摇匀,制得对照品溶液(每1 mL AFT B1 为0.2 ng).
2.3 供试品溶液的制备
取脂必妥片40 片,研细,精密称取5.0 g,加入氯化钠4 g,置具塞锥形瓶中,精密加入80%甲醇50 mL,称定重量,超声处理(250W,40 kHz)20 min,放冷后再称定重量,用80%甲醇补足减失的重量,离心3 min(5 000r/min),精密量取上清液5 mL,置25 mL 量瓶中,加80%甲醇稀释至刻度,摇匀,用玻璃纤维滤纸滤过,精密量取续滤液10 mL,通过免疫亲和柱(AflaT-est@P),流速为3 mL/min,用10%甲醇溶液洗涤烧杯和针筒等,将洗液过柱,再用水10 mL洗脱(流速为4.0 mL/min),弃去洗脱液,吹气除去柱中水滴,再用1.5 mL 甲醇,以每秒1 滴的速度洗脱,收集洗脱液,置2 mL 量瓶中,用甲醇稀释至刻度,摇匀,制得供试品溶液.
2.4 检出限测定
取“2.2”项下AFT B1 对照品溶液1 mL 至10 mL 量瓶中,加70%甲醇稀释至刻度,摇匀,制得每1 mL AFT B1 为0.02 ng,进样4 μL,计算信噪比与进样浓度,测得其检出限为,0.5 μg/kg.
2.5 线性关系考察
精密吸取AFT B1 对照品溶液,分别依次进样4、8、10、12、16、20 μL,测定色谱峰面积.将AFT B1 的色谱峰面积(Y)与进样量(X)回归,其回归方程为,
Y=5.6481 ×107X-8.2347 ×103,r=0.9999
故方法的线性范围为,0.0008 ng ~0.004 ng.
2.6 精密度实验
精密吸取AFT B1 对照品溶液(0.2 ng·mL-1)10.0 μL,按“2.1”项下色谱条件连续重复进样6次,计算仪器精密度,其RSD 为0.80%.
2.7 重复性实验
精密称取同一批号(S120904)的脂必妥片供试品6 份,按“2.3”项下供试品的制备方法平行操作,进样分析,记录峰面积,其RSD 为1.05%.
2.8 稳定性实验
精密吸取对照品溶液(0.2 ng·mL-1)于0、2、6、8、10、12 h 分别进样10.0 μL,记录峰面积,其RSD 为0.94%.
2.9 回收率实验
精密称取已知含量(0.6 ng·g-1)的脂必妥片,约2.5 g,按1∶ 1 的比例分别加入一定量的AFT B1对照品,按“2.3”项下的方法制备成供试品溶液,依法测定并计算加样回收率,结果见表1.
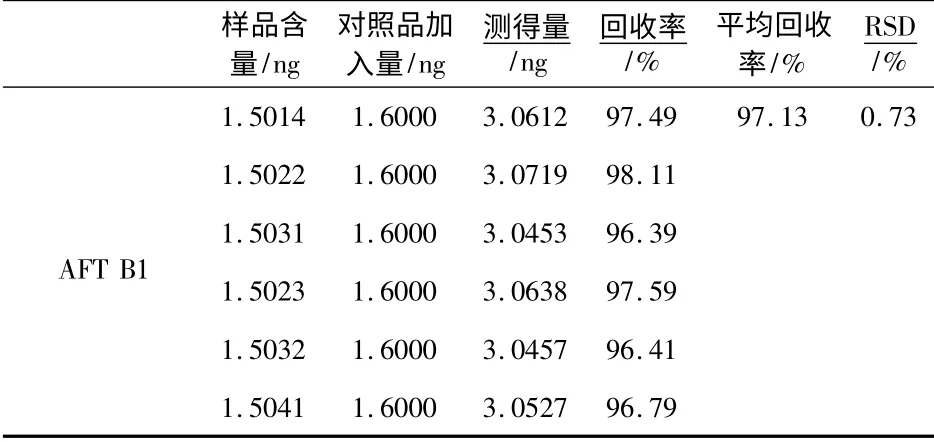
表1 回收率的测定结果
2.10 样品测定
采用标准曲线法计算含量,取供试品溶液10 μL,注入高效液相色谱仪,按“2.1”项下色谱条件测定,从随行标准曲线中计算出含量,结果见表2.

表2 样品测定结果(n=3)
3 讨 论
3.1 提取溶剂
AFT B1 易溶于带极性的溶剂而不溶于非极性溶剂中,一般采用几种有机溶剂中加入少量水可以增强有机溶剂对样品的渗透力.实验比较了甲醇—水、乙腈—水、丙酮—水和三氯甲烷等几种溶剂,均得到较高的回收率,其中以甲醇—水(80∶ 20)和丙酮—水(85∶ 15)提取效果最好,考虑到甲醇—水的适应性更广,选择前者作为样品的提取溶剂.
3.2 提取溶剂与样品量比例
实验比较了溶剂量/样品量分别为4∶ 1、8∶ 1 和10∶ 1,结果显示,溶剂量/样品量为10∶ 1 提取效率最高,样品干扰杂质最少,可以基本达到提取完全.
3.3 样品净化除杂
实验发现,样品过柱时,流速对回收率结果影响较大,经比较样品过柱流速为3.0 mL/min,水洗涤柱子流速为4.0 mL/min,能满足回收率测定要求;另样品液过柱后再用10%甲醇溶液洗涤烧杯和针筒等,将洗液一并过柱,能提高测定结果.
3.4 实验中应注意的事项
实验过程尽量避免日光照射.样品溶液采用玻璃纤维滤纸滤过.经过水洗涤后的柱子,甲醇洗脱前,柱子中水滴的残留对测定结果有较大影响.
[1]刘艳丽,程安春,汪铭书.黄曲霉毒素及其检测方法的研究进展[J].黑龙江畜牧兽医,2006,49(6):15-17.
[2]黄惠明,徐群英,胡敏.黄曲霉毒素检测方法研究的概述[J].中国卫生检验杂志,2001,11(4):510-512.
[3]杨一刚.黄曲霉毒素B1 测定方法的探讨[J].科技情报开发与经济,2004,14(8):168-169.
[4]柳洁,何碧英.黄曲霉毒素高效液相色谱检测方法研究进展[J].中国卫生检验杂志,2005,7(15):891-896.
