Cu掺杂对锂离子电池正极材料Li[NiCoMn]1/3O2的影响
2015-07-10王东吴照金
王东 吴照金

摘 要:采用共沉淀法合成锂离子电池正极材料Li[(NiCoMn)1-xCux]1/3O2(x=0、0.01和0.02),通过X射线衍射、恒流充放电和循环伏安测试手段,考察了不同掺Cu量对所合成材料的结构和电化学性能的影响。结果表明,Li[(NiCoMn)0.99Cu0.01]1/3O2与未掺杂的XRD图谱相似,过多掺杂导致杂质相CoCu2O3生成;所有样品中,Li[(NiCoMn)0.99Cu0.01]1/3O2具有最优的容量保持率和可逆性。
关 键 词:锂离子电池;正极材料;Li[NiCoMn]1/3O2;Cu掺杂
中图分类号:TM 311 文献标识码: A 文章编号: 1671-0460(2015)10-2335-03
Effect of Cu Dopig on Li[NiCoMn]1/3O2 as Cathode
Material for Lithium Ion Batteries
WANG Dong, WU Zhao-jin
(Anhui Provincial Key Laboratory of Metallurgy Engineering & Resoruces Recycling, Anhui University of Technology,
Anhui Maanshan 243000, China)
Abstract: Li[(NiCoMn)1-xCux]1/3O2 (x=0, 0.01 and 0.02) were synthesized by co-precipitation method. The structure and electrochemical properties of samples were investigated through XRD, galvanostatic charge/discharge and cyclic voltammetry. The results show that Li[(NiCoMn)0.99Cu0.01]1/3O2 has similar XRD patterns with Li[NiCoMn]1/3O2. The excess Cu doping can leads to generation of CoCu2O3. Li[(NiCoMn)0.99Cu0.01]1/3O2 possesses the best capacity retention and reversibility among all the samples.
Key words: Lithium ion batteries; Cathode material; Li[NiCoMn]1/3O2; Cu doping
三元正极材料Li[NiCoMn]1/3O2在便携式电子设备的锂电池中已广泛使用,随着其大规模用于电动汽车动力电源,废旧锂电池活性材料的回用问题亟待研究。研究表明,湿法回收废旧锂电池及三元材料再生极具前景[1]。由于锂离子电池多以铜箔为负极集流体,采用湿法回收锂离子电池正极材料中的有价元素Ni、Co、Mn时,溶液中同时存在Cu2+,目前普遍采用的方法是先将Cu2+分离去除,再行回收Ni、Co、Mn[2]。
以废旧锂离子电池为原料,再生Li[NiCoMn]1/3O2正极材料时,能否利用Cu作为有利的掺杂元素,而不是刻意的除去它?为了回答这个问题,我们必须搞清楚Cu是否能掺入Li[NiCoMn]1/3O2的层状结构中,以及对其电化学性能的影响。
本文采用试剂为原料,以Cu同时取代Ni、Co、Mn进行配料,研究Cu掺杂对Li[NiCoMn]1/3O2的结构和电化学性能的影响。
1 实验部分
1.1 材料的合成
配制1 mol/L的硫酸盐溶液(镍、钴、锰的浓度比为1∶1∶1)、1 mol/L的碳酸钠、0.5 mol/L的氨水,在空气气氛中,将上述三种溶液同时滴加到有底液的反应容器中。严格控制搅拌速率(1 000 r/min)和温度(55 ℃),调节氨水的滴加速率维持体系的pH在8附近,反应结束后进行抽滤、洗涤、真空干燥,得到前驱体[NiCoMn]1/3CO3。
Li[(NiCoMn)1-xCux]1/3O2(x=0、0.01、0.02)的制备,按照化学计量比n(Li)∶nM(M=Ni+Co+Mn+Cu)=1.05称取一定量LiOHH2O、[NiCoMn]1/3CO3、Cu2(OH)2CO3,两次球磨,分段煅烧(500 ℃5 h + 900 ℃12 h)后即为所得产物。
1.2 材料的表征
使用X射线衍射仪(XRD,D8 Advance,德国)表征Li[(NiCoMn)1-xCux]1/3O2的晶体结构。
1.3 电化学性能测试
将正极活性物质、导电剂(乙炔黑)、粘结剂(PVDF)按80∶10∶10的质量比混合研磨,以1-甲基-2-吡咯烷酮为分散剂,浆料调制到一定程度涂覆于铝片,将涂覆后的极片于普通烘箱50 ℃缓慢烘干,之后转入真空烘箱于110 ℃干燥10 h,得到所需的极片。在高纯氩气气氛手套箱中,以上述极片为正极,金属锂为负极,Celgard 2400 聚丙烯为隔膜,1.0 mol/L LiPF6的碳酸乙烯酯、碳酸二甲酯、碳酸乙基甲酯(体积比1∶1∶1)为电解液,组装CR2025扣式模拟电池。
在Arbin电池测试仪(美国)上进行恒流充放电测试,0.1C倍率下的电流密度为16 mA/g;循环伏安扫描速率为0.1 mV/s。
2 结果与讨论
2.1 XRD 分析
掺杂量为1%的试样与Li[NiCoMn]1/3O2的XRD图谱相似,如图1所示。当掺杂量为2%时,在40.2°附近出现杂质峰,经检索比对,该杂质峰对应的物质可能是CoCu2O3(PDF#76-0442)或者MnO(PDF#72-1553)。本实验所用材料是在空气气氛下,900 ℃煅烧12 h所得,而MnO在空气中加热时易转变为Mn的高价氧化物(Mn3O4、MnO2、Mn2O3等),所以样品不会含有MnO,杂质相应为CoCu2O3。Cu的离子半径均大于Ni、Co、Mn的,结合上述结果,掺杂量为1%时,认为Cu2+进入Li[NiCoMn]1/3O2晶体结构中,XRD图谱中无杂质峰、主峰向小角度方向偏移可以为证。当掺杂Cu的量等于2%时,这时的Cu可分为三种存在形式,第一部分Cu取代Ni、Co、Mn,第二部分取代配料中的Co,第三部分与多余的Co形成杂质相CoCu2O3。由XRD分析结果可知,Cu取代Ni、Co、Mn的量应控制在1%以内,不宜过多掺杂。
图1 Li[(NiCoMn)1-xCux]1/3O2的XRD图谱
Fig.1 XRD patterns of Li[(NiCoMn)1-xCux]1/3O2 samples
2.2 首次放电及循环性能
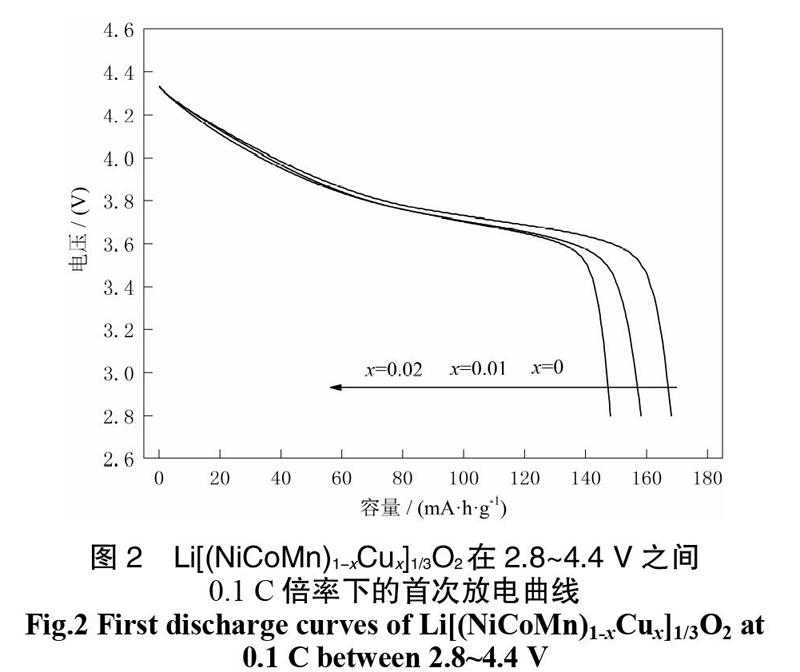
图2为Cu掺杂Li[(NiCoMn)1-xCux]1/3O2试样在电压窗口2.8~4.4 V、0.1 C倍率下的首次放电曲线。Li[(NiCoMn)1-xCux]1/3O2(x=0、0.01和0.02)的放电容量依次为168.1、158.2和148.1 mA·h/g。
图2 Li[(NiCoMn)1-xCux]1/3O2在2.8~4.4 V之间
0.1 C倍率下的首次放电曲线
Fig.2 First discharge curves of Li[(NiCoMn)1-xCux]1/3O2 at 0.1 C between 2.8~4.4 V
在以上电压范围内充放电时,只有Ni元素参加氧化还原反应[3],如果把Li[NiCoMn]1/3O2的容量185.3看成1的话,理论上掺杂量每增加1%,其放电克容量应减少0.67%(1.12 mA·h/g)。但实际容量的减少量与掺杂量不成比例且远大于理论值,这可能是由于在Cu取代Ni、Co、Mn的前提下,为了保持电荷平衡,二价镍被氧化成三价镍,另一个原因是只有部分铜掺杂到Li[NiCoMn]1/3O2的晶格中,XRD的结果已经显示有杂相,新化合物的形成必然影响充放电容量。后者可能性更大,杂质相CoCu2O3的出现,说明Cu更易于取代Co,而不是同时取代Ni、Co、Mn。
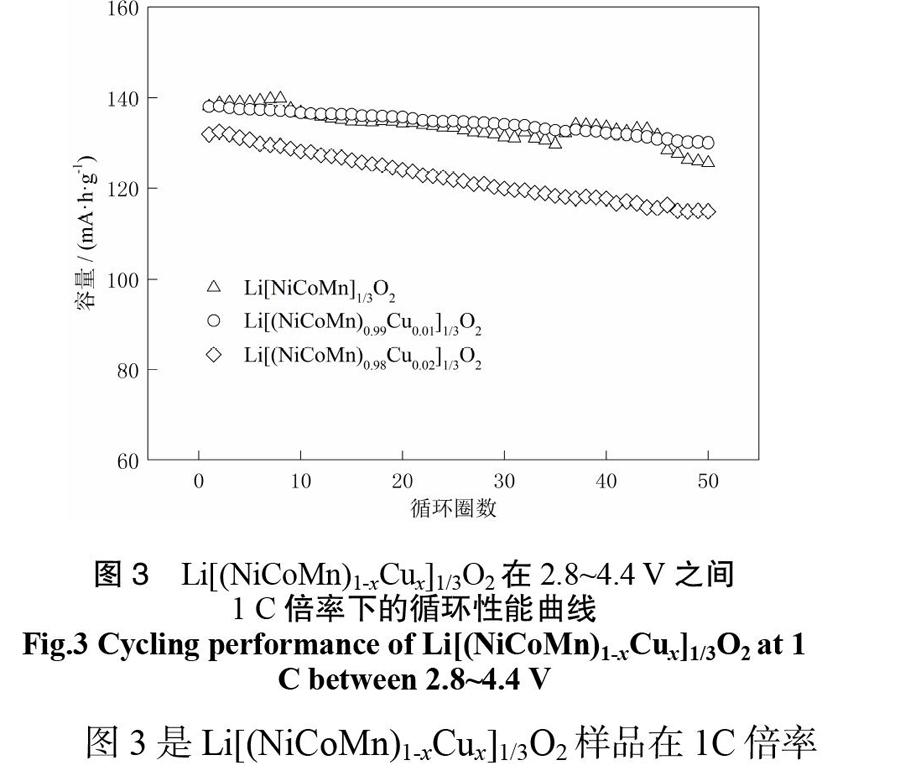
图3 Li[(NiCoMn)1-xCux]1/3O2在2.8~4.4 V之间
1 C倍率下的循环性能曲线
Fig.3 Cycling performance of Li[(NiCoMn)1-xCux]1/3O2 at 1 C between 2.8~4.4 V
图3是Li[(NiCoMn)1-xCux]1/3O2样品在1C倍率下的循环性能曲线。对应于x=0、0.01和0.02,初始容量分别为138.1、138.0、131.9 mA·h/g,经过50次充放电循环后,容量保持率分别为91.0%、94.2%、87.1%。当Cu掺杂量为1%时,Li[(NiCoMn)0.99Cu0.01]1/3O2的循环性能优于Li[NiCoMn]1/3O2,在2.8~4.4 V电压窗口之间,少量的Cu掺杂有益于Li[NiCoMn]1/3O2的循环性能,过多掺杂时,杂相的生成导致循环性能下降,所以Cu取代Ni、Co、Mn的最佳量为1%。
2.3 循环伏安(CV)分析
图4 样品在0.1 mV/S扫描速率下的CV曲线
Fig.4 CV curves of samples at the rate of 0.1 mV/S
相同条件下合成Li[(NiCoMn)1-xCux]1/3O2的CV图谱如图4所示。由图可知,2.8~4.4 V之间出现对称的氧化还原特征峰,峰形较为明显,可归属于锂离子在具有典型层状结构的Li[NiCoMn]1/3O2中的脱出和嵌入,3.6~3.7 V之间的峰为Ni2+/Ni4+的还原峰,3.8~4.0 V之间的峰为Ni2+/Ni4+的氧化峰,4.5 V的峰附近为Co3+/Co4+的氧化还原峰[4]。CV曲线中氧化还原峰电势分别用Vcathodic和Vanodic表示,ΔV(ΔV=Vcathodic-Vanodic)为氧化还原峰之间的差值,代表极化程度,数值越小说明电池的极化程度越低,可逆性越好[5]。结合图4和表1中的数据可知,Li[(NiCoMn)0.99Cu0.01]1/3O2的ΔV小于未掺杂试样,但随着Cu掺入量增加,ΔV变大。样品中,Li[(NiCoMn)0.99Cu0.01]1/3O2的ΔV最小,说明其具有最好的可逆性,这与上述Li[(NiCoMn)0.99Cu0.01]1/3O2具有最优的循环性能的结论相符。
表1 Li[(NiCoMn)1-xCux]1/3O2的CV测试结果
Table 1 CV data of Li[(NiCoMn)1-xCux]1/3O2
Li[(NiCoMn)1-xCux]1/3O2 Vcathodic/V Vanodic/V ΔV/V
x=0 3.856 3.683 0.173
x=0.01 3.840 3.683 0.157
x=0.02 3.863 3.670 0.193
3 结 论
Cu取代Ni、Co、Mn,当掺杂量大于1%时出现杂相,初步认为杂相是CoCu2O3。0.1 C倍率下,对应于x=0、0.01、0.02,首次放电容量随着Cu掺杂量的增加而降低,在1 C倍率下,经过50圈循环后的容量保持率分别为91.0%、94.2%、87.1%,CV证实了Li[(NiCoMn)0.99Cu0.01]1/3O2具有最佳的可逆性。
参考文献:
[1] 高岩,李金辉,李鹏举,等.由电池废料制备镍钴锰三元正极材料性能研究[J].电源技术,2013,37(6):934-936.
[2] 陈亮,唐新村,张阳,等.从废旧锂离子电池中分离回收钴镍锰[J].中国有色金属学报,2011,21(5):1192-1198.
[3] Ren H, Huang Y, Wang Y, et al. Effects of different carbonate precipitators on LiNi1/3Co1/3Mn1/3O2 morphology and electrochemical performance[J]. Materials Chemistry and Physics, 2009, 117(1): 41-45.
[4] 王海燕,唐爱东,黄可龙,等.LiNi1/3Co1/3Mn1/3O2正极材料的制备与倍率性能研究[J].无机化学学报,2008,24(4):593-599.
[5] Gao P, Yang G, Liu H. Lithium diffusion behavior and improved high rate capacity of LiNi1/3Co1/3Mn1/3O2 as cathode material for
lithium batteries[J]. Solid State Ionics, 2012, 207: 50-56.
氟化工的未来发展方向
“十三五”期间,我国氟化工行业应增强自主创新能力,提升行业整体技术水平,发展高端产品,延伸产业链条,力争到2020年成为产业结构更加合理、发展后劲和风险应对能力大幅增强的氟化工强国。
从全球看,发达国家氟化工产能正在向发展中国家转移,但其依旧把持高端的氟材料、ODS替代品、氟精细化学品、功能制剂等垄断控制地位;随着全球气候变暖日益受到重视,新一代低GWP(全球变暖潜能值)的产品开始大规模应用生产。从国内来看,随着工业转型升级步伐加快,汽车、电子、轻工、新能源、环保、航空航天等相关产业对高性能氟聚合物、新型制冷剂和含氟精细化学品需求迫切,发展空间较大。含氟涂料综合性能优异,预计未来我国氟涂料市场需求潜力较大,用于涂料的氟树脂也将呈现较快增长态势。《蒙特利尔议定书》修正案将气候变化纳入其中,对制冷剂产业发展将有重大影响。行业人士表示我国氟化工行业全球规模最大,但缺乏核心技术,比如低GWP的第四代制冷剂氢氟烯烃类产品(HFOs)自主技术还欠突破。下一步应从化合物筛选、性能评价、合成工艺研究等源头做起,加大原始创新研发力度,同时还要研发含氟电子气体、医药农药中间体等新产品。氟化工未来将向着深加工及产业链延伸发展。比如依托氢氟酸产品,可探索深加工开发电子级氢氟酸,作为动力锂电池、电子芯片及太阳能光伏等项目配套产品;也可发展含氟油田化学品、氟碳涂料等。