4 4
2015-07-10张应鹏谭伟杨云裳
张应鹏 谭伟 杨云裳


摘 要:设计了一种合成4,4'-二羟基联苯的新方法,以联苯为原料,经Friedel-Crafts酰基化反应、Baeyer-Villiger氧化反应、酯水解反应得到4,4'-二羟基联苯。中间体和产物的结构均经1H NMR、元素分析和熔点仪进行表征确认,并且对反应条件进行了优化,取得了较高的收率。
关 键 词:4,4'-二羟基联苯; 联苯; Friedel-Crafts酰基化; Baeyer-Villiger氧化; 酯水解
中图分类号:TQ 028 文献标识码: A 文章编号: 1671-0460(2015)10-2277-03
Study on Synthesis of 4,4'-Dihydroxybiphenyl
ZHANG Ying-peng, TAN Wei, YANG Yun-shang
(School of Petrochemical Engineering,Lanzhou University of Technology, Gansu Lanzhou 730050,China)
Abstract: A new method to synthesize 4,4'-dihydroxybiphenyl was designed by using diphenyl as raw material via Friedel-Crafts acylation,Baeyer-Villiger reaction, hydrolysis of ester. The structures of product and intermediates were confirmed by 1H NMR, elemental analysis and melting point apparatus. And the reaction conditions were optimized, higher yield was achieved.
Key words: 4,4'-dihydroxybiphenyl; Diphenyl; Friedel-Crafts acylation; Baeyer-Villiger reaction; Hydrolysis of ester
4, 4' -二羟基联苯是一种重要的有机中间体,常作为橡胶防老剂[1]和塑料抗氧剂[2],用于无色硫化橡胶制品、食品包装用橡胶制品及医用乳胶制品,也用于氯化硫冷硫化制品,如医用手套等。同时,它也是一种染料中间体和石油制品稳定剂,如合成光敏材料[3]、润滑油脂的稳定剂[4]。在合成高聚物方面[5,6],由于其耐热性极佳,常用作为聚酯、聚氨酯、聚碳酸酯、聚砜及环氧树脂等的改性单体,用以制造优良的工程塑料和复合材料等,目前其高纯度产品主要用于合成液晶聚合物[7]。4,4'-二羟基联苯应用广泛,但是由于技术、生产、工艺、环保等各方面的限制,目前国内高纯度 4,4'-二羟基联苯的生产能力一直很低,处于供不应求状态。
目前生产4,4'-二羟基联苯有以下五种方法:
(1)联苯磺化碱融法(图1)[8,9]
该方法合成路线简单、产率较高,在工业上被广泛采用。但是反应过程中采用了浓酸、强碱,造成环境污染。
(2)联苯胺的重氮化法[10]
这种方法中,重氮盐不稳定且易分解发生爆炸,反应需要在低温下进行,而且反应原料毒性较大,此法不适宜大规模工业生产(图2)。
(3)卤代联苯水解法(图3) [11]
这种方法需要在高温下发生反应,反应能耗太高。
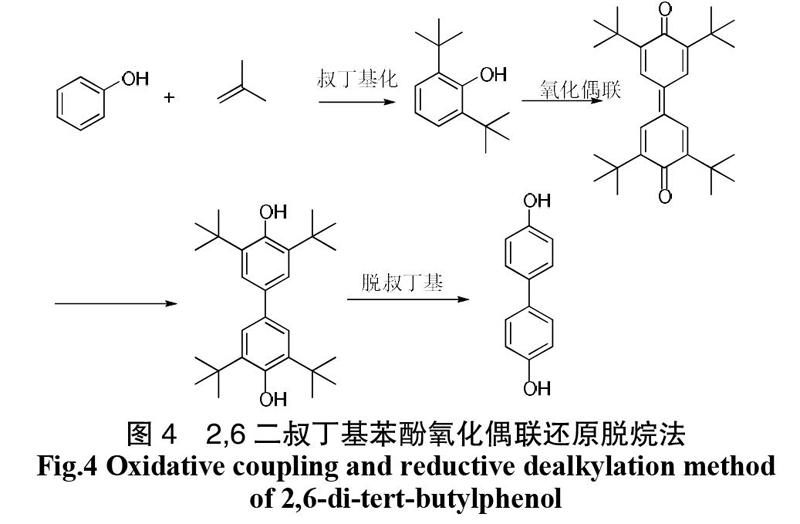
(4)2,6二叔丁基苯酚氧化偶联还原脱烷法(图4) [12]
此类方法反应步骤较多,过程复杂,产率过低。
(5) 2,6二甲基苯酚氧化偶联还原脱烷(图5)法[13]
这种方法与第四种方法类似,产率有所提高。
据此,本研究设计了一种新方法合成了4,4'-二羟基联苯,具体过程如下如图6所示。以联苯为原料,第一步Friedel-Crafts酰基化得到4,4'-乙酰基联苯;第二步通过Baeyer-Villiger氧化反应得到4,4'-二乙酰氧基联苯;第三步将4,4'-二乙酰氧基联苯水解得到4,4'-二羟基联苯。
1 实验部分
1.1 试剂与仪器
XRC-1型显微熔点仪(四川大学科学仪器厂);Bruker Avance 400型核磁共振仪(TMS为内标,CDCl3作溶剂); Vario Ⅲ 元素分析仪(德国Elementar 公司); 所用试剂均为市售化学纯。
1.2 实验过程
1.2.1 4,4'-二乙酰基联苯的合成
在500 mL烧瓶中加入7.334 g(55 mmol)无水AlCl3,250 mL CH2Cl2,冰水浴搅拌条件下滴加4.318 g(55 mmol,30 mLCH2Cl2溶解)乙酰氯,滴加速度控制在每分钟30滴,待反应体系澄清后,加入4.256 g(25 mmol,30 mLCH2Cl2溶解)联苯,滴加速度控制在每分钟30滴,滴加完毕后,反应1 h,升温至室温后,40 ℃搅拌回流24 h;反应结束后将反应液搅拌倒入冰水混合物中,减压蒸出二氯甲烷,抽滤,滤饼用蒸馏水冲洗,得到粗产品;粗产品用95%的乙醇重结晶三次。计算产率,表征产物。
1.2.2 4,4'-二乙酰氧基联苯的合成
(1)催化体系筛选
称取0.238 g(1 mmol)4,4'-二乙酰基联苯于12支柱塞试管,分别加入等量不同的催化剂,溶剂、反应温度根据催化剂而定,TLC跟踪反应,每30 min检测一次,反应时间以薄层色谱检测为准。产物提纯,计算产率。实验结果列于表1。
(2)催化剂量的筛选
由(1)得到最佳催化体系为H2O2/I2,对H2O2和I2的用量进行筛选。分别准确称取0.238 g(1 mmol)4,4'-二乙酰基联苯于12支柱塞试管,加入不同量的H2O2和I2,25 ℃反应1.5 h,提纯,计算产率。实验结果列于表2。
(3)最优条件验证
在500 mL单口圆底烧瓶中加入250 mL 冰乙酸,1.524 g (6 mmol)的碘, 23.3 mL( 300 mmol,30%水溶液)的H2O2,常温搅拌30 min后,加入7.149 g(30 mmol)4,4'-二乙酰基联苯。TLC跟踪至反应结束,反应结束后将反应液倒入蒸馏水中,固体析出完全后,抽滤,滤饼用大量蒸馏水洗涤,得到粗产物。95%乙醇重结晶三次,产物置于80 ℃真空干燥2 h。表征产物。
1.2.3 4,4'-二羟基联苯的合成
在250 mL单口圆底烧瓶中加入5.401 g(20 mmol)4,4'-二乙酰氧基联苯,150 mL乙醇,3.333 g (80 mmol,含量大于96%,30 mL水溶解)氢氧化钠,80 ℃搅拌回流1 h后,冷却至室温,将反应液倒入300 mL蒸馏水中,用3 mol/L的盐酸调节pH至酸性,当固体不再析出后抽滤,滤饼用蒸馏水洗涤至滤液为中性,得到粗产物。粗产物用95%乙醇重结晶三次,产物置于80 ℃真空干燥2 h。表征产物。
2 结果与讨论
2.1 反应条件筛选
在合成4,4'-二乙酰基联苯中,我们按照文献[14]方法,常温下进行酰基化反应,反应未得到目标产物。我们将反应置于40 ℃加热回流,得到目标产物,产率高达98%。我们推断,可能是由于取代的乙酰基钝化了对位的苯环,导致对位苯环酰化难度增加,升高反应温度有利于产物生成。
反应第二步Baeyer-Villiger氧化反应合成4,4'-二乙酰氧基联苯,我们对文献报道的氧化体系进行了筛选,结果如表1所示。
表1 催化体系的筛选
Table 1 The selection of catalyst system
序号 氧化剂 溶剂 T/℃ t/h 产率a,%
1 KHSO5 CH2Cl2 25 24 16
2 KHSO5/H2SO4 CH2Cl2 25 6 83
3 I2 AcOH 25 24 0
4 H2O2 AcOH 45 24 19
5 H2O2/ I2 AcOH 25 1.5 91
6 CF3CO3H AcOH 25 2 78
7 CH3CO3H AcOH 25 3 75
8 C6H5CO3H AcOH 25 3.5 80
9 mCPBAb AcOH 25 2 87
10 H2O2/Al2O3 AcOH 25 24 53
11 H2O2/Na2B4O7 AcOH 25 12 82
12 H2O2/BF3 AcOH 25 12 76
a: 纯化后的产率; b: 间氯过氧苯甲酸。
实验选用了12种不同的催化体系,催化剂的量相等,溶剂和反应温度是根据催化剂的性质而定,反应时间以TLC检测为准。实验1和实验2比较,KHSO5可以催化反应,但反应时间长,转化率低,加入H2SO4以后反应时间缩短,产率提高,推断酸性条件有利于KHSO5催化反应正向进行。由实验3、4、5比较,只有I2催化的时候反应不发生,H2O2虽然可以催化反应,但是催化效率不高,即使反应温度升高到45 ℃,时间延长至24 h,也只有19%的收率。H2O2/I2催化体系,H2O2和 I2协同催化,反应温度低,反应时间段,产率高达91%。比较试验6、7、8、9,有机过酸催化该反应,反应都取得了较高的收率,但有机过酸价格高、有一定的危险性及会产生羧酸盐废物。比较试验5、10、11、12,都为H2O2和路易斯酸的混合催化体系,其中试验5 H2O2/I2催化体系得到了最佳的收率。综合12组实验进行比较,我们选用H2O2/I2为最佳催化体系。
对H2O2和I2的用量进行了优化,结果如表2所示。
分别对H2O2和I2的用量进行单因素实验,当I2的量不变时,反应产率随着H2O2的量增加而增加,但是氧化剂H2O2的量超过10 equiv时,产率不再增加,故选择10 equiv为最佳量。保持H2O2的量不变,改变I2的量,实验结果显示,当I2用量为0.2 equiv时取得较高产率95%,后面即使增加I2的量,产率也没有明显提高,虽然在0.2 equiv的时候取得了最高产率96%,但在0.3 equiv的时候产率又回到95%,相差很小,推断可能是实验操作导致的误差,故我们选择0.2 equiv为最佳用量。对得到的最佳反应条件进行放大实验,产率高达94%,证明实验条件稳定、可靠。
表2 反应催化剂量的筛选
Table 2 The selection of reaction catalyst amount
序号 H2O2(equiv) I2(equiv) 产率b,%
1 2 0.15 26
2 4 0.15 46
3 6 0.15 76
4 8 0.15 83
5 10 0.15 90
6 11 0.15 91
7 12 0.15 90
8 10 0.05 63
9 10 0.10 87
10 10 0.20 95
11 10 0.25 96
12 10 0.30 95
a: 反应条件:0.238 g(1 mmol)4,4'-二乙酰基联苯,冰乙酸为溶剂,25 ℃反应1.5 h;b:纯化后的产率。
第三步4,4'-二乙酰氧基联苯水解,根据4,4'-二羟基联苯的性质,我们选用碱式水解法,在4,4'-二乙酰氧基联苯水解的过程中氢氧化钠既作为催化剂催化反应,也可以与水解后的产物乙酸和4,4'-二羟基联苯反应,促进4,4'-二乙酰氧基联苯的水解,从而加快反应速率。反应结束反应液倒入蒸馏水中,再利用4,4'-二羟基联苯不溶于水的性质,加酸使4,4'-二羟基联苯从水中沉淀下来。水解反应较为彻底,得到了高达97%的收率。
2.2 中间体和产物结构表征
4,4'-二乙酰基联苯:白色固体;产率:98%;熔点:188~189 ℃(文献值[15]:189~192 ℃);1H NMR (400 MHz, CDCl3) δ 8.06(d, J = 8.3 Hz, 4H), 7.73 (d, J = 8.3 Hz, 4H), 2.66(s, 6H);元素分析(%,C16H14O2计算值) :C 80.64(80.65),H 5.90(5.92),O 13.42(13.43)。
4,4'-二乙酰氧基联苯:白色固体;产率:95%;熔点:165-166 ℃(文献值[16]:167~168 ℃);1H NMR (400 MHz, CDCl3) δ 8.06 (d, J =8.3 Hz, 4H), 7.73 (d, J = 8.3 Hz, 4H), 3.70 (s, 6H);元素分析(%,C16H14O4计算值):C 71.12 (71.10),H 5.20(5.22),O 23.68(23.68)。