凝乳酶效价测定方法研究
2015-07-07李京王悦刘莉莎任雪范慧红
李京,王悦,刘莉莎,任雪,范慧红
(中国食品药品检定研究院,北京 100050)
凝乳酶效价测定方法研究
李京,王悦,刘莉莎,任雪,范慧红Δ
(中国食品药品检定研究院,北京 100050)
目的 考察凝乳酶效价测定方法的影响因素,改进凝乳酶效价测定方法;考察凝乳酶国家标准品稳定性、适用性。方法 考察不同奶粉底物和酶浓度对凝乳酶效价测定的影响;建立3×3量反应平行线法,并对多批样品进行测定,结果与绝对法、单点相对法进行比较;使用绝对法和统计分析对凝乳酶标准品稳定性进行考察;通过量反应平行线法考察凝乳酶标准品的适用性。结果 不同奶粉底物对绝对效价的测定有显著性影响;酶浓度与凝乳时间呈幂函数关系;与绝对效价比较,相对效价在不同实验室间结果重现性更好;3×3量反应平行线法测定剂量为0.35、0.44、0.55 U/mL,可信限率小于5%;凝乳酶国家标准品(140712-201302)2015年效价测定结果与2013年结果无统计学意义;在一定剂量范围内,凝乳酶国家标准品与复合凝乳酶或羔羊胃提取物的剂量-反应呈直线关系,2直线平行。结论 凝乳酶效价测定影响因素多,通过标准品测定相对效价可以消除不同底物、不同人员操作、终点判断等因素对测定的影响,使实验室之间结果具有可比性;3×3量反应平行线法的实验设计可以更好的控制实验误差;凝乳酶国家标准品(140712-201302)稳定性良好,适用于复合凝乳酶和羔羊胃提取物的凝乳效价测定。
凝乳酶;效价;复合凝乳酶;羔羊胃提取物;量反应平行线法
凝乳酶是一种从未断奶的小牛胃中发现的天冬氨酸蛋白酶,其主要的生物学功能是可专一地切割乳中κ-酪蛋白的苯丙氨酸(phenylalanine,Phe)105-甲硫氨酸(methionine,Met)106之间的肽键,破坏酪蛋白胶束使乳凝结[1-3]。凝乳酶的来源广泛,最早来源于小牛的第四胃,随后在其他哺乳动物的胃中也提取了凝乳酶,许多植物中也含有能使乳凝固的蛋白酶,如菠萝蛋白酶等, 另外还有微生物发酵及基因工程凝乳酶。凝乳酶由323个氨基酸残基组成多肽链,相对分子质量为35622 D,等电点为pH 4.5,干燥物活性稳定,水溶液不稳定。凝乳酶广泛的应用于乳酪生产等食品加工业,在医药行业也有所应用。
国家食品药品监督管理局批准了复合凝乳酶国家标准〔WS-10001-HD(0856)-2002〕[4]和羔羊胃提取物国家标准〔WS-1001-(HD-1538)-2005〕。复合凝乳酶为“以羔绵羊第四胃为主的提取物”,羔羊胃提取物为“羔绵羊第四胃经低温提取制得的总提取物”,上述2种药品主要用于治疗急慢性胃炎、消化不良及婴儿吐奶等,2个品种的曾用名均为“胃优乐”。
复合凝乳酶和羔羊胃提取物的国家标准中凝乳酶效价测定方法基本一致,为“相对法”,即“30 ℃,通过比较标准品与供试品使10 mL 120 g/L奶粉底物凝结的时间计算效价”。胃优乐的标准为地方标准,收载于1987年版《新疆维吾尔自治区药品标准》[5],标准中凝乳活性测定方法不使用标准品,为“绝对法”,即“30 ℃,每100秒中内凝结10 mL 120 g/L奶粉底物的酶量为一凝乳单位”。
凝乳酶效价测定的影响因素很多[6-7],如底物测、温度、pH、金属离子、终点观察等,测定误差较大。本文对凝乳酶效价测定方法的影响因素进行考察,建立3×3量反应平行线法测定凝乳酶效价,对不同实验室、不同效价测定方法进行结果比对,考察凝乳酶国家标准品的稳定性、适用性,为酶类药物国家药品标准提高和标准品标定提供思路。
1 材料与方法
1.1 材料
1.1.1 实验仪器:数控精密恒温水浴(西班牙Precisdig公司);Mettler Toledo XS-205电子天平、Mettler Toledo MP230 pH计(瑞士梅特勒-托利多公司)。
1.1.2 药品与试剂:凝乳酶国家标准品(中国食品药品检定研究院,效价为881 U/g,批号140712-201302);羔羊胃提取物(新疆生化药业有限公司,批号131212);羔羊胃提取物维B12胶囊(新疆生化药业有限公司,批号1403009);复合凝乳酶胶囊(唐山葵花药业,批号15010001)。
全脂奶粉(河北产),雀巢全脂奶粉(双城雀巢有限公司),三宇全脂奶粉(新疆焉耆三宇实业有限责任公司),其他试剂为国产分析纯。
1.2 方法
1.2.1 溶液配制
① 磷酸盐缓冲液(pH 6.3):取磷酸二氢钠7.8 g,磷酸氢二钠2.7 g,加水溶解并稀释成1000 mL,调节pH值至(6.3±0.05)。
② 氯化钙溶液:取醋酸钠2.05 g,氯化钙1.11 g,加水使溶解成1 000 mL,调节pH值至(6.3±0.1)。
③ 底物溶液:取全脂奶粉12 g,加氯化钙溶液适量,研磨均匀,置100 mL量瓶中,加氯化钙溶液至刻度,摇匀,使用8层脱脂纱布过滤,临用新制。
④ 标准品溶液:取凝乳酶国家标准品(140712-201302)0.05 g,精密称定,置研钵中,加磷酸盐缓冲液(pH 6.3)0.5 mL,研磨均匀,用移液器分次转移置10 mL量瓶中(约4.4 U/mL),加磷酸盐缓冲液(pH 6.3)稀释至刻度,分别取上述溶液0.8、1.0、1.25 mL,置10 mL量瓶中,加磷酸盐缓冲液(pH 6.3)稀释至刻度,3个剂量组约为0.35、0.44、0.55 U/mL,剂间比r=0.8,4 ℃冰箱保存,配制后2h内使用。
⑤ 供试品溶液:精密称定羔羊胃提取物0.088 g(估计效价500 U/g),照标准品溶液制备方法制备;取羔羊胃提取物维B12胶囊 10粒,分别称内容物重量,计算平均装量;精密称定内容物约0.44 g(估计效价100 U/g),精密称定,照标准品溶液制备方法制备;取复合凝乳酶胶囊10粒,分别称内容物重量,计算平均装量,取内容物约0.15 g(估计效价300 U/g),照标准品溶液制备方法制备;4 ℃冰箱保存,临用新制。
1.2.2 凝乳活力测定法:精密量取底物溶液10 mL,置试管中,在 30 ℃±0.5 ℃ 恒温水浴中保温10 min,精密加入标准品溶液1 mL,摇匀并立即计时,用玻璃棒不断蘸取溶液沿管壁流下,使成均匀薄层,当薄层出现可见颗粒时,表明已经凝乳,准确记录自标准品溶液加入后至出现凝乳现象的时间。重复测定3次,3次测定值的相对标准偏差不得大于5%。取平均值作为标准品溶液的凝乳时间。取供试品溶液1 mL,依法操作。凝乳时间与凝乳酶活力呈反比,调整标准品和供试品浓度将凝乳时间应控制在180~240 s。
1.2.3 凝乳活力计算方法
① 绝对法:按1987年版《新疆维吾尔自治区药品标准》中胃优乐凝乳活性计算方法计算,即“30 ℃,每100秒中内凝结10 mL 12%奶粉底物的酶量为一凝乳单位”,公式如下:
凝乳酶活力(U/g)=100(s)/[凝乳时间(s)×供试品溶液浓度(g/mL)×供试品溶液取样体积(mL)]
② 单点相对法:按复合凝乳酶国家标准〔WS-10001-HD(0856)-2002〕中凝乳活性计算方法计算,即“30 ℃,通过比较标准品与供试品使10 mL 12% 奶粉底物凝结的时间计算效价”,公式如下:
凝乳酶活力(U/g)=[标准品溶液凝乳时间(s)×标准品标示效价(U/g)×标准品溶液浓度(g/mL)]/[供试品溶液凝乳时间(s)×供试品溶液浓度(g/mL)]
③ 量反应平行线法:使用《中国药典》2010年版二部附录XI V生物检定统计法中3×3量反应平行线测定,即3个标准品剂量组和3个供试品剂量组,比较其在30 ℃条件下,使10 mL 120 g/L 奶粉底物溶液凝结的时间,剂量0.35、0.44、0.55 U/mL,剂间比r=0.8。BS2000软件计算,实验可靠性测验结果需通过(回归项应非常显著P<0.01,偏离平行不显著P>0.05,二次曲线不显著P>0.05,反向二次曲线不显著P>0.05),平均可信限率FL%应小于5%。

2 结果
2.1 底物对凝乳酶活力测定的影响 分别使用3种奶粉底物测定凝乳酶国家标准品(140712-201302)的绝对法效价,见表1,图1。结果表明不同奶粉底物对于绝对效价的测定有影响,welch检验结果有统计学意义。

表1 凝乳酶国家标准品(140712-201302)不同底物凝乳酶绝对效价
#P<0.01,与河北奶粉相比,compared with Hebei milk powder;*P<0.01,与雀巢奶粉相比,compared with Nestle milk powder
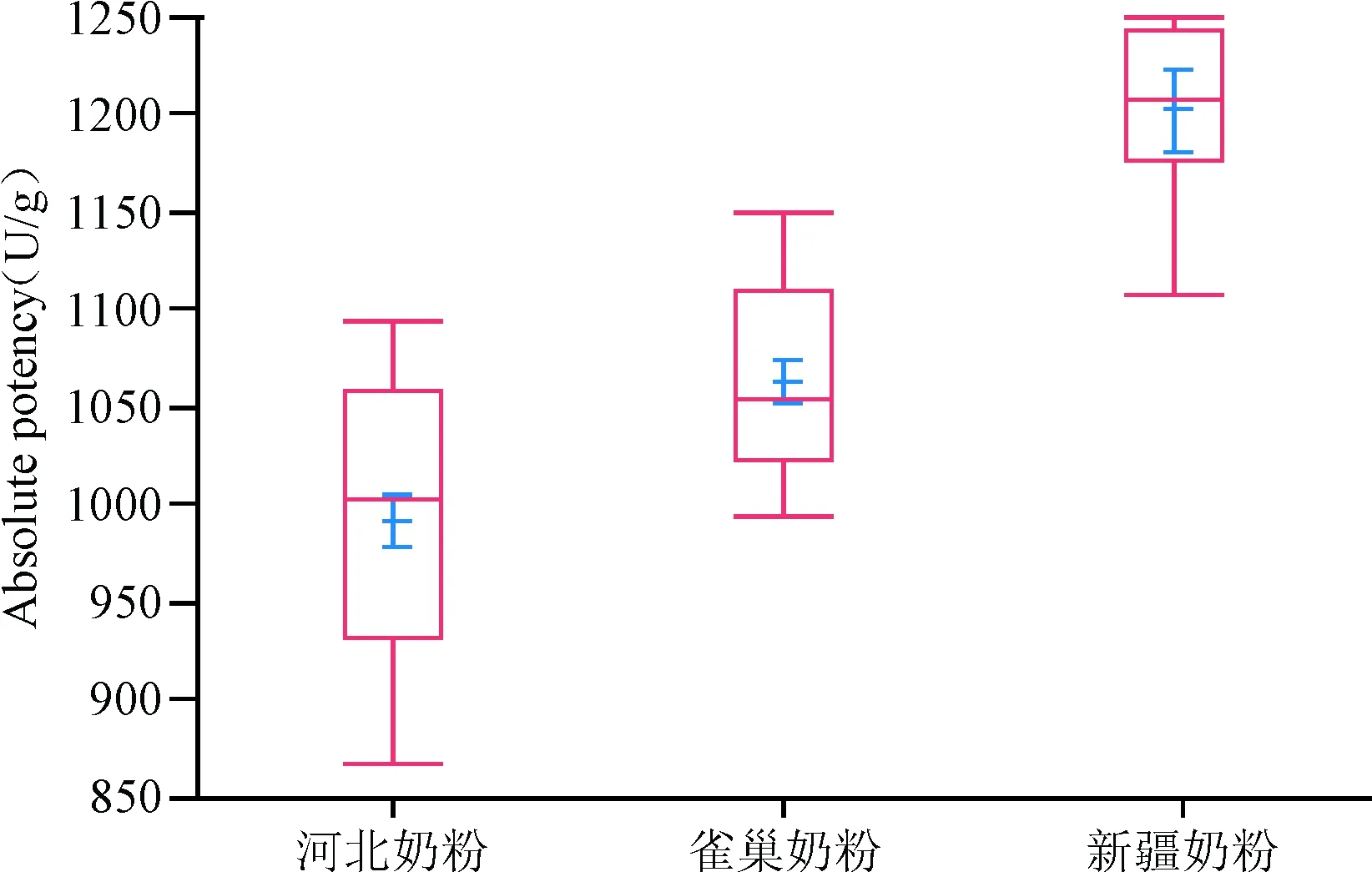
图1 凝乳酶国家标准品(140712-201302)不同奶粉底物测定绝对效价厢线图Fig.1 Box plot of the absolute potency of chymosin national standard (140712-201302) by different formula milk powder substrates
2.2 酶浓度与凝乳时间关系 测定了凝乳酶标准品(140712-201302)9个浓度的凝乳时间。对浓度(C)-凝乳时间(T)拟合线性,符合幂函数曲线(见图2A),线性方程为T=99.498C-0.861,r=0.9951;对LOG浓度与LOG凝乳时间拟合线性曲线,符合直线方程(见图2B),线性方程为LogT=-0.861 4LogC+1.997 8,r=0.995 1。
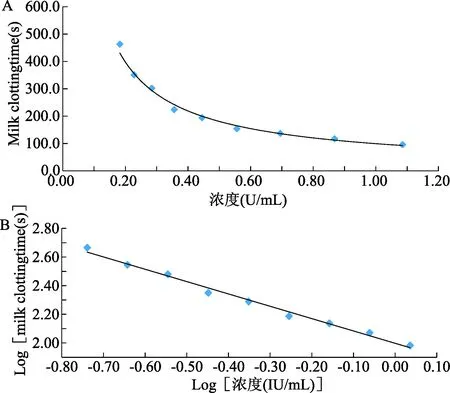
图2 凝乳酶标准品溶液浓度与凝乳时间关系图A:凝乳酶标准品浓度与凝乳时间拟合幂函数曲线;B:凝乳酶标准品浓度与Log凝乳时间拟合直线Fig.2 The relationship between the concentration of the national standard of chymosin and the time of milk clotting timeA:The power function curve of the concentration of the national standard of chymosin and time of the milk clotting time; B:The line of Log concentration of the national standard of chymosin and Log time of milk clotting
2.3 凝乳酶标准品
2.3.1 国家标准品建立:复合凝乳酶和羔羊胃提取物国家标准分别于2002年和2005年颁布,首批凝乳酶国家标准品(140712-200901)于2010年发放使用,在此之前,生产企业使用SIGMA公司的凝乳酶标准试剂(Rennin from calf stomach,货号R4877)为标准品指导生产。SIGMA公司凝乳酶纯度很高,凝乳活力大于20 000 U/g,与国内产品工艺及结构有很大区别,国内复合凝乳酶及羔羊胃提取物均为混合物,凝乳活力较低,约800 U/g,根据标准物质与供试品相似的原则[9-10],用含组分与供试品相似的原料为凝乳酶国家标准品是适合的。首批凝乳酶国家标准品在上述2种国内产品中选择一批性质稳定的原料药作为标准品原料,以现行有效的SIGMA公司凝乳酶标准试剂为标准品,按国家标准(WS-10001-HD[0856]-2002)中规定的方法,经多次实验后赋值。
2.3.2 标准品适用性考察:以凝乳酶国家标准品(140712-201302)为标准品,采用“3×3量反应平行线法”对羔羊胃提取物和复合凝乳酶进行测定,在一定剂量范围内,剂量-反应呈直线关系,2直线平行见图3、图4。凝乳酶国家标准品(140712-201302)适用于羔羊胃提取物和复合凝乳酶原料及制剂的凝乳酶活性测定。
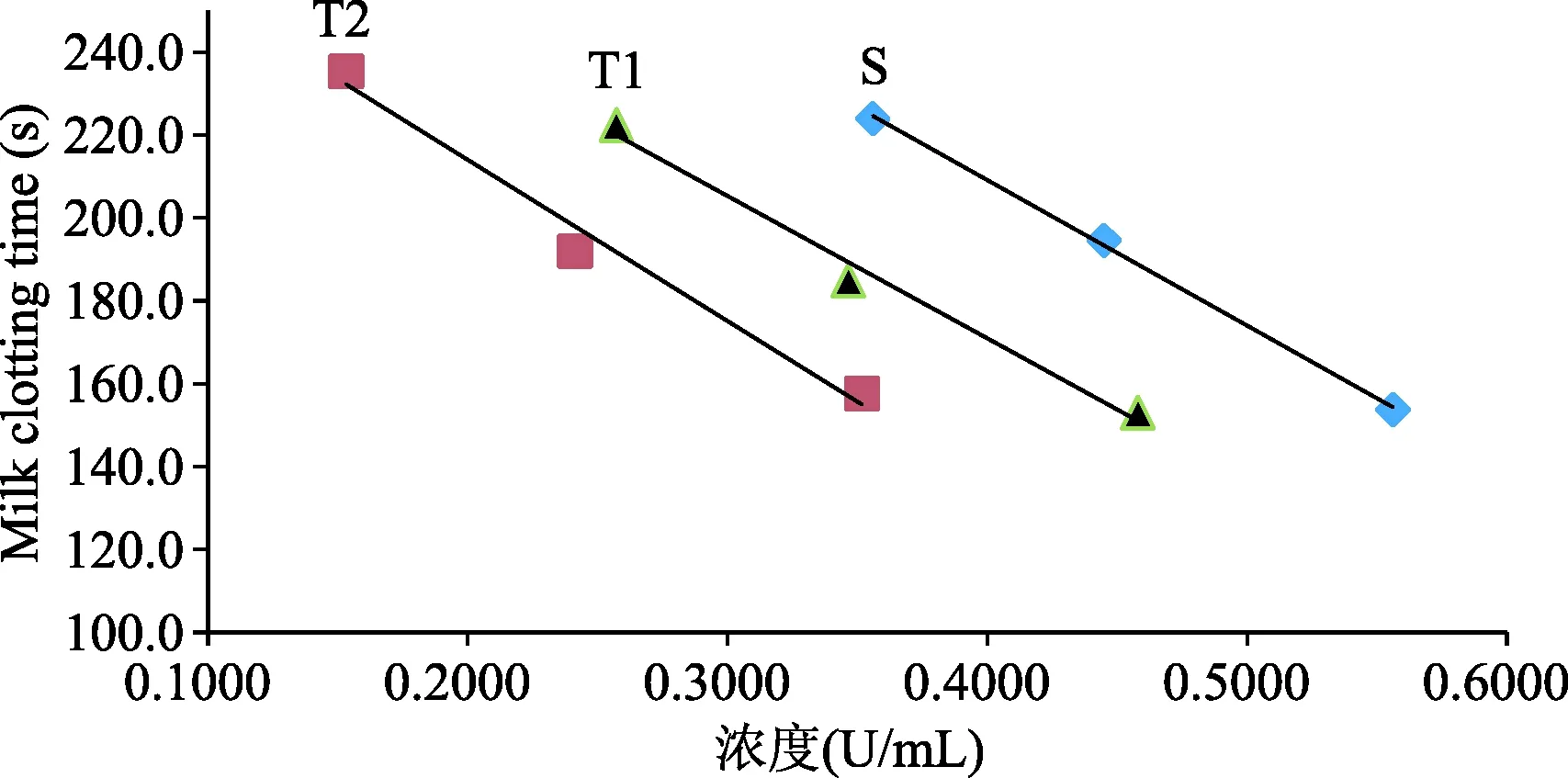
图3 羔羊胃提取物凝乳酶活力测定量-反应平行线S:凝乳酶国家标准品(140712-201302);T1:羔羊胃提取物(131212);T2:羔羊胃提取物维B12胶囊(1403009) Fig.3 Dose-response parallel line of chymosin potency determination of lamb’tripe extractS:National standard of chymosin(140712-201312); T1:lamb’tripe extract(131212); T2:lamb’tripe extract and vitamin B12 capsule(1403009)(注:为使作图时拟合直线的平行性更加清楚的显示,将T1平行向左移动0.1 U/mL,将T2平行向左移动0.2 U/mL)
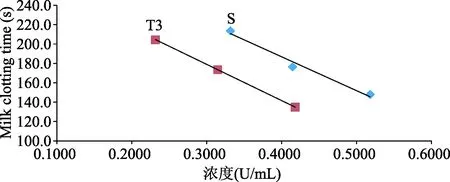
图4 复合凝乳酶凝乳酶活力测定量-反应平行线S:凝乳酶国家标准品(140712-201302);T3:复合凝乳酶胶囊(15010001)Fig.4 Dose-response parallel line of chymosin potency determination of l gastropylor complexS:National standard of chymosin(140712-201312); T3:gastropylor complex capsule(15010001)(注:为使作图时拟合直线的平行性更加清楚的显示,将T3平行向左移动0.1 U/mL)
2.3.3 标准品稳定性考察:结果表明凝乳酶标准品(140712-201302)绝对效价2013年为(976±13.0)U/g (n=15),2015年为(990±68.1)U/g (n=24), welch检验结果差异无统计学意义。见图5。
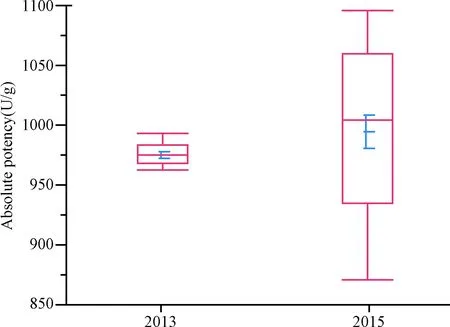
图5 凝乳酶国家标准品(140712-201302)不同时间测定绝对效价厢线图Fig.5 Box plot of the absolute potency of chymosin national standard (140712-201302) in different years
3 讨论
3.1 凝乳酶凝结牛奶过程[1]牛奶中主要有4种酪蛋白分子:α-s1、α-s2、β和κ。α和β酪蛋白是疏水的蛋白质,可被钙沉淀,而κ-酪蛋白不能被钙沉淀。当酪蛋白分泌时,它们自我联合扩大形成微胶粒,在微胶粒中,α和β酪蛋白在κ-酪蛋白作用下保持非沉淀状态,κ-酪蛋白通常能保持牛奶中的大部分蛋白为可溶的,并防止它们自发凝结。凝乳酶可以水解并使κ-酪蛋白失活,将它转化成ρ-κ-酪蛋白和一种被称为巨肽的蛋白。ρ-κ-酪蛋白不能稳定分子结构,而且能使不溶的蛋白质沉淀形成凝结。
3.2 凝乳酶活力测定影响因素考察 酶促反应受各种因素影响,对反应条件极为敏感。据文献报道[6-7],羔羊胃提取物中凝乳酶活力受温度、pH、金属离子、底物浓度等影响,在35 ℃以下稳定性较好,在30 ℃~45 ℃,随温度的升高,凝乳活力逐渐增大;在底物pH 5.5~7.5,凝乳活力随着pH的增大而降低,pH大于6.0时,凝乳活力变化不大;Al3+、Ca2+、Na+有较强的促凝作用,Cu2+、Zn2+、有明显的抑制酶活作用,K+、Mg2+、Mn2+、Fe3+对酶活力没有明显影响;底物浓度越大,凝乳活力越高,当底物浓度小于200 g/L时,随着底物浓度的增大,凝乳活力增加较快。复合凝乳酶和羔羊胃提取物国家标准中已经严格控制了反应温度为30 ℃±0.5 ℃,pH为(6.3±0.1),奶粉底物浓度为120 g/L,凝乳时间为180 s~240 s,但酶浓度的规定有所不同,复合凝乳酶为“0.4~0.6 U/mL”,羔羊胃提取物“约为1 U/mL”。在影响酶促反应的各种因素中,酶与底物是2个最基本的因素,其他因素也是通过这2者产生影响[8],因此本研究对不同奶粉底物和酶浓度进行了进一步研究。
3.3 标准品稳定性考察 凝乳酶标准品(140712-201302)是以相对法赋值的,标定时使用的SIGMA标准品现已过期,不能继续使用;不同批SIGMA标准品赋值有一定误差,不宜使用SIGMA标准品对本品稳定性进行考察;因此本研究使用了标定时采用的河北奶粉为底物,采用绝对法对标准品的赋值进行考察。
3.4 凝乳酶活力测定方法比较
3.4.1 绝对法:“绝对法”测定受实验条件、人员操作、终点观察等多个因素影响,尤其是标准中不规定奶粉底物的品牌,造成实验室之间结果重现性差。
3.4.2 单点相对法:使用标准品的“相对法”,很好的避免了因底物等实验条件不同对实验结果的影响,使实验室之间的结果具有可比性。
3.4.3 量反应平行线法:当供试品与标准品的活性组分基本相同时,在一定剂量范围内,剂量-反应呈直线关系,2直线平行。本研究在单点相对法的基础上,建立了3×3量反应平行线法测定凝乳酶效价。根据3.2.2酶浓度与凝乳时间关系的实验结果,本研究对反应浓度进行了选择。当酶浓度小于0.3 U/mL时,凝乳时间超过240 s,实验时间较长,奶粉底物溶液容易发生自发凝结,终点观察困难;当酶浓度大于0.6 U/mL 时,凝乳时间小于150 s,拟合直线趋于平直,斜率变小,反应灵敏度下降,实验误差大;因此本研究选择了0.35、0.44、0.55 U/mL 3个浓度作为量反应平行性法的反应浓度。“3×3量反应平行线法”考虑到了3个不同浓度,并且应用生物统计工具,对标准品与供试品的平行性和实验误差进行了更好的控制,本研究多次实验的结果均通过了线性、平行性的实验可靠性检测,可信限率均小于5%,“3×3量反应平行线法” 与“单点相对法”检测结果基本一致。
综上所述,凝乳酶效价测定影响因素多,通过标准品测定相对效价可以消除不同底物、不同人员操作、终点判断等因素对测定的影响,使实验室之间结果具有可比性;3×3量反应平行线法的实验设计可以更好的控制实验误差;凝乳酶国家标准品(140712-201302)稳定性良好,适用于复合凝乳酶和羔羊胃提取物的凝乳效价测定。
致谢:新疆维吾尔自治区食品药品检验所提供部分样品及检验数据,在此表示感谢!
[1] 张红梅,刘钟滨.凝乳酶的研究进展[J].同济大学学报,2004,25(3):254-257.
[2] Qian S,Xi PW,Qiao JY,et al.Purification and characterization of a chymosin from rhizopus microspores var.rhizopodiformis[J].Appl Biochem Biotechnol,2014,174(1):174-185.
[3] 高维东,宋礼,纪银莉,等.微小毛霉凝乳酶的分离纯化研究[J].微生物学杂志,2012,32(2):21-25.
[4] 国家药品标准[S].第九册.2002: 205-206.
[5] 新疆维吾尔自治区卫生厅.新疆维吾尔自治区药品标准[S].1987: 113-115.
[6] 徐明生,王毕妮,张富新.羔羊雏胃酶凝乳特性的研究[J].华北农学报,2005,20(6):103-106.
[7] 张富新.不同因素对羔羊皱胃酶凝乳活性的影响[J].农业工程学报,2001,17(4):111-114.
[8] 吴梧桐,袁勤生,徐寒梅.酶类药物学[S].第一版.北京:中国医药科技出版社,2011:21-29.
[9] 周海钧.生物标准物质的建立及其要求[J].中国药学杂志,1993,28(2):108-110.
[10] 丁丽霞,周海钧.生物标准物质的研究和技术要求[J].中国药师,2007,10(3):229-235.
(编校:王冬梅)
Study on determination methods of chymosin potency
LI Jing, WANG Yue, LIU Li-sha, REN Xue, FAN Hui-hongΔ
(National Institutes for Food and Drug Control, Beijing 100050, China)
ObjectiveTo investigate the influencing factors and improve potency methods of chymosin, to verify the stability and applicability of the national standard of chymosin.MethodsThe effects of different formula milk powder substrate and enzyme concentration on the determination of the activity of chymosin were studied.3×3 dose-response parallel line method was established.The results were compared with the different methods of absolute and relative methods.ResultsThe different formula milk powder had a significant effect on the determination of the absolute potency of the activity of chymosin.The concentration of the enzyme was a power function relationship with the milk clotting time.Compared with the absolute potency, reproducibility of the relative potency of the results was better in different laboratories.The suitable doses in 3×3 dose-response parallel line method were 0.35,0.44,0.55U/mL.The confidence limit rate was less than 5%.The potency of the national standard of chymosin (140712-201302) was not significantly different between 2013 and 2015.In a certain dose range, the dose-response of the national standard of chimosin and gastropylor complex or lamb’tripe extract was linear, and the two lines were parallel.ConclusionA lot of factors can affect on the potency of chymosin.Relative potency is determinate by reference standard which can eliminate the influence of different substrates, different operators and endpoint judgment on the determination in order to make results have comparability between laboratories.The test design of 3×3 dose-response parallel line can control the test deviation better than the single point determination.The stability of the national standard of chymosin(140712-201302) is good, and is suitable for the potency of chymosin of the products of gastropylor complex and the extract of the lamb.
chymosin;potency;gastropylor complex;lamb’tripe extract;dose-response parallel line method
李京,女,本科,副主任药师 研究方向:生化药物质量控制,E-mail:lijing317@nifdc.org.cn;范慧红,通信作者,女,博士,研究员,研究方向:生化药物质量控制,E-mail:shihuayaoshi@126.com。
TS201.25
A
1005-1678(2015)10-0118-04
