肾移植术后渗透性神经脱髓鞘综合征临床诊治经验
2015-07-07李智斌张更阮东丽刘克普马帅军杨晓剑秦卫军袁建林
李智斌 张更 阮东丽 刘克普 马帅军 杨晓剑 秦卫军 袁建林
肾移植术后发生渗透性神经脱髓鞘综合征(osmotic demyelination syndrome,ODS)罕见,病因尚不完全明确,可能与低钠血症及免疫抑制剂的使用等因素有关。第四军医大学西京医院泌尿外科于2007 年1 月至2014 年6 月实施同种异体肾移植术并规律随访受者353 例,有2 例受者肾移植术后发生ODS,经治疗后均康复。本文回顾性分析这2 例ODS 患者的临床资料,并结合相关文献分析肾移植术后ODS 发病机制和诊治措施,以提高临床对该并发症的认识。
1 临床资料
我院2007 年1 月至2014 年6 月实施同种异体肾移植术并规律随访的353 例受者中,男性272 例,女性81 例,平均(39 ±12)岁(9 ~71 岁);其中亲属活体供肾107 例,尸体供肾246 例。
1.1 病例1 临床资料
男性,22 岁,2010 年6 月10 日因“慢性肾功能不全(尿毒症期)”于我院行同种异体肾移植术(尸体肾移植),术前血清肌酐为823 μmol/L。手术过程顺利,术后即刻静脉注射甲泼尼龙琥珀酸钠2.12 g,手术当日及术后1、2、3、4 d 分别再给予0.75、0.50、0.50、0.25、0.12 g;兔抗人胸腺细胞免疫球蛋白50 mg/d,连用3 d;免疫抑制方案为环孢素+吗替麦考酚酯+ 泼尼松。术后尿量2 000 ~3 000 mL/d,血糖7.9 ~17.3 mmol/L,术后1 周血清肌酐为632 μmol/L;术后1 周移植肾超声检查示:移植肾略大,实质回声增强,肾动脉收缩期最大血流速度为24 cm/s,阻力指数为1,彩色多普勒血流成像(color doppler flow imaging,CDFI)显示肾内血流灌注差。遂诊断为移植肾功能延迟恢复(delayed graft function,DGF),予恢复血液透析(2 次/周),受者血清肌酐下降至393 μmol/L 时停止透析。出院后门诊每周复查1 次;规律饮食,体质量无明显变化,尿量1 800 ~2 400 mL/d,血清肌酐299 ~387 μmol/L,电解质正常,环孢素血药浓度谷值188.7 ~221.9 ng/mL。
术后2 个月受者因“乏力、恶心”再次入院,入院时查肾功能和血电解质:血清尿素氮18.2 mmol/L,血 清 肌 酐 899 μmol/L,钠 108. 0 mmol/L,氯72.5 mmol/L,血 糖6. 5 mmol/L;继 续 血 液 透 析(2 次/周),给予小剂量高渗盐水静脉滴注。入院次日复查血电解质:钠110.2 mmol/L,氯79.3 mmol/L,继续缓慢纠正低钠、低氯,并给予小剂量甲泼尼龙治疗(80 mg/d)。第3 天患者突然出现精神高度紧张,言语迟缓、混乱,幻视,易激惹,不配合治疗等症状;查体:双侧瞳孔等大、等圆,直径约3 mm,对光反射灵敏,四肢肌力正常,颈软无抵抗,病理征未引出。请相关科室会诊后给予氟哌啶醇5 mg 肌注,奥氮平2.5 mg/d 口服,症状逐渐好转。查头颅CT 未见明确病变;查血电解质:钠124.0 mmol/L,氯92. 4 mmol/L;随即给予连续性肾脏替代治疗(continuous renal replacement therapy,CRRT)。第4 天患者嗜睡,神志淡漠,目光呆滞,偶有惊醒;停用奥氮平,继续给予CRRT;复查血电解质:钠131.1 mmol/L,氯87.4 mmol/L。第5 天患者神志清楚,精神较差,对答切题,无幻视;查头颅MRI 示双侧脑室旁及半卵圆区脱髓鞘改变(见图1)。继续CRRT 治疗,时间间隔延长至48 h 1 次,第12 天查血清肌酐533 μmol/L,电解质正常,尿量约1 500 mL/d,神志清楚,精神良好,对答切题,神经系统查体无明显异常,停用CRRT,甲泼尼龙改为口服泼尼松(60 mg/d),随后逐渐减量。出院后定期随访,移植术后8 个月因移植肾失功恢复血液透析。
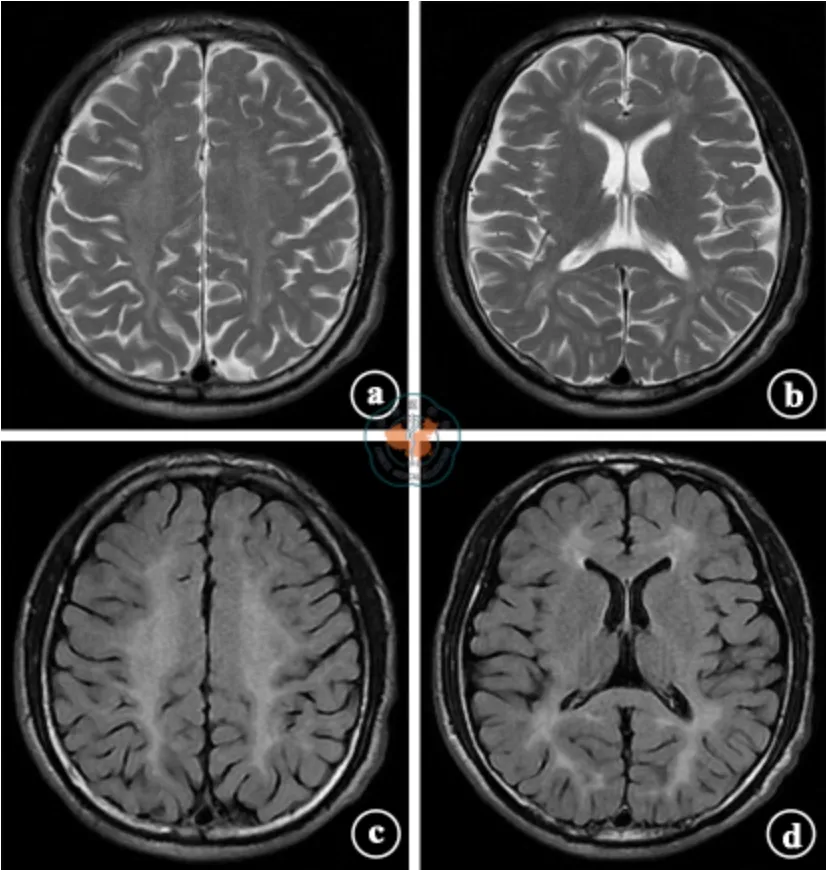
图1 病例1 患者肾移植术后2 个月再次入院第5 天头颅MRI 影像
1.2 病例2 临床资料
女性,59 岁,既往无癫痫病史,2012 年11 月17 日因“慢性肾功能不全(尿毒症期)”于我院行同种异体肾移植术(尸体肾移植),术前血清肌酐875 μmol/L,血糖9 ~16 mmol/L,手术顺利。术后即刻给予甲泼尼龙琥珀酸钠1.62 g,手术当日及术后1、2、3 d 分别再给予0.75、0.50、0.25、0.12 g;兔抗人胸腺细胞免疫球蛋白50 mg/d 静脉滴注;免疫抑制方案为他克莫司+吗替麦考酚酯+泼尼松。术后1 d 移植肾超声检查示:移植肾大小、实质回声未见异常,肾动脉血流速度略减低,收缩期最大血流速度为20 cm/s,阻力指数为0.86,CDFI 显示肾血流充盈良好。术后3 d 移植肾超声检查示:移植肾大小正常,实质回声增强,肾动脉血流速度正常,收缩期最大血流速度为24 cm/s,阻力指数为1,CDFI 显示肾血流充盈欠佳。术后尿量100 ~300 mL/d,术后3 d 复查血清肌酐为1 068 μmol/L,考虑急性排斥反应。患者拒绝行移植肾穿刺活检,遂继续给予兔抗人胸腺细胞免疫球蛋白治疗(50 mg/d)至术后1 周;复查血清肌酐为986 μmol/L,他克莫司血药浓度谷值为7.75 ng/mL;诊断为DGF,恢复腹膜透析(3 次/d)。术后1 个月移植肾超声造影示移植肾大小正常,实质回声增强,CDFI 示肾血流充盈差,大部分肾实质未见动脉血流信号,仅上极可见一支动脉(流速低,收缩期最大血流速度为18 cm/s,阻力指数为1),仅上极部分组织内可见造影剂灌注,大部分皮质内未见造影剂灌注。继续规律腹膜透析,并调整免疫抑制方案,他克莫司剂量调整为0.05 mg/kg,血药浓度谷值波动在5.22 ~8.75 ng/mL。继续每周1 次门诊随访,尿量波动在1 000 ~1 500 mL/d,血清肌酐波动在790 ~909 μmol/L。。
术后45 d 患者突然出现四肢抽搐伴意识模糊,牙关紧咬,舌根后坠,伴有口吐白沫;查体:双侧瞳孔等大,直径约3 mm,病理征未引出;症状持续约5 min自行缓解。术后60 d 上述症状再次发作,期间查血电解质和肾功能,钠最低129.9 mmol/L,氯最低93.2 mmol/L,血清尿素氮最高20.2 mmol/L,血清肌酐最高909 μmol/L;CMV-IgM 阳性;头颅CT示脑实质未见明显异常。调整他克莫司剂量为0.03 mg/kg,使 血 药 浓 度 谷 值 维 持 在8. 75 ~9.77 ng/mL;同时给予更昔洛韦口服(500 mg/次,3 次/周)。术后75 d 患者因移植肾失功切除移植肾,术后移植肾组织病理检查提示急性排斥反应。移植肾切除术后停用免疫抑制剂,术后2 d 患者出现言语混乱,意识模糊,情绪失常,伴有幻觉、谵妄;查体:双侧瞳孔等大、等圆,直径约3 mm,四肢肌力正常,病理征未引出。查肾功能和血电解质示:血清尿素氮13. 3 mmol/L,血清肌酐793 μmol/L,钠131.1 mmol/L,氯93.9 mmol/L,钾3.3 mmol/L,血糖4. 3 mmol/L;脑电图检查大致正常。遂给予CRRT(每2 天1 次),患者症状逐渐好转。移植肾切除术后7 d 患者神志清楚,精神良好;复查血电解质:钠137.6 mmol/L,氯103.6 mmol/L,钾4.0 mmol/L;头颅MRI 示:右侧脑室前角旁及半卵圆区脱髓鞘改变(见图2)。继续规律腹膜透析至电解质正常后出院,出院后规律腹膜透析,定期复查,未再出现精神症状及意识障碍。

图2 病例2 患者肾移植术后75 d 行移植肾切除术后7 d头颅MRI 影像
2 讨 论
ODS 是一种少见的急性非炎性中枢神经系统脱髓鞘性疾病,根据其发生部位可分为脑桥中央髓鞘溶解症和脑桥外髓鞘溶解症,前者主要病变部位位于脑桥基底部的中央,后者髓鞘脱失病变可累及脑桥外的其他部位,如基底节、丘脑、皮质下白质等,二者可以单独发生也可以合并出现,统称为ODS。目前,肾移植术后神经系统并发症多有报道,但肾移植术后合并ODS 鲜有报道,一方面因尚无关于肾移植术后神经系统并发症的统一分类标准,多数研究将其划归为脑病,另一方面可能与临床对该病的认识不足有关[1]。
2.1 病因及诊断
ODS 常见病因有慢性酒精中毒、营养不良、慢性肾功能不全(尿毒症期)、严重创伤、垂体手术、肝移植、恶性肿瘤等,其发生与快速纠正低钠血症明显相关[2]。目前报道较多的与器官移植相关的ODS发生于肝移植术后,发生率在5% ~10%,病死率较高,相关数据显示我国肝移植术后ODS 病死率为48. 8%[3]。本 中 心 肾 移 植 术 后OSD 发 病 率 为0.6%,可能与对该病认识不足有关,其临床表现不典型、早期检查不敏感、自限性等临床特点也导致对该病的忽视。
结合本文病例及相关文献,分析肾移植术后合并ODS 主要病因包括以下5 个方面。(1)低钠血症及其快速纠正:目前认为该因素导致ODS 的机制可能为血钠浓度快速升高导致脑胶质细胞脱水、损伤,血脑屏障间隙变宽,导致髓鞘毒性物质进入中枢神经系统引起[4]。本文2 例患者均存在低钠血症,1 例曾使用高渗盐水进行纠正。(2)血糖及肾功能异常:ODS 可继发于高血糖和氮质血症,研究者认为血糖异常和氮质血症导致血渗透压升高引起了脱髓鞘病变[5]。本文2 例患者均出现DGF 和持续的氮质血症,且术后早期应用大剂量糖皮质激素,引起血糖异常。(3)免疫抑制剂的应用:有文献报道环孢素对肝移植受者具有神经毒性[6],而他克莫司对神经病变的作用依然有争议,有研究表明其可以引起神经病变,也有研究认为该药物对神经系统有保护性作用[7]。(4)营养不良:最主要为B 族维生素的缺乏,可影响神经细胞膜髓鞘磷脂合成、脂肪酸合成异常,使髓鞘变性、退化,造成进行性脱髓鞘[8]。慢性肾功能不全(尿毒症期)患者长期透析,肾移植术前和术后均可能合并营养不良,但肝移植受者更为常见。(5)其他原因:有研究发现病毒感染、利尿剂、血磷酸盐、血液透析后等也是ODS 发生的原因[9]。本文1 例患者治疗期间检查CMV-IgM 阳性,2 例患者早期均使用一定剂量的利尿剂,也可能有一定相关性。
ODS 的临床表现并不典型,最初是通过行为障碍、神经功能障碍临床症状进行诊断,包括思维混乱、缄默、构音障碍、吞咽困难和假性延髓麻痹、腱反射亢进、截瘫、四肢瘫痪、癫痫发作等,严重时可表现为闭锁综合征和昏迷、小脑共济失调等[10]。上述症状与ODS 病变累及部位和范围有关,脑桥中央髓鞘溶解症可表现为脑干功能障碍、延髓麻痹和假性延髓麻痹、闭锁综合征、缄默症等;脑桥外髓鞘溶解症主要表现为运动障碍,其中也有少部分合并脑干和锥体束损害表现,偶见脑干损害表现[11]。
CT 检查对早期ODS 诊断不敏感,本文2 例患者起病后CT 检查均无异常。目前认为MRI 尤其是液体衰减反转恢复序列技术是确诊ODS 的检查方法,但其特征性表现并不与ODS 症状同步出现,一般滞后10 d 左右[12]。本文2 例患者均在临床症状有所好转后经MRI 检查确诊ODS。此外,ODS 有时也需要与椎基底动脉系统卒中或脑炎后遗症、脑炎、多发性硬化症、急性播散性脑脊髓炎、药物或毒素暴露、朊病毒疾病、神经退行性疾病或脑桥肿瘤等疾病相鉴别[13]。
2.2 治疗和预后
维持内环境稳定对避免肾移植术后ODS 的发生尤为重要。对于无症状的低钠血症患者,应以每小时0.5 mmol/L 的速度缓慢提升血钠浓度,24 h 升高幅度不超过10 ~12 mmol/L;对于精神状态改变和/或癫痫发作的患者,可相对快速地纠正低钠血症,最初3 ~4 h 以每小时1 ~2 mmol/L 的速度提升血钠浓度,24 h 升高幅度不超过10 ~12 mmol/L,直至发作停止[14]。此外,低钾血症在ODS 发病中似乎也起着推波助澜的作用,多数预后不良的ODS 患者为低钠血症合并低钾血症。因此,在规范化快速纠正低钠血症的同时,要监测血钾浓度并维持其稳定[14]。
同时,还需要监测免疫抑制剂血药浓度,及时调整剂量,避免药物因素引起ODS。其他可能有效的治疗包括单用皮质类固醇或联用血浆置换、静脉应用免疫球蛋白等[15-16]。Silver 等[17]在大鼠渗透性脱髓鞘综合征模型中发现,肌醇可使大鼠存活率升高,颅内脱髓鞘病灶减少。此外,应积极纠正营养不良、避免低钾血症、监测血糖变化、给予抗病毒治疗等措施。结合本文2 例患者的治疗过程,我们的经验是对于病情严重者应尽早给予CRRT,CRRT 可以缓慢、稳定地纠正离子紊乱并减少髓鞘毒性物质的蓄积,及时延缓病情进展,减少神经系统后遗症的发生。
ODS 具有一定的自限性,早期发现并积极治疗,一般患者预后良好。但也有文献报道25 例低钠血症伴有神经系统症状的ODS 患者在接受治疗后,52%的患者预后不良,其中12 例患者死亡,分析其主要相关因素为格拉斯哥昏迷评分≤10 分,严重的低钠血症(血清钠≤115 mmol/L)以及合并低钾血症,而原发病、ODS 类型、临床表现、脑电图和影像学特征等均不能作为评价预后的指标[18]。因此,预防肾移植术后ODS 的发生应引起移植医师重视。
1 康智敏,马麟麟,李继梅,等. 肾移植受者术后早期神经系统并发症[J]. 中国康复理论与实践,2010,16(9):872-874.
2 Lee EM,Kang JK,Yun SC,et al. Risk factors for central pontine and extrapontine myelinolysis following orthotopic liver transplantation[J]. Eur Neurol,2009,62(6):362-368.
3 曲凯,刘昌,王志鑫,等. 我国肝移植受者继发中枢神经系统脱髓鞘疾病回顾性分析[J/CD]. 中华移植杂志:电子版,2012,6(1):20-24.
4 Norenberg MD. Central pontine myelinolysis:historical and mechanistic considerations[J]. Metab Brain Dis,2010,25(1):97-106.
5 Shintani M,Yamashita M,Nakano A,el al. Central pontine and extrapontine myelinolysis associated with type 2 diabetic patient with hypokalemia[J]. Diabetes Res Clin Pract,2005,68(1):75-80.
6 Dunn CJ,Wagstaff AJ,Perry CM,et al. Cyclosporin:an updated review of the pharmacokinetic properties,clinical efficacy and tolerability of a microemulsion-based formulation (neoral)1 in organ transplantation[J]. Drugs,2001,61(13):1957-2016.
7 Moon JS,Souayah N. Guillain-Barré syndrome triggered by influenza vaccination in a recipient of liver transplant on FK506[J]. Liver Transpl,2006,12(10):1537-1539.
8 Ashrafian H,Davey P. A review of the causes of central pontine myelinosis:yet another apoptotic illness?[J]. Eur J Neurol,2001,8(2):103-109.
9 黄燕飞,刘金之,薛萍,等. 渗透性脱髓鞘综合征[J]. 国际神经病学神经外科学杂志,2010,37(2):144-147.
10 Epperla N,Landeck J,Sabbagh S. Osmotic demyelination syndrome[J]. WMJ,2014,113(5):197-178.
11 蒋雯巍,蒋雨平. 渗透性脱髓鞘综合征[J]. 中国临床神经科学,2007,15(3):306-309.
12 代红源,黄雨兰,罗向东,等. 渗透性脱髓鞘综合征的临床和影像学研究(附四例报道)[J]. 中华神经医学杂志,2010,9(6):633-636.
13 de Souza A. Movement disorders and the osmotic demyelination syndrome[J]. Parkinsonism Relat Disord,2013,19(8):709-716.
14 Koul PA,Khan UH,Jan RA,et al. Osmotic demyelination syndrome following slow correction of hyponatremia: Possible role of hypokalemia[J]. Indian J Crit Care Med,2013,17(4):231-233.
15 Saner FH,Koeppen S,Meyer M,et al. Treatment of central pontine myelinolysis with plasmapheresis and immunoglobulins in liver transplant patient[J]. Transpl Int,2008,21(4):390-391.
16 Escribano-Gascón AB,Casanova-Peño LI,Bartolomé-Puras M,et al. Efficacy of intravenous immunoglobulins in central pontine myelinolysis[J]. Neurologia,2008,23(6):392-394.
17 Silver SM, Schroeder BM, Sterns RH, et al. Myoinositol administration improves survival and reduces myelinolysis after rapid correction of chronic hyponatremia in rats[J]. J Neuropathol Exp Neurol,2006,65(1):37-44.
18 Kallakatta RN,Radhakrishnan A,Fayaz RK,et al. Clinical and functional outcome and factors predicting prognosis in osmotic demyelination syndrome (central pontine and/or extrapontine myelinolysis)in 25 patients[J]. J Neurol Neurosurg Psychiatry,2011,82(3):326-331.
