中晚期前列腺癌单药治疗与最大限度雄激素阻断疗法的疗效及副作用观察
2015-06-24华立新
叶 杨,汪 骏,秦 超,华立新
(1.南京医科大学第一附属医院 泌尿外科,江苏南京 210029;2.马鞍山市人民医院泌尿外科,安徽马鞍山 243000)
·临床研究·
中晚期前列腺癌单药治疗与最大限度雄激素阻断疗法的疗效及副作用观察
叶 杨1,2,汪 骏1,秦 超1,华立新1
(1.南京医科大学第一附属医院 泌尿外科,江苏南京 210029;2.马鞍山市人民医院泌尿外科,安徽马鞍山 243000)
目的 探讨中晚期前列腺癌患者单用促黄体生成素释放激素类药物与最大限度雄激素阻断疗法的疗效及安全性。方法 回顾性分析2007年1月至2012年12月在南京医科大学第一附属医院及马鞍山市人民医院接受内分泌治疗的前列腺癌患者临床资料。分为单用促黄体生成素释放激素类药物组及最大限度雄激素阻断疗组,比较两组间疾病无进展生存期、总生存期及副反应。结果 本研究共纳入患者资料392例,其中单药组120例,最大阻断组272例,平均年龄(67.6±6.6)岁,平均随访时间(33.1±8.3)月;两组间疾病无进展生存期(25.4vs. 25.3,P=0.354)及总生存期未见显著差异(34.6vs. 36.3,P=0.215)。单药组潮热(24.2%vs. 34.9%,P=0.035)、贫血(8.3%vs. 38.2%,P<0.001)、肝酶异常(5.8%vs. 23.2%,P<0.001)、乏力(8.3%vs. 18.8%,P=0.009)及便秘(3.3%vs. 12.9%,P=0.004)的发生率显著低于最大阻断组。结论 本研究比较了苏皖地区中晚期前列腺癌患者单用LHRH-a或MAB方案治疗的疗效及副作用,单用LHRH-a较MAB方案疗效相似,但部分副作用发生率较低,花费较少。
前列腺癌;内分泌治疗;疗效;副作用;雄激素阻断
前列腺癌(prostate cancer,PCa)是欧美国家最常见的泌尿系恶性肿瘤,2012年美国前列腺癌诊断数目高达24 1740例,死亡28 170,是造成美国男性死亡的第二大癌症[1]。尽管随着前列腺特异性抗原(prostate specific antigen,PSA)筛查得到普及,前列腺癌的早期诊断率大大增加,但仍有35.8%的患者在确诊时已发展为高危局限期或局部晚期前列腺癌[2]。该类前列腺癌患者目前的一线治疗方案为内分泌治疗。治疗方法有单纯去势治疗、抗雄激素单药治疗、最大限度雄激素阻断(maximal androgen blockade,MAB)治疗以及间歇内分泌治疗(intermittent hormonal therapy,IHT)等。鉴于前列腺癌的内分泌治疗仅是一种姑息性治疗手段,且有一定的副作用,故而为前列腺癌患者制定内分泌治疗方案时,必须综合考虑各方案的疗效及副作用。
国外有研究表明单用促黄体生成素释放激素类药物与最大限度雄激素阻断疗法在激素敏感性前列腺癌治疗中有着相似的疗效,在总生存率、无进展生存率等方面以上两种疗法无显著性差异[3]。但国内尚无关于单用促黄体生成素释放激素类药物与最大限度雄激素阻断疗法疗效及安全性的比较。因此,我们回顾性分析2007年1月至2012年12月在南京医科大学第一附属医院及马鞍山市人民医院接受内分泌治疗的PCa患者临床资料,探讨两种治疗方式的疗效及安全性。
1 资料与方法
1.1 病历资料 本回顾性研究纳入2007年1月至2012年12月在南京医科大学第一附属医院及马鞍山市人民医院接受内分泌治疗的PCa患者临床资料共392例,年龄37~83岁。所有患者均经前列腺穿刺病理确诊前列腺癌,记录患者诊断时年龄、PSA、Gleason评分及骨转移等相关资料。根据患者用药方案将患者归为两组,单药组120例,MAB组272例。
1.2 治疗方法 单药组:单用促黄体生成素释放激素类药物组,亮丙瑞林3.75 mg皮下注射、戈舍瑞林3.6 mg皮下注射或曲普瑞林3.75 mg皮下注射,每4周1次。MAB组:最大限度雄激素阻断疗法,在单药组治疗方案基础上增加比卡鲁胺50 mg口服1次/d或氟他胺0.25 g口服3次/d。
1.3 观察指标 所有患者治疗开始后均每月门诊复诊并复查PSA,每3个月复查血常规及肝肾功能,如出现骨痛、排尿症状加重、PSA升高等疾病进展征象时,加查骨扫描或MRI等检查,并缩短随访时间。去势抵抗性前列腺癌(castration resistant prostate cancer,CRPC)定义为:①血清睾酮达到去势水平(<50 ng/dL或<1.7 nmol/L)。②间隔1周,连续3次PSA上升,较最低值升高50%以上。通过查询数据库及电话随访方式记录患者治疗效果、生存状况及乳房胀痛等副作用出现情况。
1.4 统计学方法 用SPSS18.0处理数据,t检验比较连续变量,卡方检验比较分类变量。以P<0.05为差异有统计学意义。年龄等普通数据用均数±标准差(mean±S)表示;疾病无进展生存期及总生存期数据应用均数±标准误(mean±SE)表示。
2 结 果
本研究共纳入患者资料392例,其中单药组120例,MAB组272例,平均年龄(67.6±6.6)岁,随访时间8至53月,平均(33.1±8.3)月。单药组与MAB组在年龄(P=0.596)、PSA(P=0.967)、PSA分布(P=0.986)及ECT结果(P=0.130)无显著差异(表1)。
随访结果显示,单药组与MAB组疾病无进展生存期无显著差异(25.4±1.0vs.25.3±0.6,P=0.354),两组间总生存期也未见显著差异(34.6±1.0vs.36.3±0.6,P=0.215,图1)。
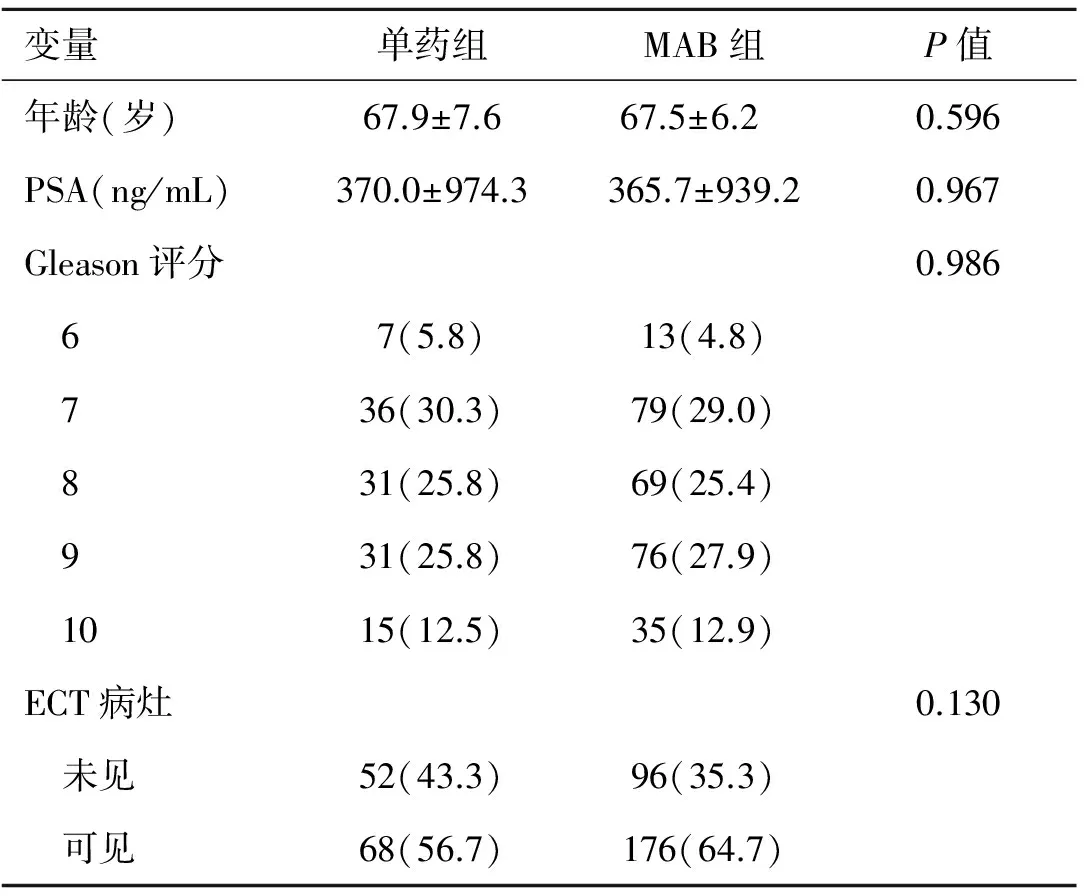
表1 单药组与MAB组基本特征比较 [例(%)]

图1 单药组与治疗组随访结果
A:疾病无进展生存期;B:总生存期。
药物副作用方面,乳房女性化(69.2%vs. 66.9%,P=0.660)、乳房胀痛(73.3%vs.76.8%,P=0.455)、性欲下降(76.7%vs.74.6%,P=0.667)及骨质疏松(51.7%vs.58.8%,P=0.188)两组间无显著差异。单药组潮热(24.2%vs.34.9%,P=0.035)、贫血(8.3%vs.38.2%,P<0.001)、肝酶异常(5.8%vs.23.2%,P<0.001)、乏力(8.3%vs.18.8%,P=0.009)及便秘(3.3%vs.12.9%,P=0.004)的发生率显著低于MAB组。
3 讨 论
前列腺是雄激素依赖性器官。1941年加拿大医生HUGGINS[4]首先发现前列腺癌是一种激素依赖性肿瘤,减少体内雄激素作用可在一定程度上抑制疾病进展,并首次提出睾丸切除术(去势)治疗晚期前列腺癌。去势治疗的目的是使血清睾酮浓度降低,目前多认为治疗效果的去势水平应在50 ng/dL,甚至20 ng/dL以下[5-6]。传统手术去势是去势治疗的金标准,手术安全,操作简单,花费较少,然而由于该术式对男性患者造成较大的负面心理影响,近年来应用范围逐渐缩小。
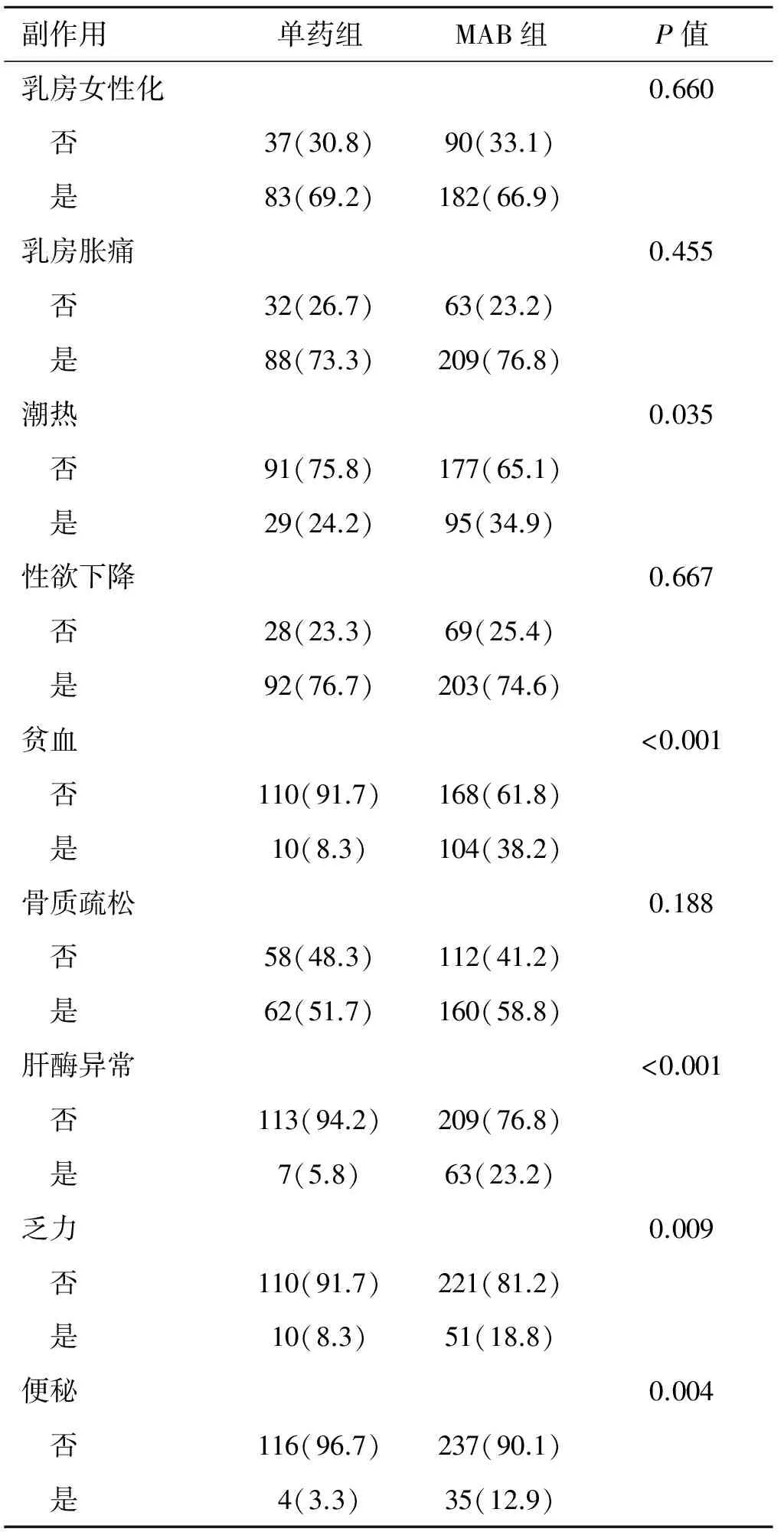
表2 单药组与MAB组副作用对比 [例(%)]
药物去势是指保留睾丸情况下,通过使用药物使得睾酮达到去势水平,LHRH-a是目前广泛使用的去势药物。药物去势存在同手术去势相似的副作用,包括性欲降低、男性乳房女性化、乳房胀痛、潮热、骨质疏松等,但保留睾丸,对患者心理影响较小,在世界范围内已成为去势治疗的主流。
雄激素受体(androgen receptor,AR)拮抗药物分为非固醇类及固醇类,作用为与体内雄激素竞争集合靶器官的AR,部分阻断睾酮进入细胞核内产生雄激素相关作用。无论是手术去势或药物去势,都只能抑制睾丸所产生的睾酮,对于少部分肾上腺产生的雄激素不能阻断,故而有学者提出去势+抗雄激素药物及最大限度雄激素阻断(MAB)疗法[7]。理论上MAB可以最大限度的阻断雄激素对前列腺癌的作用而起到比单用LHRH-a更好的疗效。然而,国外大量研究表明,MAB相较于单纯去势治疗,在疗效方面优势仍然存在争论。前列腺癌协作临床试验工作组(Prostate Cancer Trialists’ Collaborative Group,PCTCG)荟萃分析了多个中心共27项随机试验,纳入患者共8 275例,结果显示MAB组与单药组5年生存率分别为25.4%和23.6%,并无明显差异[8]。SAMSON[9]和SCHMITT[10]则显示MAB方案在疗效方面有着微弱优势。总之,MAB方案与单药方案的疗效对比尚无定论,且相关研究多为国外人群,两种治疗方式在国内人群中的疗效对比目前尚无报道。
本组研究苏皖人群中前列腺癌患者对两种治疗方案的反应,结果显示单药组与MAB组在无生化复发生存时间(25.4±1.0vs. 25.3±0.6,P=0.354)及总生存期(34.6±1.0vs. 36.3±0.6,P=0.215)均未观察到显著差异,两者疗效相似。
研究表明,雄激素影响前列腺癌并非单靠受体作用,还可以通过诱导某些生长因子产生,该类生长因子可影响细胞间信号传递从而导致肿瘤细胞的增值。阻断雄激素受体无法抑制雄激素这一作用机制。此外,有研究认为肾上腺源性的雄激素无法在继发性性腺功能减退的病人中诱发前列腺的增值,据此研究提出了肾上腺源雄激素对前列腺及前列腺癌并无直接影响。这些研究揭示了MAB在疗效上并不优于单药可能的的分子学及细胞学基础。
鉴于前列腺癌患者的预期寿命较其他肿瘤患者长,多数患者生存期在三年以上,在选择治疗方案时,应综合考虑患者意愿、经济条件、药物副作用等因素。本组研究显示,单药方案较MAB方案,虽然主要副作用乳房女性化(P=0.660)、乳房胀痛(P=0.455)、性欲下降(P=0.667)及骨质疏松(P=0.188)两组间无显著差异,但单药组潮热(P=0.035)、贫血(P<0.001)、肝酶异常(P<0.001)、乏力(P=0.009)及便秘(P=0.004)的发生率显著低于MAB组。 SCHMITT等[11]在一项共纳入样本6 320例的同类回顾性研究中发现,单药组便秘及疼痛的发生率显著低于MAB组,其他副反应亦未见显著差异。研究结果与本组研究相似,单药组仅在部分副反应发生率发面显示了差异。另一方面,单用LHRH-a每四周一次相较于MAB除每四周一次注射用药外,每日需次数不等的口服用药,患者依从性较好且花费更少。更易于为患者所接受。
总之,本研究首次比较了在国内中晚期前列腺癌患者中比较了单用LHRH-a及MAB方案的疗效及副作用,单用LHRH-a较MAB方案疗效相似,但部分副作用发生率较低,花费较少。
[1] SIEGEL R, NAISHADHAM D, JEMAL A. Cancer statistics, 2012 [J]. CA Cancer J Clin,2012, 62(1):10-29.
[2] PEYROMAURE M, DEBRB, MAO K, et al. Management of prostate cancer inChina: a multicenter report of 6 institutions [J]. J Urol,2005, 174(5):1794-1797.
[3] MATSUOKA T, KAWAI K, KIMURA T, et al. Long-term outcomes of combined androgen blockade therapy in stage IV prostate cancer [J].J Cancer Res Clin Oncol,2015, 141(4):759-765.
[4] HUGGINS C,HODGES CV. Studies on prostatic cancer. I. The effect of castration,of estrogen and of androgen injection on serum phosphatases in metastatic carcinoma of the prostate [J]. Cancer Res,1941,1:293-297.
[5] VALCAMONICO F, FERRARI L, CONSOLI F, et al.Testosterone serum levels and prostate cancer prognosis: the double face of Janus [J]. Future Oncol,2014, 10(7):1113-1115.
[6] OEFELEIN MG, FENG A, SCOLIERI MJ, et al. Reassessment of the definition of castrate levels of testosterone: implications for clinical decision making [J]. Urology,2000, 56(6):1021-1024.
[7] MATSUOKA T, KAWAI K, KIMURA T, et al. Long-term outcomes of combined androgen blockade therapy in stage IV prostate cancer [J]. J Cancer Res Clin Oncol,2015, 141(4):759-765.
[8] PROSTATE CANCER TRIALISTS’COLLABORATIVE GROUP. Maximum androgen blockade in advanced prostate cancer:an overview of the randomized trials [J]. Lancet,2000, 355(9214):1491-1498.
[9] SAMSON DJ, SEIDENFELD J, SCHMITT B, et al. Systematic review and meta-analysis of monotherapy compared with combined androgen blockade for patients with advanced prostate carcinoma [J]. Cancer,2002, 95(2):361-376.
[10] SCHMITT B, WILT TJ, SCHELLHAMMER PF, et al. Combined androgen blockade with nonsteroidal antiandrogens for advanced prostate cancer: a systematic review [J]. Urology,2001, 57(4):727-732.
[11] SCHMITT B, BENNETT C, SEIDENFELD J, et al. Maximal androgen blockade for advanced prostate cancer [J]. Cochrane Database Syst Rev,2000, (2):CD001526.
(编辑 王 玮)
Comparison of the efficacy and toxicity between luteinizing hormone releasing hormone analogue (LHRH-a) therapy and maximal androgen blockade (MAB) therapy in patients with advanced prostate cancer
YE Yang1,2, WANG Jun1, QIN Chao1, HUA Li-xin1
(1. Department of Urology, First Affiliated Hospital of Nanjing Medical University, Nanjing 210029;
2. Department of Urology, Ma’anshan People’s Hospital, Ma’anshan,Anhui 243000, China)
Objective To compare the efficacy and toxicity between luteinizing hormone releasing hormone analogue (LHRH-a) therapy and maximal androgen blockade (MAB) therapy in patients with advanced prostate cancer. Methods A series of 392 patients with advanced prostate cancer were included, 120 of whom
LHRH-a therapy (group A) and 272 received MAB therapy (group B). Progression-free survival (PFS), overall survival (OS) and complication rates were compared between the two groups. Results There was no significant difference between the two groups in PFS (25.4±1.0vs.25.3±0.6,P=0.354) and OS (34.6±1.0vs. 36.3±0.6,P=0.215). Group A had significantly lower incidence rate of hot flash (24.2%vs. 34.9%,P=0.035), anemia (8.3%vs. 38.2%,P<0.001), elevation of aminotransferase (5.8%vs. 23.2%,P<0.001), fatigue (8.3%vs. 18.8%,P=0.009) and constipation (3.3%vs. 12.9%,P=0.004). Conclusion LHRH-a therapy has similar efficacy as MAB but lower rate of side effects for patients with advanced prostate cancer.
prostate cancer; hormonal therapy; efficacy; side effect;androgen blockade
2014-12-09
2015-03-21
江苏省科技厅临床医学科技专项(No.BL2012027)
华立新,主任医师,硕士生导师,研究方向:前列腺癌的基础与临床研究.E-mail:fnh888@njmu.edu.cn
叶杨(1979-),男(汉族),硕士,主治医师.E-mail: roger123456789@139.com
R737
A
10.3969/j.issn.1009-8291.2015.06.005
