保泰松钙的合成及条件优化
2015-06-22吴玉祥
严 宾,吴玉祥
(精华制药集团南通有限公司,江苏南通226407)
保泰松钙的合成及条件优化
严 宾,吴玉祥
(精华制药集团南通有限公司,江苏南通226407)
目的研究保泰松钙的合成方法,确定合成工艺中关键参数。方法以保泰松为原料,经碱液溶解及成钙盐两步合成保泰松钙,并分别从氢氧化钠加入量、活性炭脱色温度、乙酸钙加入量及滴加温度和甲基叔丁基醚洗涤温度这5个条件对保泰松钙的合成产率及纯度进行研究。结果优化条件:氢氧化钠加入量为30.0 g、脱色温度为50.0℃、乙酸钙加入量为134.4 g、乙酸钙滴加温度为50.0℃及甲基叔丁基醚洗涤温度为40.0℃,经过优化使得保泰松钙的合成回收率提升至98.6%,纯度达99.7%。结论该优化方法操作简单,反应条件温和且合成得到的保泰松钙结构经质谱和核磁共振证实。
药用制剂/化学合成; 工艺学,制药; 消炎药,非甾类; 保泰松; 条件优化
非甾体抗炎药物是一类具有解热、镇痛、抗炎作用的药物,临床上广泛用于治疗炎症疾病如类风湿关节炎、骨关节炎、强直性脊椎炎、红斑性狼疮等,对感染性炎症也有一定疗效,还具有较好的抗肿瘤作用,是目前世界范围内使用最广泛的处方和非处方药之一[1-6]。保泰松属于3,5-吡唑烷二酮类非甾体抗炎药,具有很强的抗炎、镇痛作用而广泛应用于临床。在广泛应用的同时,保泰松所致消化道损伤的案例也在不断增加[7],在美国每年有10万例诱发上消化道并发症而住院病例,16 500例死亡病例。而将保泰松制成保泰松钙可依然保持原有的药理作用,并且对胃肠道刺激较小,长期大剂量使用不良反应小,凭借该优点,保泰松钙近期正受到越来越多的关注[8-10]。本实验对保泰松钙的合成工艺进行研究,并对该工艺进行了条件优化,现总结如下。
1 材料与方法
1.1 材料
1.1.1 药物与试剂 保泰松为精华制药集团南通有限公司产品(批号:BTZ130101),氢氧化钠、乙酸钙及活性炭均为国药集团化学试剂有限公司产品。
1.1.2 实验仪器 LC-20A高效液相色谱仪(日本岛津公司)、Q-Tof micro YA019高分辨质谱仪(美国Waters公司)、BrukerAVANCE400型核磁共振谱仪(TMS为内标,瑞士Bruker公司)等。
1.2 方法
1.2.1 检测方法 采用高效液相色谱法,固定相为14-甲硅烷基硅胶柱(4.0 mm×125.0 mm,5 μm),流动相为乙腈-水,梯度洗脱0~10 min[30∶70,体积比(V/V)],10~20 min(50∶50,V/V),20~35 min(60∶40,V/V),35~40 min(50∶50,V/V),40~50 min(30∶70,V/V);流速1.0 mL/min;柱温30℃;检测波长240nm;进样体积5 μL。
1.2.2 保泰松钙的合成
1.2.2.1 保泰松钠的合成 向反应瓶中加入氢氧化钠30.0 g(0.75 mol),缓慢加入纯化水700.0 mL,搅拌至溶解,加入保泰松215.0 g(0.70 mol),搅拌10 min,升温至50℃,搅拌至溶液澄清,加入6.0 g活性炭,搅拌30 min,趁热抽滤,得无色透明保泰松钠溶液,无需任何处理直接进行下一步反应。
1.2.2.2 保泰松钙的合成 将乙酸钙126.5 g(0.80 mol)溶于纯化水300.0 mL中,将1.2.2.1项合成的保泰松钠溶液加入反应瓶中,升温至50℃,保持15~20 min滴加乙酸钙溶液,搅拌30 min,冷却降温至内温30℃以下,抽滤,滤饼使用纯化水冲洗至中性,再用甲基叔丁基醚300.0mL于40℃下打浆洗涤20 min,抽滤,干燥,得到白色固体保泰松钙。
1.2.3 保泰松钙的合成条件优化
1.2.3.1 氢氧化钠加入量对保泰松钙合成产率及纯度的影响 氢氧化钠加入量分别为28.0、30.0、32.0、34.0 g,其他条件固定不变,考察保泰松钙合成产率及纯度变化。
1.2.3.2 活性炭脱色温度对保泰松钙的影响 将活性炭脱色温度设为40、45、50、55、60℃,其他条件固定不变,考察脱色温度对保泰松钙的影响。
1.2.3.3 乙酸钙加入量对保泰松钙合成产率的影响 乙酸钙加入量分别为118.6、126.5、134.4、142.3 g,其他条件固定不变,考察乙酸钙加入量对保泰松钙合成产率的影响。
1.2.3.4 乙酸钙滴加温度对保泰松钙合成产率及纯度的影响 乙酸钙滴加温度分别为40、45、50、55、60℃,其他条件固定不变,考察乙酸钙滴加温度对保泰松钙合成产率及纯度的影响。
1.2.3.5 甲基叔丁基醚洗涤温度对保泰松钙合成产率及纯度的影响 甲基叔丁基醚洗涤温度分别为30、35、40、45、50℃,其他条件固定不变,考察甲基叔丁基醚洗涤温度对保泰松钙合成产率及纯度的影响。
2 结 果
2.1 保泰松钙结构确证 合成白色固体保泰松钙278.5 g,回收率为98.6%,纯度为99.7%。保泰松钙的结构经质谱和核磁共振证实,具体结果如下。
2.1.1 保泰松钙质谱证实 高分辨质谱测得精确质量分数为961.395 8,显示该化合物(分子式为C38H38CaN4O4)由2个相同的分子(分子式为C19H19N2O2)通过钙连接。
2.1.2 保泰松钙核磁共振证实 在1H-NMR(DMSO,400 MHz)谱中,高场区出现σ0.86 2个甲基重叠,显示三重峰,σ1.28~2.04有6个亚甲基,相同部分对应的碳两两重叠,σ6.90~7.36有4个单取代苯环,4个单取代苯环相对应的邻间对位上的质子相互重叠。同时在核磁共振多键碳氢关系(HMBC)谱中,可观察到σ79.97有2个碳负离子,2个碳重叠,在13C-NMR谱中有38个碳原子。
2.2 保泰松钙合成条件优化结果
2.2.1 氢氧化钠加入量对保泰松钙合成产率及纯度的影响 氢氧化钠加入量的变化对保泰松钙的纯度无影响,但对其合成产率有一定影响,当氢氧化钠加入量为30.0 g时,保泰松钙合成产率最高,且在一定范围内不再随氢氧化钠加入量增加而提高。当氢氧化钠加入量少于30.0 g时,保泰松不能完全转化成保泰松钠,导致最终合成产率下降;而氢氧化钠加入量超过30.0 g后,由于反应液碱性增强导致后期水洗保泰松钙至中性的水量加大,保泰松钙随洗涤过程而溶解的量增多使得合成产率下降。见表1。

表1 氢氧化钠加入量对保泰松钙合成产率及纯度的影响
2.2.2 活性炭脱色温度对保泰松钙的影响 当活性炭脱色温度设定为50℃时,所得保泰松钙结果最优,脱色温度的降低或升高对保泰松钙的质量、合成产率影响较大。脱色温度低于50℃时,杂质不能完全被活性炭吸附影响后面成钙盐的反应导致合成产率及纯度下降;而脱色温度高于50℃后,由于保泰松钠盐结构不稳定,受热易分解,使得保泰松钙合成产率及纯度大幅下降。见表2。

表2 活性炭脱色温度对保泰松钙的影响
2.2.3 乙酸钙加入量对保泰松钙合成产率的影响 当乙酸钙加入量为134.4 g时,保泰松钙合成产率最高(98.6%),且不再随乙酸钙加入量的增加而增加。乙酸钙加入量低于134.4g,即为118.6、126.5 g时,保泰松钠不能完全转化成保泰松钙,使得终产率降低,分别为96.7%、93.5%;当乙酸钙加入量高于134.4 g,即为142.3 g时,保泰松钙会吸附过量的乙酸钙,需要加大水洗质量使得保泰松钙溶解在水中质量增加导致合成产率下降,为91.1%。
2.2.4 乙酸钙滴加温度对保泰松钙合成产率及纯度的影响 当乙酸钙滴加温度设为50℃时,保泰松钙合成产率及纯度最高。当温度低于50℃时,保泰松钠不能完全转化成保泰松钙,使得保泰松钙合成产率及纯度下降;由于保泰松钠盐结构不稳定,当温度高于50℃时,会使保泰松钠分解,导致保泰松钙合成产率及纯度下降。见表3。
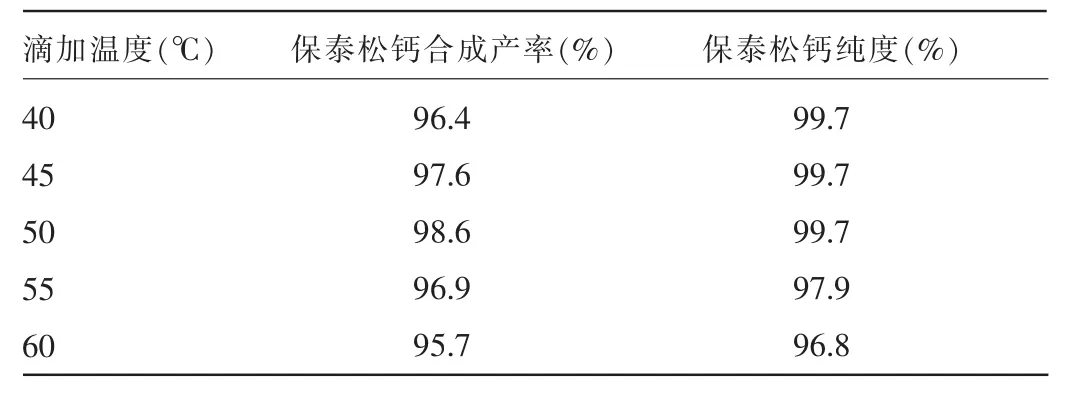
表3 乙酸钙滴加温度对保泰松钙合成产率及纯度的影响
2.2.5 甲基叔丁基醚洗涤温度对保泰松钙合成产率及纯度的影响 30~50℃内随着温度的升高,保泰松钙合成产率逐渐下降,纯度逐渐提高至不变。洗涤温度过低使得甲基叔丁基醚溶解杂质能力降低,使得纯度偏低,而洗涤温度过高使得甲基叔丁基醚在溶解杂质的同时对保泰松钙的溶解度增大,使得回收率变低,纯度未提高。综合来看,洗涤温度40℃时,保泰松钙合成产率及纯度最优。见表4。
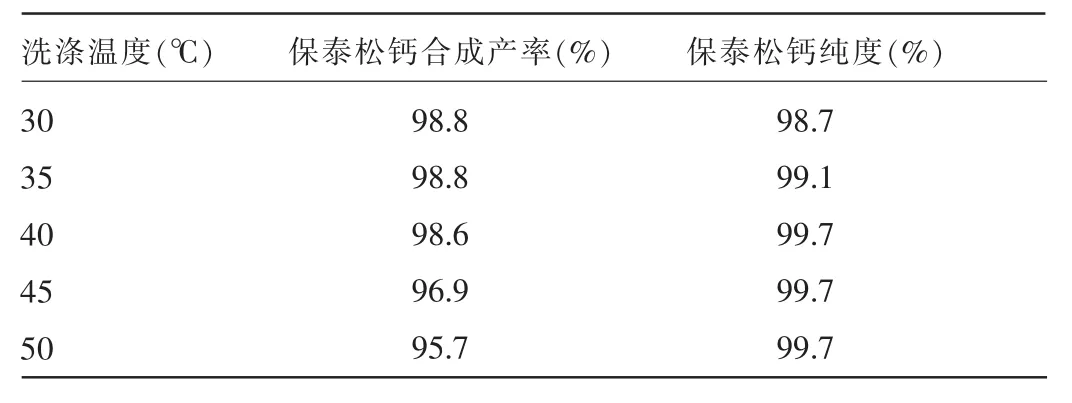
表4 甲基叔丁基醚洗涤温度对保泰松钙合成产率及纯度的影响
3 讨 论
在保泰松钙的合成实验中,分别从氢氧化钠加入量、活性炭脱色温度、乙酸钙加入量、乙酸钙滴加温度及甲基叔丁基醚洗涤温度这5个条件对保泰松钙合成产率及纯度进行考察,氢氧化钠加入量与乙酸钙加入量过少会使反应不完全,而过多会使得最终洗涤保泰松钙的水量增多,溶解保泰松钙的量增多,都使得合成产率下降。脱色、滴加及洗涤温度过低会使除杂及反应不完全,而温度过高会使保泰松钠分解变质,从而影响保泰松钙合成产率及纯度。
综合以上优化条件,以上述投料量,当氢氧化钠加入量为30.0 g,脱色温度为50℃,乙酸钙加入量为134.4 g,乙酸钙滴加温度为50℃及甲基叔丁基醚洗涤温度为40℃时以保泰松为原料合成保泰松钙为最优条件。保泰松钙最终合成产率达到98.6%,纯度为99.7%。
[1]Xia JY,Xie QM.The advancement of non-steroidal anti-inflammatory drugs and its mechanisms[J].World Pharm,2002,23:195-197.
[2]van Durme C,Wechalekar MD,Buchbinder R,et al.Nonsteroidal antiinflammatory drugs for treatment of acute gout[J].JAMA Clinical Evidence Synopsis,2015,313(2):2276-2277.
[3]Blanca-Lopez N,Barrionuevo E,Andreu I,et al.Hypersensitivity reactions to nonsteroidal anti-inflammatory drugs:from phenotyping to genotyping[J]. Curr Opin Allergy Clin,2015,15(4):285-293.
[4]Coxib and traditional NSAID Trialists′(CNT)Collaboration,Bhala N,Emberson J,et al.Vascular and upper gastrointestinal effects of non-steroidal anti-inflammatory drugs:meta-analyses of individual participant data from randomised trials[J].Lancet,2013,382(9894):769-779.
[5]Basil R,Tsioulias GJ.The evolving role of nonsteroidal anti-inflammatory drugs in colon cancer prevention:a cause for optimism[J].J Pharmacol Exp Ther,2015,353(1):2-8.
[6]Essex MN,O′Connell M,Bhadra Brown P.Response to nonsteroidal antiinflammatory drugs in African Americans with osteoarthritis of the knee[J]. J Int Med Res,2012,40(6):2251-2266.
[7]Kelley WN,Harris ED,Ruddy S,et al.Textbook of rheumatology[M].5th ed.Philadelphia:WB Saunders Company Press,1997:969-982.
[8]Yang YJ,Severin A,Chopra R,et al.3,5-Dioxopyrazolidines,novel inhibitors of UDP-N-acetylenolpyruvylglucosamine reductase(MurB)with activity against gram-positive bacteria[J].Antimicrob Agents Chem,2006,50(2):556-564.
[9]Merrington J,James M,Bradley M.Supported diazonium salts-Convenient reagents for the combinatorial synthesis of azo dye[J].Chem Commun,2002(2):140-141.
[10]MacKay RJ,French TW,Nguyen HT,et al.Effects of large doses of phenylbutazone administration to horses[J].Am J Vet Res,1983,44(5):774-780.
Synthesisofphenylbutazonecalciumanditsconditionoptimization
YanBin,WuYuxiang
(NantongPharmaceuticalCo.,Ltd.,JinhuaPharmaceuticalGroup,Nantong,Jiangsu226407,China)
ObjectiveTo study the synthetic method of phenylbutazone calcium and to determine the key parameters of synthetic technology.MethodsWith phenylbutazone as the raw material,phenylbutazone calcium was synthesized by dissolution with alkaline solution and calcium salt forming.The yield rate and purity of phenylbutazone calcium synthesis were researched from the 5 conditions of the adding amount of sodium hydroxide,active carbon decolorization temperature,adding amount of calcium acetate and dropwise adding temperature and washing temperature of methyl tertiary butyl ether.ResultsThe optimized conditions were the sodium hydroxide mass of 30.0 g,the decolorization temperature of 50.0℃,the calcium acetate amount of 134.4 g,and the dropwise add temperature of calcium acetate was 50.0℃and the wash temperature of 40.0℃.The recovery rate of phenylbutazone calcium synthesis by optimization was increased to 98.6%and the purity was reached to 99.7%.ConclusionThis method is easy to operate and its reaction condition is gentle,moreover the structure of synthesized phenylbutazone calcium is verified by the mass spectrumandnuclearmagneticresonance(NMR).
Pharmaceutical preparations/chemical synthesis; Technology,pharmaceutical; Anti-Inflammatory agents,non-steroidal; Phenylbutazone; Conditions optimization
10.3969/j.issn.1009-5519.2015.19.006
A
1009-5519(2015)19-2906-02
2015-07-14)
严宾(1980-),男,江苏南通人,硕士研究生,工程师,主要从事医药化工研究工作;E-mail:yanbin19800918@163.com。
