[60]PCBM的合成及纯化工艺
2015-06-15胡洪超崔英德
胡洪超,崔英德
(1西北工业大学材料学院,陕西 西安710072;2广州科技职业技术学院,广东 广州510550)
引 言
目前的能源消耗主要形式是化石燃料的燃烧,新能源为辅。作为不可再生资源,化石能源的储产比不断下降,到2011年底,全球已探明石油储量按目前产量 (2011年)足以维持54年,天然气则可以维持64年,估计技术上可开采的资源包括2400亿桶致密油和200万亿立方米页岩气[1-4]。另一方面化石燃料的燃烧排放大量二氧化碳,其造成的温室效应引起全球对气候变暖的担忧[5-8]。在此背景下,各国对新能源的研究和开发越来越重视。在新能源中尤以太阳能光伏技术为甚[9-10]。太阳能光伏技术经过几十年的发展,硅基太阳能电池技术已经日臻成熟,但其生产中会带来严重污染及大量能源的消耗,因此太阳能光伏的研究重点转向低成本的有机太阳能电池。有机太阳能电池核心由给体材料和受体材料组成,PCBM是有机太阳能电池常用的受体材料。
PCBM是富勒烯的衍生物,常见的有 [60]PCBM 和 [70]PCBM, [60]PCBM 全称 [6,6]-苯基-C61-丁酸异甲酯, [70]PCBM 全称 [6,6]-苯基-C71-丁酸异甲酯,其继承了富勒烯的共轭笼状碳分子结构使得其具有极好的电子容纳能力,具有很高的电子迁移性。富勒烯引入了苯环、碳链和酯基团使得其具有较好的溶解性。在研究中发现其余常见的聚合物电子给体材料如高规整聚3-己基噻吩 (rr-p3HT)能形成良好的相分离。以上特点使其成为有机太阳能电池电子受体的标准物质,从1995年PCBM首先被用于聚合物太阳能电池中到现在,尽管给体材料研究热点从聚亚乙烯 (PPV)到聚3-己基噻吩 (rr-p3HT)再到聚芴等不断进化,但受体材料一直是以PCBM 为主[11-20]。因此PCBM在有机太阳能电池的研究和未来应用中占据非常重要的地位。
PCBM 由富勒烯C60或C70和5-苯基-5-(对甲苯磺酰肼基)戊酸甲酯在邻二氯苯中回流制取[21-24]。C60,C70的制备法有激光法、电弧法和火焰法。激光法为微量的制备方法,火焰法可以得到较高的富勒烯产率,但实验条件难以控制;电弧法能够宏观量地制备出富勒烯,制备装置简单,易操作,但产率不高,仅为8.26%。这3种方法制成的富勒烯包含C60、C70及高碳富勒烯,因此纯净的富勒烯C60或C70等获取难度较大,价格高昂。PCBM的合成产率也不高,以 [60]PCBM为例,收率仅为约35%,以消耗C60计算为83%,分离纯化到99%以上工艺复杂。这些因素造成了高纯度PCBM获取成本高昂。适用于聚合物太阳能电池用的高纯度PCBM价格昂贵,99.9%的 [70]PCBM 市面售价高达120000CNY·g-1。
本文以C60,对甲苯磺酰肼和4-苯甲酰基丁酸为原料采用一锅法合成 [60]PCBM,重点探讨提高以消耗C60计算的产率和纯化工艺技术。
1 实验部分
1.1 主要试剂及纯化
邻二氯苯 (天津市科密欧化学试剂有限公司,分析纯)与浓硫酸按体积比1∶1混合,振荡摇匀,水洗,无水CaCl2干燥,用玻璃填充柱过滤,加入五水P2O5,120℃下减压蒸馏,收集馏分。取1g硼氢化钠加入1L甲醇 (广州试剂厂,分析纯)中,缓慢连续通入氩气,在30℃下将溶液回流24 h,加入约1g新切钠片 (先用甲醇洗涤),30℃下按前述方法回流24h,在70℃蒸馏。在30℃下,1 L甲苯 (天津市科密欧化学试剂有限公司,分析纯)中加入100ml浓硫酸,振荡两次,水洗一次,再加入0.1mol·L-1氢氧化钠溶液洗涤一次,再水洗一次,加入20g五氧化二磷,回流30min后蒸馏。往1L吡啶 (广州试剂厂,分析纯)中加入20g烘干过的氢氧化钾,放置2周后取上层清液使用。对甲苯磺酰肼 (上海国药,分析纯),未进一步纯化。4-苯甲酰基丁酸 (上海国药,分析纯),未进一步纯化。C60(苏州大德纳米科技,95%),未进一步纯化。甲醇钠,自制。
1.2 仪器
美国Nicolet 800型红外光谱仪 (KBr压片),日本岛津UV-3150型紫外可见分光光度计,瑞士Brucker DMX-300型核磁共振波谱仪,英国Waters HPLC/MS。
1.3 合成
4-苯甲酰基丁酸与甲醇以浓盐酸催化酯化,然后用对甲苯磺酰肼与产物反应合成5-苯基-5-(对甲苯磺酰肼基)戊酸甲酯,在吡啶溶液中将产物与甲醇钠回流得到5-苯基-5-(对甲苯磺酰肼基)戊酸甲酯,见反应步骤1。将得到的5-苯基-5-(对甲苯磺酰肼基)戊酸甲酯和C60在邻二氯苯中回流即可得[60]PCBM,见反应步骤2 。


4-苯 甲 酰 基 丁 酸 3.85g (0.02mol),氯 苯100ml和甲醇20ml加入250ml三口烧瓶中,搅拌溶解。缓慢滴加浓盐酸5ml(0.06mol),搅拌加热至90℃,回流反应12h。反应毕后用1mol·L-1的碳酸氢钠溶液中和反应液至中性,然后用100ml乙酸乙酯萃取反应液3次,取乙酸乙酯层。用100ml水洗涤乙酸乙酯溶液2次,加入无水氯化钙,50℃下减压蒸馏除去乙酸乙酯。在硅胶柱中将产物洗脱分离,洗脱剂为乙酸乙酯/正己烷 (体积比3∶1),得无色油状4-苯甲酰基丁酸甲酯 3.5g,产率85%。
4-苯甲酰基丁酸甲酯2.1g (0.01mol)、对甲苯磺酰肼2.3g (0.012mol)和30ml甲 醇 在100ml三口烧瓶中,搅拌回流反应6h,回流温度为4℃。反应毕后冷却至室温,密封24h。将产物快速冷冻到-15℃,析出白色晶体。抽滤,用4℃的甲醇洗涤滤饼,在40℃真空下干燥滤饼至恒重,得白色固体5-苯基-5-(对甲苯磺酰肼基)戊酸甲酯3.6g,产率95%。
常温下将5-苯基-5-(对甲苯磺酰肼基)戊酸甲酯2.25g (0.006mol)溶于50ml吡啶,将溶液加入250ml三口烧瓶,充入氮气保护。往三口烧瓶中 加 入 甲 醇 钠 0.35g (0.0065mol), 搅 拌20min。将2.16g C60溶于100ml邻二氯苯中,然后逐滴将此C60溶液加入三口烧瓶中。加热回流反应24h。
1.4 产物的纯化
反 应 产 物 在 0.01mmHg (1mmHg=133.322Pa)下用旋转蒸发仪浓缩至约80ml。用100ml的氯苯预洗40×10cm的硅胶柱。用预洗过的硅胶柱分离浓缩液,硅胶管中分成3层,紫红色,棕色和红褐色,先用200ml氯苯洗涤,然后用500ml甲苯洗涤。首先洗涤出来的是未反应完的C60,将收集起来的C60溶液旋转蒸发浓缩至约20ml,转移至150ml离心管,加入100ml乙醚,超声振荡5min,离心分离,滤去清液,再重复上面步骤2次,0.01mmHg,70℃下真空干燥,残余固体质量1.25g,已反应比例为42.1%。棕色层采用同样方式获得干燥固体0.23g。用甲醇代替乙醚洗涤红褐色层3次,真空干燥得固体物0.95g,产率34%,基于已反应的C60为81%。
将 [60]PCBM产物经过硅胶分别用氯苯和甲苯洗涤后获得的浓度达到95.8%,但仍与电子级的要求相差较大。为获得高纯度的 [60]PCBM,结合HPLC,以图1的工艺对产物进一步纯化。采用buckprep(4.6×250nm)色谱柱作为过滤载体,周期性间歇式过滤。每个周期为8min,第0~0.5min,高压泵和阀门2、阀门4同时打开;第0.5~4.5min,高压泵和阀门1、阀门4同时打开;第4.5~5.5min,高压泵和阀门1、阀门3同时打开;第5.5min~8min,高压泵和阀门1、阀门4同时打开。泵出口压力为3MPa,出口流速5.4ml·min-1。
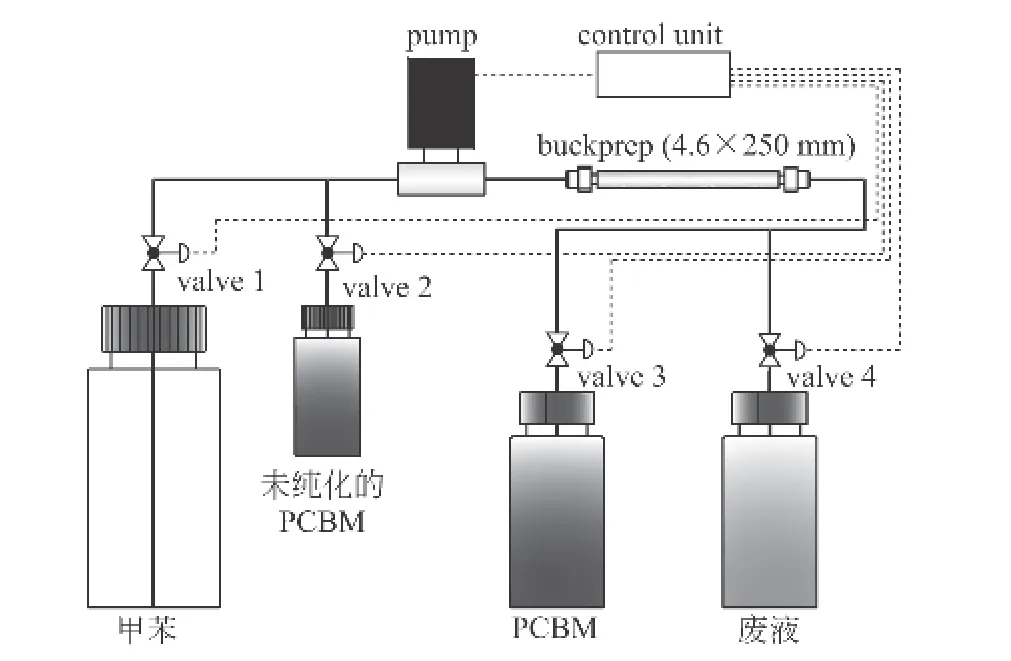
图1 [60]PCBM纯化工艺Fig.1 Purification of[60]PCBM
经过此工艺流程, [60]PCBM产物由初始95.8%纯化至99.5%,见表1 。

表1 深度纯化前后HPLC数据Table 1 Data of deeper purification
2 结果与讨论
2.1 产物的表征
产物的FTIR谱图 (图2)(KBr压片)中,3422cm-1处为苯环 C—H 伸缩振动吸收峰;2940cm-1处为饱和 C—H 伸缩振动吸收峰;1736cm-1处为酯键 C=O伸缩振动吸收峰;1600~1493cm-1处为苯环骨架振动吸收峰;1445、1349cm-1处 为—CH3、—CH2—特 征 吸 收 峰;1427、1186、572、525cm-1处为C60的特征吸收峰;1248cm-1处为酯键C—O—C非对称伸缩振动吸收峰。
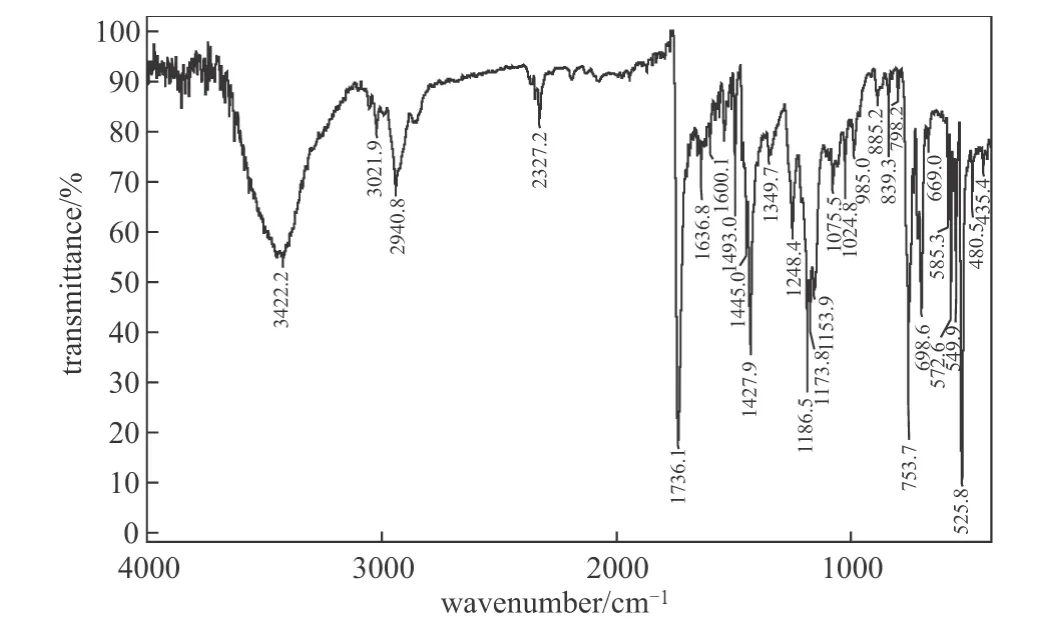
图2 纯化后产物IR图Fig.2 IR spectrum of purication sample
产物的1H NMR谱图见图3。1H NMR(500 MHz,CDCl3)δ7.96 (d,2H;o-H,arom),7.56(m,2H;m-H,arom),7.28 (m,1H;p-H,arom),3.70 (s,3H;OCH3),2.92 (m,2H;PhCCH2),2.57 (t,J=7.5Hz,2H;CH2CO2R),2.21 (m,2H;CH2CH2CO2R)。
综合IR谱和1H NMR谱的表征结果可以判断产物为预期的 [60]PCBM。

图3 纯化后产物1 H NMR图Fig.3 1 H NMR spectrum of purication sample
2.2 产物收率提高的改进
C60价格昂贵,提高反应收率对降低 [60]PCBM的成本有重大作用。[60]PCBM的合成收率产率34%。因只有42.1%的C60参加反应,基于已经反应的C60计算,C60的转化率为81%,有19%的C60生成了副产物。在化学工业生产中面对产率不高时常常将回收的原料及副产物重新投入反应中以获取相对消耗的原料的高转化率。其原因有两点:一是未反应的产物得以重新反应,另一点是,副产物重新投入反应中可抑制新的副反应的发生。基于此原理,将之前从硅胶柱过滤收集到的未反应C60和副产物与1g新鲜C60一起重复反应步骤的合成工艺,并纯化,获得产物1.18g,按新鲜C60来计算产率为
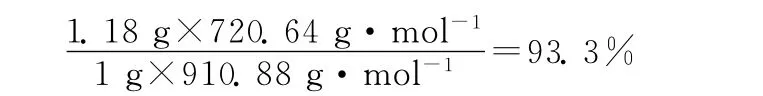
从实验中验证了此方案的可行性,将回收的C60和副产物重新加入,抑制了新的副产物产生,使得新鲜C60转化为 [60]PCBM的收率由81%提高 到 93.3%, 即 用 1g C60收 获 1.18g [60]PCBM。副产物重新回炉的方案明显提高C60收获率。
3 结 论
以4-苯甲酰基丁酸、对甲苯磺酰肼和C60等为原料,采用一锅法逐步合成 [60]PCBM,用硅胶柱为分离载体,获取纯度为95.8%的产物。为了提高产物纯度,结合HPLC分离技术,使产物纯度提高至99.5%。用1H NMR和IR表征,证明其为目标产物。为提高收率,将回收的C60和副产物与新鲜C60一起投入反应体系,按新鲜C60来计算收获率达到93.3%。通过这两步工艺的改善,获得了99.5%的高纯度产物,并且使C60的利用率大幅提高。
[1] BP.BP Energy Outlook 2030 [M].London,2013.
[2] IEA.World Energy Outlook 2000 [M].OECD,2000.
[3] IEA.World Energy Outlook 2011 [M].OECD,2011.
[4] IEA.World Energy Outlook [M].Paris,2012.
[5] Ivanova M.UNEP in global environmental governance:design,leadership,location [J].GlobalEnvironmental Politics,2010,10 (1):30-59.
[6] National Research Council.Committee on Health.Hidden Costs of Energy:Unpriced Consequences of Energy Production and Use[M].National Academies Press,2010.
[7] Shindell D.Integrated Assessment of Black Carbon and Tropospheric Ozone:Summary for Decision Makers [M].United Nations Environment Programme,2011.
[8] Cofala J,etal.Emissions of Air Pollutants for the World Energy Outlook 2011Energy Scenarios [M].Laxenburg,Austria:International Institute for Applied Systems Analysis(IIASA),2011.
[9] China National Development and Reform Commission (中国国家发展和改革委员会).Long Term Development Plan for Renewable Energy[M].Beijing,2007.
[10] IEA.Energy Technology Perspectives[M].Paris,2008.
[11] Kale T S.Molecular Designs for Organic Semiconductors:Design,Synthesis and Charge Transport Properties [M].2011.
[12] Shaheen S E,etal.2.5%efficient organic plastic solar cells[J].AppliedPhysicsLetters,2001,78:841.
[13] Brabec C J,etal.Origin of the open circuit voltage of plastic solar cells [J].AdvancedFunctionalMaterials,2001,11(5):374-380.
[14] Li Y.Molecular design of photovoltaic materials for polymer solar cells:Toward suitable electronic energy levels and broad absorption [J].AccountsofChemicalCesearch,2012,45(5):723-733.
[15] Sariciftci N S,etal.Photoinduced electron transfer from a conducting polymer to buck sterfullerene [J].Science,1992,258 (5087):1474.
[16] Scharber M C,etal.Design rules for donors in bulk heterojunction solar cells towards 10%energy conversion efficiency [J].AdvancedMaterials,2006,18 (6):789-794.
[17] Zerza G,etal.Ultrafast charge transfer in conjugated polymer-fullerene composites [J].SyntheticMetals,2001,119 (1-3):637-638.
[18] Ye Huaiying (叶怀英),Li Wen (李文),etal.Research progress of polymer materials for organic solar cells [J].Chin.J.Org.Chem.(有机化学),2012,32:266-283.
[19] Li G,Zhu R,Yang Y.Polymer solar cells [J].Nat.Photon,2012,6 (3):153-161.
[20] McGehee M D.Nanostructured organic-inorganic hybrid solar cells[J].MRSBulletin,2009,34 (2):95-100.
[21] Fan Lishen (范 利 生 ),etal.Preparation and thermal stability of novel polymer solar cell electron acceptor materials[J].FineChemicals(精细化工),2013,30 (3):248-252.
[22] Li Yongfang (李永舫).High efficiency conjugated polymer donor and fullerene derivative acceptor photovoltaic materials for polymer solar cells [J].PolymerBulletin(高分子通报),2011,(10):33-49.
[23] Zheng Liping (郑立平),etal.Synthesis of three novel C60derivatives and their photovoltaic cell performance[J].Acta ChimicaSinica(化学学报),2004,(1):16.
[24] Hummelen J C,etal.Preparation and characterization of fulleroid and methanofullerene derivatives [J].TheJournal ofOrganicChemistry,1995,60 (3):532-538.
