苯加氢烷基化制环己基苯催化剂的制备与工艺条件的考察
2015-06-06单玉华司坤坤李明时鲁墨弘
曹 鹰,单玉华,司坤坤,栾 灵,李明时,鲁墨弘
(常州大学 江苏省精细石油化工重点实验室,江苏 常州 213164)
苯加氢烷基化制环己基苯催化剂的制备与工艺条件的考察
曹 鹰,单玉华,司坤坤,栾 灵,李明时,鲁墨弘
(常州大学 江苏省精细石油化工重点实验室,江苏 常州 213164)
采用等体积浸渍法制备了Ni-Cu/Hβ双功能催化剂,采用XRD、N2吸附-脱附、TEM和NH3-TPD方法对催化剂进行了表征,并将其用于催化苯加氢烷基化制备环己基苯的反应,考察了催化剂的制备条件(Ni负载量、Ni和Cu的来源、助催化剂的种类)和反应条件(反应时间、反应温度、氢气压力、催化剂用量)对反应的影响。实验结果表明,适宜的催化剂制备条件和反应条件为:Ni和Cu的来源分别为乙酸镍和硝酸铜、负载量分别为4%(w)和0.2%(w);反应温度210 ℃、氢气压力2 MPa、反应时间1 h、催化剂用量5%(w)(基于苯的质量)。在此条件下,苯的转化率可达57.74%,环己基苯的选择性可达71.38%。催化剂的金属活性位和酸性是苯加氢烷基化的关键因素。
镍-铜/Hβ;双功能催化剂;苯;加氢烷基化反应;环己基苯
环己基苯是一种重要的化工中间体,通过环己基苯的氢过氧化反应可制备苯酚和环己酮[1-3]。与异丙苯法制备苯酚和丙酮[4]相比,采用环己基苯氢过氧化反应制备苯酚和环己酮,不存在丙酮过剩的问题。环己基苯还可用作液晶材料中间体,也可用作锂电池二次电池有机电解液的添加剂[5-6]。
金属催化剂催化苯加氢合成体系[7-9]已被广泛研究,而在酸催化下苯可与环己烯进行烷基化反应生成环己基苯。Bull[10]首次报道了在Ni/P2O5催化剂作用下苯加氢烷基化生成环己基苯,随后研究人员又进行了对甲苯磺酸和吡啶类离子液体催化苯与环己烯生成环己基苯以负载金属的MCM分子筛催化苯加氢烷基化反应等研究[11-13]。Fahy等[14]研究了稀土处理后的13X分子筛负载Ni和Pt的催化剂,Pt能促进苯的烷基化反应,稀土元素能平衡金属活性和酸性,但苯的转化率低。邱俊等[15]报道了Pd/ Hβ双功能催化剂催化苯加氢烷基化反应,在H2压力2.5 MPa、温度200 ℃和空速3 h-1的条件下,苯转化率为24.3%、环己基苯选择性为88.0%、环己基苯收率仅为21.38%,苯转化率和环己基苯收率较低。Borodina等[16]报道了负载Ni和Ru的分子筛催化剂催化乙苯烷基化反应,选择性为78%,但乙苯转化率仅为30%。Abu Bakara等[17]研究了低温下苯在Pt-Ni/MCM-41催化剂作用下的反应。董帅帅等[18]报道了Ru/Hβ双功能催化剂催化苯加氢烷基化反应,在H2压力2.5 MPa、温度200 ℃和反应时间4 h的条件下,苯转化率达67.57%、环己基苯选择性可达47.8%,环己基苯的选择性较低且反应时间较长。
本工作以Ni为活性组分、Cu为助剂、Hβ分子筛为载体,制备了Ni-Cu/Hβ双功能催化剂;采用XRD、N2吸附-脱附、TEM和NH3-TPD方法对催化剂进行了表征,并将其用于苯加氢烷基化制备环己基苯的反应,考察了催化剂的制备条件和反应条件对该反应的影响。
1 实验部分
1.1 主要仪器与试剂
D/Max 2500PC型X射线衍射仪:日本理学公司;ASAP 2010C型表面孔径吸附仪:Micromeritics公司;GC-7800型气相色谱仪:滕州京鲁伟业科学仪器有限公司,30 m×0.250 mm×0.25 μm的DB-210毛细管柱;Chembet-3000型化学吸附仪:Quantachrome公司;JEM-2100型高分辨透射电子显微镜:日本电子株式会社。
苯:AR,国药集团化学试剂有限公司;Hβ分子筛原粉:南开大学催化剂厂,硅铝比50;环己烷(AR)、环己基苯(工业级):江苏永华精细化工有限公司;乙酸镍(AR)、环己烯(CP):阿拉丁试剂公司;硝酸铜:AR,上海新宝精细化工厂。
1.2 催化剂的制备
依次称取1.696 1 g乙酸镍和0.076 0 g硝酸铜,配制成45 mL溶液,将9.56 g Hβ分子筛加入到15 mL溶液中进行等体积浸渍,然后置于超声波中超声1 h,在80 ℃下恒温真空干燥,重复3次。将干燥后的固体研磨,在马弗炉中于500 ℃下煅烧4 h,最后在混合气(N2与H2体积比9∶1)中于400 ℃下还原4 h,得到催化剂4%(w)Ni-0.2%(w)Cu/Hβ催化剂。改变金属来源、助金属种类及Ni负载量,采用相同的方法制备其他催化剂。
1.3 催化剂的活性评价
催化剂的活性评价实验在100 mL高压反应釜中进行,将32 g苯和1.6 g催化剂加入反应釜中,用N2置换空气3次,放空N2,将反应釜加热至反应温度,待温度稳定后通入H2,连通反应气体钢瓶保持反应压力不变,待到设定反应时间时用针阀取料,通过离心分离将取料带出的少许固体催化剂分离,取上层清液进行气相色谱分析。转化率及选择性的计算式如下:

式中,X为苯的转化率,%;nC为转化的苯的物质的量,mol;nF为投料的苯的物质的量,mol;SCHB,SCH,SDCH分别为环己基苯、环己烷和双环己基苯的选择性,%;nCHB,nCH,nDCH分别为转化为环己基苯、环己烷和双环己基苯的苯的物质的量,mol。
2 结果与讨论
2.1 催化剂的表征
试样的XRD谱图见图1。从图1中2θ=7.8°,22.4°处的特征衍射峰可看出,Hβ分子筛完全结晶且未发现其他晶相。从图1还可看出,Ni和Cu的负载没有破坏Hβ分子筛的结构。

图1 试样的XRD谱图Fig.1 XRD patterns of the samples.(1) 4%(w)Ni-0.2%(w)Cu/Hβ;(2) Hβ Sources of Ni and Cu:nickel acetate and cupric nitrate,the same below,except Table 2.Cu;Ni
试样的比表面积、孔体积和孔径见表1。从表1可看出,与Hβ分子筛相比,负载Ni和Cu后催化剂的比表面积明显增大,孔体积与孔径变化不大。

表1 试样的比表面积、孔体积和孔径Table 1 BET specific surface area(SBET),pore volume(VP) and pore diameter(DP) of the samples
4%(w)Ni-0.2%(w)Cu/Hβ催化剂的TEM照片见图2。由图2可见,该催化剂中Ni和Cu金属粒子较均匀地分散在Hβ分子筛载体上,平均粒径为10~15 nm,金属粒子的分散性较好。
4%(w)Ni-0.2%(w)Cu/Hβ催化剂的NH3-TPD谱图见图3。由图3可见,该催化剂除在225 ℃附近出现脱附峰外,还在475 ℃附近出现更强的脱附峰,说明催化剂除了有弱酸中心外,更多的是强酸中心。

图2 4%(w)Ni-0.2%(w)Cu/Hβ催化剂的TEM照片Fig.2 TEM images of the 4%(w)Ni-0.2%(w)Cu/Hβ catalyst.

图3 4%(w)Ni-0.2%(w)Cu/Hβ催化剂的NH3-TPD谱图Fig.3 NH3-TPD curve of the 4%(w)Ni-0.2%(w)Cu/Hβ catalyst.
2.2 催化剂制备条件对反应的影响
2.2.1 Ni负载量的影响
Ni负载量对Ni-0.2%(w)Cu/Hβ催化剂催化苯加氢烷基化反应的影响见图4。从图4可看出,随Ni负载量的增加,苯的转化率逐渐增大,在Ni负载量达4%(w)后,苯的转化率增幅减小;环己基苯的选择性不断减小,环己烷和双环己基苯的选择性不断增加。当Ni负载量达4%(w)时,反应能达到较好的平衡,环己基苯的选择性和苯的转化率均较理想。因此,选择Ni负载量达4%(w)较适宜。
2.2.2 Ni和Cu的来源
Ni和Cu的来源对4%(w)Ni-0.2%(w)Cu/Hβ催化剂催化苯加氢烷基化反应的影响见表2。由表2可见,Ni和Cu的来源不同时,苯的转化率相差较大,环己基苯的选择性相差不是很大,副产物环己烷很少。以乙酸镍和硝酸铜为Ni和Cu的来源时,苯的转化率和环己基苯的选择性较理想。

图4 Ni负载量对Ni-0.2%(w)Cu/Hβ催化剂催化苯加氢烷基化反应的影响Fig.4 Effects of Ni loading on the catalytic performances of the Ni-0.2%(w)Cu/Hβ catalyst for the hydroalkylation of benzene to CHB. Reaction conditions:210 ℃,p(H2)=2 MPa,1 h,catalyst dosage 5%(w)(based on the mass of benzene),32 g benzene. CHB:cyclohexylbenzene;DCH:dicyclohexylbenzene;CH:cyclohexane.Conversion of benzene;Selectivity to CHB;Selectivity to DCH;Selectivity to CH

表2 Ni和Cu的来源对4%(w)Ni-0.2%(w)Cu/Hβ催化剂催化苯加氢烷基化反应的影响Table 2 Effects of the sources of Ni and Cu on the catalytic performances of the 4%(w)Ni-0.2%(w)Cu/Hβ catalyst for the hydroalkylation of benzene to CHB
2.2.3 助催化剂的影响
助剂对4%(w)Ni/Hβ催化剂催化苯加氢烷基化反应的影响见表3。由表3可看出,与Ni/Hβ催化剂相比,Pt的加入加快了加氢反应速率,使环己烷的选择性大幅增加;Pd,Ru,Ir,Re的加入也加快了加氢反应速率,但环己烷的选择性较低,环己基苯的选择性也偏低,双环己基苯的选择性偏高;Cu的加入使苯的转化率与环己基苯的选择性均有所提高,且环己烷和双环己基苯的选择性变化不大,Cu本身并没有加氢活性,但作为过渡金属元素,具有d轨道,可与环己烯产生很强的作用力,促使环己烯从催化剂上脱附,故助催化剂Cu的加入使得金属的加氢活性与分子筛的酸性能达到较好的平衡。

表3 助剂对4%(w)Ni/Hβ催化剂催化苯加氢烷基化反应的影响Table 3 Effects of promoters on the catalytic performances of the 4%(w)Ni/Hβ catalyst for the hydroalkylation of benzene to CHB
2.3 反应条件对反应的影响
2.3.1 反应时间的影响
反应时间对4%(w)Ni-0.2%(w)Cu/Hβ催化剂催化苯加氢烷基化反应的影响见图5。由图5可见,随反应时间的延长,环己烷的选择性变化不大,苯的转化率与双环己基苯的选择性增加,环己基苯的选择性降低。这可能是由于环己基苯在反应时间充裕的条件下继续与环己烯反应生成了双环己基苯,说明反应时间是苯加氢烷基化选择性合成环己基苯的重要影响因素之一。与邱俊等[15]报道的苯加氢烷基化反应在3 h时苯的转化率达24.3%、环己基苯的选择性达88.0%相比,本实验在反应1 h时苯的转化率可达57.74%、环己基苯的选择性可达71.38%,环己基苯的收率有所提高且反应时间缩短了2 h。综合来看,最佳反应时间为1 h。
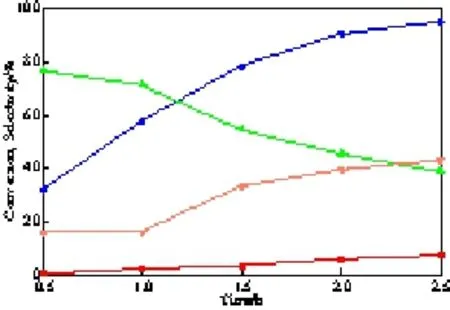
图5 反应时间对4%(w)Ni-0.2%(w)Cu/Hβ催化剂催化苯加氢烷基化反应的影响Fig.5 Effects of reaction time on the catalytic performances of 4%(w) Ni-0.2%(w)Cu/Hβ for the hydroalkylation of benzene to CHB. Reaction conditions:210 ℃,p(H2)=2 MPa,catalyst dosage 5%(w) and 32 g benzene.Conversion of benzene;Selectivity to CHB;Selectivity to DCH;Selectivity to CH
2.3.2 氢气压力的影响
氢气压力对4%(w)Ni-0.2%(w)Cu/Hβ催化剂催化苯加氢烷基化反应的影响见图6。由图6可见,随氢气压力的增加,苯的转化率从57.74%增至90.01%,但环己基苯的选择性从71.38%降至46.21%,且双环己基苯的选择性迅速增长,环己烷的选择性增加缓慢且较小,说明其受压力影响较小。从图7可看出,氢气压力的增加不利于苯加氢烷基化反应,氢气压力为2 MPa时最佳。
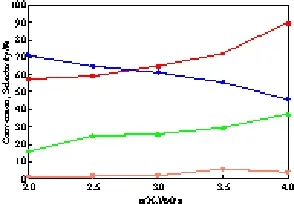
图6 氢气压力对4%(w)Ni-0.2%(w)Cu/Hβ催化剂催化苯加氢烷基化反应的影响Fig.6 Effects of hydrogen pressure on the catalytic performances of 4%(w)Ni-0.2%(w)Cu/Hβ for the hydroalkylation of benzene to CHB. Reaction conditions:210 ℃,1 h,catalyst dosage 5%(w) and 32 g benzene.Conversion of benzene;Selectivity to CHB;Selectivity to DCH;Selectivity to CH
2.3.3 反应温度的影响
反应温度对4%(w)Ni-0.2%(w)Cu/Hβ催化剂催化苯加氢烷基化反应的影响见图7。

图7 反应温度对4%(w)Ni-0.2%(w)Cu/Hβ催化剂催化苯加氢烷基化反应的影响Fig.7 Effects of reaction temperature on the catalytic performances of 4%(w)Ni-0.2%(w)Cu/Hβ for the hydroalkylation of benzene to CHB. Reaction conditions:p(H2)=2 MPa,1 h,catalyst dosage 5%(w) and 32 g benzene.Conversion of benzene;Selectivity to CHB;Selectivity to DCH;Selectivity to CH
由图7可见,随反应温度的升高,苯的转化率提高;环己基苯的选择性从66.16%升至71.38%后降至66.94%,说明过高的反应温度会降低环己基苯的选择性,这可能是因为反应温度过高,使环己基苯进一步加氢;双环己基苯的选择性从24.55%降至14.20%;环己烷的选择性变化不大,受温度影响较小。210 ℃下环己基苯的选择性与文献[18]报道的环己基苯的选择性(47.8%)相比,提高了23.58百分点。综合来看,最佳反应温度为210 ℃。
2.3.4 催化剂用量的影响
催化剂用量对4%(w)Ni-0.2%(w)Cu/Hβ催化剂催化苯加氢烷基化反应的影响见图8。由图8可见,苯的转化率随催化剂用量的增加而增大,环己烷、环己基苯和双环己基苯的选择性都是先增大后减小,当催化剂用量为3.75%(w)(基于苯的质量)时,环己烷和双环己基苯的选择性达到最大,但环己基苯的选择性并未达到最大;当催化剂用量达5%(w)时,环己基苯的选择性达到最大值71.38%,且苯的转化率达57.74%。由此得出,在催化剂用量为5%(w)时,目标产物收率较高。

图8 催化剂用量对4%(w)Ni-0.2%(w)Cu/Hβ催化剂催化苯加氢烷基化反应的影响Fig.8 Effects of catalyst dosage on the catalytic performances of 4%(w)Ni-0.2%(w)Cu/Hβ for the hydroalkylation of benzene to CHB. Reaction conditions:210 ℃,p(H2)=2 MPa,1 h,32 g benzene.Conversion of benzene;Selectivity to CHB;Selectivity to DCH;Selectivity to CH
3 结论
1)多次等体积浸渍制得的Ni-Cu/Hβ催化剂显示了良好的活性与选择性,Ni提供了较高的加氢活性,Cu的加入使Ni的加氢活性与分子筛的酸性达到较好的平衡。
2)苯加氢烷基化合成环己基苯的最佳催化剂制备条件和反应条件为:Ni和Cu的来源分别为乙酸镍和硝酸铜、负载量分别为4%(w)和0.2% (w);反应温度210 ℃、氢气压力2 MPa、反应时间1 h、催化剂用量5%(w)。在此条件下,苯的转化率达57.74%,环己基苯的选择性达71.38%。
[1] Koichi Sato,Satoshi Hamakawa,Mayumi Natsui,et al. Palladium-Based Bifunctional Membrane Reactor for One-Step Conversion of Benzene to Phenol and Cyclohexanone[J]. Catal Today,2010,156(3/4):276 - 281.
[2] 侯蓉,单玉华,储海霞,等. 环己基苯催化氧化合成苯酚和环己酮[J]. 石油化工,2012,41(9):1023 - 1027.
[3] Exxonmobil Chemical Patents Inc. Process for Producing Phenol from Cyclohexylbenzene Hydroperoxide:WO,2013052216 A1[P]. 2013-11-04.
[4] 孙然功,凌志,邹长军,等. 异丙苯法苯酚丙酮装置副产苯酚焦油催化裂化研究[J]. 石油化工应用,2010,29 (2/3):31 - 33.
[5] 广州市天赐高新材料科技有限公司. 一种动力型锂离子电池用电解液:中国,1925206[P]. 2007-03-07.
[6] 比亚迪股份有限公司. 一种混合添加剂及其配制的锂离子二次电池电解液:中国,l 953267[P]. 2007-04-25.
[7] Zhou Gongbing,Pei Yan,Jiang Zheng,et al. Doping Effects of B in ZrO2on Structural and Catalytic Properties of Ru/B-ZrO2Catalysts for Benzene Partial Hydrogenation[J]. J Catal,2014,311(7):393 - 403.
[8] Liao Hongguang,Ouyang Donghong,Zhang Jing,et al. Benzene Hydrogenation over Oxide-Modified MCM-41 Supported Ruthenium-Lanthanum Catalyst: The Influence of Zirconia Crystal Form and Surface Hydrophilicity[J]. Chem Eng J, 2014,243(11):207 - 216.
[9] Huang Haiyan,Yu Ying,Chung K H. Performance of Au/ Nafion/Pt Electrodes in Benzene-Water Electrochemical Hydrogenation[J]. Int J Hydrogen Energy,2014,39(25): 13832-13837.
[10] Bull R T. Catalytic Hydrogenation of Aromatic Hydrocarbons in Liquid Media in the Presence of Nickel Black and Phosphoric Anhydride[J]. Soc Chim,1934,1(5):391 - 406.
[11] 嘉兴学院. 一种制备环己基苯的方法:中国:101811924 A [P]. 2010-08-25.
[12] Exxonmobil Chemical Patents Inc. Activation and Use of Hydroalkylation Catalysts:WO, 2012050751 A1[P]. 2012-04-19.
[13] Exxonmobil Chemical Patents Inc. Process for Producing Cyclohexylbenzene:WO,20121122031 A1[P]. 2012-08-23.
[14] Fahy J,Trimm D L,Cookson D J. Four Component Catalysis for the Hydroalkylation of Benzene to Cyclohexyl Benzene[J]. Appl Catal:A,2001,211(2): 259 - 268.
[15] 邱俊,小村贞一,窒田好浩,等. Pd/Hβ双功能催化剂上苯加氢烷基化合成环己基苯[J]. 催化学报,2007,28(3):246 - 250.
[16] Borodina I B,Ponomareva O A,Yushchenko V V,et al. Hydroalkylation of Benzene and Ethylbenzene over Metal-Containing Zeolite Catalysts[J]. Microporous Mesoporous Mater,2007,105(1/2):181 - 188.
[17] Abu Bakara N H H,Bettahara M M,Abu Bakarb S M, et al. Low Temperature Activation of Pt/Ni Supported MCM-41 Catalysts for Hydrogenation of Benzene[J]. J Mol Catal A:Chem,2010,333(1/2):11 - 19.
[18] 董帅帅,单玉华,徐文杰,等. 苯加氢烷基化合成环己基苯催化剂研究[J]. 现代化工,2013,33(8):73 - 77.
(编辑 王 萍)
Catalyst and Process of Benzene Hydroalkylation to Cyclohexylbenzene
Cao Ying,Shan Yuhua,Si Kunkun,Luan Ling,Li Mingshi,Lu Mohong
(Key Lab of Jiangsu Fine Chemical Engineering,Changzhou University,Changzhou Jiangsu 213164,China)
Bifunctional Ni-Cu/Hβ catalysts for the hydroalkylation of benzene to cyclohexylbenzene were prepared by impregnation method and characterized by means of XRD,N2adsorptiondesorption,TEM and NH3-TPD. The effects of the catalyst preparation conditions,namely Ni loading,cocatalysts and sources of Ni and Cu,and reaction conditions,namely reaction temperature,hydrogen pressure,reaction time and catalyst dosage on the hydroalkylation were investigated. The results showed that,the conversion of benzene and selectivity to cyclohexylbenzene reached 57.74% and 71.38% respectively under the appropriate conditions of Ni loading 4%(w),Cu loading 0.2%(w),NiAc2and Cu(NO3)2as the Ni and Cu sources,reaction temperature 210 ℃,hydrogen pressure 2 MPa, reaction time 1 h and catalyst dosage 5%(w)(based on the mass of benzene). The active metallic sites and acidic sites on the catalysts were the key factors for the hydroalkylation of benzene.
nickel-copper/Hβ;bifunctional catalyst;benzene;hydroalkylation;cyclohexylbenzene
1000 - 8144(2015)02 - 0175 - 06
TQ 241.1
A
2014 - 08 - 02;[修改稿日期] 2014 - 11 - 06。
曹鹰(1988—),男,江苏省常州市人,硕士生,电话 0519 - 86330360,电邮 cy552110935@163.com。联系人:单玉华,电话 0519 - 86330360,电邮 yvhvashan@126.com。
