18个不同产地蒺藜药材中蒺藜皂苷元的HPLC含量测定
2015-06-01李昊月李瑞海贾天柱
李昊月,冯 琳,李瑞海,贾天柱
18个不同产地蒺藜药材中蒺藜皂苷元的HPLC含量测定
李昊月,冯 琳,李瑞海*,贾天柱
目的 采用HPLC法测定蒺藜中蒺藜皂苷元(25R-Spirostan-4-ene-3,12-dione)的含量。方法 采用色谱柱Welch Ultimate LP-C18(250 mm×4.6 mm,5 μm);流动相:甲醇-水(80∶20);检测波长:203 nm;柱温:30 ℃;流速:1.0 mL/min;进样量:20 μL。结果 蒺藜皂苷元对照品在0.82~7.38 μg与峰面积呈良好的线性关系(r=0.999 7),平均回收率为99.3%,RSD=1.67%(n=6)。结论 所建立的方法灵敏、准确、重复性好,可用于蒺藜药材的含量测定。18个产地的蒺藜样品中以内蒙产的蒺藜皂苷元含量最高。
蒺藜;皂苷元;含量测定;高效液相色谱法
0 引言
蒺藜为蒺藜科蒺藜(TribulusterrestrisL.)的干燥成熟果实。具有平肝解郁,活血祛风,明目,止痒之功效,临床常用于头痛眩晕,胸胁胀痛,乳闭乳痈,目赤翳障,风疹瘙痒[1]。蒺藜在我国有着悠久的用药历史,最早见于《神农本草经》,被列为上品,历代医家对其多有论述和应用,目前为临床常用药,并被收载入我国药典。现代研究证明,蒺藜皂苷类成分具有治疗心脑血管疾病等作用。本文以蒺藜皂苷元(25R-Spirostan-4-ene-3,12-dione)为对照品,用HPLC对蒺藜进行含量测定,结果表明,该方法准确可靠,适用于蒺藜的含量测定。
1 仪器与试剂
1.1 仪器 Agilent 1100 Series高效液相色谱仪(美国),安捷伦色谱工作站,紫外检测器;KQ3200超声波清洗器(江苏昆山),HH-4数显恒温水浴锅(江苏省金坛市荣华仪器制造有限公司),SF-130B高速粉碎机(上海冠联制药装备有限公司),鼓风恒温干燥箱(沈阳市医疗器械厂),十万分之一电子天平(德国电子天平)。
1.2 试药 蒺藜皂苷元对照品(25R-Spirostan-4-ene-3,12-dione)(本实验室分离纯化,纯度99.1%);不同产地蒺藜药材经鉴定均为符合药典要求;高效液相色谱用水为蒸馏水,甲醇为色谱纯;其他试剂为分析纯。
2 方法与结果
2.1 蒺藜皂苷元的含量测定方法
2.1.1 色谱条件 Welch Ultimate LP-C18(250 mm×4.6 mm,5 μm);流动相:甲醇-水(80∶20),流速:1.0 mL/min;检测波长:203 nm;柱温:30 ℃[2]。
2.1.2 供试品溶液制备 取蒺藜药材,粉碎,精密称取1 g,加甲醇10 mL,加热回流处理3次,每次1 h。过滤,合并滤液,蒸干。加甲醇转移并定容至10 mL容量瓶中,经0.45 μm微孔滤膜过滤,备用。
2.1.3 对照品溶液制备 精密称定蒺藜皂苷元(25R-Spirostan-4-ene-3,12-dione)对照品适量,配成0.123 mg/mL,备用。
2.1.4 测定结果 分别精密吸取对照品溶液和供试品溶液20 μL。依次进样,在上述色谱条件下测定,记录色谱图,见图1。
2.2 含量测定方法学考察
2.2.1 标准曲线的制备 精密称取苷元对照品20.5 mg,以甲醇溶解并定容于50 mL量瓶中,分别精密量取1.0、3.0、5.0、7.0、9.0 mL,以甲醇溶解并定容于10 mL量瓶中,分别量取20 μL,注入HPLC色谱仪中,记录结果,按上述色谱条件测定,以标准品溶液的进样浓度(X)为横坐标、峰面积(Y)为纵坐标,绘制标准曲线。得回归方程:Y=264.947 X-8.693,r=0.999 7,结果表明,苷元在0.82~7.38 μg范围内其浓度和峰面积具有良好的线性关系。
2.2.2 精密度试验 取对照品溶液,在“2.1.1”项色谱条件下,连续进样6次,记录峰面积。峰面积的RSD值为1.07%,表明仪器精密度良好。

图1 HPLC图谱
2.2.3 稳定性试验 取样品14号分别于0、2、4、6、8、10进样测定,结果RSD值为1.29%,表明供试品溶液在10 h内稳定。
2.2.4 重复性试验 取样品14号6份,按“2.1.2”项样品处理,测定,按外标法以峰面积计算含量,结果RSD值为0.96%,表明方法重复性良好。
2.2.5 回收率试验 分别精密称取蒺藜样品14号1 g,加1.23 mg/mL对照品1 mL,按“2.1.2”项下方法处理,按“2.1.1”项下色谱条件进行测定,按外标法以峰面积计算回收率,结果RSD值为1.67%,表明方法重复性良好。结果见表1。
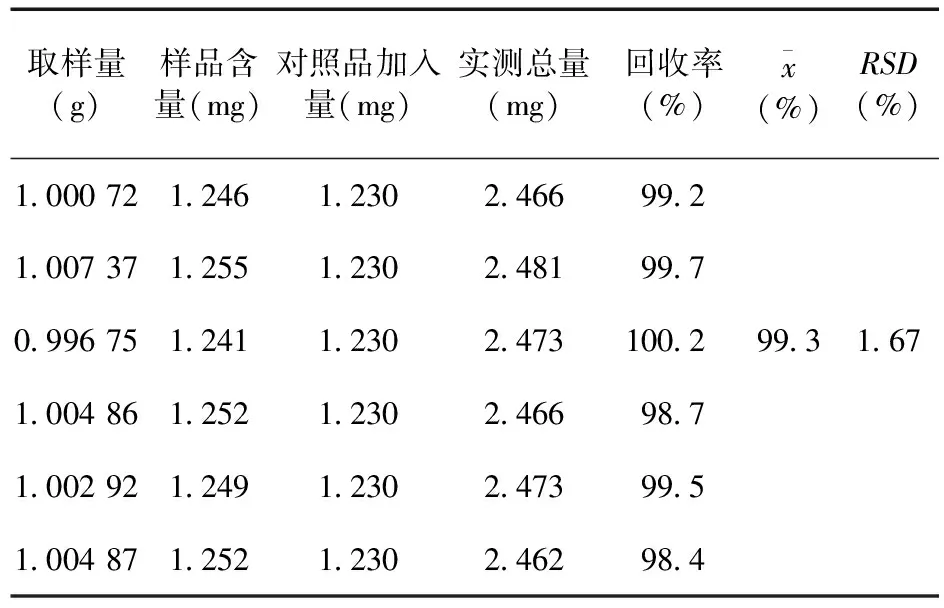
表1 回收率试验结果
2.3 各个产地蒺藜药材含量测定结果 见表2。

表2 蒺藜的产地及蒺藜皂苷元的含量(mg/g)
3 讨论
3.1 在提取方法的选择中,在溶剂选择上分别采用甲醇、氯仿、石油醚及乙醇回流后盐酸回流[3]进行对比,在提取方法上采用超声、加热回流和索式提取不同提取时间进行对比。结果表明,以甲醇热回流提取含量较高。
3.2 有报道,测定蒺藜皂苷元的含量多采用蒸发光散射检测器[4]。本研究曾采用蒸发光散射检测器[5]和紫外检测器203 nm进行对比,均有较好的色谱结果。而且结果显示蒺藜皂苷元在紫外检测条件下,色谱峰对称,分离度良好,由于紫外检测器应用广泛,方便,故本研究采用紫外检测器。
3.3 从18个不同产地蒺藜药材的测定结果看,测定的样品均含有蒺藜皂苷元(25R-Spirostan-4-ene-3,12-dione),其中以内蒙产的蒺藜含量最高(2.29 mg/g)。各产地含量相差较大,其原因除与产地不同有关以外,还可能和各药材中有生品及炮制品有关,而炮制品中也有炒制颜色深浅、有无刺的区别。本研究结果也表明其中生品中蒺藜皂苷元含量较低,而经炮制后有较大的提高。本试验为蒺藜药材制定合理的炮制方法和质量控制方法等方面的研究奠定基础。
[1] 张健,李俊,莫琪,等.蒺藜提取物的药理研究进展[J].中医药研究,1998,14(6):56-57.
[2] 李瑞海.中药蒺藜活性成分及质量评价研究[D].沈阳:辽宁中医药大学,2006.
[3] 国家药典委员会.中华人民共和国药典(二部)[S].北京:中国医药科技出版社,2010:234-235.
[4] 祁海宏,王春,严伟民.高效液相色谱法-蒸发光散射检测测定蒺藜皂苷1的含量[J].中国药事,2006,20(3):158-159.
[5] 李瑞海,冯琳.不同产地蒺藜药材中蒺藜皂苷元的HPLC-ELSD含量测定[J].辽宁中医药大学学报,2009,11(10):155-156.
关于投稿的统计学要求
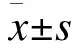
Determination of the content ofTribulusterrestrissaponin from 18 different areas by HPLC
LI Hao-yue,FENG Lin,LI Rui-hai*,JIA Tian-zhu
(Liaoning University of Traditional Chinese Medicine,Shenyang 110032,China)
Objective To determine the content inTribulusterrestrissaponin(25R-Spirostan-4-ene-3,12-dione)by HPLC method.Methods Welch Ultimate LP-C18column(250 mm×4.6 mm,5 μm)was used,the mobile phase consisted of methanol-water(80∶20),the detection wavelength was 203 nm,column temperature was 30 ℃;the flow rate was 1.0 mL/min,sample volumn was 20 μL.Results It showed a good linear relationship with the peak area in 0.82~7.38 μg(r=0.999 7),the average recovery was 99.3%,RSD=1.67%(n=6).Conclusion The method is sensitive,accurate,reproducible,and can be used for determination of the content of theTribulusterrestris.The highest content in the 18 areas is from Inner Mongolia
TribulusterrestrisL.;Saponin;Determination of content;HPLC
2014-06-13
辽宁中医药大学,沈阳 110032
*通信作者
10.14053/j.cnki.ppcr.201501019
