锂参与合成MOF-5用于CO2/CH4混合气体分离
2015-06-01SomboonChaemchuen罗志雄FrancisVerpoort
Somboon Chaemchuen 周 奎,2 姚 宸,2 罗志雄 Francis Verpoort*,,2,
(1武汉理工大学材料复合新技术国家重点实验室,武汉430070)
(2武汉理工大学材料科学与工程学院,武汉430070)
(3武汉理工大学化学化工与生命科学学院,武汉430070)
锂参与合成MOF-5用于CO2/CH4混合气体分离
Somboon Chaemchuen1周 奎1,2姚 宸1,2罗志雄3Francis Verpoort*,1,2,3
(1武汉理工大学材料复合新技术国家重点实验室,武汉430070)
(2武汉理工大学材料科学与工程学院,武汉430070)
(3武汉理工大学化学化工与生命科学学院,武汉430070)
利用溶剂热法合成了不同锂含量的MOF-5(xLi-MOF-5,x=0,1,3,5)。在MOF-5结晶过程中,锂离子被合并入其骨架结构中。实验表明,合并入骨架的锂能够改变MOF-5的结构和表面化学性质。不同的xLi-MOF-5能够不同程度降低骨架相互穿插的程度从而导致其吸附分离能力的大幅改变。其中,3Li-MOF-5具有最高的二氧化碳捕获能力(5.47 mmol·g-1),对40%CO2/60% CH4混合气体具有最优吸附选择性。
MOF-5;CO2/CH4分离;锂掺入;穿插结构
0 引言
多孔金属有机骨架材料(Metal-Organic Frameworks,MOFs)正逐渐成为化学领域和材料科学领域里发展最快的研究课题之一,不仅是因MOFs具有丰富有趣的拓扑学结构,而且具有作为与结构应用相关的功能材料的潜力。由于MOFs具有极高比表面积,MOFs在吸附材料领域受到广泛关注,其主要应用于气体(如氢气,二氧化碳等)储存和混合气体(如二氧化碳/氮气,氧气/氮气,二氧化碳/甲烷等混合气体)分离[1-2]。沼气(其主要成分为甲烷和二氧化碳)是一种理想的环境友好型的可再生能源。为了提高其燃烧效率,需要“升级”沼气(分离出其中的二氧化碳,提高其甲烷浓度),这是沼气应用的难点问题,而MOFs材料有望解决这一问题。
要分离混合气体,就要求材料对混合组分的气体具有不同的亲和度。对MOFs材料的修饰或功能化能够不同程度的影响不同客体分子与MOFs材料之间的相互作用。因此,合适的修饰或功能化能改变MOFs骨架结构[3],影响MOFs催化性能[4],提高MOFs吸附选择性等[5]。在MOFs的几何学结构,孔径和静电作用共同作用下,改变材料对混合气体的分离效率[6]。计算机模拟和实验性研究表明碱金属或碱土金属离子能改变MOFs材料的孔径,提供期望获得的表面化学性质[7],这是由于金属离子分散到MOFs的孔道中,改变了MOFs内部的静电场结构。半径较小的金属离子既能够有效的保留孔道空间,又能有效提高该位点电势,增强与客体分子的静电作用,因此在此类研究中,电荷/半径比最大的锂离子最为受关注。在已知的改性研究中,研究者通常都是采用“后合成法”(post-synthesis method)将锂离子掺入到MOFs中,研究对其储氢性能的影响。迄今还没有报道过锂离子参与MOFs结晶过程的文章。本文通过合成并表征xLi-MOF-5(x=0,1,3,5,表示合成时加入的锂盐与锌盐的摩尔百分比),研究锂离子对MOF-5结构和性能的影响。值得一提的是,MOFs材料中普遍存在骨架“穿插”现象(或称“穿插”现象)[8](图1)。
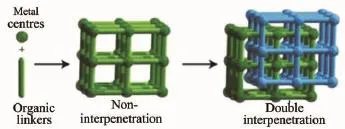
图1 MOF材料合成中的非穿插结构和双重穿插结构Fig.1 Non-interpenetration and double interpenetration structure in MOF synthesis
以MOF-5为例,普遍认为其形成原因是在MOF-5的初级骨架形成后,由于部分的未反应的锌离子进入初级骨架的孔穴中,这些锌离子有几率与配体配位并在三维空间形成骨架结构,也就是“穿插”。“穿插”结构会降低空隙空间的可利用性,往往导致材料比表面积下降,但是同时,“穿插”产生了防止骨架塌陷的排斥力,从而可以显著提高框架的稳定性。本文将会讨论锂离子在参与MOF-5合成反应时对MOF-5结构穿插的影响。
1 实验部分
1.1 试剂与仪器
六水合硝酸锌(Zn(NO3)2·6H2O,AR,沪试);对苯二甲酸(H2BDC,99%,Aladdin);硝酸锂(LiNO3,99%,Aladdin);N,N′-二甲基甲酰胺(DMF,99.5%,Aladdin)。DMF在使用前利用活化分子筛除水。
实验采用X-射线衍射仪(德国Bruker D8 Advance,铜靶,管流40 mA,管压40 kV,步宽0.02°,扫描速度6°·min-1),傅里叶红外光谱仪(德国Bruker VERTEX)和比表面积及孔隙分析仪(美国Micromeritics ASAP2020),同步热分析仪(德国耐驰STA449F3,升温速率10℃·min-1,氮气保护),等离子发射光谱仪(美国PerkinElmer Optima4300DV)对样品进行表征。每次取60~100 mg样品进行气体吸附等温线测量。用于测试的CO2、CH4和N2气体的纯度大于99.999%。测试前,样品在150℃真空条件下脱气3 h(预处理)。微孔比表面积选取相对压强0.02<P/P0<0.2之间的数据,由Brunauer-Emmett-Teller(BET)和Langmuir法计算得出。
1.2 实验过程
0Li-MOF-5合成:将0.440 g Zn(NO3)2·6H2O(1.5 mmol)和0.184 g H2BDC(1.12 mmol)溶于DMF(10 mL)和水(180 μL)组成的混合溶液中。待反应物混合均匀后,转移到特氟龙反应釜中,在120℃下反应48 h。得到的晶体用DMF洗涤并在150℃下干燥12 h,记作0Li-MOF-5。
xLi-MOF-5合成:以1Li-MOF-5为例,将0.440 g Zn(NO3)2·6H2O(1.5 mmol)和0.184 g H2BDC(1.12 mmol)溶于DMF(10 mL)和水(180 μL)组成的混合溶液中,然后在混合溶液中加入0.015 mmol LiNO3(即Zn(NO3)2·6H2O物质的量的1%)。待反应物混合均匀后,转移到特氟龙反应釜中,在120℃下反应48 h。得到的晶体用DMF洗涤并在150℃下干燥12 h。3Li-MOF-5以及5Li-MOF-5的合成方法与之相似,只需依次改变LiNO3的加入量(用量分别为0.045和0.075 mmol,即Zn(NO3)2·6H2O物质的量的3%和5%)。由于MOF-5材料极易水解导致骨架坍塌,因此所得产品存储在无水环境中。
2 结果与讨论
2.1 结构表征
如图1所示,xLi-MOF-5材料XRD图谱中有高强度尖锐衍射峰,表明样品结晶度很高,并且衍射峰位置与模拟的MOF-5的XRD图谱峰完全匹配[8-9],说明晶体相为MOF-5。同时,我们注意到谱峰强度有所变化,较为明显的是9.7°和6.8°衍射峰相对强度(记作R1),13.8°和6.8°衍射峰强度(记作R2)(表1)。 Hafizovic等[8]和Chen等[9]研究发现MOF-5中R1值和R2值与MOF-5骨架结构的“穿插”度相关:残留在MOF-5骨架中的含锌化合物(氧化锌等)和溶剂分子使得R1值增加,较低的R1值意味着MOF-5结构中没有杂质(含锌化合物或溶剂分子)残留,较高的R2值表明结构穿插程度较高。xLi-MOF-5的R1值和R2值随着锂离子的增加而减少,说明MOF-5结构中残留的杂质减少,并且结构穿插度降低,利于提高MOF-5的比表面积。在MOF-5晶体生长过程中首先形成初始骨架,而锂离子能进入到初始骨架的孔穴中,从而降低了锌离子进入初始骨架的几率,减少了含锌杂质的残留;初始骨架中锌离子或含锌团簇的减少也防止了“穿插”结构的形成。总之,结果表明锂离子的掺入可以减少在MOF-5晶体生长过程中含锌化合物的残留,一定程度上抑制“穿插”结构的形成,提高其比表面积。

表1 xLi-MOF-5的孔性质、结构穿插性、气体吸附选择性Table1 Porosity,structural interpenetration and adsorption selectivity for xLi-MOF-5
2.2 傅里叶红外光谱分析
将样品置于烘箱中150℃下干燥12 h以除去孔隙中的溶剂和杂质分子。xLi-MOF-5的傅里叶红外光谱图如图2所示。一方面,MOF-5的红外光谱中3 200~3 100 cm-1之间吸收峰对应O-H伸缩振动,伴随着锂离子加入量的增加xLi-MOF-5在3 200~3 100 cm-1之间的吸收峰逐渐减小至消失,因此锂离子可能与羧基形成单齿配位;另一方面,在1 600 cm-1附近的吸收峰对应双齿桥式配位羧基的伸缩振动,随着锂的增加,与羧基桥式配位的金属由最初单一的锌离子逐渐转变成与锌离子和锂离子共同配位,因而峰形有所变化,由此推断,锂离子还可能以双齿桥式配位形式存在。因此,我们推测锂离子以几种不同配位形式存在于xLi-MOF-5结构中,其配位形式大致有几种(图4)。
2.3 金属含量分析(等离子发射光谱)
1Li-MOF-5,3Li-MOF-5,5Li-MOF-5中锌离子浓度依次分别为29.41wt%,30.22wt%,29.71wt%;锂离子浓度依次分别为:0.005wt%,0.013wt%,0.012wt%。由于不同样品中DMF溶剂分子或表面吸附的水分子不同,因此锂离子/锌离子浓度比值更能说明样品中锂离子相对含量,依次分别为:1.7×10-4,4.3× 10-4,4.0×10-4。3Li-MOF-5中的锂离子含量最高。
2.4 热重分析

图2 MOF-5的模拟PXRD和脱除溶剂后xLi-MOF-5系列的PXRD图Fig.2 PXRD patterns for simulated MOF-5 and xLi-MOF-5 series after solvent removal
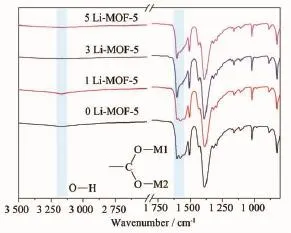
图3 xLi-MOF-5系列傅里叶红外光谱图Fig.3 FTIR spectra for xLi-MOF-5 series

图4 xLi-MOF-5系列中对苯二甲酸的多种配位方式Fig.4 Versatile BDC ligand coordination modes in xLi-MOF-5 series
样品的热重分析结果如图5所示,20~90℃的热损失是由吸附在样品表面的水分子解吸附引起的,100~300℃的热损失是由MOF-5结构中的DMF溶剂分子解吸附引起的,365℃附近有很陡的热损失是样品骨架结构开始坍塌分解成ZnO。对于不同的xLi-MOF-5,由于溶剂和水分不同,在20~300℃区间的热损失也不同(约10%~14%)。365~600℃之间的热损失来自于配体BDC的分解,依次分别为:36.70%,35.55%,37.12%,36.33%;600℃时残留的重量主要来自于ZnO,依次分别为:51.55%,46.40%,50.55%,48.71%。因此,各样品中Zn/BDC相对含量可由ZnO/BDC重量之比来定义,依次分别为:1.40,1.31,1.36,1.34。可见,0Li-MOF-5中Zn含量最高,锂加入后MOF-5的Zn含量相对减小。结合XRD分析结果,推测这是由于锂参与MOF-5合成时,结构孔洞中含锌杂质的含量降低所致。此外,所有样品的分解温度都在365℃左右,由此可见,锂的掺入对MOF-5的热稳定性影响不大。

图5 xLi-MOF-5系列热重分析曲线Fig.5 TGA for xLi-MOF-5 series
2.5 气体吸附性能
xLi-MOF-5系列的氮气等温吸附线如图6所示,所有的等温线都表明在低压时有大量气体吸附,说明材料为微孔材料。并且随着x的增加,xLi-MOF-5材料的氮气吸附量都有较明显上升。但是,5Li-MOF-5相对于3Li-MOF-5氮气吸附量增加不明显。在较高的相对压力下(P/P0>0.8),我们可以观察到等温线出现了吸附滞后环,是材料中的介孔或大孔吸附形成的[9-10]。这是由MOF-5材料中的含锌化合物小颗粒堆积形成的孔。xLi-MOF-5的微孔性质总结列于表1中。

图6 xLi-MOF-5系列氮气等温吸附线Fig.6 N2isotherm for xLi-MOF-5 series
此外,表1还描述了0℃,106 kPa压强下的CO2和CH4单组分气体的吸附量。利用这些数据,并结合理想吸附溶液理论(Ideal Adsorbed Solution Theory)[11-12]来模拟计算CO2/CH4吸附选择性。计算结果见表1。
xLi-MOF-5对CO2/CH4吸附选择性随着锂离子的增加而先增后减,在本组实验中3%锂离子是最优加入量。再结合之前关于“后合成”(post-synthesis)锂离子改性MOFs材料的研究结果[13-15],我们可以推测:(1)锂离子的掺入提高了吸附过程中的电-四极矩作用和电诱导偶极矩作用,提高吸附剂(MOF-5)对CO2的亲和性,而对CH4影响则不明显,归因于CH4的四极矩为0。(2)若锂离子含量过高,会导致锂离子在MOF-5主体材料中分散不均匀形成堆积,从而相互排斥,减弱了对客体分子(吸附质)的影响。(3)本文前面已经讨论了锂离子对MOF-5结构穿插的影响,锂离子可以有效降低结构穿插度,使得MOF-5材料具有较高比表面积。上述三方面共同作用,对气体的吸附造成影响。MOF-5的合成中加入适量的锂离子,可以提高其CO2吸附量和CO2/CH4吸附选择性。
3 结论
合成了一系列xLi-MOF-5材料,对其结构和吸附性能进行了表征。傅里叶红外光谱结果揭示了锂离子与对苯二甲酸以单齿配位或双齿桥式配位形式存在于MOF-5的结构中。PXRD图谱中相对峰强度比R1和R2表明了锂离子参与MOF-5的结晶过程中,可以有效减少MOF-5结构中的杂质(含锌化合物等)并降低结构“穿插”度,提高其比表面积。此外,锂离子还能影响MOF-5对CO2吸附量和CO2/CH4吸附选择性,在0℃,106 kPa压强下,计算得出3Li-MOF-5对40%CO2和60%CH4混合组分的吸附选择性最好。锂离子参与合成MOF-5,为MOFs改性提供了一种新思路,在MOFs应用尤其是气体分离吸附应用方面有着巨大潜力。
[1]Li J R,Ma Y,McCarthy M C,et al.Coord.Chem.Rev., 2011,255(15):1791-1823
[2]Chaemchuen S,Kabir N A,Zhou K,et al.Chem.Soc.Rev., 2013,42(24):9304-9332
[3]LI Song(李崧),DENG Lin-Xing(邓临新),HE Jun-Jie (何俊杰),et al.Chinese J.Inorg.Chem.(无机化学学报), 2014,30(10):2401-2407
[4]ZHANG Yi(张毅),YANG Xian-Gui(杨先贵),WANG Qin-Yin(王庆印),et al.Chem.J.Chinese Universities(高等学校化学学报),2014,35(3):613-618
[5]Vaidhyanathan R,Iremonger S S,Shimizu G K,et al. Science,2010,330(6004):650-653
[6]YangQ,ZhongC.J.Phys.Chem.B,2006,110(36):17776-17783
[7]Park H J,Suh M P.Chem.Commun.,2012,48(28):3400-3402
[8]Hafizovic J,Bjørgen M,Olsbye U,et al.J.Am.Chem. Soc.,2007,129(12):3612-3620
[9]Chen B,Wang X,Zhang Q,et al.J.Mater.Chem.,2010,20 (18):3758-3767
[10]Hidrobo A,Retuert J,Araya P.J.Chil.Chem.Soc.,2003,48 (3):37-40
[11]BabaraoR,HuZ,JiangJ,etal.Langmuir,2007,23(2):659-666
[12]Wu J,Zhou L,Sun Y,et al.AIChE J.,2007,53(5):1178-1191
[13]Kubo M,Hagi H,Shimojima A,et al.Chem.Asian J., 2013,8(11):2801
[14]Mulfort K L,Farha O K,Stern C L,et al.J.Am.Chem. Soc.,2009,131(11):3866-3868
[15]Xiang Z,Hu Z,Yang W,et al.Int.J.Hydrogen Energy, 2012,37(1):946-950
Lithium Incorporating Simultaneous with MOF-5 Synthesis for CO2/CH4Mixed-Gas Separation
Somboon Chaemchuen1ZHOU Kui1,2YAO Chen1,2LUO Zhi-xiong3Francis Verpoort*,1,2,3
(1State Key Laboratory of Advanced Technology for Materials Synthesis and Processing,Wuhan University of Technology,Wuhan 430070,China)
(2School of Materials Science and Engineering,Wuhan University of Technology,Wuhan 430070,China)
(3School of Chemistry-Chemical Engineering and Life Science,Wuhan University of Technology,Wuhan 430070,China)
Variance lithium content MOF-5(xLi-MOF-5,x=0,1,3,5)were prepared by using solvothermal method.Lithium cation can be incorporated with MOF-5 during its crystallization process.The experiment demonstrated that lithium incorporation have significantly led different structure and surface chemistry in MOF-5. Different xLi-MOF-5 can reduce framework interpenetration level dissimilarly and lead material with substantially different adsorption separation properties.The 3Li-MOF-5 shows the highest CO2capacity(5.47 mmol·g-1)and the best selectivity on 40%CO2/60%CH4mixed gas.
MOF-5;CO2/CH4separation;lithium incorporation;interpenetration structure
O614.111
A
1001-4861(2015)03-0509-05
10.11862/CJIC.2015.078
2014-09-22。收修改稿日期:2014-12-25。
国家自然科学基金(No.41140051)资助项目。
*通讯联系人。E-mail:Francis@whut.edu.cn
