改性沸石去除染料废水中性红的研究
2015-06-01杨耕耘陈国忠杨红侠燕山大学环境与化学工程学院河北秦皇岛066004秦皇岛市节能监察监测中心河北秦皇岛066000燕山大学机械工程学院河北秦皇岛066004
贺 君,杨耕耘,陈国忠,杨红侠,李 飞,姜 洋(.燕山大学环境与化学工程学院,河北秦皇岛066004;.秦皇岛市节能监察监测中心,河北秦皇岛066000;.燕山大学机械工程学院,河北秦皇岛066004)
改性沸石去除染料废水中性红的研究
贺君1,*,杨耕耘1,陈国忠2,杨红侠1,李飞3,姜洋1
(1.燕山大学环境与化学工程学院,河北秦皇岛066004;
2.秦皇岛市节能监察监测中心,河北秦皇岛066000;
3.燕山大学机械工程学院,河北秦皇岛066004)
摘要:研究了天然沸石对中性红的吸附及其作用机理,考察了pH值、振荡时间等因素对天然沸石吸附中性红的影响。以天然沸石为原料,采用焙烧改性、NaCl改性、超声改性3种方法获得改性沸石。采用静态吸附实验研究了改性方法对中性红的吸附性能及影响因素,及改性沸石吸附中性红的吸附动力学实验及吸附等温线。优化得到了最佳吸附pH值、时间和最佳改性方法;计算平均自由能得出吸附过程是物理过程,并且符合准一级动力学吸附模型。
关键词:沸石;改性;中性红;吸附
0 引言
印染行业是严重的水环境污染源之一。近年来随着化学纤维织物的发展,仿真丝的兴起和印染后整理技术的进步,PVA浆料、人造丝碱解物(主要是邻苯二甲酸类物质)、新型助剂等难生化降解有机物大量进入印染废水。目前对于印染废水的处理主要有①物理法-吸附法;②化学处理法(混凝法、氧化法、电解法) ;③生物处理法(厌氧-好氧-生物炭接触氧化工艺、厌氧-好氧生物转盘) ;④碱减量废水处理方法。其中吸附法处理脱色效率高、操作简单、使用方便[1]。
天然沸石是一种含水的碱金属或碱土金属的铝硅酸矿物,作为一种多功能、高效、廉价的废水处理材料,具有热稳定性良好、吸附平衡时间短、离子残留量低、对酸度适应范围较宽、可循环使用等特性,并且对环境无毒副作用,因而越来越受到国内外学者的普遍关注,已成为近几年来废水处理新材料研发的主要方向之一,且具有十分广阔的应用前景[2-5]。但其本身吸附容量有限,经常需要进行改性处理。
本文将天然沸石进行改性处理,提高其对中性红染料废水的去除率和吸附容量,旨为天然沸石在印染废水处理中的应用提供技术支撑。
1 实验材料和方法
1.1材料和仪器
材料:浙江缙云产的粒径为0.45~0.90 mm的天然斜发沸石,蒸馏水和分析纯药剂。
仪器: HZQ-C恒温摇床(中国哈尔滨市东联电子技术开发有限公司) ; JJ-3六联电动搅拌器(江苏金坛市城国胜实验仪器厂) ; HH-S4电热恒温水浴锅(金坛市医疗仪器厂) ; PHS-4型智能酸度计(江苏江分电分析仪器有限公司) ;精密电子天平,SetraEL-200S;电热恒温干燥箱(天津市中环实验电炉有限公司) ;超声波清洗机; 722S可见分光光度计;玻璃仪器。
1.2实验方法
1.2.1改性沸石的制备
1)高温焙烧改性
高温加热可除去沸石孔穴和通道中的水分子、碳酸盐和有机物,使孔道更通畅,增大内表面积,有助于离子扩散,从而可提高沸石的吸附能力[2]。设定温度为150℃、200℃、300℃、400℃、500℃、600℃,将天然沸石放于马弗炉中,在设定的温度下焙烧1 h后,自然冷却后放入干燥器备用。
2) NaCl溶液盐改性
NaCl溶液盐改性的方法,对天然沸石的离子交换能力将会有一定影响,配置浓度分别为2%、4%、6%、8%、10%的NaCl溶液,将5 g天然沸石分别放于不同浓度的NaCl溶液中振荡12 h,然后用去离子水洗净,在烘箱内于100℃下烘5 h,烘干后备用。
3)超声波改性
超声波的空化效应及引发的物理化学变化是有机物超声降解的根本原因[6],其能够降解很多种难降解有机物[7-8]。
超声时间设定为5 min、10 min、15 min、20 min、25 min。将经过200℃焙烧的沸石至于4%NaCl盐溶液中分别超声不同时间后用去离子水洗净烘干后备用。
1.2.2中性红的吸附
取一定质量浓度中性红溶液50 mL,与0.2 g的天然沸石或改性沸石在250 mL的烧杯中发生吸附交换反应。在搅拌一定反应时间后,吸附后的溶液经1 500 r/min转速离心10 min后,测定离心液中的中性红吸光度,计算其浓度,进而计算去除率和吸附容量。
1.2.3中性红的测定方法
采用可见分光光度法,在pH值为4.5左右,在530 nm处测量吸光度,根据吸光度与中性红的质量浓度在一定范围内呈线性关系进行中性红的测定。
1.2.4去除率和吸附容量的计算方法
天然沸石对中性红的吸附效果和反应时间的紧密相关,在反应达到平衡前吸附时间越长,去除率越高,吸附量越高,其中吸附量计算公式为去除率计算公式为其中,V为体积,L; C0为溶液初始浓度,mg/L; C为吸附平衡后溶液浓度,mg/L; m为沸石质量,g; q为吸附量,mg/g。

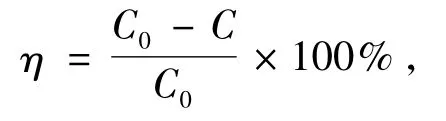
2 结果与讨论
2.1接触时间对中性红去除的影响
去除率和吸附量随时间变化的趋势如图1所示。由图1可知,天然沸石吸附中性红,在最初反应的140 min内,70%的中性红染料可以被天然沸石快速吸附。这是因为在吸附开始时,由于溶液中初始的中性红浓度较高,浓度梯度比较大,所以开始时吸附速率比较快,随着吸附交换的进行,天热沸石的吸附容量逐渐饱和,吸附变化趋势开始趋于平缓,达到动态吸附平衡状态。因此可以确定天然沸石吸附中性红的平衡时间是140 min。
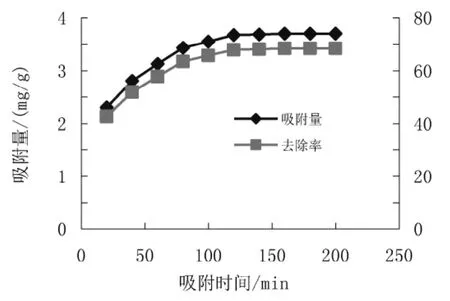
图1 不同时间下天然沸石吸附效果Fig.1 Absorption effects of natural zeolite under different times
2.2去除中性红的最佳pH值的确定
pH值对吸附的影响效果如图2所示。

图2 沸石处理印染废水在不同pH值下的吸附影响Fig.2 Adsorption effects of natural zeolite under different pH value
由图2可以看出,pH值对天然沸石对中性红的吸附效率影响很大。当pH值约为5.06时,吸附量为2.435 mg/g,去除效率达到最大值77.86%。这是由于溶液pH值不同,溶液中所含有的H+浓度不同,这可以影响溶液中可吸附交换的中性红形态和天然沸石自身的特征,并且存在竞争吸附,所以必然影响天然沸石去除中性红的效率。
2.3不同温度改性方法对吸附中性红的影响
温度改性数据变化趋势如图3。
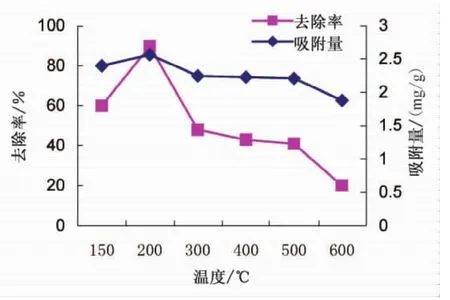
图3 不同温度改性沸石处理效果Fig.3 Adsorption effects of modified zeolite under different temperatures
由图3可知,改性沸石对中性红的去除效率在200℃时最大,吸附量为2.564 mg/g,去除率为89.7%,比未焙烧的天然沸石去除率提高了9%左右。这是因为高温焙烧可除去天然沸石孔穴和通道中的水分子、碳酸盐和有机物,使孔道更通畅,增大了内表面积,有助于离子扩散,从而可提高沸石的吸附能力[5]。温度高于200℃之后,去除效率和吸附容量急剧下降,主要是由于过高的温度会破坏天然沸石原有的晶体结构,孔隙遭到破坏,因而会降低其吸附能力。
2.4NaCl溶液化学改性对吸附中性红的影响
通过用不同大小的阳离子交换天然沸石内原有的阳离子,改变阳离子的数目或在天然沸石的孔口附近交换上新的阳离子等方法可以改变天然沸石孔道的尺寸,沸石和阳离子之间的相互影响和相互作用将赋予沸石新的吸附性能。
采用不同浓度的NaCl溶液改性天然沸石后对吸附中性红的影响趋势线如图4。可以看出,当NaCl浓度为4%时,改性沸石对中性红溶液的去除效果和吸附量最好,去除率达到91.10%,这是因为NaCl中的Na+(半径98 pm)置换沸石孔道中原有的Ca2 +(105 pm)等半径较大离子,使沸石孔容增大、空间位阻变小,吸附和离子交换性能得到提高[9]。随着NaCl浓度的增加,吸附效果变化趋于平缓,因此采用NaCl化学改性方法时,NaCl的最佳质量分数为4%。
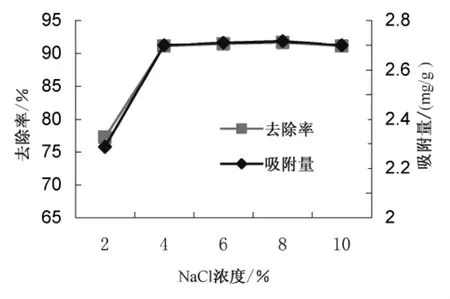
图4 不同浓度NaCl改性沸石处理效果Fig.4 Absorption effects of modified zeolite under different concentrations of NaCl
2.5超声波和NaCl联合改性
采用超声波和4% NaCl联合改性的吸附效果如图5。

图5 超声波和NaCl改性沸石的处理效果Fig.5 Absorption effects of modified zeolite by ltrasonic and NaCl
由图5可知,在超声波震荡5 min的条件下,去除率和吸附容量比单独使用NaCl改性要提高2%,但震荡时间过长会造成沸石结构的损坏,导致吸附效果下降。
2.6吸附热力学分析
中性红初始浓度对沸石平衡吸附量的影响数据记录如图6所示。

图6 不同温度下中性红初始浓度对沸石平衡吸附量的影响Fig.6 Effects of the initial concentration of the neutral red on the equilibrium adsorption of zeolite under different temperatures
由图可见,在25℃,35℃和45℃3个温度下,中性红的初始浓度对沸石吸附容量影响的变化趋势比较一致,平衡吸附量随着浓度的增大而增大。采用常见的Langmuir、Freundlich和D-R等温吸附模型,分析天然沸石对中性红的等温吸附机理,3种吸附模型的公式如下[10-11]:

式中,Ce为吸附平衡时溶液中中性红的浓度(mg/L) ; qe为吸附平衡时沸石的吸附量(mg/g) ; qm为最大吸附量(mg/g) ; b为Langmuir吸附常数(L/mg) ; KF为Freundlich吸附系数(mg/g) ; n为Freundlich常数;ε为Polanyi吸附能[ε=RTln(1 +1/Ce)],R为理想气体常数(kJ/mol·K),T为绝对温度(K),E为平均自由吸附能(kJ/mol)。
3种不同吸附模式下的各个参数分别列于表1。

表1 3种不同吸附模式下的数据参数记录Tab.1 Parameters of three different adsorption mode
由表1可知,在298、308和318 K 3个温度下,Langmuir,Freundlich等温吸附模型都能较好地描述改性沸石对中性红溶液的等温吸附过程,对比线性相关系数R2,可以发现Langmuir等温吸附模型更加符合,按照该模型的特点分析,可知天然沸石对中性红的吸附是单分子层吸附。吸附常数b、KF随温度升高而增大,说明升高温度有利于吸附反应进行,其吸附过程是吸热反应; Freundlich等温吸附模型中的的吸附常数n值大于1,说明该吸附过程容易进行。D-R等温吸附模型表明,改性沸石对中性红吸附的平均吸附能均小于8~16 kJ/mol,表明改性沸石对中性红溶液的吸附过程为物理吸附过程[4]。
2.7吸附动力学分析
Lagergren一级动力学方程是进行固液吸附体系模型分析的常用模型之一,其表达式如下[12-14]:
ln(1-Qt/Qe) =-K1t,式中,K1为一级速率常数,min-1; t为吸附所用时间; Qt和Qe分别为t时刻和达到平衡时中性红在沸石上的吸附量,mg/g。
用动力学模型对实验数据进行拟合,结果如图7和表2所示。
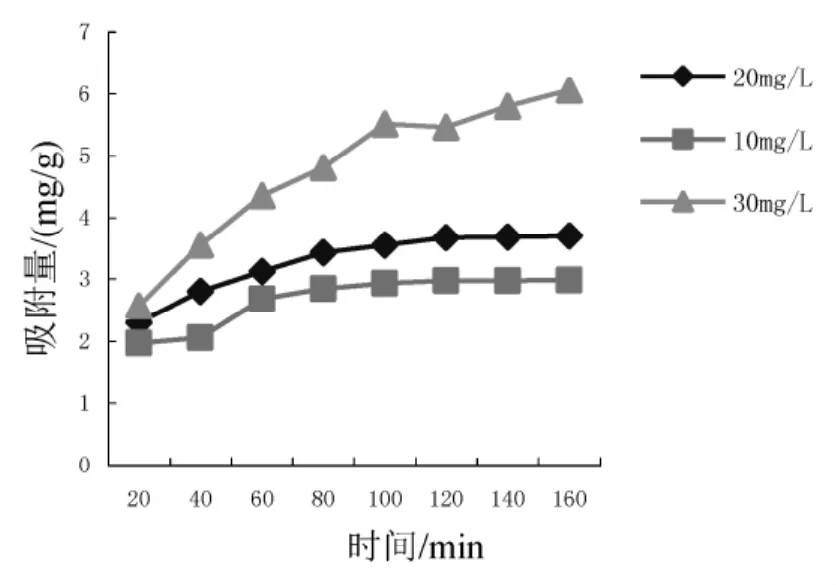
图7 不同中性红质量浓度下接触时间对吸附的影响Fig.7 Effects of the contact time on absorption under different concentration of neutral red
由表2的拟合结果可知,沸石吸附中性红符合准一级动力学方程,再次说明吸附是物理吸附,并且物理吸附是吸附过程的速度控制步骤[10]。
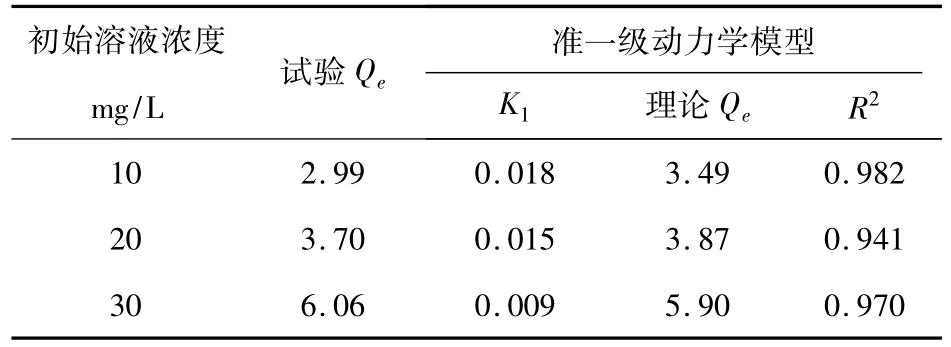
表2 动力学模型拟合数据Tab.2 Fit data of dynamic model
3 结论
1)天然斜发沸石吸附中性红在反应时间为140 min时,达到吸附平衡,前期吸附较为快速,去除率可以达到60%。天然沸石在pH值约为5.06时,中性红的去除率为77.86%。
2)在沸石改性中,200℃高温焙烧改性可以使沸石对中性红去除率提高到89.7%,NaCl改性使中性红去除率提高到91.6%,超声波NaCl联合改性可以提高到93.5%。
3)改性沸石吸附中性红的吸附行为更加符合Langmuir等温吸附模型,说明改性沸石对中性红的吸附是单分子层吸附。提高温度有利于吸附反应进行,表明该吸附反应为吸热反应; Freundlich吸附等温模型的常数n值大于1,说明该吸附过程容易进行。
4) D-R等温吸附模型拟合结果,在298、308、318 K时,改性沸石对中性红吸附的平均吸附能均小于8~16 kJ/mol,表明改性沸石对中性红溶液的吸附过程为物理吸附。改性沸石吸附中性红能较好的符合准一级动力学方程,物理吸附是吸附过程的速度控制步骤。
参考文献
[1]王慧娟,张蔚萍,高恩丽,等.印染废水处理技术探讨[J].广州化工,2013,41(5) : 18-20.
[2]陈宜滨,李宝霞,陈婉妹.改性沸石处理氨氮废水实验研究[J].福州大学学报(自然科学版),2011,39(3) : 465-466.
[3]马万山,严泽群,刘德汞.多孔质沸石颗粒处理印染废水实验研究[J].非金属矿,2001,24(1) : 42-43.
[4]王金明,易发成.浙江天然沸石对Cs+的吸附性能研究及其晶体结构表征[J].硅酸盐通报,2010,29(3) : 670-671.
[5]郑建,张剑.改性沸石在水处理中的研究和应用进展[J].水资源与水工程学报,2011,22(1) : 167-168.
[6]席细平,重芳,王伟.超声波技术应用现状[J].山西化工,2007,2(1) : 25-29.
[7]Petrier C.Ultrasound and environment sonochemical destruction of hloroaromatic derivatives[J].Environmental Science&Technology,1998,32(5) : 1316-1318.
[8]Petrier C,Micolle M,Merlin G,et al.Characteristics of pentachlorophenate degration in aqueous solution by means of ultrasound [J].Environmental Science&Technology,1999,26 (8) : 1639-1643.
[9]Bowman R S.Application of surfactant-modified zeolites to environmental remediation[J].Microporous and Mesoporous Materials,2003,61(1) : 43-46.
[10]Covelo E F,Vega F A,Andrade M L.Sorption and desorption of Cd,Cr,Cu,Ni,Pb and Zn by a fibric histosol and its orano-mineral fraction[J].Journal of Hazardous Materials,2008,159(2/3) : 342-347.
[11]Saeed M M,Hasany S M,Ahmed M.Adsorption and thermodynamic characteristics of Hg(Ⅱ) -SCN complex onto polyurethane Foam[J].Talanta,1999,50(3) : 625-634.
[12]Kwon J S,Yun S T,Lee J H,et al.Removal of divalent heavy metals (Cd,Cu,Pb and Zn) and arsenic(Ⅲ) from aqueous solutions using scoria: kinetics and equilibria of sorption[J].Journal of Hazardous Materials,2010,174(1/3) : 307-313.
[13]Tang Qiang,Tang Xiaowu,Hu Manman,et al.Removal of Cd(Ⅱ) from aqueous solution with activated firmiana simplex leaf: behaviors and affecting factors[J].Journal of Hazardous Materials,2010,179(1/3) : 95-103.
[14]Coskun R,Soykan C,Sacak M.Removal of some heavy metal ions from aqueous solution by adsorption using poly (ethylene terephthalate) -g-itaconic acid/acrylamide fiber[J].Reactive&Functional Polymers,2006,66(6) : 599-608.
Study on neutral red removal from dye wastewater by modified zeolite
HE Jun1,YANG Geng-yun1,CHEN Guo-zhong2,YANG Hong-xia1,LI Fei3,JIANG Yang1
(1.School of Environmental and Chemical Engineering,Yanshan University,Qinhuangdao,Hebei 066004,China; 2.Qinhuangdao Energy-saving Monitoring Center,Qinhuangdao,Hebei 066000,China; 3.College of Mechanical Engineering,Yanshan University,Qinhuangdao,Hebei 066004,China;)
Abstract:The absorption performance and mechanism of natural zeolite towards neutral red solution was investigated by the absorption experiments.The pH value and reaction time for absorption effects were studied.Using natural zeolite as raw material,modified zeolite was obtained by the roasting modification,NaCl modification,ultrasonic modification.Static absorption experiments were carried out to study the modification methods towards neutral red solution,and absorption kinetics and adsorption isotherm of neutral red experiments.The best adsorption pH and reaction time is optimized and the best modification methods is obtained.According to the average free energy,the absorption process is a physical process,and fits better to the pseudo-first-order kinetics model.
Key words:zeolite; modification; neutral red; absorption
作者简介:*贺君(1978-),男,河北秦皇岛人,副教授,主要研究方向为水污染治理技术,Email: hejun@ ysu.edu.cn。
基金项目:河北省自然科学基金资助项目(B2012203037) ;秦皇岛市科技支撑计划项目(201401A004)
收稿日期:2014-09-17
文章编号:1007-791X(2015) 01-0068-05
DOI:10.3969/j.issn.1007-791X.2015.01.010
文献标识码:A
中图分类号:X703
