耐药结核病化学治疗指南(2015)
2015-05-25中国防痨协会
中国防痨协会
《耐药结核病化学治疗指南(2015)》编撰说明
·临床指南·
耐药结核病化学治疗指南(2015)
中国防痨协会
《耐药结核病化学治疗指南(2015)》编撰说明
中国是耐药结核病高负担国家(HBC)之一,尤其是耐多药结核病(MDR-TB),是目前结核病控制工作中遇到的重大挑战和主要障碍。2010年中国结核病流行病学抽样调查结果显示,中国每年约有10万例新发耐多药结核病患者,广泛耐药结核病(XDR-TB)更是占据所有菌株的2.1%,足以说明中国结核病耐药疫情的严重性。众所周知,控制耐药结核病流行的重要手段之一仍是通过有效的化学治疗治愈现症耐药结核病患者,以消除其传染源。为更好地对耐药结核病的化学治疗提供指导,中国防痨协会早在2002年就组织有关专家并且由肖和平教授执笔编撰了《耐多药结核病化学治疗的意见(试行)》。随着对耐药结核病认识的加深和化学治疗的发展,2002年《耐药结核病化学治疗的意见(试行)》已经不能完全适应实际情况的需要。2008年中国防痨协会组织有关专家,由肖和平教授牵头,在参考WHO出版的《耐药结核病规划管理指南(2008年紧急更新版)》和中国实际情况的基础上,经过1年多的努力,在《耐多药结核病化学治疗的意见(试行)》的基础上编撰了《耐药结核病化学治疗指南(2009)》。该指南于2010年先后在《中国防痨杂志》、《中华结核和呼吸杂志》发表,2011年2月由人民卫生出版社正式出版,在全国各地发行,深受同行们的欢迎,对耐药结核病的控制发挥了重要作用。
中国防痨协会考虑到结核病流行态势的变化、耐药结核病的严重威胁,以及近几年耐药结核病化学治疗的进展和治疗耐药结核病经验的积累,需要向全国的结核病防治工作者提供更为先进的耐药结核病化学治疗知识和理念、最新的信息和有效应对耐药结核病的建议,乃于2013年再次组织专家并由肖和平教授领衔对《耐药结核病化学治疗指南(2009)》进行了讨论和修改。经过近2年来的反复研讨,结合2014年WHO出版的CompanionhandbooktotheWHOguidelinesfortheprogrammaticmanagementofdrug-resistanttuberculosis,逐字逐句推敲,于2015年2月完成了《耐药结核病化学治疗指南(2015)》的编撰。
本指南的重点是对耐药结核病尤其是利福平耐药结核病、耐多药结核病和广泛耐药结核病提出了当前相对成熟的抗结核药物的应用和有效规范治疗方案制定的建议,而对正在研究尚未上市的新药暂不做介绍或评价。本指南同时提供了耐药结核病的定义、治疗转归的标准,将有助于数据收集分析的一致性,也有利于对初复治耐药结核病、利福平耐药结核病、耐多药结核病和广泛耐药结核病患者的化学治疗方案及其疗程展开进一步研究。
本指南重点关注的是耐药结核病患者的化学治疗,但需要强调DOTS策略仍是结核病控制的基石,是预防耐药结核病发生和传播的最有效手段。
有关单位、领导和众多专家对上一版及本版的编写、出版、发行做出了重要的贡献,在此致以衷心感谢。
最后,希望广大结核病防治工作者对本指南存在的不足或错误,不吝指正,提出宝贵意见,使其不断改进,更好地为大家服务。
中国防痨协会
2015年2月
由中国防痨协会组织编撰的《耐药结核病化学治疗指南(2009)》从2010年4月首发在《中国防痨杂志》至今已经过去了5年,中国和世界结核病防治情势已经发生了重大变化,防控与诊治新理念、新观点、新技术、新方案不断涌现。为了适应新的形势、与时俱进,中国防痨协会重新组织编撰了《耐药结核病化学治疗指南(2015)》,供广大结核病防治工作者在学习、研究与临床实践中参考。
定 义
1. 单耐药结核病(mono-resistant tuberculosis,MR-TB):结核病患者感染的结核分枝杆菌(Mtb)经体外药物敏感性试验(drug susceptibility testing,DST)证实对1种一线抗结核药物耐药。
2. 多耐药结核病(poly-resistant tuberculosis,PR-TB):结核病患者感染的Mtb经体外DST证实对1种以上一线抗结核药物耐药(但不包括同时对异烟肼和利福平耐药)。
3. 耐多药结核病(multidrug-resistant tuberculosis,MDR-TB):结核病患者感染的Mtb经体外DST证实至少同时对异烟肼和利福平耐药。
4. 广泛耐药结核病(extensively drug-resistant tuberculosis,XDR-TB):结核病患者感染的Mtb经体外DST证实在耐多药的基础上至少同时对一种氟喹诺酮类和一种二线注射类抗结核药物耐药。
5. 利福平耐药结核病(rifampicin-resistant tuberculosis,RR-TB):结核病患者感染的Mtb经体外DST证实对利福平耐药,包括对利福平耐药的上述任何耐药结核病类型:MR-TB、PDR-TB、MDR-TB和XDR-TB。
总 论
本指南适用于所有类型的耐药肺结核和耐药肺外结核的化学治疗。
一、Mtb的耐药特点
熟悉和掌握Mtb对抗结核药物的耐药特点将有助于耐药结核病抗结核药物的选择和化学治疗方案的制定。
(一)药物暴露与药物耐药
细菌对抗生素的接触可称之为药物暴露(drug exposure),药物暴露后即有可能产生药物耐药。由于抗生素的药物暴露、特别是不合理的用药,将使残存细菌在抗生素的压力下适应性生长,从而导致该药疗效下降甚至无效,造成细菌耐药。可以说,抗生素本身就是细菌耐药的筛选剂。
结核病患者既往抗结核用药史提示,患者感染的Mtb与抗结核药物的接触,可视为抗结核药物暴露,不仅表现为Mtb临床分离株对既往使用过的某种或某些抗结核药物的耐药性增加,也是复发结核病患者耐药率明显升高的主要原因。初治失败的结核病患者,其感染的Mtb因与抗结核药物长期接触,对已使用过的药物耐药率明显增加。即使是间隔多年后复发的结核病患者,对原方案内的药物耐药率仍明显升高,体现了既往药物暴露对细菌耐药的直接影响。当然,抗结核药物的使用不当是Mtb发生耐药的主要原因。耐药Mtb菌株的传播,是药物暴露导致药物耐药的另一种类型。因药物暴露发生在Mtb进入被感染者机体以前,感染该耐药菌株被称之为原发或初始耐药菌感染,是这类耐药结核病治疗疗效不佳的主要原因。
需要引起注意的是氨基糖苷类、氟喹诺酮类等药,既往作为抗感染药使用时也会对潜伏的Mtb产生药物暴露,并可能导致耐药的发生。研究表明,既往使用过氟喹诺酮类药物进行抗感染治疗的结核病患者,其体内的Mtb对该类药物的耐药率明显上升。因此,不能排除结核病的感染者,应尽量避免使用氨基糖苷类或氟喹诺酮类药物进行诊断性抗炎治疗。
(二)自然耐药
自然耐药也可称之为天然耐药(natural drug resistance,NDR),指从未接触过任何抗结核药物的Mtb菌株(野生菌株),对从未接触过的某些药物产生耐药。Mtb自然耐药的原因并不清楚,可能与屏障机制等多种机制有关,也可能因基因突变产生所致。如牛分枝杆菌对吡嗪酰胺(pyrazinamide,PZA)自然耐药,非洲分枝杆菌对氨硫脲(thioacetazone,Thz)自然耐药。自然耐药也并非绝对不变,部分Mtb野生菌株在持续繁殖中产生耐药突变,也是一种自然耐药,同时也属于原发耐药,这种菌株称之为野生型耐药突变株。Mtb对不同抗结核药物自然耐药的发生频率见表1。Mtb的自然耐药不足以影响正规抗结核化学治疗的效果,但需注意以上情况对疗效可能产生影响。
(三)原发耐药
原发耐药(primary drug resistance)是指接受抗结核治疗前结核病患者即对某种或某些药耐药。原发耐药产生的原因在于耐药结核分枝杆菌的传播。原发耐药常见于对1种或2种药(链霉素或异烟肼)耐药,同时耐2种药物较少见。
(四)初始耐药
因既往用药不详,或既往抗结核用药不足1个月的患者存在的耐药现象称之为初始耐药(initial drug resistance)。初始耐药包括原发耐药,也包含用药史缺失或隐瞒用药史的部分获得性耐药。由于初始耐药的产生是耐药结核分枝杆菌感染的结果,尤其当以前曾有过治疗史的患者在新发现患者中的比例很小时,这种耐药水平对结核病控制规划的调节不甚敏感。因此,初始耐药水平已成为检验结核病控制规划成效的标志。

表1 结核分枝杆菌自然耐药的发生频率
注 R:利福平,H:异烟肼,S:链霉素,PAS:对氨基水杨酸,Pto:丙硫异烟胺,Km:卡那霉素,Cs:环丝氨酸,Vm:紫霉素,FQ:氟喹诺酮类药物
(五)获得性耐药
抗结核药物使用达到或超过1个月后发生的耐药,称之为获得性耐药(acquired drug resistance),也叫继发性耐药。获得性耐药通常耐2种或2种以上药物,耐多药结核病相对多见,对结核病化学治疗效果的影响更为严重。
(六)交叉耐药
交叉耐药是指对某一种抗结核药物产生耐药突变,可能也对该类药物中的其他或全部药物产生耐药。对不同种类药物的交叉耐药少见。交叉耐药具有复杂性、不完全性、甚至矛盾性。越来越多的证据显示,对于大多数药来说,耐药表型和基因突变存在联系。但也不是所有的基因突变都会导致耐药,同时很多的基因突变并未被阐明。
1.单向交叉耐药:Mtb对A药耐药时,对B药并不耐药;但对B药耐药时,对A药也同时耐药。如为2种以上药物,对A药耐药时,对B、C药并不耐药;而对C药耐药时,对A、B药均同时耐药。明确有单向交叉耐药性的药物有乙(丙)硫异烟胺和氨硫脲;阿米卡星(卡那霉素)与链霉素,如耐链霉素的结核分枝杆菌使用阿米卡星(卡那霉素)往往有效,但耐阿米卡星(卡那霉素)时对链霉素也通常耐药。
2.双向交叉耐药:Mtb对A药耐药的同时对B药也耐药;而对B药耐药的同时也对A药耐药。确定有双向交叉耐药性的药物有异烟肼和异烟腙、利福类药物(利福平、利福定、利福喷丁和利福布汀等)、阿米卡星和卡那霉素、乙硫异烟胺和丙硫异烟胺、氟喹诺酮类药物(氧氟沙星、左氧氟沙星、环丙沙星、加替沙星和莫西沙星等)、环丝氨酸和特立齐酮、紫霉素和卷曲霉素、紫霉素和结核放线菌素。但双向交叉耐药也有不完全性。有资料表明少数菌株对利福平耐药,但在体外可能对利福布汀敏感;对氧氟沙星耐药,但仍可以考虑用莫西沙星替代。详见表2。
(七)耐药的稳定性
Mtb产生耐药后的耐药稳定性并非一成不变,随着Mtb菌株的传代,耐药性会产生或多或少的变化,不同药物、不同程度的耐药性将表现出不同程度的稳定性或易变性。临床上耐药产生后初期并不稳定,表现为波浪形,耐药菌和敏感菌交替出现或混合存在;而随着时间的推移,药物暴露产生的筛选作用之下耐药Mtb逐渐成为优势细菌,耐药程度增高,耐药的稳定性增强,保持时间长。也可能在Mtb耐药性不严重的情况下,其耐药性可能会随着Mtb的传代逐渐减弱甚至消失,从而恢复对药物的敏感性,称之为Mtb产生耐药后的复敏现象。但也不尽如此,针对不同的抗结核药物,Mtb耐药的稳定性也各不相同,大体可分为以下三类。
1.耐药稳定性强类:(1)链霉素:Mtb对链霉素产生的耐药性比较稳定。对链霉素耐药者,在停用链霉素1~2年后,其耐药程度没有多大变化。此时如果使用异烟肼或(和)对氨基水杨酸,Mtb耐链霉素的稳定性可受到一定程度的影响,耐药性减弱。(2)氨硫脲:稳定性很好,少见有复敏现象。(3)环丝氨酸和乙(丙)硫异烟胺:一旦耐药则不易恢复,稳定性强,停药后亦是如此。(4)氟喹诺酮类药物:耐药后不易恢复,较难复敏。无论是临床分离耐药株或诱导耐药菌株,经10代以上的传代,未见氟喹诺酮类药物的最低抑菌浓度(minimum inhibitory concentration,MIC)值有变化,仍需进一步观察[杨华,胡忠义,沙巍,等.结核分枝杆菌对氧氟沙星耐药的体外诱导及稳定性研究.中华预防医学杂志,2014,4(48):318-323.]。

表2 不同抗结核药物的交叉耐药性
注 本表格内容引自:World Health Organization.Companion handbook to the WHO guidelines for the programmatic management of drug-resistant tuberculosis.WHO/HTM/TB/2014.11. Geneva:World Health Organization,2014.
2.耐药稳定性中等类:主要的代表性药物为利福平。耐利福平的Mtb一般在停药后仍有少部分可恢复对利福平的敏感性,复敏率约4.2%,分别发生于停药后的第6、15、31、52个月等时段。
3.耐药稳定性差类:(1)异烟肼:Mtb对异烟肼耐药的稳定性是所有已知抗结核药物中最差的,耐药性很容易减弱。停止使用异烟肼36周,Mtb对异烟肼的复敏率大约为88.5%。Mtb对异烟肼耐药性的减弱不但会经常发生在停药后,甚至在用药期间也有可能发生。异烟肼的复敏现象在临床上观察到,并得到了实验室的证实[Richardson ET, Lin SY, Pinsky BA, et al.First documentation of isoniazid reversion inMycobacteriumtuberculosis.Int J Tuberc Lung Dis,2009,13(11):1347-1354.]。(2)对氨基水杨酸:有研究提示,使用对氨基水杨酸120 d而形成耐药的患者,在停用对氨基水杨酸一段时间后,绝大多数都恢复了敏感性,复敏率约83.3%。
(八)中国耐药结核病疫情
为方便耐药结核病化学治疗时药物的选择和治疗方案的制定,将2010年中国结核病流行病学抽样调查结果展示的一线和二线抗结核药物的耐药情况列于表3、4,以供参考。
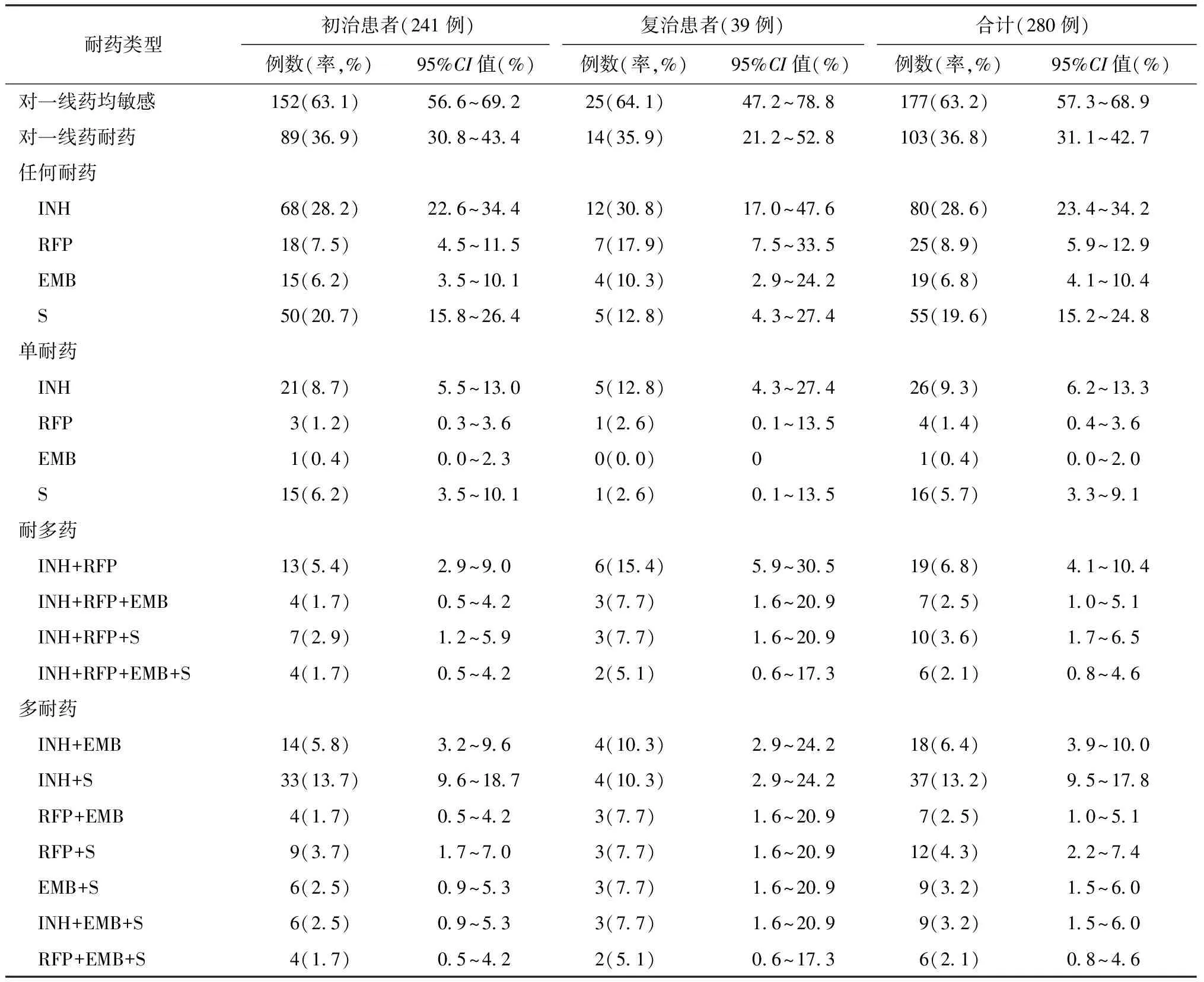
表3 结核分枝杆菌临床分离株对一线抗结核药物不同耐药类型的统计分析
注 INH:异烟肼;RFP:利福平;EMB:乙胺丁醇;S:链霉素。本表格内容引自:王宇.全国第五次结核病流行病学抽样调查资料汇编.北京:军事医学科学出版社,2011.

表4 结核分枝杆菌临床分离株对二线抗结核药物不同耐药类型的统计分析
注 Ofx:氧氟沙星;Lfx:左氧氟沙星;Km:卡那霉素;Am:阿米卡星;Cm:卷曲霉素;Pto:丙硫异烟胺;PAS:对氨基水杨酸。本表格内容引自:王宇.全国第五次结核病流行病学抽样调查资料汇编.北京:军事医学科学出版社,2011.
二、耐药结核病实施化学治疗的基础
耐药结核病实施化学治疗的基础(条件)包括:(1)需要具备有质量保证的实验室提供的药物敏感性试验(drug sensitivity test,DST)结果及本地区耐药检测资料,作为方案制定和药物选择的依据。(2)掌握本地区既往用药情况和患者既往用药史,了解患者既往各种抗结核药物应用总量及联合用药情况,便于选择用药。(3)充分评估本地区耐药患者的数量、类型和发展趋势,以及二线抗结核药物使用的种类、频度,以便有把握地挑选用于耐药结核病治疗的药物品种。(4)每一例耐药结核病患者必须有一线抗结核药物尤其是异烟肼和利福平的DST结果,有条件的地区或单位可开展对二线抗结核药物的DST,以确定耐药的种类,为制定合理的耐药结核病化学治疗方案提供依据。(5)具备提供充足药物的资金和渠道。(6)具备制定合理化学治疗方案和处理药物不良反应的能力。
三、耐药结核病实施化学治疗的方式
以下3种方式可供参考。
1.标准化治疗:依据国家或本地区耐药结核病检测资料、针对不同耐药类型群体设计统一的耐药结核病化学治疗方案进行治疗,该治疗方案将涵盖绝大多数患者。本指南所提供的各种耐药结核病化学治疗方案可供中国各地针对耐药结核病实施标准化治疗时参考。
2.个体化治疗:依据结核病患者临床分离菌株的DST结果、既往用药史、耐药结核病接触史和患者的依从性进行综合考虑后实施的治疗方法。由于部分一线和大部分二线抗结核药物DST的可靠性及其临床应用价值尚未完全确定,DST不能100%预测药物的有效或无效,例如链霉素、乙胺丁醇、吡嗪酰胺、第4组和第5组药物。因此,WHO建议不应完全依据这些药物的DST结果设计个体化治疗方案。异烟肼、利福平、氟喹诺酮类和二线注射剂的DST结果准确、重复性好,如果这些药物的DST结果是从质量得到保障的实验室中获得的,个体化治疗方案可以基于这些药物的DST结果进行设计。
3.经验性治疗:指高度怀疑但未确诊为耐药结核病之前,依据当地具有代表性的耐药结核病检测资料、患者既往用药史、耐药结核病接触史及对药物的耐受性,结合临床经验而实施的耐药结核病化学治疗方法。本指南原则上不推荐经验性耐药结核病化学治疗,即便需要,也应该在专家组的指导下进行。
经验性治疗方法的使用旨在避免耐药结核分枝杆菌的传播和患者病情的加重,以及人道方面的考虑。但是,一旦获得可靠的DST结果后,应结合患者的临床病史和对药物的耐受性,及时对原方案进行调整,给予标准化或个体化耐药结核病化学治疗方案。
四、耐药结核病化学治疗方案的设计
耐多药和广泛耐药结核病化学治疗方案的设计应由专家组集体讨论决定,而非专家的个人行为。以下要素可供耐药结核病化学治疗方案设计时参考。
1. 药物效果:评价抗结核药物有效性,主要有如下参考标准:(1)被选药物没有在患者既往治疗失败的方案中被使用过;(2)DST结果提示被选药物为敏感药物(异烟肼、利福平、第2组和第3组药物的DST结果往往可靠,其他药物的DST结果的可靠性较低);(3)被选药物与已知耐药药物间没有较高的交叉耐药性。
有DST结果者符合上述所有条件或“(2)+(3)”为有效,暂无DST结果者符合上述条件中的“(1)+(3)”为有效。有效的抗结核药物是组成方案的核心药物。不符合上述条件,经过专家组讨论后仍可入选的药物为可能有效,但不能作为方案中的核心药物对待。
同时要注意了解与药物有效性密切相关的代表性数据,包括新发、复发、失访后再治疗,以及一线抗结核药物治疗失败的初始或复治、二线抗结核药物治疗失败等,这些数据对于耐药结核病化学治疗方案的设计非常关键。
2. 药物数量:至少含有4种有效的抗结核药物和吡嗪酰胺组成。无4种有效的抗结核药物组成方案时或方案中某种药物的有效性不确定或有疑问时,方案中药物使用的数量可超过5种,这些情况常见于广泛耐药结核病。
3. 药物剂量:年龄和体质量是药物剂量确定的基本要素,为避免新的耐药产生,应尽可能足量使用。明确会产生胃肠道反应或不良反应较大的药物,可采用开始从低剂量递增的方法在1~2周内达到足量,如丙硫异烟胺、对氨基水杨酸和环丝氨酸等。
4. 用药方法:原则上采用全程每日用药法和顿服法。吡嗪酰胺、乙胺丁醇和氟喹诺酮类药物应每天一次顿服。顿服法也适用于第4组口服二线抗结核药物,但为减少不良反应,提高患者的可接受性,乙硫异烟胺和(或)丙硫异烟胺、环丝氨酸和对氨基水杨酸习惯上还是分次服用。注射类抗结核药物应每天一次给药,即不要将一天剂量分开使用。注射类抗结核药物的间歇疗法(每周3次),可以在强化期延长或药物毒性对患者危害风险增大的情况下考虑,该方法宜在痰菌培养转阴后实施。
5. 用药阶段:方案由2个阶段组成,第1阶段为强化期,第2阶段为继续期。强化期的最佳持续时间取决于痰菌是否阴转,如果阴转,意味着治疗成功的概率增加。因此,建议强化期结束时痰菌仍未阴转的患者可酌情延长其强化期。
6. 疗程:根据耐药和疗效情况而定,总疗程一般为9~30个月。详见“耐药结核病的化学治疗方案”和“耐药结核病化学治疗的转归”。
7. 治疗管理:实施全程督导下的化学治疗管理模式(DOT)。
8. 方案书写:方案中强化期和继续期采用“/”隔开。药物书写以药物名缩写表示,备选药物放在括号内。方案中药物书写顺序一般按药效降序排列,注射类抗结核药物排在口服药前。药与药之间采用“-”符号隔开,如H-R-Z-E。药名缩写前数字代表用药的月数,药名缩写下方数字代表每周用药次数,药名缩写下方无数字表示每日用药。
五、耐药结核病化学治疗药物的选择
1.顺序选药法:参照药物的五组分类,由第1组顺序向下选择合适的抗结核药物的选药方法,适合于非耐利福平的MR-TB、PDR-TB。
2. 五步选药法:以二线注射类和氟喹诺酮类药物为首选,在选择好4种有效的二线抗结核药物的基础上常规加用吡嗪酰胺的方法,适用于RR-TB、MDR-TB和XDR-TB(表5)。
3. 避免在同一方案中选用2种同一类药物:例如,注射类抗结核药物中的阿米卡星与卷曲霉素,以及氟喹诺酮类药物中的莫西沙星与加替沙星等。

表5 五步选药法(适用对象:RR-TB、MDR-TB和XDR-TB)
注 本表格内容主要参考:World Health Organization.Companion handbook to the WHO guidelines for the programmatic management of drug-resistant tuberculosis.WHO/HTM/TB/2014.11. Geneva:World Health Organization,2014.
4. 避免使用与已知耐药药物具有双向交叉耐药的品种:例如,卡那霉素和阿米卡星、乙硫异烟胺和丙硫异烟胺,以及环丝氨酸和特立齐酮;当其中任一药物耐药时,不能再选用同组中的另一种药物。inhA基因存在突变时,仍然可以使用乙硫异烟胺(丙硫异烟胺),但不能作为核心药物对待。
5. 推荐全程使用吡嗪酰胺:耐药尤其是耐多药肺结核患者往往存在肺部的慢性炎症,理论上讲,吡嗪酰胺在炎症产生的酸性环境中更为有效。如果治疗效果好,在保证患者能够继续保持具有至少3种有效药物的基础上,吡嗪酰胺可以与注射类抗结核药物同时停用。
6. 中枢神经系统耐药结核病的药物选择:耐药肺外结核选择药物的策略与耐药肺结核相同,惟一的例外是中枢神经系统受累的患者。如果耐药结核病累及中枢神经系统,方案中应采用能通过血脑屏障经脑膜充分渗透到中枢神经系统的药物。异烟肼、吡嗪酰胺、乙硫异烟胺(丙硫异烟胺)和环丝氨酸都具有良好的脑膜渗透性,而卡那霉素、 阿米卡星、链霉素只有在脑膜炎症存在的情况下脑膜渗透性提高。对卷曲霉素脑膜渗透性的研究较少,疗效不肯定。对氨基水杨酸和乙胺丁醇脑膜渗透性较差或无渗透性。氟喹诺酮类药物脑膜渗透性不一,动物研究表明莫西沙星具有更好的渗透性。氯法齐明或克拉霉素的脑脊液渗透性缺乏数据。利奈唑胺可渗透至中枢神经系统中,并在脑膜炎的治疗中使用。亚胺培南具有良好的中枢神经系统渗透性,但用于治疗小儿脑膜炎时,有较高的癫痫发作风险,推荐首选美罗培南。
7. 抗结核新药的选择:本指南纳入了已经在国外上市的贝达喹啉和德拉马尼2种抗结核新药,并被归类于第5组。根据现有的临床研究资料,贝达喹啉和德拉马尼无论对耐多药、广泛耐药结核病,还是敏感的结核分枝杆菌均有明确的杀菌效果,显然不同于其他的第5组抗结核药物。为了确保抗结核新药的合理使用,有待贝达喹啉和德拉马尼在中国正式上市后另行制定、颁布使用规范。
六、耐药结核病化学治疗的实施路径
1. 无DST结果的复治结核病:(1)根据就诊患者的病史(病程)和既往治疗史,评估耐药的可能性,同时送检痰液行结核分枝杆菌培养、菌种鉴定和DST。(2)根据既往用药的种类、总量和联合用药的情况,采用未曾应用过的药物和估计有效的药物,设计经验性化学治疗方案予以治疗。(3)获得可靠的DST结果后,符合者可继续原有的经验性化学治疗方案;不符合者可根据其结果对方案进行相应调整,实施标准化或个体化治疗。
2. DST结果提示耐药的结核病:(1)根据DST结果确定耐药类型,根据患者对药物的耐受情况给予标准化或个体化治疗。(2)同时再次送检痰液行结核分枝杆菌培养、菌种鉴定和DST,目的是验证以往的细菌学检测结果和及时发现新的耐药药物。(3)再次获得DST结果后,符合者继续采用原方案治疗;不符合时,应与实验室沟通,必要时重复DST或送交专家组讨论。
3. 耐药结核病初治化学治疗方案有效者的处理步骤:耐药结核病初治化学治疗方案有效,是指初治结核病患者在接受初治化学治疗方案过程中,疗前DST结果显示耐药,但患者接受初治化学治疗方案以来痰菌一直阴性,病灶有吸收。建议处理步骤如下。(1)未满疗程者:继续使用原初治方案至满疗程;疗程结束后予以密切观察,观察期间每3个月复查痰涂片和痰培养。(2)已满疗程并治愈者:予以密切观察,观察期间每3个月复查痰涂片和痰培养。(3)观察周期:疗程结束后对非耐利福平的MR-TB、PDR-TB患者观察12个月,RR-TB、MDR-TB和XDR-TB 患者的观察周期可延长至24个月。(4)治疗过程中或观察期间发现痰菌再度阳性、经菌种鉴定为结核分枝杆菌和DST结果提示耐药时,启动耐药结核病化学治疗流程。
抗结核药物
本部分涉及的抗结核药物介绍,最终以其药品说明书为准。目前,一些可用于结核病治疗的其他抗感染药品(抗生素)说明书中未包括治疗结核病的内容,如适应证、疗程、剂量等,在其说明书未得到修改前可遵循相关规范和指南用药。
针对利福平耐药、耐多药和广泛耐药结核病患者,超说明书用药不可避免,而且可能是合理的。例如,(1)氨基糖苷类药物的长疗程使用:二线注射剂中的卡那霉素和阿米卡星同属于氨基糖苷类抗结核药物,是治疗耐多药结核病的核心药物,注射用药时间可长达6个月之久;如果是广泛耐药结核病,则需使用12个月。卡那霉素和阿米卡星的药品说明书并未介绍这样的使用方法。(2)超适应证用药:氟喹诺酮类药物也是治疗耐多药结核病的核心药物,早在20世纪80年代已被证实具有抗结核作用。WHO于1996年正式推荐用于治疗耐药结核病,但说明书上至今没有用于结核病的适应证。(3)超剂量用药:WHO在2006年提出采用16~20 mg·kg-1·d-1高剂量异烟肼用于治疗耐多药结核病,尽管对此存在很大争议,但国内外均已在试用。另外,药品产地的不同直接影响着患者对高剂量用药的耐受性。根据我国权威部门设计的阿米卡星用药剂量,耐多药结核病患者可以接受国外进口阿米卡星的剂量分别为0.5~0.75 g/d(体质量<50 kg)和1 g/d(体质量≥50 kg),和国产阿米卡星的常规剂量0.4 g/d(体质量<50 kg)和0.6 g/d(体质量≥50 kg)(参考相关药物说明书);进口与国产阿米卡星用药剂量有较大的差距,但至今尚未看到这2种剂量的药物不良反应率有何差异。无论是超适应证、超剂量或是超疗程用药都是属于超说明书用药的范畴,此时抗结核药物的使用应该是在药品说明书的基础上,通过参考相关的规范和指南如WHO和我国出台的有关耐药结核病化学治疗指南等,加以完善,使之更趋合理。对于尚无明确定论的用药方法,如高剂量异烟肼的长期使用,应谨慎而行。
一、抗结核药物的分组
抗结核药物可分为一线和二线;一线抗结核药物有异烟肼、利福平、乙胺丁醇、吡嗪酰胺、利福布汀、利福喷丁和链霉素,其余归类于二线抗结核药物。
为了方便耐药结核病化学治疗药物的选择和方案的设计,WHO根据药物的杀菌活性、临床疗效和安全性,在一线和二线抗结核药物分类的基础上,将抗结核药物进一步划分为5组。本指南结合中国的实际情况,将5组抗结核药物列于表6。

表6 不同组别抗结核药物一览表
对于表6的几点说明
一、一线口服类抗结核药物
本组药物药效最强、耐受性最佳。如果具有实验室证据和临床治疗史提示该组中的药物有效,就应该选用。
1.异烟肼:有些患者表现为对低浓度的异烟肼耐药、高浓度异烟肼敏感,采用高剂量异烟肼(16~20 mg·kg-1·d-1)可能有效,但不能作为核心药物对待。
2.新一代利福霉素类药物:利福喷丁和利福布汀与利福平有高度交叉耐药,原则上不推荐用于耐利福平结核病。利福喷丁和利福布汀均放在第一组的意义有所不同。利福喷丁同利福平一样,可用于初、复治结核病,也可用于对利福平敏感的单耐药或多耐药结核病治疗。利福布汀主要是针对Mtb和人类获得性免疫缺陷病毒(HIV)双重感染者的抗结核治疗,以及对利福平敏感的单耐药或多耐药结核病。
体外DST证实,利福喷丁或利福布汀敏感的耐利福平结核病患者,在无足够有效药物组成化学治疗方案的情况下,结合其既往用药史,可以酌情选用利福喷丁或利福布汀,但不能作为核心药物对待。有体外DST研究结果提示[高丽,肖和平,胡忠义,等. 耐多药结核分枝杆菌对利福布汀和利福平的交叉耐药性分析. 中华结核和呼吸杂志,2012,35(5):333-335.],低浓度耐利福平的耐多药结核分枝杆菌对于利福布汀仍然敏感。以往临床研究结果也提示[朱莉贞,傅瑜,初乃惠,等. 利福类联合多种药物长疗程方案治疗耐多药肺结核.中华结核与呼吸杂志,2006,29(8):520-523.],含利福喷丁或利福布汀联合化学治疗方案治疗耐多药肺结核仍有一定的临床效果,其中利福布汀组略优于利福喷丁组。
3.吡嗪酰胺:即使实验室结果表明吡嗪酰胺耐药,仍然推荐常规用于耐药结核病,理由是:①耐药尤其是耐多药肺结核患者往往存在肺部的慢性炎症,理论上讲,吡嗪酰胺在炎症产生的酸性环境中更为有效;②目前吡嗪酰胺DST结果不可靠,检测方法有待改进。
4.乙胺丁醇:如果经过评估达到了有效药物的标准,可以考虑加入到耐药结核病化学治疗方案中。由于乙胺丁醇DST结果的可靠性较差,即使敏感,也不作为方案中的核心药物。
二、注射类抗结核药物
所有耐药结核病患者都应在强化期接受注射类抗结核药物治疗。
1.链霉素:考虑到链霉素常规用于抗结核治疗,临床使用频率较高,以及耐多药结核病患者对链霉素的高耐药比例,即使DST结果证实链霉素敏感,一般也不推荐链霉素用于治疗耐多药结核病。但是,在临床菌株对所有二线注射类药物耐药而链霉素敏感的情况下,仍可以考虑使用链霉素,链霉素和二线注射类药物之间的交叉耐药性较小。
2.二线注射类抗结核药物:卡那霉素、阿米卡星或卷曲霉素一般被推荐作为治疗耐多药结核病第一选择用药。卡那霉素和阿米卡星较卷曲霉素具有更低的成本、较链霉素具有更低的毒性。卡那霉素和阿米卡星具有高度交叉耐药性,但阿米卡星具有更低的MIC和相对较低的不良反应,因此常规推荐阿米卡星而非卡那霉素。如果rrs基因突变,卷曲霉素与阿米卡星、卡那霉素可能有交叉耐药性。卷曲霉素较氨基糖苷类药物的耳毒性小。如果临床分离株同时耐链霉素和卡那霉素,或阿米卡星和卡那霉素,建议选择卷曲霉素。在经济条件许可的情况下,当阿米卡星和卷曲霉素均敏感时,考虑到药品的不良反应和患者的依从性,推荐直接使用卷曲霉素。
三、氟喹诺酮类药物
在耐多药结核病化学治疗方案中,氟喹诺酮类药物往往是最有效的抗结核药物,建议优先选择高代氟喹诺酮类药物;左氧氟沙星或莫西沙星是治疗耐多药结核病的首选氟喹诺酮类药物。加替沙星因其对糖代谢的影响,应谨慎选用。氧氟沙星抗结核作用弱,环丙沙星的抗结核作用更差,均不推荐用于治疗耐药结核病。
四、二线口服类抗结核药物
丙硫异烟胺的抗结核效果最佳。结核分枝杆菌inhA基因的突变与低浓度异烟肼耐药和高浓度丙硫异烟胺耐药相关。如果inhA基因存在突变,尽管仍然可以在耐多药结核病化学治疗方案中酌情使用丙硫异烟胺,但不作为核心药物对待。环丝氨酸、对氨基水杨酸应该纳入至耐多药结核病化学治疗方案中,除对氨基水杨酸与对氨基水杨酸-异烟肼有交叉耐药外,二者与其他抗结核药物无交叉耐药性。由于丙硫异烟胺和对氨基水杨酸的组合通常会导致较高的胃肠道不良反应和甲状腺功能减退症的发生率,因此,只有在需要3种第4组药物一起使用时,这2种药物才会被联合应用。相比于环丝氨酸,特立齐酮的临床应用数据有限。第4组药物可以从低剂量开始,3~10 d内逐步加至足量,以减少不良反应发生的频率、降低不良反应的严重程度。
对氨基水杨酸异烟肼为异烟肼与对氨基水杨酸的化学合成物。体外DST结果提示,对氨基水杨酸异烟肼对异烟肼敏感菌株同样具有杀菌效力,对耐异烟肼菌株仍有相当好的效果[申晓娜,赵雁林,肖和平,等.对氨基水杨酸异烟肼及异烟肼体外抗结核分枝杆菌活性分析.中华结核和呼吸杂志,2014,37(2): 132-134.]。因此,对氨基水杨酸异烟肼可用于:①对异烟肼敏感的耐药结核病;②经DST证实对对氨基水杨酸异烟肼敏感的耐异烟肼结核病患者。
对氨基水杨酸钠为对氨基水杨酸的注射用剂型,包含在对氨基水杨酸中,故未列入表中。
五、其他种类抗结核药物
本组药物是指疗效和长期使用安全性数据有限的抗结核药物(包括抗结核新药)。WHO不推荐第5组药物常规用于耐药结核病的治疗。除贝达喹啉和德拉马尼外,其余药物未注册用于治疗耐多药结核病。当不能够从第1~4组药物中选择到足够药物组成耐多药结核病化学治疗方案时,可从第5组药物中酌情选择2~3种药物。广泛耐药结核病更是需要从第5组药物中选择用药。
1.利奈唑胺:体外实验和动物研究均显示了良好的抗结核活性,被认为是一种最有效的抗结核药物和广泛耐药结核病化学治疗方案中的一个关键药物。但该药有许多严重的不良反应,包括骨髓抑制(贫血、白细胞减少症、血小板减少症和全血细胞减少)、周围神经病变和乳酸性酸中毒。当严重的不良反应发生,通常需要停止用药或每日剂量从600 mg降至300 mg。每日300 mg的剂量较少引起不良反应,但还不清楚低剂量是否同样有效或是否会导致结核分枝杆菌对利奈唑胺产生耐药。上海的研究结果提示,利奈唑胺治疗广泛耐药结核病有一定效果[Tang S, Zhang Q, Yu J, et al. Extensively drug-resistant tuberculosis at a tuberculosis specialist hospital in Shanghai,China:clinical characteristics and treatment outcomes. Scand J Infect Dis,2011,43(4):280-285.]。
2.氯法齐明:体外试验提示氯法齐明对耐药结核分枝杆菌有效[桂徐蔚,肖和平.氯法齐明对不同耐药类型结核分枝杆菌的体外抑菌活性研究.中华结核呼吸杂志,2011,34(8): 579-581.]。有报道,方案中使用9~12个月的氯法齐明,获得了不错的临床效果。75%~100%的患者在使用数周内发生皮肤色素沉着,治疗结束后的数月或数年方可逆转。
3.阿莫西林-克拉维酸钾:β-内酰胺类抗生素不是有效的抗结核药物,但β-内酰胺酶抑制剂在体外具有抗结核活性,体内杀菌活性的证据有限。阿莫西林-克拉维酸钾的抗结核作用相对较弱,由于便宜和不良反应较少,常在临床上使用。
4.亚胺培南-西司他丁和美罗培南:使用不方便,只能通过静脉点滴用药,而且给药成本高,在资源有限的情况下一般不推荐使用。
5.氨硫脲:抗结核疗效确切,是一种弱的抑菌剂。把氨硫脲放在第5组是因为其对耐药结核病的疗效还未确定。本品与乙硫异烟胺(丙硫异烟胺)和异烟肼有交叉耐药性。艾滋病患者禁忌使用氨硫脲,因为可能导致Stevens-Johnson综合征和死亡等严重不良反应发生。亚洲血统的患者对该药的耐受性较差。基于上述原因,临床上鲜有使用。
6.克拉霉素:对结核分枝杆菌杀菌活性不确定。一些研究表明,克拉霉素可与口服一线抗结核药物产生协同作用,但与二线抗结核药物无协同作用。大多数专家认为,克拉霉素的抗结核作用非常弱,对耐多药结核病患者没有治疗作用。
高剂量异烟肼不是一种独立的药物,故未作为第5组药物纳入表6中。
二、一线口服类抗结核药物
耐药结核病往往对其中一种或多种药物耐药。基于一线抗结核药物在疗效和安全性方面的优势,认为仍然可以根据患者的既往用药史、DST结果、药物的交叉耐药性和耐药稳定性及药物间的相互影响,从中选择用药。
(一)异烟肼(isoniazid,INH或H)
1. 分子式及相对分子质量:C6H7N30,137.14。
2. 作用机制:本品作用机制尚未完全阐明,可能是抑制敏感细菌分枝菌酸的合成而使细胞壁破裂。
3. 特点:异烟肼是目前使用的重要抗结核药物,对结核分枝杆菌有高度选择性抗菌活性,可影响其细胞壁的合成。异烟肼对生长旺盛的结核分枝杆菌呈杀菌作用,对静止期结核分枝杆菌仅有抑菌作用。异烟肼易渗入吞噬细胞,对细胞内外的结核分枝杆菌均有杀菌作用,故称“全效杀菌药”。本品耐药性最不稳定,即便在耐药情况下仍能具有一定的抗结核作用,并可延缓或防止结核分枝杆菌对其他抗结核药物产生耐药性。有报道采用高剂量异烟肼(16~20 mg·kg-1·d-1)治疗耐多药结核病取得了良好的效果,尤其是对低浓度异烟肼耐药者。但是,高剂量异烟肼的安全性未获得可靠的数据证实。有专家建议,如果菌株证实有katG的基因突变,不要使用异烟肼。该katG的突变目前可以通过线性探针检测。
本品口服后吸收快,分布于全身组织和体液中,包括脑脊液(脑膜炎时与血浆浓度近似,非脑膜炎时只有血浆浓度的20%)、胸腔积液、腹腔积液、皮肤、肌肉、乳汁和干酪样组织。可穿过胎盘,进入胎儿血液循环。血浆蛋白结合率仅0%~10%。口服4~6 h 后血药浓度因患者的乙酰化快慢而异,乙酰化的速率由遗传所决定。主要在肝脏经乙酰化代谢成无活性代谢产物,其中有的代谢产物具有肝毒性。慢乙酰化者常有肝脏N-乙酰转移酶缺乏,未乙酰化的异烟肼可被部分结合。异烟肼的半衰期(T1/2)在快乙酰化者为0.5~1.6 h,慢乙酰化者为2~5 h,肝、肾功能损伤者可能延长。
本品约70%经肾在24 h内排出,大部分为无活性代谢物。快乙酰化者93%以乙酰化型在尿液中排出,慢乙酰化者为63%;快乙酰化者尿液中7%的异烟肼呈游离型或结合型,而慢乙酰化者则为37%。本品亦可从乳汁排出,少量可自唾液、痰液和粪便中排出。相当量的异烟肼可经血液透析与腹膜透析清除。
4. 用法用量:(1)每日用药:4~6 mg·kg-1·d-1;成人0.3 g/d;儿童10~15 mg·kg-1·d-1;不宜超过0.3 g/d。每日量一次顿服。(2)隔日用药:成人每次0.6 g。(3)用药途径:一般采用口服法,可静脉滴注。
5. 不良反应:(1)使用常规剂量时,不良反应少见,慢乙酰化代谢者较易出现神经炎等不良反应。(2)异烟肼对肝脏的损伤,一般认为与药品过敏或药品中毒有关。单用异烟肼预防治疗的患者,约10%~20%出现一过性转氨酶升高,大多无自觉症状,严重药物性肝损伤者少见。大多数药物性肝损伤于用药2个月内出现,并且随着年龄增长而增加,20岁以下者少见。异烟肼与利福平并用时肝毒性增加。(3)异烟肼的其他不良反应,包括过敏反应、内分泌障碍(如性欲减退、痛经、男子乳房发育、甲状腺功能障碍等);血液系统可有粒细胞减少、嗜酸粒细胞增多、高铁血红蛋白血症;老年患者可偶见排尿困难、便秘。其他不良反应还包括视神经炎、关节痛、中枢神经系统的变化、药物诱发的狼疮、腹泻等。
6. 注意事项:(1)老年人、产后妇女和接受哺乳的婴儿,或合并有HIV感染、慢性肝病、糖尿病、尿毒症等疾病,以及癫痫、酒精滥用、营养不良、外周神经病变或大剂量服用异烟肼者时,可加用维生素B6,但应与异烟肼分开服用。鉴于维生素B6在试管内能降低异烟肼的抗菌作用,故异烟肼常规剂量应用时一般无需加服维生素B6。(2)本品可加强香豆素类抗凝血药、某些抗癫痫药、降压药、抗胆碱药、三环抗抑郁药等的作用,合用时需注意。(3)肝功能异常、有精神病和癫痫病史者、孕妇等慎用。(4)多脂肪饮食、抗酸药尤其是氢氧化铝可抑制本品的吸收,不宜同服,空腹吸收效果最好。
(二)利福平(rifampicin,RFP,R)
1. 分子式及相对分子质量:C43H58N4012,822.95。
2. 作用机制:本品为杀菌剂,通过与依赖于DNA的RNA多聚酶的β亚单位牢固结合,抑制细菌RNA的合成,防止该酶与DNA连接,从而阻断RNA转录过程,最终抑制蛋白质合成。
3. 特点:本品为脂溶性,易进入细胞内杀灭其中的敏感细菌,对革兰阳性、阴性菌和结核分枝杆菌等均有抗菌活性。单独用于治疗结核病时可迅速产生细菌耐药性,故必须与其他抗结核药物合用。亦可与其他药物联合用于麻风、非结核分枝杆菌感染的治疗。
本品口服吸收良好,血浆蛋白结合率80%~91%,进食或高脂肪饮食后服药可使达峰时间延迟和峰浓度降低或减少吸收。吸收后可分布至全身大部分组织和体液中,包括脑脊液。当脑膜有炎症时脑脊液内药物浓度增加。在唾液中亦可达到有效治疗浓度。本品可通过胎盘,进入胎儿血液循环。T1/2为3~5 h,多次给药后缩短为2~3 h。本品在肝脏中可被自身诱导微粒体氧化酶的作用而迅速去乙酰化,成为具有抗菌活性的代谢物25-O-去乙酰利福平,水解后形成无活性的代谢物由尿液排出。
本品主要经胆汁从肠道排泄,有肠-肝循环,但去乙酰利福平则无肠-肝循环。60%~65%的给药量经粪便排出,6%~15%的药物以原形、15%为活性代谢物经尿液排出;7%则以无活性的3-甲酰衍生物排出。亦可经乳汁分泌。在肾功能减退患者中本品无蓄积。由于自身诱导肝微粒体氧化酶的作用,在服用利福平的6~10 d后消除增加;用高剂量后由于经胆系排泄达到饱和,本品的排泄可能延缓。利福平不能经血液透析或腹膜透析清除。
4. 用法用量:(1)每日用药:8~12 mg·kg-1·d-1;成人体质量<50 kg,0.45 g/d;体质量≥50 kg,0.6 g/d;儿童10~20 mg·kg-1·d-1;成人与儿童用药剂量均不宜超过0.6 g/d。每日量一次顿服,空腹。(2)隔日用药:成人0.6 g/d。(3)用药途径:口服或静脉滴注。
5. 不良反应:(1)患者可出现转氨酶升高、黄疸和肝脏肿大等,其转氨酶多表现为一过性无症状的升高,在治疗过程中可自行恢复。老年人、嗜酒、营养不良者、原有肝胆疾病患者易发生肝脏损伤。利福平与异烟肼并用可增加肝毒性。(2)消化道不良反应常见上腹不适、厌食、恶心、呕吐、腹痛、腹泻或便秘等,轻者不影响继续用药。(3)精神系统障碍可出现头痛、嗜睡、眩晕、疲乏、肢体麻木、视力障碍、共济失调等症状。(4)过敏反应,如药热、皮疹、荨麻疹、嗜酸粒细胞增多、白细胞及血小板减少、凝血酶原减少、溶血、紫癜、急性肾功能衰竭等。(5)流行性感冒(简称“流感”)样综合征,常在间歇给药方案中出现。(6)体液橘红染色。
6. 注意事项:(1)孕妇、酒精中毒、肝功能损伤者慎用。注意利福平的肝酶诱导作用。(2)利福平用于间歇疗法时,最高剂量不宜超过0.6 g。(3)对利福霉素类药过敏者禁忌使用。
(三)利福布汀(rifabutin,Rfb)
1. 分子式及相对分子质量:C46H62N4011,847.00。
2. 作用机制:与利福平相似,主要是抑制DNA依赖性RNA多聚酶。
3. 特点:本品为杀菌剂,是由利福霉素-S衍生而来的半合成抗生素,适用于与其他抗结核药物联合治疗结核分枝杆菌所致的各型结核病,亦可用于非结核分枝杆菌感染的治疗,还适用于晚期HIV感染者预防鸟-胞内分枝杆菌复合体(MAC)的播散。
本品具有高亲脂性,血浆蛋白结合率约85%。吸收后分布广泛,易进入组织、细胞内,生物利用度为85%,高脂肪餐使吸收减慢但并不影响吸收总量。利福布汀在肺组织中的浓度可达到血清中的10~20倍。本品代谢后生成5种代谢产物,其中以25-O-去乙酰利福布汀和31-OH-利福布汀最为重要,前者的活性与母药相似,占药物全部抗菌活性的10%。本品53%的口服用药通过尿液排出,30%从粪便排出。利福布汀在血浆中清除缓慢,T1/2约(45±17)h。
老年人与健康成年人相比,利福布汀的药代动力学更易变化,剂量的选择应该慎重。目前尚未研究过18岁以下人群的利福布汀药代动力学。针对肾功能不全者的研究提示,与肌酐清除率(creatnine clearance rate,CCR)61~74 ml/min者相比,严重肾功能不全患者(CCR<30 ml/min)血药浓度-时间曲线下面积(AUC)增加了71%,轻、中度肾功能不全患者(CCR30~61 ml/min)增加了41%。建议对于CCR<30 ml/min的患者应减少使用利福布汀的剂量。
4. 用法用量:(1)成人:体质量<50 kg,0.15~0.3 g/d;体质量≥50 kg,0.3 g/d。(2)儿童:剂量尚未确定。(3)每日量一次顿服。(4)用药途径:口服。
5. 不良反应:(1)皮疹、胃肠道反应、中性粒细胞减少,偶尔出现血小板机能不全。(2)发生率小于1%的不良反应包括流感样综合征、肝炎、溶血、关节痛、骨髓炎、呼吸困难。(3)尚不能完全确立的不良反应包括惊厥、麻木、失语、非特异性心电图T波改变。(4)需要关注的不良反应还有眼部疼痛、视觉改变或畏光。
6. 注意事项:(1)HIV感染和(或)AIDS患者合并活动性结核病时,患者在没有其他抗结核药物联合治疗的情况下,利福布汀不能用于预防MAC播散,易导致结核分枝杆菌对利福布汀和利福平产生耐药。(2)因在动物实验中本品对胎儿骨骼生长有影响,故妊娠妇女只有在利大于弊时方可使用。(3)老年人、合并严重肾功能损伤者用药时,注意调整剂量。(4)利福布汀和利福平存在高度交叉耐药,利福布汀对耐利福平菌株的敏感度不足20%。(5)基于抗结核和抗病毒药物间的相互影响,在耐药结核病合并艾滋病的情况下,宜选用利福布汀。(6)对利福霉素类药物过敏者禁忌使用。
(四)利福喷丁(rifapentine,Rft)
1. 分子式及相对分子质量:C47H64N4012,877.03。
2. 作用机制:利福喷丁作用机制同利福平。
3. 特点:本品为半合成广谱杀菌药,MIC为0.12~0.25 mg/L,比利福平强2~10倍。常与其他抗结核药物联合用于治疗初治与复治结核病,不宜用于结核性脑膜炎;与其他抗麻风药联合用于麻风病的治疗可能有效;亦可用于非结核分枝杆菌感染的治疗,如堪萨斯分枝杆菌、蟾分枝杆菌感染,但鸟分枝杆菌对本品耐药。
本品半衰期长为其特点,T1/2为19.9 h,更适合直接督导下的短程化疗(directly observed treatment short-course,DOTS)。体内抗结核试验表明,给小鼠一次灌胃利福喷丁10 mg/kg,其体内抗结核活性可维持4~5 d,而利福平不足1 d;以相同剂量利福喷丁每周1次用药,可获得利福平每周6次用药相似的疗效。本品与利福平存在100%的交叉耐药,单独使用多产生耐药性。
利福喷丁口服吸收缓慢,在胃肠道中吸收不完全,但本品的微晶生物利用度可提高。血浆蛋白结合率>98%。本品吸收后在体内分布广,尤其在肝组织中分布最多,其次为肾,其他组织中亦有较高浓度,但不易透过血-脑屏障。利福喷丁主要在肝内去乙酰化,但比利福平慢,生成活性代谢产物25-去乙酰利福丁,其血浆蛋白结合率为93%。本品有肝-肠循环,由胆汁排入肠道的原药部分可被再吸收。本品和25-去乙酰利福喷丁主要经胆汁随粪便排出,仅部分由尿中排出。
4. 用法用量:(1)成人:体质量<50 kg,0.45 g/次;体质量≥50 kg,0.6 g/次,每周1~2次;每次不宜超过0.6 g,空腹顿服。(2)儿童:10 mg·kg-1·次-1,每周1次。≥12岁:体质量<45 kg,0.45 g/次,每周1次;体质量≥45 kg,0.6 g/次,每周1次。(3)用药途径:口服。
5. 不良反应:同利福平,但较轻微。
6. 注意事项:同利福平。(1)对本品及利福平、利福布汀过敏者禁用。(2)肾功能衰竭和(或)血液透析时无需调整剂量(约17%通过肾脏排泄)。(3)不建议与大部分抗逆转录病毒药物合并使用。
(五)吡嗪酰胺(pyrazinamide,PZA,Z)
1. 分子式及相对分子质量:C5H5N30,123.12。
2. 作用机制:作用机制可能与吡嗪酸有关,吡嗪酰胺渗透入吞噬细胞后并进入结核分枝杆菌菌体内,菌体内的酰胺酶使其脱去酰胺基,转化为吡嗪酸而发挥抗菌作用。另因吡嗪酰胺在化学结构上与烟酰胺相似,通过取代烟酰胺而干扰脱氢酶,阻止脱氢作用,妨碍结核分枝杆菌对氧的利用,而影响其正常代谢。本品对半静止状态下的结核分枝杆菌有杀菌作用,但机制不明。
3. 特点:本品为烟酰胺的衍生物,仅对结核分枝杆菌有效,对其他分枝杆菌及其他微生物无效。对结核分枝杆菌具有抑菌或杀菌作用,但取决于药物浓度和细菌敏感度。本品仅在pH偏酸时(pH≤5.6)有抗菌活性。结核分枝杆菌容易对本品迅速产生耐药性,单用时约6周即可产生耐药,与其他抗结核药物并用可延缓耐药性的产生。吡嗪酰胺与其他抗结核药物无交叉耐药。
本品主要是在细胞内抗菌,在胞内的杀菌活性可因氟喹诺酮类药的应用而得到加强,如果患者仅使用过标准的初、复治化学治疗方案,即吡嗪酰胺的使用的总疗程大约在4~5个月,仍然有治疗耐药结核病的价值。基于大多数耐多药结核病患者伴有肺部慢性炎症,吡嗪酰胺在炎症的酸性环境中可充分发挥作用的原理,在无可靠DST证明吡嗪酰胺耐药的情况下,推荐吡嗪酰胺在耐药结核病的治疗中全程使用。
吡嗪酰胺口服后吸收快而完全,广泛分布于全身组织和体液中,包括肺、脑脊液、肾、肝及胆汁;脑脊液内药物浓度可达同期血药浓度的87%~105%。血浆蛋白结合率为10%~20%。主要在肝内代谢,水解生成活性代谢产物吡嗪酸,继而羟化成为无活性的代谢物。经肾小球滤过排泄,24 h内用药量的70%主要以代谢物从尿中排出(其中吡嗪酸约33%),3%以原形排出。T1/2为9~10 h,肝、肾功能减退时可能延长。血液透析4 h可降低吡嗪酰胺血药浓度的55%,血中吡嗪酸降低50%~60%。
4. 用法用量:(1)每日用药:20~30 mg·kg-1·d-1;成人体质量<50 kg,1.5 g/d;体质量≥50 kg,1.75 g/d;儿童30~40 mg·kg-1·d-1;成人与儿童用药剂量不宜超过2 g/d;每日量一次顿服或分次服用。(2)隔日用药:成人体质量<50 kg,1.5 g/d;体质量≥50 kg,2 g/d。(3)肾功能不全患者25~35 mg/kg,每周3次用药。(4)用药途径:口服。
5. 不良反应:(1)吡嗪酰胺可引起转氨酶升高,肝脏肿大。长期大剂量应用时可发生中毒性肝炎,造成严重肝细胞坏死、黄疸、血浆蛋白减少等。肝损伤与剂量和疗程有关,常规用量下较少发生肝损伤,老年人、酗酒和营养不良者肝损伤的发生率增加。(2)吡嗪酰胺的代谢产物吡嗪酸能抑制肾小管对尿酸的排泄(促进尿酸的重吸收),从而引起高尿酸血症,导致痛风发作,引起关节疼痛。(3)胃肠道反应,可有食欲不振,恶心呕吐。过敏反应,偶见发热及皮疹,重者可出现黄疸。个别患者可发生光敏反应,皮肤暴露部位呈红棕色。
6. 注意事项:(1)糖尿病、痛风、严重肝功能减退者、孕妇慎用;对本品过敏者禁用。(2)本品毒性较强,除非必须,通常儿童不宜应用。
(六)乙胺丁醇(ethambutol,EMB或E)
1. 分子式及相对分子质量:C10H24N2O2·2HCl,277.23。
2. 作用机制:本品抑制分枝杆菌细胞壁的合成,可渗入分枝杆菌体内干扰RNA的合成从而抑制细菌的繁殖,但是作用机制尚未完全阐明。
3. 特点:本品对结核分枝杆菌和非结核分枝杆菌中的堪萨斯和鸟等分枝杆菌有抑菌作用,在pH中性环境中作用最强。本品为抑菌药,仅对生长繁殖期的结核分枝杆菌有作用,其对细胞壁的破壁作用有效地促进了其他药进入细菌体内的速度,提升了胞内药物的浓度,与其他一线抗结核药物有协同作用,且可延缓其他药品耐药性的产生;对静止期细菌几乎无影响。经复治标准化学治疗方案治疗失败者,如无可靠的DST结果证明乙胺丁醇敏感,原则上不推荐使用。乙胺丁醇在试管内耐药性出现较慢,临床应用3~4个月可出现耐药。迄今未发现本品与其他抗结核药物有交叉耐药性。
本品口服给药,生物利用度75%~80%,血浆蛋白结合率为20%~30%。吸收后广泛分布于全身各组织和体液中(脑脊液除外)。红细胞内药物浓度与血浆浓度相等或为血浆的2倍,并可持续24 h;肾、肺、唾液和尿液内的药物浓度都很高;但胸腔积液和腹腔积液中的浓度则很低。本品不能渗入正常脑膜,但结核性脑膜炎患者脑脊液中可有微量渗入;可通过胎盘进入胎儿血液循环;可从乳汁分泌,乳汁中的药物浓度约相当于母体血药浓度。主要经肝脏代谢,约15%的给药量代谢成为无活性代谢物。给药后约80%在24 h内经肾小球滤过和肾小管分泌排出,其中至少50%以原形排泄,约15%为无活性代谢物。在粪便中以原形排出约20%。T1/2为3~4 h,肾功能减退者可延长至8 h。相当量的乙胺丁醇可经血液透析和腹膜透析从体内清除。
4. 用法用量:(1)每日用药:15~25 mg·kg-1·d-1,不宜超过1.5 g/d。上限剂量仅在强化期使用,继续期推荐15 mg·kg-1·d-1。成人体质量<50 kg,0.75 g/d;体质量≥50 kg,1.0 g/d;儿童15~25 mg·kg-1·d-1。每日量一次顿服或分2次服用。(2)隔日用药:成人体质量<50 kg,1.0 g/d;体质量≥50 kg,1.25~1.5 g/d。(3)肾功能不全患者15~25 mg/kg,每周3次用药。(4)用药途径:口服。
5. 不良反应:(1)主要不良反应是视神经毒性,早期表现为视力模糊、眼球胀满感、异物感、流泪、羞明等。严重者可出现视力减退、视野缺损、辨色力减弱,也可引起失明,视神经毒性与剂量呈正相关。(2)一般口服常用量(15 mg·kg-1·d-1)的不良反应较少且轻微,除视神经损伤外的其他不良反应有过敏、瘙痒、皮疹、头痛、眩晕、关节痛、胃肠道反应、全身不适、精神反应、肝功能异常、粒细胞减少等。
6. 注意事项:(1)本品不宜用于小儿,婴幼儿禁用。(2)有痛风、视神经炎、不能准确表达症状者慎用。(3)肾功能减退时排泄减少,可引发蓄积中毒,故肾功能减退者慎用。(4)球后视神经炎的发生与剂量相关,肾功能减退或肾衰竭时风险加大。(5)治疗期间应注意检查视野、视力、红绿鉴别力等。
三、注射类抗结核药物
(一)链霉素(streptomycin,Sm或S)
1. 分子式及相对分子质量:(C21H39N7012)2·3H2SO4,1457.40。
2. 作用机制:本品主要作用于结核分枝杆菌的核糖体,诱导遗传密码的错读,抑制信使RNA转译,干扰转译过程中的校对,从而抑制蛋白质合成。
3. 特点:链霉素属氨基糖苷类抗生素,半效杀菌药,对多种革兰阴性杆菌及葡萄球菌的某些菌株有效,对结核分枝杆菌的作用最为突出,呈强抑菌作用,高浓度有杀菌作用。碱性环境可增强其抗菌作用。在抗结核注射剂中链霉素抗结核活性最强。大多数非结核分枝杆菌对本品耐药。单用链霉素迅速发生耐药,耐药菌的毒力不减,也不可再转敏感,而且可产生链霉素依赖菌。故耐药后一般不考虑再用。
本品肌内注射后吸收良好,蛋白结合率20%~30%。主要分布于细胞外液,并可分布于除脑以外的所有器官、组织。本品到达脑脊液和支气管分泌液中的量很少(脑膜有炎症时渗透增加),可到达胆汁、胸腔积液、腹腔积液、结核性脓肿和干酪样组织。在尿液中浓度高,可穿过胎盘组织。本品在体内不代谢,主要经肾小球过滤排出,80%~98%在24 h内排出,约1%从胆汁排出,此外亦有少量从乳汁、唾液和汗液中排出。本品有相当量可经血液透析清除。
4. 用法用量:(1)每日用药:15~18 mg·kg-1·d-1,不超过1.0 g/d。成人0.75 g/d;儿童20~40 mg·kg-1·d-1;不宜超过1.0 g/d;>59岁10 mg·kg-1·d-1,不宜超过750 mg/d,或15 mg·kg-1·次-1,一周3次。(2)间歇治疗:成人每次0.75~1.0 g,每周2~3次。(3)肾功能不全:12~15 mg·kg-1·次-1,每周2~3次,不可每日使用。(4)用药途径:肌内注射(有鞘内注射和腹腔内注射的报道)。
5. 不良反应:(1)常见的不良反应有口唇麻木、肌肉抽搐,注射后不久即可出现。此反应与药品所含杂质如甲醛链霉胍和甲醛链霉素等有关。(2)对第八对颅神经的损伤是链霉素的严重不良反应,主要引起前庭功能障碍,如眩晕、恶心、呕吐、共济失调、步履蹒跚;其次是耳蜗损伤,可出现耳鸣、耳聋,此毒性常为永久性损伤。出现此类症状应立即停药。(3)肾毒性一般为轻度损伤,多见管型尿和蛋白尿,血尿素氮、肌酐升高。严重者必须停药。(4)可出现皮疹、发热、关节痛等过敏反应,应停药,以免引起更严重毒性反应。过敏性休克大多于注射后1~2 min或10 min之内出现,表现为突然发作的呼吸困难、面色先苍白后发绀、昏迷、抽搐、口吐白沫、大小便失禁等,严重者可致死。过敏性休克比青霉素发生率低,一旦发生则死亡率高。(5)可出现电解质紊乱。
6. 注意事项:(1)本品与阿米卡星和卷曲霉素具有单向交叉耐药性,对阿米卡星或卷曲霉素耐药时使用链霉素无效。(2)老年人应减量。儿童慎用,孕妇禁用,病情特别需要时,可采用间歇应用,一周2~3次。(3)链霉素与其他氨基糖苷类药先后连续局部或全身应用,可增加耳毒性、肾毒性以及神经肌肉阻滞作用的可能性。(4)本品不可与其他氨基糖苷类药同时使用。(5)利尿剂与氨基糖苷类药合用时,药物的耳毒性风险增加。(6)条件允许情况下可对患者的血药浓度进行密切随访。
(二)卡那霉素(kanamycin,Km)
1. 分子式及相对分子质量:C18H36N4011·nH2SO4,484.50。
2. 作用机制:参阅阿米卡星。
3. 特点:本品对结核分枝杆菌有杀菌作用,且对链霉素耐药菌株仍然敏感,主要用于对本品仍敏感的复治、耐药患者的治疗,用于抗结核治疗时,需与其他抗结核药物品配伍。本品的耳毒性和肾毒性高于链霉素。
口服不吸收,肌内注射吸收40%~80%。其余参阅阿米卡星。
4. 用法用量:(1)成人:15~20 mg·kg-1·d-1,不超过1.0 g/d。体质量<50 kg,0.5 g/d;体质量≥50 kg,0.75 g/d;不宜超过1.0 g/d。(2)儿童:15~30 mg·kg-1·d-1,不超过1.0 g/d,每周5~7次。(3)老年:0.5 g/d或0.75 g,隔日1次。(4)肾功能不全患者12~15 mg·kg-1·次-1,每周3次。
5. 用药途径:深部肌内注射。
6. 不良反应:(1)发生率较高者有听力减退、耳鸣或耳部饱满感等耳毒性,血尿、排尿次数减少或尿量减少、食欲减退、极度口渴等肾毒性,以及步履不稳、眩晕(耳毒性:影响前庭)、恶心或呕吐(耳毒性:影响前庭;肾毒性)。(2)发生率较少者有呼吸困难、嗜睡或软弱。
7. 注意事项:(1)不可用于听神经障碍及肾功能不良者。禁止与强利尿剂并用,禁止做胸腔、腹腔注射,避免呼吸抑制。(2)禁用于氨基糖苷类药物过敏者。(3)由于与链霉素等氨基糖苷类药物有单项交叉耐药,故需注意临床用药顺序。链霉素耐药时再考虑采用本药。(4)使用本品需注意定期做尿常规、肾功能和电解质检测。(5)停药后发生听力减退、耳鸣或耳部饱满感,提示可能为耳毒性,必须引起注意。
(三)阿米卡星(amikacin,Am)
1. 分子式及相对分子质量:C22H43N5013·nH2SO4,585.61。
2. 作用机制:通过干扰蛋白质的合成阻止细菌生长。
3. 特点:本品为氨基糖苷类广谱抗生素,对结核分枝杆菌有杀菌作用,治疗各类型结核病,且对链霉素耐药菌株仍然敏感,主要用于链霉素耐药者。
本品和卡那霉素的作用相似,两者具完全交叉耐药性,但本品对结核分枝杆菌的杀菌活性更高,而不良反应低于卡那霉素。因此,在耐药结核病化疗中提倡选用阿米卡星。本品与卷曲霉素有部分双向交叉耐药性,对卷曲霉素耐药菌株部分有效。
本品肌内注射后迅速被吸收,蛋白结合率低。主要分布于细胞外液,正常婴儿脑脊液中浓度可达同时期血药浓度的10%~20%,当脑膜有炎症时,则可达同期血药浓度的50%,但在心脏心耳组织、心包液、肌肉、脂肪和间质液内的浓度很低。5%~15%的药量重新分布到各种组织,可在肾脏皮质细胞和内耳液中积蓄。可穿过胎盘,尿中药物浓度高,滑膜液中可达治疗浓度。支气管分泌物、胆汁及房水中浓度低,腹腔积液中很难检测到。本品在体内不代谢。主要经肾小球滤过排出,9 h内排出84%~92%。成人中T1/2为2~2.5 h,胎儿3.7 h,新生儿4~8 h(与出生时体质量和年龄成反比)。血液透析与腹膜透析可自血液中清除相当量的药物。
4. 用法用量: (1)成人:15~20 mg·kg-1·d-1,不超过1.0 g/d。强化期15 mg·kg-1·次-1(0.75~1 g/d,不超过1 g/d;最佳剂量15~20 mg·kg-1·d-1),每周5~7次;如需要,继续期治疗可以采用15 mg·kg-1·次-1,每周3次;年龄>59岁者,推荐强化期10 mg·kg-1·次-1(不超过750 mg/d),每周5~7次,继续期每周2~3次。中国因产地不同,成人常规用量0.4~0.6 g/d,一般不超过0.8 g/d。(2)儿童:强化期15~30 mg·kg-1·次-1(不超过1 g/d),每周5~7次;继续期15~30 mg·kg-1·次-1(不超过1 g/d),每周3次。(3)用药途径:深部肌内注射或静脉滴注,肌内注射时注意变换注射部位以避免局部不适。
5. 不良反应:(1)注射部位疼痛。(2)肾毒性(蛋白尿)。(3)耳毒性(听力丧失),前庭毒性(眩晕、共济失调、头晕),老年、长期使用都可增加耳毒性。(4)血清电解质异常(包括低钾和低镁)。(5)外周神经炎和皮疹。
6. 药物相互作用:(1)与髓袢利尿剂(速尿)合用可加重耳毒性。(2)可增加非去极化肌松剂的效力。
7. 注意事项:(1)因与卡那霉素有完全性双向交叉耐药性,故不可用于对卡那霉素耐药患者。(2)不宜用于孕妇及肾功能不良者。(3)慎用或禁用于肾功能减退、脱水、使用强利尿剂者,特别是老年患者。(4)严重肝病可能快速发展为肝肾综合征者慎用。(5)本品禁止静脉推注。(6)注意定期复查肾功能。(7)本品干扰正常菌群,长期应用可导致非敏感菌过度生长。
(四)卷曲霉素(capreomycin,Cm)
1. 分子式及相对分子质量:C25H46N14011S,750.78。
2. 作用机制:卷曲霉素属多肽类药,作用机制尚不明确。
3. 特点:对结核分枝杆菌具有杀菌作用,适用于复治、耐药结核病的治疗。本品对链霉素耐药菌株仍然敏感,对卡那霉素或阿米卡星耐药菌株部分敏感,是治疗耐药结核病的重要药物之一。
本品很少经胃肠道吸收,需肌内注射。在尿中浓度甚高,也可穿过胎盘进入,不能渗透进入脑脊液。T1/2为3~6 h,主要经肾小球滤过以原形排出。给药12 h内以原形排出50%~60%,少量经胆汁排出。肾功能损伤患者T1/2延长,血清中可有卷曲霉素蓄积。本品可经血液透析清除。
4. 用法用量:(1)成人:15~20 mg·kg-1·d-1,不超过1.0 g/d。体质量<50 kg:0.75 g/d;体质量≥50 kg:1.0 g/d。(2)儿童:15~30 mg·kg-1·d-1,不超过1.0 g/d。(3)老年:剂量酌减。年龄>59岁:10 mg·kg-1·次-1,5~7次/周;或15 mg·kg-1·次-1,每周3次;每次最大剂量0.75 g。(4)肾功能衰竭和(或)透析:12~15 mg·kg-1·次-1,每周2~3 次,不可每日使用。(5)用药途径:一般深部肌内注射,或静脉滴注。
5. 不良反应:(1)发生率相对较多的不良反应:血尿、尿量或排尿次数显著增加或减少,食欲减退或极度口渴。(2)发生率较少的不良反应:过敏反应、耳毒性、肾毒性、神经肌肉阻滞等。(3)其他不良反应:电解质紊乱,尤其是低钾血症。
6. 注意事项:(1)用药期间应做电解质、肾功能尿常规检查。有电解质紊乱的患者,需在电解质获得纠正后使用。(2)必须与其他抗结核药物联合应用。(3)用药期间严密观察头晕、耳鸣、听力减退等反应。(4)本品与阿片类镇痛药并用,有抑制呼吸的作用。(5)与抗真菌药、万古霉素、杆菌肽、抗癌药并用,可增加肾毒性和耳毒性。(6)禁止应用于有听力障碍或肾功能障碍、重症肌无力、帕金森症患者。禁用于妊娠和哺乳期妇女及对本品过敏者。
四、氟喹诺酮类药物
常用于耐药结核病的氟喹诺酮类药物主要包括左氧氟沙星(levofloxacin)、莫西沙星(moxifloxacin)和加替沙星(gatifloxacin)。对结核分枝杆菌的最低抑菌浓度,加替沙星和莫西沙星(MIC:0.25 μg/ml)优于左氧氟沙星(MIC:0.5 μg/ml)和氧氟沙星(MIC:1.0 μg/ml),其抗菌活性是左氧氟沙星的2倍、氧氟沙星的4倍。当2倍于最低抑菌浓度时即为最低杀菌浓度(MBC),在巨噬细胞中莫西沙星(MBC 0.5 μg/ml)明显强于左氧氟沙星(MBC 2 μg/ml)和氧氟沙星(MBC 4 μg/ml)。抗结核作用强弱依次为:莫西沙星>左氧氟沙星>氧氟沙星,加替沙星可获得与莫西沙星相似的效果。氧氟沙星被认为其抗结核活性较其他氟喹诺酮类药物弱,而不推荐用于耐药结核病。加替沙星具有严重的不良反应,如低血糖、高血糖和新发糖尿病,应酌情使用。莫西沙星或左氧氟沙星是治疗耐药尤其是耐多药结核病的首选氟喹诺酮类药物。
近期国内外研究结果提示,高代氟喹诺酮类药物对低代氟喹诺酮类药物的耐药菌仍有一定的抗菌活性,因此在怀疑或DST证实低代氟喹诺酮类药物耐药时,仍可考虑使用高代氟喹诺酮类药物,但此时不应将其视为耐药结核病化疗中的核心药物。考虑到这类药物间的交叉耐药性,只要条件许可,仍推荐直接使用最高代氟喹诺酮类药物,以确保其发挥最佳效果,并使耐本类药物的概率降至最低。氟喹诺酮类药物与现有其他抗结核药物无交叉耐药性。
(一)氧氟沙星(ofloxacin,Ofx)
1. 分子式及相对分子质量:C18H20FN3O4,361.38。
2. 作用机制:主要通过作用于细菌脱氧核糖核酸(DNA)旋转酶(拓扑异构酶Ⅱ),致使细菌染色体上DNA链断裂,并抑制DNA旋转酶A亚单位,从而抑制DNA的复制、转录,达到阻止DNA复制、转录而杀菌的目的。当DNA旋转酶A亚单位的gyrA基因突变,意味着对氟喹诺酮类药物出现中高度耐药;gyrB基因突变发生者将出现低度耐药。
3. 特点:具广谱抗菌作用,尤其对需氧革兰阴性杆菌抗菌活性高,对结核分枝杆菌和非结核分枝杆菌亦有抗菌活性。
本品口服后吸收完全,生物利用度达95%~100%,血浆蛋白结合率为20%~25%。食物对本品的吸收影响很少,多次给药后稳态血药浓度约在给药后第3天达到。吸收后在体内分布广泛,全身组织和体液中均可达有效浓度。胆汁中药物浓度可达血药浓度的4~8倍,在肺、肾组织中可达3倍以上。骨、前列腺、皮肤及软组织或体液中均可超过同期血药浓度而达有效水平。本品尚可穿过胎盘进入胎儿体内,也可通过乳汁分泌。主要以原形自肾排泄,少量(3%)在肝内代谢。口服后24 h内尿中排出给药量的75%~90%,自粪便中排出少量。T1/2约为4.7~7.0 h,肾功能减退时可延长。
4. 用法用量:(1)每日用量:15~20 mg·kg-1·d-1;体质量<50 kg,0.4 g/d;体质量≥50 kg,0.6 g/d;不宜超过0.8 g/d。每日量1次或分次服用。(2)用药途径:口服或静脉滴注。
5. 不良反应:(1)中枢神经系统损伤:表现为头痛、眩晕、失眠。重者出现幻觉、抑郁、精神异常及精神错乱,甚至引发癫痫发作。有精神病史及癫痫病史者禁用。(2)胃肠道反应:腹部不适、腹泻、恶心或呕吐。(3)过敏反应和光敏反应:皮肤瘙痒、皮疹(多为麻疹样斑丘疹),偶可发生渗出性多形性红斑。光敏反应较少见。(4)肝肾损伤:约1%~3%的患者使用氟喹诺酮类药物后出现轻度药物相关的血清转氨酶轻度升高,而且是可逆的,通常情况下不需要停药。不同品种的氟喹诺酮类药物对肝肾影响程度不一,如氧氟沙星和左氧氟沙星偏重于对肾脏的影响,莫西沙星则偏重于对肝脏的影响。(5)血液系统损伤:可引起白细胞减少、血小板减少、贫血等。(6)肌腱炎:肌腱疼痛、肿胀、断裂等肌腱障碍。(7)QTc间期延长:氟喹诺酮类药物的使用与QTc间期延长相关,能导致尖端扭转性室性心动过速(TdP),从而危及生命。不同品种的氟喹诺酮类药物对QTc间期延长作用有差异,本品此作用相对较轻。(8)糖代谢异常:氟喹诺酮类药物可影响糖尿病患者的血糖控制水平。不同品种的氟喹诺酮类药物的影响程度不一,莫西沙星出现高血糖症的比例为0.6%,发生低血糖者占1.0%;左氧氟沙星出现高血糖症者占0.39%,发生低血糖者占0.93%,本品相对较轻。
6. 注意事项:(1)本品属于浓度依赖型,以一次顿服为佳。(2)需与其他抗结核药物品联合应用。(3)18岁以下青少年、尤其是儿童不宜应用本品。(4)有精神病史者、癫痫病史者慎用或禁用。(5)应用此品时,注意不与含铝、镁、铁、锌、钙制剂同服,防止干扰氟喹诺酮类药物吸收。亦不可与茶碱、咖啡因同服,预防茶碱中毒。(6)与抗结核药物联合应用时,需注意中枢神经系统、造血系统、肌肉骨骼、肝肾功能的损伤,以及出现过敏反应和光敏反应。(7)用药后避免日光照射,也可涂抹防晒霜预防光敏毒性。(8)氟喹诺酮类药物可引起过敏性休克、喉头水肿等严重过敏反应,因此本品禁用于对任何氟喹诺酮类药物过敏者。(9)肾功能障碍者慎用,老年患者应用此药需检测肾功能。哺乳期妇女应用此药时需暂停授乳。(10)应用本品可引起血糖波动,需注意调节降糖药用量。(11)碱性药品(碳酸氢钠、氢氧化铝、胃得乐、西咪替丁、碳酸钙)和抗胆碱药(阿托品、东莨菪碱、颠茄),可减少氟喹诺酮类药物的吸收,避免长期并用。(12)禁止非甾体消炎镇痛药(阿司匹林、丁苯羟酸、双氯芬酸)与氟喹诺酮类药物并用,防止加剧中枢神经系统毒性反应和诱发癫痫发作。(13)同时应用茶碱、咖啡因等药时,氟喹诺酮类药物可干扰细胞色素P450系统而减少茶碱在体内的消除,故需注意调整剂量或做血药浓度监测,预防茶碱中毒。
(二)左氧氟沙星(levofloxacin,Lfx)
为氧氟沙星光学异构体的左旋体。
1. 分子式及相对分子质量:C18H20FN3O4·1/2(H2O),370.38。
2. 作用机制:参阅氧氟沙星。
3. 特点:MIC为0.5 μg/ml,体外抗菌活性是氧氟沙星的2倍,主要用于敏感菌所致的感染。具有抗结核作用,主要用于耐药结核病的治疗。
本品口服吸收好,生物利用度约为99%,血浆蛋白结合率为30%~40%。组织渗透性较好,在胆汁、气管、肺、肾、前列腺、皮肤中具有相对聚集作用,组织浓度可达血药浓度的2~3倍。其中肺组织中药物浓度可达同期血药浓度的2~5倍,皮肤组织、水疱液、扁桃体、前列腺组织、女性生殖道组织、泪液、痰液、唾液中药物浓度约为同期血药浓度的1~2倍。脑脊液浓度较低,为血药浓度的16%~20%。与食物同服时,达峰时间略推迟(约1 h),血药峰浓度略降低(约降低14%)。本品在体内代谢甚少,主要通过肾脏排泄,T1/2为4~6 h,肾功能减退时,该药T1/2延长,清除缓慢,需调整剂量。本品不被血液透析和腹膜透析清除。
4. 用法用量:(1)成人:10~15 mg·kg-1·d-1;体质量<50 kg,0.4 g/d;体质量≥50 kg,0.5 g/d;可用至0.6 g/d;WHO推荐成人剂量0.75 g/d,最大剂量可达到1.0 g/d。每日量1次或分次使用;(2)儿童:≤5岁:15~20 mg·kg-1·d-1,分早、晚2次服用;>5岁:10~15 mg·kg-1·d-1,1次/d。(3)肾功能衰竭和(或)透析:当CCR<30 ml/min,750~1000 mg/次,每周3次,不可每日服用。(4)用药途径:口服或静脉滴注。
5. 不良反应:同氧氟沙星。
6. 注意事项:同氧氟沙星。
(三)莫西沙星(moxifloxacin,Mfx)
1. 分子式及相对分子质量:C21H24FN3O4,401.4314。
2. 作用机制:通过对细菌的拓扑异构酶Ⅱ(DNA旋转酶)和拓扑异构酶Ⅳ的抑制作用阻断细菌DNA复制而起抗菌作用。
3. 特点:莫西沙星为新一代氟喹诺酮类药物,具广谱抗菌作用,用于各种感染的治疗,对结核分枝杆菌具有较强的杀菌活性,主要用于耐药结核病的治疗。
口服后吸收良好,生物利用度约90%,血浆蛋白结合率约50%。高脂肪餐不影响本品的吸收,但同服抗酸药可减少吸收。口服吸收后在体内广泛分布,在肺泡巨噬细胞、肺泡上皮衬液、上颌窦黏膜、支气管黏膜、鼻息肉中的药物浓度与同期血药浓度之比为1.7~21.2不等。可通过血-脑屏障,渗透性良好。
莫西沙星主要通过肝脏代谢,经尿排出只占22%,血浆T1/2为11~15 h。在肝内通过与葡糖苷酸和硫酸酯结合而代谢,不经细胞色素酶P450系统。该药的代谢物M1硫酸酯结合物占给药量的38%,主要由粪中排出;口服或静脉给药量的14%转化为葡糖苷酸结合物(M2),主要自尿排出。M2和M1的Cmax分别约为母体同期血药浓度的40%和<10%。
老年健康志愿者口服及静脉给药后,Cmax、AUC和T1/2β与年轻者相比无明显差别,提示老年人应用时不需调整剂量。在轻、中、重度肾功能减退者中,该药的药代动力学参数均无明显改变,提示肾功能减退患者不需调整剂量。在肝功能减退呈轻度(Child-Pugh A)和中度(Child-Pugh B)患者中,莫西沙星原药的AUC分别较健康受试者增加78%和102%,Cmax增加79%和84%;代谢物M1和M2的AUC及Cmax亦有不同程度升高;但轻度和中度肝功能减退患者均不需调整剂量。严重肝功能减退者(Child-Pugh C)的药代动力学研究资料尚缺乏。
4. 用法用量:(1)每日用量:7.5~10 mg·kg-1·d-1;成人0.4 g/d。每日量一次或分次服用,以1次顿服为佳。(2)用药途径:口服或静脉滴注。
5. 不良反应:同氧氟沙星,对QTc间期延长的作用更强。
6. 注意事项:同氧氟沙星。(1)肾功能受损包括透析患者应用莫西沙星不需减量。(2)莫西沙星可以与食物一同服用,但是需要注意在服用该药前2 h或服用后4 h,不要服用乳制品、抗酸剂(尤其是含铝类药)、维生素、硫糖铝等可能影响吸收的食物或药品。
(四)加替沙星(gatifloxacin,Gfx)
1. 分子式及相对分子质量:C19H22FN3O4,375.40。
2. 作用机制:同莫西沙星。
3. 特点:MIC为0.25 μg/ml,优于氧氟沙星和左氧氟沙星,具有较强的抗结核作用。有报道加替沙星可引起血糖异常,包括症状性低血糖症和高血糖症,特别在糖尿病患者中易发生。但也有报道经格列本脲治疗已控制病情的糖尿病患者多次口服本品,虽服药后血清胰岛素浓度降低,但无血糖水平变化。
加替沙星口服吸收良好,口服后吸收完全,且不受饮食因素影响,绝对生物利用度为96%,血清蛋白结合率低(约20%),在体内广泛分布于组织和体液中。唾液中药物浓度与血药浓度相近,唾液与血液中药物浓度比为0.88;在肺泡巨噬细胞、肺实质中药物浓度与同期血药浓度之比分别为26.5和4.09;在窦黏膜、支气管黏膜、痰液、肺上皮细胞衬液、宫颈、阴道、前列腺液及精液等组织和体液中的药物浓度均高于同期血药浓度,比值为1.01~1.78。本品在体内很少代谢,无肝酶诱导作用,主要以原形自尿排出,口服或静脉给药后48 h内自尿中排出给药量的70%以上,尿排出代谢物<1%,给药量的5%以原形从粪便中排出。T1/2β为7~14 h。
老年(≥65岁)受试者单次服用400 mg后,与年轻女性相比,老年女性Cmax增加21%,AUC增加32%,此与肾功能随年龄增加而减退有关,不需调整剂量。
慢性肝病伴中度肝损伤者(肝硬化分级Child-Pugh B)口服单剂加替沙星400 mg后,其Cmax及AUC0~∞分别增高32%和23%。但中度肝损伤者不需调整剂量。严重肝损伤者的药代动力学资料尚缺乏。
不同程度肾功能减退患者接受加替沙星400 mg后,其表观总清除率(CL/F)降低和AUC增加。中度肾功能减退者(CCR 30~49 ml/min)CL/F降低57%,重度肾功能减退者(CCR<30 ml/min)CL/F降低77%。中、重度肾功能减退者AUC分别增高2倍、4倍。因此CCR<40 ml/min的患者需减量应用加替沙星。
4. 用法用量:(1)每日用量:成人0.4 g/d。每日量1次或分次服用,以1次顿服为佳。肾功能不全时加替沙星需减量。当CCR<30 ml/min时,推荐400 mg/次,每周3次。(2)用药途径:口服或静脉滴注。
5. 不良反应:同氧氟沙星,但对糖代谢的影响更大。可发生严重的低血糖、高血糖、血糖异常或糖尿病。
6. 注意事项:同氧氟沙星。合并糖尿病患者不推荐使用加替沙星。
五、二线口服类抗结核药物
(一)乙硫异烟胺(ethionamide,Eto)
1. 分子式及相对分子质量:C8H10N2S,166.24。
2. 作用机制:本品为异烟酸的衍生物,其作用机制尚不清楚,但可能与抑制肽类的合成或抑制霉菌酸的合成有关。
3. 特点:本品对结核分枝杆菌有抑菌作用,抗菌活性仅为异烟肼的1/10。对渗出性及浸润性干酪病变疗效较好。常与其他抗结核药物联合应用以增强疗效和避免病原菌产生耐药性。氨硫脲常与乙硫异烟胺有部分交叉耐药,耐氨硫脲的结核分枝杆菌常对乙硫异烟胺敏感,但耐乙硫异烟胺时,则很少对氨硫脲敏感。
本品口服后吸收快,生物利用度约为100%。广泛分布于全身组织、体液中,在各种组织中和脑脊液内的药物浓度与同期血药浓度接近。可穿过胎盘进入胎儿血液循环。血浆蛋白结合率约30%。主要在肝内代谢,代谢为亚砜,仍有部分活性;然后生成无活性代谢产物。主要经肾脏排泄,其中1%为原形,5%为活性代谢产物,其余均为失活性代谢产物。T1/2约2~3 h。
4. 用法用量:(1)成人:体质量<50 kg,0.5~0.6 g/d;体质量≥50 kg,0.75~0.8 g/d;不宜超过1 g/d。每日量分2~3次服用,也可1次顿服,睡前或和食物同服。(2)儿童:12~15 mg·kg-1·d-1,不宜超过1 g/d。服用方法同成年人。(3)用药途径:口服。
5. 不良反应:(1)服药后有恶心、呕吐、腹痛、腹泻、厌食、胃部不适等症状,多于服药2~3周后发生;如不能耐受,可酌减剂量或暂停服药,待症状消失后继续服用。如合用碳酸氢钠,或服用肠溶片,可减轻反应。在发生呕吐时,可同时使用止吐药。(2)少数患者有糙皮病症状、精神抑郁、视力紊乱和头痛、末梢神经炎、致畸、经期紊乱、男子乳房女性化、脱发、关节痛、皮疹、痤疮等。
6. 注意事项:(1)不适宜间歇用药。(2)对异烟肼、吡嗪酰胺和烟酸过敏者,可能对本品也过敏。(3)孕妇禁用(致畸性),哺乳期妇女使用本品对乳儿的危害不能排除。(4)20%~30%的患者可对肝功能有影响,引起氨基转移酶升高,并可发生黄疸,故每月应测肝功能1次。(5)大剂量可引起体位性低血压。(6)逐渐增加剂量可减少胃部不适。(7)肾功能衰竭和(或)透析者无需改变剂量。(8)有专家建议所有服用乙硫异烟胺的患者应同时服用维生素B6,但缺乏证据。使用时成人推荐剂量100 mg/d,儿童用药剂量为1~2 mg·kg-1·d-1或10~50 mg/d。
(二)丙硫异烟胺(protionamid,Pto)
1. 分子式及相对分子质量:C9H12N2S,180.28。
2. 作用机制:本品为异烟酸的衍生物,其作用机制尚不清楚,但能抑制霉菌酸的合成。
3. 特点:对结核分枝杆菌有抑菌作用,对结核分枝杆菌的MIC为0.6 μg/ml,能抑制异烟肼在肝内的乙酰化,增加异烟肼的抗结核作用。
治疗各类型的结核病,需与其他抗结核药物联合应用;适用于复治、耐药结核病或用于不能使用其他药品治疗者;适用于非结核分枝杆菌病的治疗。
本品药代动力学同乙硫异烟胺。
4. 用法用量:同乙硫异烟胺。
5. 不良反应:参考乙硫异烟胺,与乙硫异烟胺相比,本品不良反应较轻。(1)发生率较多的不良反应有:精神忧郁(中枢神经系统毒性),同时服用环丝氨酸可能加大神经系统毒性;胃肠道不适和食欲不振,可以通过进食和卧床休息减轻;金属味觉;肝毒性。(2)发生率较少的不良反应有:步态不稳或麻木、针刺感、烧灼感、手足疼痛(周围神经炎)、精神错乱或其他精神改变(中枢神经系统毒性)、巩膜或皮肤黄染(黄疸、肝炎)。(3)发生率极少的不良反应有:视力模糊或视力减退、合并或不合并眼痛(视神经炎)、月经失调或怕冷、性欲减退及乳腺发育(男子)、脱发、皮肤干而粗糙、可逆性甲状腺功能减退(可予甲状腺素替代治疗)、关节疼痛、僵直肿胀。(4)如持续发生以下情况者应予注意:腹泻、唾液增多、流口水、食欲减退、口中金属味、恶心、口痛、胃痛、胃部不适、呕吐(胃肠道紊乱、中枢神经系统毒性)、眩晕(包括从卧位或坐位起身时)、嗜睡、软弱(中枢神经系统毒性)。
6. 注意事项:参考乙硫异烟胺。(1)不适宜间歇用药。(2)慢性肝病患者、精神病患者、孕妇禁用。(3)因胃肠道反应不能接受者,可酌情减量,或从小剂量开始,逐步递增用量。同时采用抗酸药、解痉药等可减轻胃肠道反应。(4)本品亦引起烟酰胺的代谢紊乱,部分患者宜适当补充B族维生素,尤其补充维生素B6、维生素B2。(5)需定期检测肝功能,营养不良者、糖尿病患者和酗酒者需适当缩短检测周期。(6)长期服药者不宜长时间在阳光下曝晒,避免发生光敏反应。
注 乙硫异烟胺和丙硫异烟胺均属于硫胺类药物,两者药效相似,具有完全性交叉耐药性,可视为同一种药,但不良反应以乙硫异烟胺略多。我国仅生产丙硫异烟胺。丙硫异烟胺在耐多药结核病化疗方案中常作为一个基本的组成部分。
丙硫异烟胺(或乙硫异烟胺)与异烟肼有部分的交叉耐药性,一旦耐药则不易恢复敏感性,停药后亦是如此。
考虑到丙硫异烟胺(或乙硫异烟胺)的消化道反应,可从小剂量(300 mg)开始使用,3~5 d后逐渐加大至足量。
(三)环丝氨酸(cycloserine,Cs)
1. 分子式及相对分子质量:C3H6N2O2,105.09。
2. 作用机制:本品系D-丙氨酸类,通过竞争性抑制L-丙氨酸消旋酶和D-丙氨酸-D-丙氨酸合成酶,抑制细菌细胞壁的合成。
3. 特点:对结核分枝杆菌和其他分枝杆菌具有抗菌活性,对结核分枝杆菌的MIC为5~20 μg/ml。主要用于复治、耐药尤其是耐多药和广泛耐药结核病治疗。本品与其他抗结核药物没有交叉耐药,与其他抗结核药物联合应用时可延缓其耐药性的产生。
环丝氨酸口服后吸收快而完全(70%~90%),广泛分布于机体的组织和液体中,如肺、胆汁、腹腔液、胸膜腔液、滑膜液、淋巴液和痰液。有非常好的脑脊液渗透性(脑脊液中的浓度可达到血清浓度的80%~100%,脑膜炎时更高)。能通过胎盘,进入胎儿血液循环。也可经乳汁分泌。本品60%~70%通过肾小球过滤,以原形经尿排出,少量随粪便排泄,少量通过代谢清除。肾功能减退者本品可蓄积。T1/2为10 h,肾功能减退者延长。本品可通过血液透析清除。
4. 用法用量:(1)每日用量:成人15 mg·kg-1·d-1,常用量每日0.5 g,每日量不宜超过1.0 g。推荐体质量<50 kg,0.5 g/d;体质量≥50 kg,0.75 g/d。每日量分2~3次服用,如0.75 g/d分2次使用时,推荐上午0.25 g,晚上0.5 g。儿童用药剂量:10 mg·kg-1·d-1,不宜超过1 g/d。服用方法同成年人。(2)用药途径:口服。
5. 不良反应:(1)常见:神经精神症状,包括头痛、易怒、睡眠障碍、有进攻性,以及震颤、齿龈炎、皮肤苍白、抑郁、意识模糊、眩晕、不安、焦虑、噩梦、严重的头痛和嗜睡。(2)偶见:视觉改变、皮疹、麻木、手脚刺痛或烧灼感、黄疸、眼睛疼痛。(3)罕见:Stevens-Johnson综合征、惊厥、自杀意念。
6. 注意事项:(1)最初2周每12 h口服本品250 mg,然后根据情况小心加量,最大加至每6~8 h口服250 mg,并监测血药浓度。(2)进食:会轻度减少药的吸收(最好空腹服药),70%~90%可被吸收;抗酸剂和橙汁对吸收无显著影响。(3)妊娠或哺乳:安全等级C。哺乳时同时补充婴儿维生素B6。(4)肾脏疾病:严重肾损伤患者要减少环丝氨酸的用量,甚至不用。当CCR低于30 ml/min,建议剂量为250 mg/d;或500 mg/次,每周3次;但上述剂量是否合适尚未确定。(5)仔细监测神经毒性的症状;如有可能,测量血药浓度,调整用药方案。(6)严重焦虑、精神抑郁或精神病者禁用,有癫痫发作史者禁用,酗酒者禁用。(7)与异烟肼或丙硫异烟胺联合应用时,两药均可促进其血药浓度升高,加重中枢神经系统毒性作用,如嗜睡、眩晕、步态不稳。(8)与苯妥英钠联合应用,使后者代谢减慢、毒性作用增强。(9)肾功能不全和(或)透析患者使用剂量可调整为250~500 mg/d,每周3次。(10)成人剂量1 g/d时,建议同时服用维生素B6,每服用250 mg的环丝氨酸可给予50 mg维生素B6。
注 早在利福平问世以前,环丝氨酸就已经是复治化学治疗方案中的主要成分之一。其特点是除本身不易产生耐药性,还可以防止细菌对丙硫异烟胺(或乙硫异烟胺)耐药;但环丝氨酸耐药后的稳定性强,再次使用无效,停药后亦不易恢复敏感性。
(四)特立齐酮(terizidone,Trd)
1. 分子式及相对分子质量:C14H14N4O4,302.29。
2. 特点:本品又名苯环丝氨酸,含有2个分子的环丝氨酸,与环丝氨酸同属吩嗪类衍生物,可替代环丝氨酸。两者的作用机制、药效和不良反应等相似,具完全性交叉耐药。
3. 用法用量:(1)每日用药:成人体质量<50 kg,0.6 g/d;体质量≥50 kg,0.6~0.9 g/d。儿童用量参照环丝氨酸。儿童与成人用药剂量均不宜超过0.9 g/d。每日量分2~3次服用。(2)用药途径:口服。
注 特立齐酮毒性较环丝氨酸低,不良反应较环丝氨酸少。但是,针对肝功能不全及CCR<30 ml/min者,尚无推荐剂量。目前,有关特立齐酮的研究及安全性、有效性的报道较少,有报道血液透析患者普遍能够较好地耐受特立齐酮。
(五)对氨基水杨酸(p-aminosalicylicacid,PAS)
1. 分子式及相对分子质量:C7H6NNaO2·2H2O,211.14。
2. 作用机制:本品的结构类似对氨基苯甲酸,通过对结核分枝杆菌叶酸合成的竞争性抑制作用而抑制结核分枝杆菌的生长繁殖。
3. 特点:对氨基水杨酸对结核分枝杆菌有抑菌作用,对非结核分枝杆菌无效。与异烟肼、链霉素联合应用可加强后两者的抗结核作用。必须与其他抗结核药物配伍应用。与杀菌药联合有延缓耐药产生的作用。适用于复治、耐药结核病。
本品口服吸收良好,较其他水杨酸类吸收快。吸收后迅速分布至肾、肺、肝等组织和各种体液中,在干酪样组织中可达较高浓度,在胸腔积液中也可达到很高浓度,但在脑脊液中的浓度很低(患脑膜炎时有增加)。血浆蛋白结合率低(15%)。T1/2为45~60 min,肾功能损伤者可达23 h。本品在肝中代谢,50%以上经乙酰化成为无活性代谢物。给药量的85%在7~10 h内经肾小球滤过和肾小管分泌迅速排出,14%~33%为原形,50%为代谢物。本品亦可经乳汁分泌。血液透析能否清除本品不明。
4. 用法用量:一般不适宜间歇用药。(1)成人:片剂,体质量<50 kg,8 g/d;体质量≥50 kg,10 g/d。颗粒剂,8 g/d。针剂(对氨基水杨酸钠,PAS-Na),用量参照片剂。不宜超过12 g/d。(2)儿童:200~300 mg·kg-1·d-1。(3)每日量1次顿服或分2~3次服用。(4)用药途径:①口服;②静脉滴注:根据成人或儿童用量,用生理盐水或5%葡萄糖液将本品稀释成3%~4%浓度,避光下滴注,2~3 h完成。
5. 不良反应:(1)胃肠道症状:食欲不振、恶心、呕吐、胃烧灼感、腹上区疼痛、腹胀及腹泻,甚至可致溃疡和出血,饭后服药可减轻反应。(2)肝脏损伤:转氨酶升高、胆汁淤滞、出现黄疸等。(3)过敏反应:皮肤瘙痒、皮疹、剥脱性皮炎、药热及嗜酸粒细胞升高等,应立即停药。(4)肾脏刺激症状:如结晶尿、蛋白尿、管型尿、血尿等。(5)甲状腺功能低下:合用乙硫异烟胺时会增加甲状腺功能低下的风险。(6)罕见不良反应:可逆性甲状腺功能减退(可予甲状腺素替代治疗),与乙硫异烟胺合用时此风险增大;大剂量能抑制凝血酶原的生成,使凝血时间延长。
6. 注意事项:(1)需与其他抗结核药物配伍应用。(2)使用本品需定期做肝、肾功能检查;本品偶可引起低血钾、低血钙、白细胞和粒细胞减少,需定期做血常规和电解质检查。(3)静脉滴注本品时,其药液需新鲜配置并避光保存,变色后不能使用,以避免分解成间位氨基酸引起溶血。(4)本品可干扰利福平的吸收,与之联用时两者给药时间宜相隔6~8 h;本药可降低强心苷的吸收,与之并用时需注意调整后者的剂量。(5)可促使抗凝血药、苯妥英钠作用增强,并用时注意观察是否存在出血征象。(6)与阿司匹林并用,加重肠道刺激,严重时可产生溃疡。(7)不宜长期与丙磺舒、氯化铵、维生素C联合应用。丙磺舒可减慢对氨基水杨酸的排泄,长期服用可提高对氨基水杨酸的血药浓度,并易引起肝功能损伤。氯化铵、维生素C可酸化尿液,长期联用易造成对氨基水杨酸结晶,引起肾损伤。(8)肝、肾功能减退者慎用。(9)发生过敏反应,应立即停药并进行抗过敏治疗。(10)使用颗粒剂时,建议和酸性饮料一起服用。
注 对氨基水杨酸的主要应用价值在于自身能抑制结核分枝杆菌,还可以预防耐异烟肼菌群的产生,是异烟肼的有效联用药。对氨基水杨酸和异烟肼联合应用不但对耐异烟肼菌株可能有效,还可以防止耐药的进一步加剧。可用于从未使用过对氨基水杨酸或对其敏感的耐药结核病患者。
(六)对氨基水杨酸异烟肼(isoniazid aminosalicylate,Pa)
本品化学名称为4-吡啶甲酰肼-4-氨基水杨酸,系异烟肼与对氨基水杨酸的化学合成物。
1. 分子式及相对分子质量:C13H14O4N4,290.27。
2. 作用机制:尚未阐明,可能与抑制敏感细菌分枝菌酸(myolic acid)的合成而使细胞壁破裂有关。参见异烟肼和对氨基水杨酸。
3. 特点:本品在血液中可维持较高、较持久的异烟肼浓度。临床分别服用等量的异烟肼和本品后发现,前者12 h的异烟肼血药浓度仅有0.03 mg/L,本品异烟肼的浓度却有2.6 mg/L;前者14 h的异烟肼血药浓度已为0,本品仍高达2 mg/L,为MIC的2倍。这不仅增强了药物的杀菌作用,同时也延迟了细菌耐药性的产生。临床上可用于对异烟肼敏感的单耐药和多耐药结核病,以及部分耐异烟肼但对对氨基水杨酸-异烟肼仍敏感的耐药结核病。其余参见异烟肼和对氨基水杨酸。
4. 用法用量:(1)成人:10~20 mg·kg-1·d-1;体质量<50 kg,0.8 g/d;体质量≥50 kg,1.0 g/d;不宜超过1.2 g/d。(2)儿童:20~40 mg·kg-1·d-1。(3)每日量一次顿服或分次服用。(4)用药途径:口服。
5. 不良反应:偶有头晕、头痛、失眠、发热、皮疹、恶心、乏力、黄疸、周围神经炎、视神经炎及血细胞减少等不良反应发生。
6. 注意事项:(1)孕妇、哺乳期妇女、肝肾功能不良者和有精神病史、癫痫病史及脑外伤史者慎用。(2)精神病、癫痫患者、严重肝功能障碍患者禁用。(3)治疗过程中出现视神经炎症状,需立即进行眼部检查,并定期复查。(4)抗酸药尤其是氢氧化铝,可抑制本品吸收,不宜同服。(5)本品可加强香豆素类抗凝血药,某些抗癫痫药、降压药、抗胆碱药、三环抗抑郁药的作用,合用时需注意。(6)儿童、老年人用药:未进行该项实验且无可靠参考文献。
六、其他种类抗结核药物
这类药是指疗效和长期安全性不确切的抗结核药物,包括抗结核新药。这类药原则上不用于单耐药和多耐药结核病,只有在耐多药和广泛耐药结核病化学治疗中,当第1~4组抗结核药物不足以组成有效的化学治疗方案时考虑选用。
(一)贝达喹啉(bedaquiline,Bdq;富马酸贝达喹啉)
1. 分子式及相对分子质量:C32H31BrN2O2,555.51。
2. 作用机制:贝达喹啉是一种二芳基喹啉类抗分枝杆菌药,可抑制分枝杆菌ATP(5′-三磷酸腺苷)合成酶,该酶是结核分枝杆菌能量生成所必需的。通过抑制该合成酶质子泵的活性影响结核分枝杆菌的ATP合成,发挥抗菌及杀菌作用。
3. 特点:适用于作为联合治疗的一部分治疗成人耐多药肺结核。本品不适用于治疗潜伏性结核感染、肺外结核病或非耐药结核病。本品应在直接面视督导下治疗。
贝达喹啉的代谢主要以氧化代谢的方式进行,生成N-单去甲基代谢物。N-单去甲基代谢物对临床疗效无显著作用,在人体内其平均暴露量较低,是母药的23%~31%;抗分枝杆菌活性也仅为母药的1/4~1/6。N-单去甲基代谢物浓度似乎与QT延长有关。
4. 用法用量:(1)成人:前2周400 mg/d,1次/d;后22周200 mg/次,每周3次,两次用药之间至少间隔48 h,每周总剂量600 mg;餐时服用;总疗程24周(由于在临床试验中缺乏继续服用>24周的经验,因此更长时间的用药应权衡风险与获益,慎重判断)。(2)儿童剂量暂未确定。(3)如果前2周中服药有遗漏,不需要弥补,而只需完成余下的服药疗程。从第3周开始,若有漏服应尽快补服,然后恢复每周3次的方案。(4)肾功能不全:轻度至中度肾功能不全,不需要调整剂量。严重肾功能不全的用药经验不足,需谨慎使用。
5. 不良反应:(1)常见:胃肠道反应(恶心、呕吐、腹痛、纳差)、关节疼痛、头痛(相对于安慰剂组,使用贝达喹啉组咯血和胸痛更为常见)。(2)少见:QT间期延长、高尿酸血症、磷脂在身体组织中的积累、转氨酶增高、胰腺炎。
6. 药物相互作用:贝达喹啉通过细胞色素P450系统(CYP)中的CYP3A4进行代谢,因此在与CYP3A4诱导剂联用期间,其全身暴露量及治疗作用可能减弱。所以,在本品治疗期间,应避免与全身用药的利福霉素类药(如利福平、利福喷丁和利福布汀)或其他强效CYP3A4诱导剂联用。
将本品与强效CYP3A4抑制剂联用时可能增加贝达喹啉的全身暴露量,从而可能增加发生不良反应的风险。因此,除非药物联用的治疗获益超过风险,应避免将本品与全身用药的强效CYP3A4抑制剂连续联用超过14 d。建议对本品相关的不良反应进行适当的临床监测。
7. 注意事项:(1)在一项安慰剂对照试验中(基于120周访视窗),观察到本品治疗组的死亡风险(9/79,11.4%)较安慰剂治疗组(2/81,2.5%)增加。在24周本品用药期间,发生了1例死亡。无法解释两组间的死亡差异,未观察到死亡与痰培养转阴、复发、其他抗结核药物的敏感性、HIV感染状态、或者疾病严重程度之间存在相关性。(2)QT间期延长:QT间期>500 ms、室性心律失常患者禁用。治疗开始之前及本品治疗开始之后至少2、12和24周时,应进行心电图检查。基线时应检测血清钾、钙和镁,并在异常时进行纠正。若出现QT间期延长,应进行电解质的监测。患者接受本品治疗时,下列情况可增加QT间期延长的风险,因此应密切监测心电图:①尖端扭转型室性心动过速病史;②先天性长QT综合征病史;③甲状腺功能减退和缓慢性心律失常病史;④失代偿性心力衰竭病史;⑤血清钙、镁或钾水平低于正常值下限。(3)当贝达喹啉与延长QT间期其他药共用时,有相加或协同作用(如氯法齐明、氟喹诺酮类药、德拉马尼、噁唑类抗真菌药等)。(4)一旦发生晕厥应立即进行临床评估及心电图检查。(5)肝功能损伤:本品用于轻度或中度肝损伤患者时不需要进行剂量调整。尚未获得在重度肝损伤患者中的药代动力学研究数据,但建议严重肝脏疾病患者禁用。(6)肾功能损伤:肾脏排泄贝达喹啉原形的量很少(<0.001%)。轻度或中度肾损伤的患者用药时不需要进行剂量调整,重度肾损伤或肾病终末期需要血液透析或腹膜透析的患者应谨慎使用。
(二)德拉马尼(delamanid,Dlm)
1. 分子式及相对分子质量:C25H25F3N4O6,534.48。
2. 作用机制:德拉马尼是一种硝基咪唑噁唑类衍生物,其作用的药理机制涉及抑制分枝杆菌细胞壁成分甲氧基分枝菌酸和酮基分枝菌酸的合成。德拉马尼的代谢产物未显示抗分枝杆菌活性。
3. 特点:适用于作为联合治疗的一部分,治疗成人耐多药肺结核。体外试验结果表明,分枝杆菌对德拉马尼产生自然耐药的发生率类似于异烟肼,较利福平高。有文献报道了德拉马尼在治疗期间发生耐药。结核分枝杆菌的辅酶F420相关基因的突变可能是其对德拉马尼产生耐药的机制。已有的研究提示,德拉马尼与目前使用的抗结核药物无交叉耐药性。
餐后口服德拉马尼的生物利用度相比于空腹状态提高了约2.7倍。增加德拉马尼的服用剂量,血药浓度不会因此而成比例增加。德拉马尼与所有血浆蛋白高度结合,总蛋白结合率≥99.5%,T1/2为30~38 h。血浆中德拉马尼的生物转化主要通过白蛋白代谢,通过CYP3A4代谢相对较少。德拉马尼在人体的完整代谢及分布尚未完全阐明。
4. 用法用量:(1)成人:推荐剂量为每次100 mg,2次/d,连续服药24周(由于在临床试验中缺乏继续服用>24周的经验,因此更长时间的用药应权衡风险与获益,慎重判断)。(2)儿童、18岁以下青少年和老年患者(>65岁):安全性和有效性尚不明确。无可用参考数据。(3)餐后服用。(4)用药途径:口服。
5. 不良反应:以下列出的不良反应系德拉马尼临床研究中所见,尚不能完全确定为德拉马尼所特有,其中部分不良反应可能是由背景治疗方案药引起,有待进一步研究考证。(1)心血管系统:心悸、QT间期延长。(2)消化系统:恶心、腹泻、胃痛、食欲下降。(3)神经系统:头痛、感觉异常、震颤、头晕、耳鸣。(4)精神症状:失眠、精神不振。(5)骨骼肌肉:关节或肌肉疼痛。(6)血液系统:网织红细胞增多。(7)代谢异常:低血钾、高尿酸血症。(8)呼吸系统:咯血。
6. 注意事项:具体如下。
1)治疗开始前后的重要检查:治疗前必须进行心电图检查,治疗期间每月应检查一次。如果在德拉马尼首次给药前或治疗期间观察到QT间期>500 ms,则不应给药或停止治疗。如果治疗期间QT间期持续超过450 ms,则应该接受频率更高的心电图监测。同时注意血清电解质的变化,如有异常则及时纠正。
2)心脏危险因素:在有以下风险因素的患者中不得启动德拉马尼治疗,除非经权衡潜在获益大于潜在风险。此类患者在整个德拉马尼治疗期间应该接受高频率的心电图监测。①已知先天性QT间期延长或已知可延长QT间期的任何临床疾病或QTc>500 ms。②症状性心律失常病史或患有临床相关性心动过缓。③任何心律失常的诱因性心脏疾病,例如严重高血压、左心室肥大(包括肥厚型心肌病)或充血性心力衰竭伴随左心室射血分数下降。④电解质紊乱,尤其是低钾血症、低钙血症或低镁血症。⑤正在服用已知可延长QTc间期的药物。包括(但不限于)以下药物:抗心律失常药(如胺碘酮、丙吡胺、多非利特、伊布利特、普鲁卡因胺、奎尼丁、氢化奎尼丁、索他洛尔);抗精神病药(如吩噻嗪、舍吲哚、舒托必利、氯丙嗪、氟哌啶醇、美索达嗪、匹莫齐特或硫利达嗪);抗抑郁药;某些抗生素,包括大环内酯类(如红霉素、克拉霉素)、氟喹诺酮类(莫西沙星、司帕沙星)、三唑类抗真菌药、喷他脒和沙奎那韦等;某些非镇静性抗组胺药(特非那定、阿司咪唑、咪唑斯汀);其他药包括西沙必利、氟哌利多、多潘立酮、苄普地尔、二苯马尼、普罗布考、左美沙醇、美沙酮、长春碱类和三氧化二砷。⑥低白蛋白血症:在一项临床研究中,接受德拉马尼治疗的患者中低白蛋白血症的存在可增加QTc间期延长的风险。因此,在服药前以及服药期间,应定期进行心电图、电解质及血清白蛋白检查,出现异常时应给予适当处置。⑦与CYP3A强抑制剂联合使用:德拉马尼与CYP3A强抑制剂(洛匹那韦-利托那韦)联合使用导致代谢产物DM-6705的暴露量增加30%,而该代谢产物暴露量的增加会导致QT间期延长。因此,如果认为必须要将德拉马尼与任何CYP3A强抑制剂联合使用,则建议在整个德拉马尼治疗期间对患者进行高频率的心电图监测。⑧与氟喹诺酮类联合使用:所有延长超过60 ms的QT间期都与氟喹诺酮合并用药有关。因此,如果为了组成适当的耐多药结核病治疗方案而不可避免地需要联合使用这两类药(不推荐使用莫西沙星),则建议在整个德拉马尼治疗期间对患者进行高频率的心电图监测。
3)肝功能异常:在中度至重度肝功能异常患者中不建议使用德拉马尼。
4)肾功能异常:从尿液回收的德拉马尼不足口服剂量的5%。轻度肾功能异常(50 ml/min 5)HIV感染:目前,在接受抗HIV治疗的MDR-TB患者中尚无德拉马尼应用经验。然而,在健康成人中开展的德拉马尼与3种主要抗逆转录病毒药(替诺福韦、洛匹那韦利托那韦,以及依非韦伦)联合应用的研究显示,抗病毒药的暴露量均未受影响;德拉马尼的暴露量在与替诺福韦、依非韦伦联合应用后没有变化,与洛匹那韦利托那韦联合应用后略有增加。 6)妊娠:德拉马尼在妊娠女性中的应用数据极其有限。动物研究显示德拉马尼具有生殖毒性,不建议妊娠女性或育龄期女性使用德拉马尼,除非采取可靠的避孕措施。 7)哺乳:尚不明确德拉马尼或其代谢产物是否会在人类乳汁中分布。动物试验中的已有药代动力学数据表明德拉马尼和(或)其代谢产物可在乳汁中分布。由于不能排除其对母乳喂养婴幼儿的潜在风险,因此不建议在德拉马尼治疗期间进行母乳喂养。 8)生育能力:德拉马尼对雄性和雌性动物的生育能力无影响,但缺乏德拉马尼对人类生育能力影响方面的临床数据。 9)对驾驶和机械使用的影响:尚未研究对驾驶和机械使用能力的影响。然而,如果患者出现任何可能会影响驾驶或机械使用能力的不良反应(例如头痛和震颤很常见),则建议患者在治疗期间不要驾驶或操作机械。 (三)利奈唑胺(linezolid,Lzd) 1. 分子式及相对分子质量:C16H20FN304,337.35。 2. 作用机制:本品为合成的抗革兰阳性杆菌药物,其作用为抑制细菌蛋白质合成,特点是与细菌核糖体50S亚单位结合,抑制mRNA与核糖体连接,阻止70S起始复合物的形成,从而抑制细菌蛋白质的合成。 3. 特点:本品结构特殊,与其他抗生素无交叉耐药性,特别对耐甲氧西林金葡球菌(MRSA)、耐万古霉素肠球菌(VREF)等微生物有良好的抗菌作用,为治疗耐万古霉素肠球菌感染的惟一药物。利奈唑胺对支原体属和衣原体属、结核分枝杆菌、鸟分枝杆菌亦有一定抑制作用。已有研究提示,利奈唑胺治疗耐多药和(或)广泛耐药结核病取得了比较好的临床效果,但尚需更多的观察。 本品口服吸收快速且完全,生物利用度100%。为时间依赖性抗生素。在体内广泛分布于血液灌注良好的组织,脑脊液浓度为血药浓度的1/3(已用来治疗脑膜炎)。血浆蛋白结合率为31%。在体内氧化生成2个失活代谢产物:氨基乙氧乙酸(A)和羟乙基氨基乙酸(B)。非肾清除率约占利奈唑胺总清除率的65%。稳态时,有30%的药物以原形药物、40%以代谢产物B 的形式、10%以代谢产物A 的形式随尿排泄。利奈唑胺的肾脏清除率低[表观清除率(CL/F)与肾脏清除率(CLr)分别为120 ml/min和40 ml/min],提示有肾小管重吸收。大约有6%和3%的药物分别以代谢产物B 和A 的形式经粪便排出。消除T1/2为4.5~5.5 h。 4. 用法用量:(1)成人:300~600 mg/d,不宜超过600 mg/d。(2)儿童;10 mg·kg-1·次-1,每8 h一次,不宜超过600 mg/d。(3)用药途径:口服或静脉点滴。 5. 不良反应:主要不良反应有腹泻、头痛、恶心。另外,还有口腔念珠菌、阴道念珠菌感染,低血压,消化不良,局部腹痛,瘙痒、舌变色及骨髓抑制,多发神经炎,精神改变等。 6. 注意事项:(1)对本品过敏者禁用;孕妇与哺乳期妇女慎用。(2)口服用药时如有胃部不适,与食物一起服用。(3)本品可能引起血小板减少症,对于易出血者、有血小板减少症、与有减少血小板药物同服或使用本品超过2周的患者,均应监测血小板计数。(4)本品可引起伪膜性结肠炎。(5)本品具有单胺氧化酶抑制剂的作用,如与肾上腺素能药物同服,可引起可逆性血压增高;如与5-羟色胺神经药联合应用,应注意发生5-羟色胺综合征。但本品与华法林、苯妥英、氨曲南、庆大霉素、右美沙芬无相互作用。 (四)氯法齐明(氯苯吩嗪,clofazimine,Cfz) 1. 分子式及相对分子质量:C27H22C12N4,473.40。 2. 作用机制:本品抗菌作用可能通过干扰麻风杆菌的核酸代谢,与其DNA结合,抑制依赖DNA的RNA聚合酶,阻止RNA的合成,从而抑制细菌蛋白的合成,发挥其抗菌作用。 3. 特点:本品可进入巨噬细胞,不仅对麻风分枝杆菌有缓慢杀菌作用,与其他抗分枝杆菌药物合用对结核分枝杆菌及溃疡分枝杆菌等部分非结核分枝杆菌亦有效。在体外具有抗结核活性,而体内活性数据不多。 口服吸收率为45%~62%,个体差异大,与食物同服可增加其吸收。本品具有高亲脂性,主要沉积于脂肪组织和单核-吞噬细胞系统内,被全身的巨噬细胞摄取,其组织浓度高于血浆浓度。组织半衰期约70 d。大多数药物经粪便、胆汁排泄,少量由尿液、痰液、皮脂、汗液排泄,乳汁中也含有药物。 4. 用法用量:(1)成人:最初2个月200~300 mg/d,以后100 mg/d。(2)儿童:资料有限。(3)每日量1次或分次服用。(4)用药途径:口服。 5. 不良反应:(1)光敏反应、皮肤黏膜着色为其主要不良反应。服药2周后即可出现皮肤和黏膜红染,呈粉红色、棕色,甚至黑色。着色程度与剂量、疗程成正比。停药2个月后色素逐渐减退,约1~2 年才能褪完。本品可使尿液、汗液、乳汁、精液和唾液呈淡红色,且可通过胎盘使胎儿着色,但未有致畸报道。应注意个别患者因皮肤着色反应而导致抑郁症,曾有报道,个别患者继皮肤色素减退后,因精神抑郁而自杀。(2)用本品治疗后,约70%~80%的患者皮肤有鱼鳞病样改变,尤以四肢和冬季为主。停药后2~3个月可好转。(3)本品可致食欲减退、恶心、呕吐、腹痛、腹泻等胃肠道反应。(4)个别患者可产生眩晕、嗜睡、肝炎、上消化道出血、皮肤瘙痒等。(5)个别患者可产生皮肤色素减退、阿-斯综合征(Adams-Stokes综合征)。 6. 注意事项:(1)对本品过敏者禁用,有胃肠疾患史或肝功能损伤及对本品不能耐受者慎用。(2)应与食物或牛奶同时服用。(3)每日剂量超过100 mg时应严密观察,疗程应尽可能短。(4)对诊断干扰方面,要注意可致血红细胞沉降率加快,以及血糖、血白蛋白、血清氨基转移酶、胆红素升高,血钾降低。(5)用药期间,患者出现腹部绞痛、恶心、呕吐、腹泻时应减量、延长给药间期或停药。偶有服药期间发生脾梗死、肠梗阻或消化道出血而需进行剖腹探查者。因此,应高度注意服药期间出现急腹症症状者。(6)本品能透过胎盘并进入乳汁,使新生儿和哺乳儿皮肤染色。孕妇避免应用本品,哺乳期妇女不宜应用本品。 (五)阿莫西林-克拉维酸钾(amoxicillin and clavulanate potassium,Amx-Clv) 1. 分子式及相对分子质量:阿莫西林,C16H19N3O5S·3H2O,419.46;克拉维酸钾,C8H8KNO5,237.25。 2. 作用机制:对抗结核分枝杆菌所产生的β-内酰胺酶。 3. 特点:本品为阿莫西林和克拉维酸的复方制剂。阿莫西林为广谱青霉素类抗生素,克拉维酸本身只有微弱的抗菌活性,但具有强大的广谱β内酰胺酶抑制作用,两者合用,可保护阿莫西林免遭β内酰胺酶水解,并可扩大其抗菌谱。本品适用于敏感菌引起的各种感染,但因不能进入哺乳动物的细胞内而影响了抗结核效果。 阿莫西林与克拉维酸配伍后对各自的药代动力学参数无显著影响。药物对胃酸稳定,口服后阿莫西林和克拉维酸均吸收良好,食物对两者吸收的影响不显著。本品在多数组织和体液中分布良好,但血-脑屏障通透性差。阿莫西林和克拉维酸的血浆蛋白结合率分别为18%和25%。阿莫西林和克拉维酸均可被血液透析清除。 4. 用法用量:(1)剂型与剂量。WHO推荐“7/1”和“8/1”的剂型。成人80 mg·kg-1·d-1,或2600~3000 mg/d,分2次给药。中国因产地不同,剂量和剂型不尽相同,注意严格参照说明书执行。(2)剂型有三种。阿莫西林-克拉维酸钾片:875 mg/125 mg、500 mg/125 mg、500 mg/62.5 mg、250 mg/125 mg;阿莫西林-克拉维酸钾口服混悬液(5 ml):400 mg/57 mg、500 mg/62.5 mg;阿莫西林-克拉维酸钾针剂:1000 mg/200 mg。(3)用药途径可以为口服、静脉注射或静脉滴注。 5. 不良反应:(1)常见胃肠道反应如腹泻、恶心和呕吐等。(2)皮疹,尤其易发生于传染性单核细胞增多症者。(3)可见过敏性休克、药物热、哮喘、骨髓抑制、多发神经炎等。(4)偶见血清氨基转移酶升高、嗜酸粒细胞增多、白细胞降低,以及念珠菌或耐药菌引起的二重感染。 6. 注意事项:(1)青霉素皮试阳性反应者、对本品和其他青霉素类药物过敏者及传染性单核细胞增多症患者禁用。患者每次开始服用本品前,必须先进行青霉素皮试。(2)对头孢菌素类药物过敏者及有哮喘、湿疹、枯草热、荨麻疹等过敏性疾病史和严重肝功能障碍者慎用。(3)本品与其他青霉素类和头孢菌素类药物之间有交叉过敏性。若有过敏反应产生,则应立即停用本品,并采取相应措施。(4)阿莫西林经肾脏代谢,当肾功能衰竭时应调整剂量。CCR>30 ml/min时不需减量;CCR 10~30 ml/min者每12小时用阿莫西林250~500 mg;CCR<10 ml/min 者阿莫西林每24小时用250~500 mg。(5)血液透析患者:根据病情轻重,每24小时用阿莫西林250~500 mg。血液透析可影响本品中阿莫西林的血药浓度,因此在血液透析过程中及结束时各加用一次剂量。(6)本品可通过胎盘,脐带血中浓度为母体血药浓度的1/4~1/3,故孕妇禁用。本品可分泌入母乳中,可能使婴儿致敏并引起腹泻、皮疹、念球菌属感染等,故哺乳期妇女慎用或用药期间暂停哺乳。(7)由于本品在胃肠道的吸收不受食物影响,故可在餐时或餐后服用以减少胃肠道反应。 (六)亚胺培南-西司他丁(imipenem-cilastatin,Ipm-Cln) 1. 分子式及相对分子质量:亚胺培南,C12H17N304S·H2O,317.36;西司他丁, C16H25N2O5SNa,380.40。 2. 作用机制:亚胺培南可与多种青霉素结合蛋白(PBPs),尤其是PBP1a、PBP1b和PBP2结合,抑制细菌细胞壁合成,导致其细胞溶解和死亡。 3. 特点:亚胺培南为碳氢霉素类抗生素,既有极强的广谱抗菌活性,又有β-内酰胺酶抑制作用。本品具有第一代头孢菌素强大的抗革兰阳性菌的作用特点,又具有第三代头孢菌素对革兰阴性杆菌产生的广谱内酰胺酶的高度稳定性,对革兰阴性杆菌,包括耐药革兰阴性杆菌有极强的抗菌活性,极易对β-内酰胺类抗生素产生耐药性的绿脓杆菌、金黄色葡萄球菌、粪链球菌、脆弱拟杆菌等,对本品也高度敏感。 亚胺培南在胃酸中不稳定,因此不能口服给药。临床应用亚胺培南与西司他丁为1∶1复合制剂,与西司他丁合用时亚胺培南的AUC可增加5%~36%。亚胺培南在人体内分布广泛,在肺组织、痰液、渗出液、女性生殖系统、胆汁、皮肤等组织和体液中可达到对多数敏感菌的有效治疗浓度。亚胺培南血浆蛋白结合率约为20%,西司他丁约为40%,两者的T1/2均为1 h。其代谢产物主要经尿液排出,血液透析可清除亚胺培南与西司他丁。 4. 用法用量:(1)成人体质量<50 kg,1500 mg/d;体质量≥50 kg,2000 mg/d,不宜超过4000 mg/d。WHO推荐每日剂量为2000 mg亚胺培南/2000 mg西司他丁。使用时因产地不同,剂量和剂型不尽相同,注意严格参照说明书执行。(2)儿童剂量为60 mg·kg-1·d-1,不宜超过2000 mg/d。(3)成人肾功能不全CCR为20~40 ml/min时,剂量为750 mg/12 h;CCR<20 ml/min时,剂量为500 mg/12 h。(4)每日量分2~3次使用。(5)用药途径可以是静脉滴注或肌内注射。每500 mg本品静脉滴注时间应>15~30 min;肌内注射时本品500 mg以1%利多卡因2 ml稀释,750 mg以3 ml稀释,混匀后注射。 5. 不良反应:(1)常见者有腹泻、恶心、呕吐。Less common: Seizure (noted with CNS infection), palpitations,(2)不常见者有癫痫发作(合并中枢神经系统感染),儿童脑膜炎使用亚胺培南引起癫痫风险较大(对于脑膜炎及儿童推荐使用美罗培南),心悸,pseudomembranous colitis.伪膜性结肠炎。 6. 注意事项:(1)妊娠和(或)哺乳情况下,临床应用资料较少。(2)肾脏疾病时,CCR20~40 ml/min,每12小时750 mg;CCR<20 ml/min,每12小时500 mg。不推荐本品用于体质量<30 kg的肾功能不全儿童患者。(3)肝脏疾病时,有报道约6%的患者有转氨酶增高。(4)不能耐受碳青霉烯类者禁用。(5)我国缺乏亚胺培南-西司他丁治疗耐多药和广泛耐药结核病的临床经验和资料。 (七)美罗培南(美洛培南,meropenem,Mpm) 1. 分子式及相对分子质量:C17H25N3O5S·3H2O,437.51。 2. 作用机制:美罗培南是碳青霉烯β-内酰胺类抗生素,其作用机制与用法与亚胺培南相似,通过抑制细菌细胞壁的合成而产生抗菌作用,美罗培南容易穿透大多数革兰阳性和阴性细菌的细胞壁,而达到其作用靶点青霉素结合蛋白(PBPS)。除金属β-内酰胺酶以外,其对大多数β-内酰胺酶(包括由革兰阳性菌及革兰阴性菌所产生的青霉素酶和头孢菌素酶)的水解作用具有较强的稳定性。 3. 特点:美罗培南不宜用于治疗对甲氧西林耐药的葡萄球菌感染,有时对其他碳青霉烯类的耐药菌株亦表现出交叉耐药性。体外试验显示,对一些绿脓杆菌的分离菌株,美罗培南与氨基糖苷类抗生素合用可产生协同作用。与亚胺培南比较,它对肾脱氢肽水解酶Ⅰ更稳定,不需要与酶抑制剂如西司他丁合用,用于治疗敏感菌所致感染。 本品在大多数组织和体液中分布良好,在痰、肺组织、胆管、腹腔渗出液、尿液、女性生殖系统和皮肤、软组织中可达到或超过抑制大多数敏感菌所需浓度。正常脑脊液中浓度较低,但脑膜有炎症时脑脊液药物浓度提高。血浆蛋白结合率约2%。主要通过肾小管分泌和肾小球滤过从尿中排泄,经过12 h的代谢,约有70%的药物以原形从尿中排泄。血浆清除半衰期为1 h,肾有损伤者,半衰期会延长,儿童半衰期会轻微延长。 4. 用法用量:(1)成人:常用剂量为500~1000 mg,每8 小时1次。WHO推荐1000 mg/d,3次/d;或2000 mg/d,2次/d。(2)儿童:小于3个月龄和体质量不足50 kg的儿童给药10~20 mg/kg,每8 小时1次;脑膜炎患儿可增至40 mg/kg,每8 小时1次。(3)肾功能不全:肾损伤的患者需要减少美罗培南的用量,根据CCR调整。①CCR 26~50 ml/min:每12 小时给1次常用量;②CCR 10~25 ml/min:每12小时给半剂用量;③CCR<10 ml/min:每24 小时给半剂用量。(4)缓慢注射给药,每次需3~5 min以上,静脉滴注需要15~30 min以上。 5. 不良反应:参见亚胺培南。(1)过敏反应:主要有皮疹、瘙痒、药物热等过敏反应;偶见过敏性休克。(2)消化系统:主要有腹泻、恶心、呕吐、便秘、味觉异常、牙舌变色等症状。可发生非敏感菌(如粪肠球菌、获得性耐药铜绿假单胞菌、真菌)的二重感染。可能导致轻微至危及生命的伪膜性结肠炎。对使用美罗培南后引起腹泻或腹痛加剧的患者,应确诊其是否为艰难梭菌引起的伪膜性结肠炎。(3)肝脏:偶见肝功能异常、胆汁淤积性黄疸等。(4)肾脏:偶见排尿困难和急性肾功能衰竭。(5)中枢神经系统:偶见失眠、焦虑、意识模糊、眩晕、神经过敏、感觉异常、幻觉、抑郁、痉挛、意识障碍等中枢神经系统症状,与亚胺培南比较不容易引起癫痫。(6)血液系统:偶见胃肠道出血、鼻出血和腹腔积血等出血症状,偶可出现抗人球蛋白试验(Coomb试验)阳性。(7)注射给药时可致局部疼痛、红肿、硬结,严重者可致血栓性静脉炎。 6. 注意事项:(1)对碳氢霉烯类抗生素、青霉素类或其他β-内酰胺类抗生素过敏感染患者慎用。(2)对肾功能不全患者不必要进行剂量调整,应认真监测患者的肾功能。(3)本品不推荐用于耐甲氧西林葡萄球菌引起的感染。(4)我国缺乏美罗培南治疗耐多药和广泛耐药结核病的临床经验和资料。 (八)氨硫脲(thioacetazone,Thz) 1. 分子式及相对分子质量:C10H12N4OS,236.29。 2. 作用机制:本品对结核分枝杆菌具有抑菌作用,可能与本药阻碍分枝杆菌核酸合成,以及与铜生成一种活性复合物有关。对麻风分枝杆菌亦有作用。 3. 特点:本品为抗结核药物,对结核分枝杆菌的MIC为1 mg/L。其抗结核作用逊于对氨基水杨酸,在碱性液中作用稍强。结核分枝杆菌接触氨硫脲后无延缓生长期现象发生,故氨硫脲不能用于间歇疗法。单用本药4~6个月约有30%的结核分枝杆菌菌株可对本品产生耐药。由于其耐药稳定性好,发生耐药后少见有复敏现象,不能再次使用。与乙硫异烟胺或丙硫异烟胺有单向交叉耐药性,即耐本药者对乙硫异烟胺或丙硫异烟胺仍敏感,而耐乙硫异烟胺或丙硫异烟胺时则对本药不再敏感,发生后一种情况时不应再使用氨硫脲。 本品口服后吸收良好,消除半衰期约为12 h,约20%以原形随尿排出。肾功能衰竭者本品可在体内蓄积。 4. 用法用量:(1)成人剂量,体质量<50 kg,100 mg/d;体质量≥50 kg,150 mg/d,不宜超过150 mg/d。(2)儿童剂量为5 mg·kg-1·d-1;体质量<10 kg,25 mg/d;10~20 kg,50 mg/d;20~40 kg,100 mg/d。(3)每日量分2~3次服用。(4)用药途径为口服。 5. 不良反应:氨硫脲的不良反应与剂量有关,如剂量>100 mg/d,不良反应发生率为68%;<100 mg/d,不良反应发生率为 26%。(1)消化道症状:恶心、呕吐及腹泻等胃肠道反应最多见。(2)肝毒性:可发生伴有黄疸的严重肝损伤,偶可致死;多见于同时接受异烟肼治疗患者。(3)血液系统:表现为粒细胞减少、血小板减少等骨髓抑制现象;也可发生溶血性贫血。(4)耳毒性:可出现头晕、眩晕、共济失调、耳鸣、听力下降。(5)过敏反应:可出现皮疹,偶见剥脱性皮炎或 Stevens-Johnson综合征(多形糜烂性红斑,见于皮肤、口、鼻黏膜和眼结膜)。(6)肾脏损伤:尿中出现蛋白、管型、红细胞,以及血尿素氮升高。 6. 注意事项:(1)成人最初25~50 mg/d,以后渐增至100~150 mg/d。(2)氨硫脲可引起严重的药物性皮炎,尤其在HIV阳性患者中常见,甚至可引起Stevens-Johnson综合征及死亡,建议避免用于结核病合并HIV感染和(或)AIDS患者。(3)不宜与链霉素合用,因其可加重对前庭的毒性作用。(4)不宜与氨基比林、氯霉素等同时使用,以防增加造血系统毒性。(5)加用小量硫酸铜能增加疗效。(6)对本品过敏、肝肾功能不全、糖尿病及贫血患者禁用。(7)我国缺乏氨硫脲治疗耐多药和广泛耐药结核病的临床经验和资料。 (九)克拉霉素(clarithromycin,Clr) 1. 分子式及相对分子质量:C38H69NO13,747.96。 2. 作用机制:本药属大环内酯类抗生素,其机制是通过阻碍细胞核蛋白50S亚基的联结,抑制蛋白质的合成而产生抑菌作用。对非结核分枝杆菌有较强的抗菌活性,特别是鸟-胞内分枝杆菌复合体,但对某些分离株仅在体外具有活性。对人体结核病的治疗价值尚未证实。部分体外试验的数据并不乐观,结果提示结核分枝杆菌对大环内酯类耐药,其特性表现为erm基因的表达。 3. 特点:对革兰阳性菌及部分革兰阴性菌有抑制作用。对鸟分枝杆菌和其他分枝杆菌均具一定活性。在结核病灶巨噬细胞内克拉霉素能达到较高浓度。与多种抗结核药物有协同作用,如异烟肼和利福平。 本品对胃酸较稳定,口服后经胃肠道迅速吸收,生物利用度为55%。食物可稍延缓克拉霉素的吸收,但不影响生物利用度。体内分布广泛,肺组织中的药物浓度比血浓度高。在血浆中,蛋白结合率为65%~75%,消除半衰期为4.5~4.8 h,主要经粪便及尿液排泄。轻度肾功能不全者、或老年人、或轻度至中度肝功能不全者无需调整用药剂量。 4. 用法用量:(1)成人剂量,体质量<50 kg,500~750 mg/d;体质量≥50 kg,750~1000 mg/d,不宜超过1000 mg/d。(2)儿童剂量为7.5 mg·kg-1·次-1。(3)每日量分1~2次服用。(4)本品经肝肾双通道代谢,对于严重肾功能不全者,给药间隔应延长,如500 mg/d,隔日使用。(5)用药途径为口服。 5. 不良反应:(1)胃肠道反应有食欲降低、恶心呕吐、腹泻,长期大量应用可致肠菌群失调,产生伪膜性肠炎等。(2)肝功能损伤,偶可见ALT、AST、胆红素升高。(3)血液检测可见白细胞减少、血小板减少、凝血酶原时间延长等。(4)听力损伤、耳鸣、平衡失调或眩晕。 6. 注意事项:(1)动物实验中该品对胚胎及胎儿有毒性作用,同时该品及其代谢产物可进入母乳中,故孕妇及哺乳期妇女禁用或停止哺乳。(2)12岁以下儿童应用本品需谨慎,因为对儿童的安全试验指标还没有完全确定。(3)肝、肾功能不全者需慎用。严重肾功能不全者应减少使用剂量,CCR低于30 ml/min者剂量减半。(4)不能和贝达喹啉、西沙必利、匹莫齐特、阿司咪唑、特非那定、麦角胺及二氢麦角胺合用。(5)本品可抑制茶碱的正常代谢,故不宜和茶碱类药物合用,以防茶碱浓度升高而引起中毒、甚至死亡。必须使用时应到医院进行茶碱血药浓度监测,以防意外。(6)已知对大环内酯类抗生素过敏时禁用。 七、抗结核药物使用的基本方法 抗结核药物的使用略有别于其他抗生素,使用不当,不但影响耐药结核病治疗的效果,而且可能导致新的耐药发生。 以下方法将有助于耐药结核病化学治疗中抗结核药物的合理使用。 (一)5项基本原则 坚持并强化结核病化学治疗的5项基本原则。结核病的化学治疗强调早期、联合、适量、规律和全程用药,耐药结核病的化学治疗不仅要坚持这5项基本原则,而且需要根据耐药结核病的特点加以适当调整,尤其重点强调以下3点。 1. 早期:明确诊断及时用药,不仅有利于耐药结核病患者自身的早日康复,更大的意义还在于及时控制耐药结核分枝杆菌的进一步传播,有效降低其对家庭和社会的危害。 2. 联合:WHO一直推荐抗结核药物的联合治疗,利用多种抗结核药物的交叉杀菌作用,提高杀菌、灭菌能力,防止产生耐药性。联合多种抗结核药物组成有效的抗结核化学治疗方案是耐药结核病化学治疗的核心,药物联合的效果至少应该是相加,能达到协同则更佳,而非拮抗。由于部分耐药结核病患者同时合并有其他疾病而需要使用其他药物,因此也应注意抗结核药物与其他药物的相互作用,避免药物不良反应的加剧或药效降低。详见表7。 表7 抗结核药物与其他药的相互作用 续表7 注 表中列举了抗结核药物与一些常见药物的相互作用;联合用药栏中分A、B两栏,即A药与B药同时并用(包括同时或先后,通过相同途径或不同途径给予A、B 2种或2类药)。相互作用栏包括合用后药物作用(包括疗效和不良反应)所起的变化。本栏说明后附有括号,其中的罗马数字表示所发生的相互作用类型:Ⅰ.促进胃肠蠕动引起的相互作用;Ⅱ.减弱胃肠蠕动引起的直接相互作用;Ⅲ.竞争血浆蛋白;Ⅳ.酶抑作用;Ⅴ.酶促作用;Ⅵ.尿液pH值改变而引起药物重吸收的变化;Ⅶ.竞争排泄;Ⅷ.协同或相加;Ⅸ.拮抗;此外,尚有一些不属于以上9类或作用机制不够明确的相互作用(相互作用栏亦包括了对相互作用提出处理意见的内容)。 本表内容引自:《中国国家处方集》编委会.中国国家处方集(化学药品与生物制品卷).北京:人民军医出版社,2010:905-977. 3. 适量:耐药结核病的化学治疗能否取得成功,在很大程度上取决于药物剂量是否到位,不分年龄、不按千克体质量、不考虑患者既往肝肾功能等基本情况,固定一种剂量的做法是不可取的。而且还要对每一种药物都要有深刻的了解。以氟喹诺酮类药物为例,氧氟沙星的最大剂量可用到800 mg/d,左氧氟沙星的疗效是氧氟沙星的2倍,但不应机械地根据它们的杀菌活性将左氧氟沙星的剂量换算成400 mg/d,而应该根据患者的千克体质量,上限可用到750 mg/d,以最大限度地发挥左氧氟沙星的抗结核作用。 对于某些低浓度耐药、高浓度敏感的抗结核药物,可以通过适当提高用药剂量来解决耐药问题,例如采用高剂量异烟肼16~20 mg·kg-1·d-1治疗耐多药结核病。其他的抗结核药物是否也存在使用高剂量的可行性(如利福喷丁),值得进一步探索。 (二)用药方法 1. 两阶段用药法:两阶段用药法是根据实践经验和科学实验中发现的事实而提出的,是一种将化疗全程分为强化期和继续期2个治疗阶段的用药方法,又称之为二步治疗。两阶段用药法的理论基础是在强化期要抓住结核分枝杆菌大量繁殖、药物最能发挥杀菌效能的有利时机,采取强有力的化疗方案,尽快地杀死繁殖期菌群,使菌量急剧减少,缩短传染期,防止或减少继发性耐药菌的产生,杀灭可能存在的原发耐药菌及自然突变耐药菌。继续期则主要针对病灶内仍残留的少数代谢低下或半静止状态的结核分枝杆菌,这部分细菌相对比较顽固,因此该期的化学治疗所需时间长于强化期。 耐药结核病尤其是耐多药结核病的化学治疗在上述基础上明显延长了强化期和继续期,并在强化期全程使用注射类抗结核药物。注射剂的使用及整个疗程的延长,使得耐药结核病的化学治疗在疗程的2个阶段中得到了进一步加强。 2. 每日用药与间歇疗法:抗生素后效应(post antibiotic effect,PAE)和药物作用后所产生的细菌延缓生长期是抗结核药物间歇疗法的理论基础。间歇疗法在药物使用上的一个特点就是每次用药剂量要大于每日用药的每次剂量,鉴于用于耐药尤其是耐多药结核病化学治疗以二线抗结核药物为主体,不良反应往往大于一线抗结核药物。因此,原则上不推荐在耐药结核病的化学治疗过程中采用间歇疗法,而建议每日用药,注射用药是个例外。当患者不能接受每日注射用药时,可采用间歇用药,但不同于间歇疗法,每次用药量并不增加。 3. 顿服与分次服用:绝大多数口服抗结核药物为浓度依赖型药物,应采用顿服法,其注射类抗结核药物也往往是这样,强调一日量一次注入,以求达到最佳的杀菌血药浓度。但是,第5组抗结核药物中的一部分属于时间依赖型药物,例如阿莫西林-克拉维酸钾和克拉霉素等,则以一日量分次使用为佳。当然,对于消化道反应严重者,即便是浓度依赖型药物也可以采用分次服用的方法,以提高耐药结核病患者的依从性。 4. 阶梯增量用药:部分耐药结核病患者对某些抗结核药物有严重的消化道反应,有发生中断用药的风险。例如丙硫异烟胺,可考虑从小剂量开始逐步加量使用,以提高患者消化道对药物的耐受性。 (三)用药剂量 掌握好抗结核药物使用的常规剂量,不仅有助于提高耐药结核病的治愈率,还有可能减少新的耐药和不良反应的发生。不允许忽视患者的年龄、体质量和个体依从性而盲目地、无差别地采用固定剂量,典型案例非利福平莫属。为了方便临床用药,中国以利福平药品说明书为依据,按照患者的体质量分为<50 kg和≥50 kg 2种用药剂量类型,前者利福平用量为0.45 g/d,后者0.6 g/d。但是,临床上无论体质量多少一律使用0.45 g/d的现象时有发生。对于体质量≥50 kg的患者意味着低剂量用药,长此下去势必增加发生对利福平耐药的风险。反之,<50 kg体质量的患者长期使用0.6 g/d的剂量,则有发生利福平不良反应的可能,伤害患者的重要脏器,尤其是肝脏,甚至因不良反应停用利福平或致利福平的不规律使用,进而直接影响治疗效果,也为日后对利福平的耐药埋下伏笔。 抗结核药物的产地不同,其用药剂量也可能存在差异。根据中国权威部门参照WHO指南进行的设计,耐多药结核病患者可以接受国外进口阿米卡星的常规剂量分别为0.5~0.75 g/d(<50 kg)和1 g(≥50 kg),和国产阿米卡星的常规剂量0.4 g/d(<50 kg)和0.6 g/d(≥50 kg)有较大的差距,但至今尚未看到这2种剂量的药物不良反应发生率有何差异。 本指南不推荐在未获得可靠研究结果前,国产阿米卡星套用进口阿米卡星的使用剂量,使用时应重点参考原产地的药品说明书。 本指南推荐的成年人耐药结核病化学治疗药物常用剂量见表8。 表8 成年人耐药结核病化学治疗药物常用剂量和用法表a 注a:儿童、老年人和其他特殊人群的用药剂量和用法请参考本指南各组抗结核药物的介绍和药品说明书;b:使用高剂量异烟肼时,可按体质量每日16~20 mg/kg计算;c:每周使用次数;d:WHO推荐的常规用量高于本表,见“注射类抗结核药物”;e:WHO推荐的常规用量高于本表,见“氟喹诺酮类药”;f:缺乏继续服用>24周的经验;g:按WHO推荐的“7/1”和“8/1”比例计算每日剂量;h:WHO推荐每日剂量为2000 mg亚胺培南/2000 mg西司他丁 肾脏是药物排泄的主要通道之一,在患者肾功能不全的情况下,掌握好每一种用于耐药结核病化学治疗药物的使用剂量和方法是防范药物加剧肾功能不全的有效手段。详见表9。 八、常见药物不良反应与处理 耐药结核病的化学治疗需要多种药物联合使用,药物不良反应繁多且较难预测,尤其是二线抗结核药物,常常导致患者的依从性差、治疗中断或治疗失败,甚至促使耐药加剧。因此,在抗结核治疗之前,医生应熟悉耐药结核病化疗方案中所选药的适应证、禁忌证、用药剂量和方法、了解患者的基础疾病和既往不良反应发生的情况,向患者宣教坚持治疗的必要性、每种药品可能的不良反应和毒性反应,以期增强患者应对可能出现的不良反应的思想准备。另外,在治疗过程中,应密切观察药品的不良反应,采取必要的干预措施及时、有效处理可能发生或已经发生的药物不良反应,最大限度地保证耐药结核病化学治疗的连续性。 表9 耐药结核病肾功能不全患者部分抗结核药物使用剂量的调整a 注a:部分药因缺乏具体数据而未在本表中列出,使用时请参考本指南各组抗结核药物的介绍和药品说明书。b:肌酐清除率估算公式:男,体质量(kg)×(140-年龄)/72×血清肌酐(mg/dl)或体质量(kg)×(140-年龄)/0.818×血清肌酐(μmol/L);女,0.85×体质量(kg)×(140-年龄)/72×血清肌酐(mg/dl)或0.85×体质量(kg)×(140-年龄)/0.818×血清肌酐(μmol/L);血肌酐法定计量单位换算公式:1 mg/dl=88.4 μmol/L。c:尽量按标准剂量给药,以充分利用大多数抗结核药物浓度依赖的特性,患者不能耐受时除外。d:由于会增加耳毒性和中毒性肾损伤的风险,肾功能不全患者慎用。e:也可以调整为500 mg,隔日1次,但是否合适均无定论;注意监测神经毒性症状(有条件情况下,可进行血药浓度监测,作为剂量调整的依据)。f:对氨基水杨酸钠盐剂型可能导致钠负荷过重,应避免对肾功能不全患者使用,以避免钠潴留 耐药结核病化学治疗过程中常见的药物不良反应包括胃肠道反应、皮肤病变、全身性过敏反应、精神、神经毒性、听觉毒性、视觉毒性、肾毒性、肌肉骨骼和内分泌等。在确定药物不良反应时,均应除外非药物性因素,如出现胃肠道反应时需除外胃炎、肝炎、胆管疾病、肠炎、消化性溃疡、妊娠等;出现皮疹应除外蚊虫叮咬、接触性皮炎、糖尿病患者的皮肤干燥等。 (一)药物不良反应的监测 及时发现和处理药物不良反应,是保障耐药结核病患者坚持完成全程治疗的关键环节,DOT的重要优势就在于能够对药物的不良反应实施常态监测。药物不良反应监测项目和频率见表10。 (二)药物不良反应的处理 表11提供了针对耐药结核病化学治疗实施过程中可能出现的药物不良反应的处理对策。表中未列出的不良反应及其相应处理措施,请参考本指南提供的各组抗结核药物说明和相关专业书籍。用药前务必认真阅读生产厂家提供的药品说明书,以便对所用药的剂量、使用方法和可能出现的不良反应有一个较为全面而深刻的认知。 处理不良反应常需要使用辅助药物以消除或减轻不良反应,表12提供了处理耐药结核病化学药物不良反应的常用辅助药物。 表10 药物不良反应监测项目与频率 注a:建议治疗前进行常规检测,以了解患者的基线情况 表11 耐药结核病化学治疗的常见药物不良反应与处理对策 续表11 续表11 续表11 注a:表示该药品与不良反应的关系较其他药品更为密切 表12 抗结核药物治疗所致各类不良反应的常用辅助药 注 本表内容引自:World Health Organization.Companion handbook to the WHO guidelines for the programmatic management of drug-resistant tuberculosis.WHO/HTM/TB/2014.11. Geneva: World Health Organization,2014. 本部分主要介绍各种耐药结核病类型的化学治疗方案。见表13。耐多药结核病治疗的难度大,广泛耐药结核病更是难以获得有效的治疗。正确的对于单耐药和多耐药结核病患者的化学治疗,可望降低耐多药结核病的发生;如果耐多药结核病治疗得当,则可阻止其进一步发展成为广泛耐药结核病。 耐药结核病化学治疗的部分药物存在着超说明书或超适应证使用的情况。因此,在选用药物纳入治疗方案时,必须仔细评估药物的获益与风险,与患者及其家庭成员进行坦诚沟通,签署知情同意书后方可实施。 以下推荐方案中,如果因为对药物耐药、或患者不能耐受而不足以组成有效方案时,建议根据方案制定的基本原则采取个体化治疗。 一、单耐药结核病 单耐药结核病是指结核病患者感染的结核分枝杆菌经体外DST证实对1种一线抗结核药物耐药,最多见于单耐异烟肼,也可单耐利福平和单耐其他一线抗结核药物。 2010年中国结核病流行病学抽样调查结果显示:单耐药结核病患者中,单耐异烟肼:初治8.7%,复治12.8%,合计9.3%;单耐利福平:初治1.2%,复治2.6%,合计1.4%;单耐乙胺丁醇:初治0.4%,复治0.0%,合计0.4%;单耐链霉素:初治6.2%,复治2.6%,合计5.7%。按由高至低排序,依次为异烟肼(9.3%)、链霉素(5.7%)、利福平(1.4%)和乙胺丁醇(0.4%),总体上一线抗结核药物单耐药发生率复治结核病高于初治结核病患者。上述一线抗结核药物单耐药发生率的特点是指导临床上对于单耐药结核病患者进行化学治疗的重要参数。 1. 单耐药结核病化学治疗方案制定的基本原则:(1)强化期至少选择4种、继续期至少选择3种有效的一线抗结核药物,只有在无足够数量的有效的一线抗结核药物组成方案时,方考虑从二线抗结核药物中选择用药。有效药物的参考标准见总论中“耐药结核病化学治疗方案的设计”。(2)原则上不推荐选用第4组二线口服抗结核药物和第5组其他种类抗结核药物。(3)单耐异烟肼或单耐利福平者,推荐从氟喹诺酮类药物中选择左氧氟沙星,同时推荐吡嗪酰胺全疗程使用。不推荐选择其他利福霉素类药物用于耐利福平的单耐药结核病,如利福布汀或利福喷丁。(4)单耐链霉素者或不能耐受链霉素者,在无一线有效的药物可选用时,也可选择1种二线注射类药物。(5)使用注射类药物时,推荐注射用药周期为3个月。(6)疗程一般为9~12个月,单耐利福平者可按照情况延长至18个月。 2. 单耐异烟肼结核病化学治疗方案:有2个推荐方案。(1)推荐方案1:3S-R-Z-E/6R-Z-E。方案注解:总疗程9个月。强化期3个月,每日使用链霉素、利福平、吡嗪酰胺和乙胺丁醇。继续期6个月,每日使用利福平、吡嗪酰胺和乙胺丁醇。适用对象为病变范围不广泛的初治单耐异烟肼结核病患者。(2)推荐方案2:9R-Lfx-Z-E。方案注解:总疗程9个月,每日使用利福平、左氧氟沙星、吡嗪酰胺和乙胺丁醇;适用对象:①复治单耐异烟肼结核病患者;②病变范围广泛的初治单耐异烟肼结核病患者;③不能耐受链霉素的单耐异烟肼结核病患者。 表13 耐药结核病不同耐药种类的化学治疗方案推荐表 注a:病变范围广泛是指肺结核合并肺外结核患者或肺结核患者符合以下情况之一者:①轻微散布性病变,分布于一侧或两侧,其总和超过一侧肺的体积;②浓密融合性病变,分布于一侧或两侧,其总和超过一侧肺的1/3;③有空洞存在,无论多寡和部位,空洞直径超过4 cm(引自:范秉哲,裘祖源.结核病学. 第二十二章.北京:人民卫生出版社,1964:235.) 3. 单耐利福平结核病化学治疗方案:也有2个推荐方案。(1)推荐方案1:3S-H-Lfx-Z-E/9H-Lfx-Z-E。方案注解:总疗程12个月。强化期3个月,每日使用链霉素、异烟肼、左氧氟沙星、吡嗪酰胺和乙胺丁醇。继续期9个月,每日使用异烟肼、左氧氟沙星、吡嗪酰胺和乙胺丁醇。适用对象为病变范围不广泛的初治单耐利福平结核病患者。(2)推荐方案2:3S-H-Lfx-Z-E/15H-Lfx-Z-E。方案注解:总疗程18个月。强化期3个月,每日使用链霉素、异烟肼、左氧氟沙星、吡嗪酰胺和乙胺丁醇。继续期15个月,每日使用异烟肼、左氧氟沙星、吡嗪酰胺和乙胺丁醇。适用对象为:①复治单耐利福平结核病患者;②病变范围广泛的初治单耐利福平结核病患者。 ⒋ 其他单耐药结核病化学治疗方案:目前其他一线抗结核药物DST的准确度较异烟肼和利福平低,其结果需结合流行病学资料和临床情况加以综合分析后再酌情制定化学治疗方案,确保方案中含有4种有效的抗结核药物即可。 二、多耐药结核病 多耐药结核病是指结核病患者感染的Mtb经体外DST证实对1种以上一线抗结核药物耐药(但不包括同时对异烟肼和利福平耐药)。 2010年中国结核病流行病学抽样调查结果显示:多耐药结核病患者中,异烟肼+乙胺丁醇耐药:初治5.8%,复治10.3%,合计6.4%;异烟肼+链霉素耐药:初治13.7%,复治10.3%,合计13.2%;利福平+乙胺丁醇耐药:初治1.7%,复治7.7%,合计2.5%;利福平+链霉素耐药:初治3.7%,复治7.7%,合计4.3%;乙胺丁醇+链霉素耐药:初治2.5%,复治7.7%,合计3.2%;异烟肼+乙胺丁醇+链霉素耐药:初治2.5%,复治7.7%,合计3.2%;利福平+乙胺丁醇+链霉素耐药:初治1.7%,复治5.1%,合计2.1%。按由高至低排序,依次为异烟肼+链霉素(13.2%)、异烟肼+乙胺丁醇(6.4%)、利福平+链霉素(4.3%)、乙胺丁醇+链霉素(3.2%)、异烟肼+乙胺丁醇+链霉素(3.2%)、利福平+乙胺丁醇(2.5%)和利福平+乙胺丁醇+链霉素(2.1%),复治高于初治。 1.多耐药结核病化学治疗方案制定的基本原则:(1)强化期至少选择4种、继续期至少选择3种有效的一线和二线抗结核药物。当耐2种以上一线抗结核药物时,吡嗪酰胺耐药的可能性明显增大,除非有可靠证据说明吡嗪酰胺有效,否则不应该将其作为核心药物对待,方案中药物书写排序时应置于最后。(2)原则上不推荐选用第5组其他种类抗结核药物。(3)含耐异烟肼或耐利福平的多耐药结核病,推荐从氟喹诺酮类药物中选择左氧氟沙星。不推荐选择其他利福霉素类药物用于耐利福平的多耐药结核病患者,如利福布汀或利福喷丁。(4)含耐链霉素者或不能耐受链霉素的多耐药结核病患者,应选择1种二线注射类药物,首推卷曲霉素。(5)注射用药周期一般为3个月,含耐利福平的多耐药结核病患者的注射用药应延长至6个月。(6)疗程一般为12~18个月,含耐利福平的多耐药结核病患者的总疗程以20个月为宜。 2. 多耐药结核病化学治疗方案:分为如下4种情况介绍推荐方案。(1)耐异烟肼等2种一线抗结核药物:推荐方案为3S-R-Lfx-Z-E/9R-Lfx-Z-E。方案注解:总疗程12个月。强化期3个月,每日使用链霉素、利福平、左氧氟沙星、吡嗪酰胺和乙胺丁醇。继续期9个月,每日使用利福平、左氧氟沙星、吡嗪酰胺和乙胺丁醇。(2)耐利福平等2种一线抗结核药物:推荐方案为6S-H-Lfx-Z-E/12H-Lfx-Z-E。方案注解:总疗程18个月。强化期6个月,每日使用链霉素、异烟肼、左氧氟沙星、吡嗪酰胺和乙胺丁醇。继续期12个月,每日使用异烟肼、左氧氟沙星、吡嗪酰胺和乙胺丁醇。(3)耐异烟肼等3~4种一线抗结核药物:推荐方案为3S-R-Lfx-Pto-Z/15R-Lfx-Pto-Z。方案注解:总疗程18个月。强化期3个月,每日使用链霉素、利福平、左氧氟沙星、丙硫异烟胺和吡嗪酰胺。继续期15个月,每日使用利福平、左氧氟沙星、丙硫异烟胺和吡嗪酰胺。(4)耐利福平等3~4种一线抗结核药物:推荐方案为 6S-H-Lfx-Pto-Z/14H-Lfx-Pto-Z。方案注解:总疗程20个月。强化期6个月,每日使用链霉素、异烟肼、左氧氟沙星、丙硫异烟胺和吡嗪酰胺。继续期14个月,每日使用异烟肼、左氧氟沙星、丙硫异烟胺和吡嗪酰胺。 三、耐多药结核病 耐多药结核病是至少同时对异烟肼、利福平等多种药物耐药的结核病,可见于对3种、4种甚至5种一线抗结核药物全部耐药,大多来源于复治结核病患者。 2010年中国结核病流行病学抽样调查结果显示,异烟肼+利福平耐药:初治5.4%,复治15.4%,合计6.8%;异烟肼+利福平+乙胺丁醇耐药:初治1.7%,复治7.7%,合计2.5%;异烟肼+利福平+链霉素耐药:初治2.9%,复治7.7%,合计3.6%;异烟肼+利福平+乙胺丁醇+链霉素耐药:初治1.7%,复治5.1%,合计2.1%。按由高至低排序,依次为异烟肼+利福平(6.8%)、异烟肼+利福平+链霉素(3.6%)、异烟肼+利福平+乙胺丁醇(2.5%)和异烟肼+利福平+乙胺丁醇+链霉素(2.1%),复治明显高于初治。 1. 耐多药结核病化学治疗方案制定的基本原则:(1)强化期应包括至少4种有效的二线抗结核药物(含1种注射类抗结核药物)及吡嗪酰胺,继续期至少含有3种有效的二线抗结核药物,推荐吡嗪酰胺全疗程使用。基于第4、5组二线抗结核药物DST结果的可靠性较差,方案制定时要根据有效药物评价参考标准对入选药物加以综合分析、严格把关。(2)首选二线注射类和氟喹诺酮类药物。二线注射类药物首推卷曲霉素;阿米卡星和卡那霉素同时敏感时,基于二者的药效和不良反应,推荐直接使用阿米卡星。氟喹诺酮类药物推荐使用高代产品,有条件者可直接选用最高代氟喹诺酮类药物,如莫西沙星;如果要使用贝达喹啉,则尽可能避免使用莫西沙星。(3)口服二线抗结核药物的选用顺序,推荐丙硫异烟胺、环丝氨酸和对氨基水杨酸,根据需要也可选择二线抗结核药物中的2种或3种,至少保证方案中有2种口服二线抗结核药物。由于乙硫异烟胺(丙硫异烟胺)和对氨基水杨酸的组合通常会导致较高发生率的胃肠道不良反应和甲状腺功能减退症,联合应用时需加以关注和及时处理。(4)如果未能在第2~4组药物中选择到有效的4种二线抗结核药物,可从第5组药物中选择至少2种其他种类药物。(5)总疗程一般为24个月。耐多药结核病应用注射类抗结核药物的时间为强化期,常规使用6个月。强化期6个月末痰菌仍阳性者、或病变范围广泛的复治患者,强化期注射用药可延长至8个月。目前,没有证据说明超出8个月的强化期有助于提高耐多药结核病的疗效。但是,如果第8个月末痰菌培养仍未阴转提示治疗可能失败。 2. 耐多药结核病患者的化学治疗方案:推荐方案为6Cm(Am)-Lfx(Mfx)-Pto(PAS,E)-Cs(PAS,E)-Z/18Lfx(Mfx)-Pto(PAS,E)-Cs(PAS,E)-Z。方案注解:总疗程24个月。强化期6个月,每日使用卷曲霉素、左氧氟沙星、丙硫异烟胺、环丝氨酸和吡嗪酰胺;对于病变范围广泛的复治患者及强化期结束时痰菌未阴转者,强化期可延长至8个月,此时继续期的时间相应缩短。继续期18个月,每日使用左氧氟沙星、丙硫异烟胺、环丝氨酸和吡嗪酰胺。耐卷曲霉素或不能耐受卷曲霉素者用敏感的阿米卡星替代,耐左氧氟沙星可用敏感的莫西沙星,不能耐受环丝氨酸或不能耐受丙硫异烟胺者可选用有效或可能有效的对氨基水杨酸或乙胺丁醇。 四、广泛耐药结核病 广泛耐药结核病患者感染的Mtb经体外DST证实在耐多药的基础上至少同时对1种氟喹诺酮类药物和1种二线注射类药物耐药,大多来源于复治或耐多药结核病治疗失败或复发的患者。 2010年中国结核病流行病学抽样调查结果显示,广泛耐药结核病的发生率为初治1.2%、复治7.7%、合计2.1%,广泛耐药结核病的发生率复治明显高于初治患者。 1.广泛耐药结核病化学治疗方案制定的基本原则:(1)强化期至少6种、继续期至少4种有效或可能有效、或未曾应用过的药物组成化学治疗方案。(2)选择1种敏感的注射类抗结核药物。如果某种注射类药物确实有效,但药物不良反应限制了该药的使用;此时由于治疗广泛耐药结核病的可选药物极为有限,可以尝试雾化吸入,但不能将该药作为核心药物对待。注射类药物雾化吸入治疗结核病的有效性和安全性尚不可知,仍有发生肾毒性和耳毒性的可能。如果DST显示所有注射类抗结核药物耐药,建议从中选择患者既往未曾应用过的注射剂。(3)氟喹诺酮类药物中首选莫西沙星或加替沙星。(4)选择有效的或患者既往未曾使用过的二线口服药。(5)使用吡嗪酰胺及其他可能有效的第1组药;如果异烟肼低浓度耐药,可使用高剂量异烟肼(16~20 mg/kg)。(6)第5组抗结核药物在广泛耐药结核病患者的化学治疗中,选择用药的空间较其他类型耐药结核病更为广阔,可从中选择2~3种可能有效或患者未曾应用过的药物。利奈唑胺是第5组药物中最有效、也是广泛耐药结核病化学治疗方案中的关键药物之一,其次为氯法齐明。价格昂贵和严重不良反应妨碍了这2种药的使用。以下推荐方案中的克拉霉素和阿莫西林-克拉维酸钾价格便宜、不良反应小。如果条件许可,仍可酌情选用利奈唑胺和氯法齐明。(7)疗程一般为30个月。注射用药时间一般为12个月,可按照情况适当延长,必要时可全疗程使用。(8)缺乏足够药物组成有效方案时,建议采用姑息疗法,给予患者对症治疗、营养支持和心理疏导。 2. 广泛耐药结核病化学治疗方案:推荐方案为12Cm-Mfx-Pto(PAS)-Cs(PAS)-Clr-“Amx-Clv”-Z/18Mfx-Pto(PAS)-Cs(PAS)-Clr-“Amx-Clv”-Z。方案注解:总疗程30个月。强化期12个月,每日使用卷曲霉素、莫西沙星、丙硫异烟胺、环丝氨酸、克拉霉素、阿莫西林-克拉维酸钾、吡嗪酰胺。继续期18个月,每日使用莫西沙星、丙硫异烟胺、环丝氨酸、克拉霉素、阿莫西林-克拉维酸钾、吡嗪酰胺。不能耐受丙硫异烟胺或环丝氨酸者可选用对氨基水杨酸。经济条件许可或患者能够耐受的情况下,尤其是无二线口服药物可以选择时,建议选用利奈唑胺和(或)氯法齐明。 五、特殊人群耐药结核病 根据特殊人群耐药结核病患者的类型和群体特点,参照上述方案规定的基本原则制订相应的化学治疗方案。以下建议可供制订方案时参考。 (一)儿童耐药结核病 儿童耐药结核病一般为原发性,系耐药结核分枝杆菌传播所致。治疗时尽量以DST结果指导治疗,避免对儿童不必要地使用毒性大的药物。耐药结核病是威胁生命的疾病,对于儿童没有绝对禁忌的抗结核药物。由于对儿童应用二线抗结核药物长期治疗的经验不多,设计治疗方案时应仔细考虑每一种药物的利弊。特别是在治疗开始时,与家庭成员进行坦诚沟通至关重要。(1)接触史:有结核病密切接触史的儿童原发或初始耐药结核病,制定化学治疗方案时应注意参考密切接触者的抗结核药物使用史和DST结果。(2)药物剂量:除乙胺丁醇外,一般按照药物剂量范围的高限使用。治疗过程中需根据患儿体质量变化及时调整药物剂量,一般每个月评估1次。(3)乙胺丁醇:需要使用乙胺丁醇的儿童,推荐剂量为15 mg/kg,而不是成人应用时的25 mg/kg,因为对儿童进行视神经炎监测更为困难。(4)氟喹诺酮类药物:动物试验显示,氟喹诺酮类药物妨碍幼犬软骨发育,但并没有关于人类使用氟喹喏酮类药物的类似报道。对于儿童耐药结核病,通常认为氟喹喏酮类药物用于治疗利大于弊。原则上不推荐氟喹喏酮类药物用于体质量<10 kg的儿童,病情危重且无其他有效药可选择时可谨慎使用。由此出现的风险和收益需要在用药前和患儿家属讨论达成共识。(5)二线口服抗结核药物:丙硫异烟胺、环丝氨酸和对氨基水杨酸用于儿童耐药结核病的疗效良好,且易耐受。耐受性差可调整为一日量分次服用。 (二)老年耐药结核病 70岁或以上患者,药物使用的数量和剂量要适当减少和减量。(1)注射类抗结核药物:按照情况适当减量及隔日应用,70岁或以上患者不建议使用。必须使用时,治疗前应检测听力,治疗过程中密切检测听力、肾功能和尿常规等。(2)经肝脏代谢药物:适当减量,并增加肝功能检测频次。 (三)妇女耐药结核病 1. 妊娠:强烈建议进行耐药结核病治疗的育龄妇女避孕,频繁而严重的药物不良反应对母亲和胎儿均构成潜在的威胁。患者和亲属要根据医生交代的治疗利弊情况亲自参与决定是否继续妊娠。如果选择终止妊娠,应在有效的治疗后择期决定流产术,术后继续按要求进行耐药结核病化学治疗。所有患者一旦确立诊断应当立即治疗,由于大部分药物的致畸作用发生在妊娠早期,治疗如推迟到妊娠3个月之后开始则可避免,但推迟治疗可能导致孕妇病情快速进展。本指南推荐根据妊娠不同时期进行分阶段治疗的方案,需要通过患者、患者家属和医生在分析治疗利弊后依据社会伦理情况共同达成。 妊娠期间分阶段治疗有如下建议。①妊娠期全程:原则上禁用注射类抗结核药物,尤其是氨基糖苷类药物。病情危重不得已需要使用注射类抗结核药物时,卷曲霉素可为一种选择。②妊娠3个月内(胎儿未成型期):评估是否有条件延迟到妊娠3个月后再开始化学治疗。如需要立即治疗可选择异烟肼或对氨基水杨酸异烟肼、吡嗪酰胺、对氨基水杨酸、环丝氨酸、阿莫西林-克拉维酸钾。选用环丝氨酸时需要评估患者的精神状况及有无精神系统异常的家族史。有条件时应作环丝氨酸的血药浓度监测,同时常规加用维生素B6。③妊娠3个月后(胎儿成型期):可选用异烟肼或对氨基水杨酸异烟肼、利福平或利福布汀或利福喷丁、吡嗪酰胺、对氨基水杨酸、环丝氨酸、阿莫西林-克拉维酸钾。 产后应立即加强抗结核治疗,增加一种注射类抗结核药物和其他有效药物,以确保方案中含4种有效的抗结核药物。此时强化期和继续期的顺序可适当模糊,保障注射用药期至少达到相关耐药治疗方案的基本要求。 2. 哺乳:推荐活动性耐药结核病的哺乳妇女进行全程抗结核治疗,及时、正确的化学治疗是避免将耐药Mtb传染给婴儿的最佳方法。在接受治疗的母亲乳汁中,能检测出多数抗结核药物,其浓度仅等同于婴儿化学治疗剂量的很小一部分。目前,尚不十分清楚耐药结核病全程治疗对接受哺乳的婴儿造成的影响,因此需要在与患者及其家属充分沟通后进行治疗或决定是否可以哺乳。 3. 避孕:所有具有生育能力的未孕女性患者应严格避孕。利福平会因药物拮抗作用导致避孕效果降低。对于使用不含利福平治疗方案的患者,口服避孕药没有禁忌。对于利福平敏感的单耐药或多耐药患者,使用口服避孕药同时接受利福平治疗的女性患者可以有2个选择:即遵照医嘱使用含大剂量雌激素(50 μg)的口服避孕药或采用其他方式避孕。呕吐是避孕和抗结核药物所共有的不良反应,分开服用有助于减轻呕吐症状或减少发生的频率。呕吐反应严重者必要时可采用物理方法避孕。避孕套是不想服用口服避孕药和避免性传播疾病的有效工具,但患者必须意识到,避孕套不是最有效的避孕手段,特别是使用不当时。此时可以考虑注射甲羟孕酮或者使用其他避孕手段。 (四)耐药结核病合并糖尿病 耐药结核病合并糖尿病时,治疗难度增大,效果往往欠佳。糖尿病增加抗结核药物的不良反应,尤其是肾脏功能障碍和周围神经病变,而乙硫异烟胺(丙硫异烟胺)可能使得控制胰岛素水平更困难。建议治疗时认真阅读被选药物的说明书,掌握药物间的相互作用,必要时邀请糖尿病专家会诊,保障抗结核和降糖药物的合理使用。 (五)HIV感染合并耐药结核病 (1)单耐异烟肼:仍可选择2S-H-R-Z-E/6H-R-E或3H-R-Z-E/6H-R-E的标准复治方案。(2)利福平:敏感者应全程使用利福平(有条件者选用利福布汀),并每日给药。不能耐受者,可采用间歇给药(每周3次),但间歇给药者较每日给药者的复发率高2~3倍。(3)氨硫脲:因为可能导致的严重不良反应,HIV感染者禁忌使用氨硫脲。(4)克拉霉素:考虑到抗病毒药与克拉霉素的相互作用,不推荐使用克拉霉素。(5)药物不良反应:①抗病毒与抗结核药物可能有共同的药物毒性。一些抗病毒药物可导致高达50%的患者出现注意力不集中、多梦和眩晕,但是很少出现情绪障碍和精神病。如出现精神病及癫痫,应警惕是否由环丝氨酸所致。②细胞色素酶P450 2B6慢代谢基因型会导致抗病毒药物的血药浓度增加,可能与异烟肼抑制抗病毒药物的旁路代谢有关。使用异烟肼时应注意监测抗病毒药物相关的中枢神经症状。(6)抗病毒治疗三原则:①建议所有需要使用二线抗结核药物的耐药结核病合并HIV感染患者,不管CD4计数水平如何,都应该在抗结核治疗后尽早开始抗逆转录病毒治疗,最晚不迟于8周。②对于免疫功能严重低下者(CD4<50个/mm3)应在抗结核治疗后2周内进行抗逆转录病毒治疗。③抗逆转录病毒治疗首先选用非核苷类逆转录酶抑制剂——依法韦仑(efavirenz)。 一、耐药结核病化学治疗方案调整指征 调整指征如下:(1)患者依从性差。(2)患者发生较为严重的药物不良反应。(3) DST结果提示方案存在缺陷。(4)治疗失败。 二、耐药结核病化学治疗方案调整的基本要求 1. 符合耐药结核病化学治疗原则:详见相关章节。 2. 经过集体讨论认可:经过集体(专家组)讨论认可,以有效保证方案的调整符合本指南耐药结核病化学治疗的基本原则、制定新方案的科学性和合理性,避免个人经验的片面性。 3. 选择敏感或未曾使用过的抗结核药物:按照DST结果选择敏感药,获得DST结果前或无足够药组成方案时,也可选用患者未曾使用过的抗结核药物。 4. 避免单一加药:避免在治疗过程中随意增加一种药,或在已经证明治疗失败的方案中单一加药,以避免新加的药物发生耐药的风险。 5. 调整后治疗方案疗程的计算:调整后的新方案疗程应重新开始计算。因调整方案前患者治疗疗效不能得到有效保证,或用药可能不规律;为保证有效的治疗效果,新的耐药结核病化学治疗疗程应从方案调整并实施之日起重新开始计算。 三、耐药结核病化学治疗方案调整范例 1. 依从性差:依从性涉及众多影响因素,例如患者个人态度、相关的知识、对疾病的信念,也包括医疗卫生系统、经济方面和社会方面等诸多因素。大多数情况下,通过对相关因素进行仔细分析和认真处理后,患者的依从性往往可能因此而提高,继续原有方案治疗。只有在处理无效的情况方可考虑调整治疗方案。 胃肠道反应是影响依从性的众多因素之一,可将有胃肠道反应的药物调整为:(1)晚上服用;(2)分次服用;(3)少量进食后服药。如此,胃肠道反应往往可以得到缓解。尽可能避免减量用药。必要时配合使用止吐药(胃复安甚至昂丹司琼)及加用少量镇静剂。经上述调整后症状改善不满意,对日常生活影响大,需考虑进行方案调整。 耐多药结核病患者强化期需要使用二线注射类抗结核药物至少6个月或更长时间。临床实践证明,相当一部分患者因注射部位疼痛,难以承受如此长时间的注射用药。可根据疗效,适当缩短注射用药的疗程或调整为隔日用药,以提高患者的依从性,但最好在痰菌转阴后调整。 2. 药物不良反应:严重的药物不良反应可能导致耐药结核病患者中断治疗、治疗失败、病情加重甚至死亡。耐药结核病的治疗用药多、疗程长、药物不良反应多见,治疗中要加强做好药物不良反应的检测(如主动检测,使用电话或短信等及时联系)。轻度的药物不良反应无须调整方案。较严重的药物不良反应,经对症处理无效时,应考虑更换相应药物甚至重新调整治疗方案。例如,利奈唑胺治疗耐药结核病有效甚至被认为是关键药物之一,但该药有许多严重的不良反应,包括骨髓抑制(贫血、白细胞减少症、血小板减少症和全血细胞减少)、周围神经病变和乳酸性酸中毒等,一旦发生经对症处理和减量使用(300 mg/d)均无效时,需要停止使用该药。注射类抗结核药物导致的早期听力损伤,通过调整用药频率(每周2~3次),或改为卷曲霉素,听力损伤仍持续甚至加重,应停止使用注射类抗结核药物。 需要特别注意的严重药物不良反应主要有过敏、肝毒性、肾毒性、电解质紊乱、甲状腺功能低下、耳毒性、精神病学障碍、QT间期延长等。详见表11。 3. DST结果提示方案存在缺陷:相当一部分耐药结核病的治疗始于经验性治疗,治疗方案常常需要根据DST结果做进一步调整。有的患者治疗期间DST结果显示耐药发生变化而需要根据疗效调整方案。所有耐多药结核病患者在治疗开始时应进行二线抗结核药物的DST,如果明确存在二线药物耐药,需要根据疗效调整治疗方案。 4. 疗效不佳或治疗失败:以细菌学检查结果为主要评价指标,结合临床情况(症状、影像学)对疗效和治疗转归进行客观分析,以决定是否需要延长疗程或中止治疗。通常情况下,对利福平敏感的单耐药和多耐药结核病患者持续5个月痰培养阳性、耐利福平的单耐药和多耐药结核病患者持续8个月痰培养阳性、耐多药结核病患者持续12个月痰培养阳性时,提示治疗可能失败,往往需要调整方案。 以下情况需注意:(1)单独一次痰培养阳性可能是疗效不佳,也可能是实验室污染或误差所致。痰涂片阳性、培养阴性提示痰涂片阳性可能是由于死菌存在所致。(2)强化期末痰涂片或培养阳性患者应延迟进入继续期,如果临床症状及影像学提示病情好转,不需要重新调整治疗方案。(3)治疗期间如果发现对氟喹诺酮类药物或二线注射剂获得性耐药的证据,治疗失败的可能性增加。(4)确认治疗失败后应着手制定新的治疗方案。 5. 其他特殊情况:妊娠、哺乳、儿童和老年人等特殊群体的治疗方案调整原则参照本指南的相关部分。 一、对利福平敏感的耐药结核病化学治疗的转归 包括对利福平敏感的单耐药和多耐药结核病患者。 1. 治愈:完成规定疗程,疗程结束时连续2次痰涂片或培养阴性,每次间隔至少30 d,第2次阴性结果在疗程最后1个月末。 2. 完成治疗:完成规定疗程,疗程最后1个月末因无痰使其痰涂片或痰培养无法进行,此前痰涂片或培养阴性。 3. 失败:未达到治愈或完成治疗的标准。 4. 死亡:治疗过程中由于任何原因所致的死亡。 5. 丢失:由于任何原因致治疗中断连续2个月或以上。 6. 不能评价:包括患者转诊到其他医疗机构或不知其治疗转归。 7. 治疗成功:包括治愈和完成治疗。 二、利福平耐药结核病(rifampicin resistance-tuberculosis,RR-TB)化学治疗的转归 包括耐利福平的单耐药、多耐药、耐多药和广泛耐药结核病。 1. 治愈:完成规定疗程,疗程结束时连续3次痰培养阴性,每次间隔至少30 d,第3次阴性结果在疗程结束时的最后1个月末。 2. 完成治疗:完成规定疗程,因无痰未能在疗程结束时获得连续3次、每次间隔至少30 d的痰培养阴性结果,此前痰培养阴性。 3. 失败:未达到治愈或完成治疗的标准。 4. 死亡:患者在治疗过程中由于任何原因所致的死亡。 5. 丢失:患者由于任何原因治疗中断连续2个月或以上。 6. 不能评价:包括患者转诊到其他医疗机构或不知其治疗转归。 7. 治疗成功:包括治愈和完成治疗。 三、耐药结核病化学治疗转归的有关术语说明 1. 细菌学阴转:连续2次痰培养结核分枝杆菌阴性,且每次间隔至少30 d。阴转时间为第1次痰培养阴性的标本收集时间。 2. 细菌学复发:在细菌学阴转后,患者连续2次痰培养结核分枝杆菌阳性,每次间隔至少30 d。 3. 耐药结核病化学治疗的终止:完成规定疗程,达到或未达到治疗成功的标准。未达到治疗成功标准者应重新启动耐药结核病化学治疗。 4. 耐药结核病化学治疗的中止:治疗过程中出现以下情况之一者,经集体讨论后确认需要中止正在进行的耐药结核病化学治疗,重新调整治疗方案。 1)治疗启动后痰培养持续阳性,经菌种鉴定为结核分枝杆菌者:①对利福平敏感的单耐药和多耐药结核病患者持续5个月痰培养阳性;②耐利福平的单耐药和多耐药结核病患者持续8个月痰培养阳性;③耐多药结核病患者持续12个月痰培养阳性;④广泛耐药结核病患者持续16个月痰培养阳性。 2)治疗过程中出现严重的药物不良反应,经积极对症处理后无效。 3)治疗过程中出现新的耐药,尤其是发现氟喹诺酮类、二线注射类药物耐药的证据,需要更换治疗方案中2种及以上药物。 注 国内外认可的菌种鉴定和耐药分子诊断技术适用于本指南耐药结核病化学治疗转归的评价。 单耐药和多耐药结核病患者的化学治疗管理可参考初治和复治肺结核患者的化学治疗管理,耐利福平结核病和广泛耐药结核病患者的化学治疗管理则可参照耐多药结核病患者的化学治疗管理执行。下面重点就耐多药肺结核患者的化学治疗管理做一阐述。 耐多药肺结核患者治疗疗程长达24个月甚至更长,治疗难度大,一旦治疗失败将会引起更大的公共卫生问题。为保证患者在治疗过程中坚持规律用药,完成规定的疗程,必须在治疗全过程对患者采取有效的治疗管理措施。 (一)治疗管理方式 耐多药肺结核患者均应采取全程督导化学治疗,即在治疗全过程中,患者每次用药均在接受过专门培训的医护人员直接督导下进行。不推荐耐多药肺结核患者采用家庭督导服药方式。 对耐多药肺结核患者主要采用住院与门诊治疗相结合的方式进行治疗管理。这是由于多数耐多药肺结核患者病情严重,有并发症和(或)合并症;治疗时间长、使用药品种类多,故容易出现严重药物不良反应。因此,确诊后应首先住院治疗,待病情相对稳定、治疗方案确定后,可出院继续在社区或村卫生室进行治疗管理。对于那些因经济困难等原因不愿意住院治疗的患者,可采用全程门诊治疗方式。 (二)住院治疗管理 住院期间,医院负责患者治疗方案制定、健康教育、治疗管理、发现和处理药物不良反应等。 (1)结核病临床医生讨论制定患者的化学治疗方案;(2)主管护士每日督导患者用药,做到:送药到手,看服到口,并及时填写“患者治疗服药卡”;(3)按治疗监测要求对患者进行痰涂片、痰培养、胸片、肝肾功能、电解质等检查;(4)监测患者药物不良反应的发生情况,做到及时发现、及时处理;(5)密切关注患者心理健康,对患者进行耐多药肺结核治疗相关的健康教育,特别是坚持完成全疗程治疗与痊愈的关系、常见的药物不良反应和与医生联系的方法等;(6)主管医生在患者出院时向患者开具后续治疗方案、随访复查时间等,并通知疾病预防控制中心落实患者出院后的治疗管理。 (三)门诊治疗管理 1. 落实治疗服药地点:县(区)疾病预防控制中心接到患者出院通知单后,与患者居住地的乡医、村医(社区医生)和患者“四见面”,落实患者治疗服药地点和督导人员。患者应到指定的治疗服药地点接受治疗,服药时间由督导人员与患者商定。 2. 督导患者服药:患者每次服药必须在医务人员或接受过专门培训的督导员监督下进行,必须做到看服到口,每次服药后由督导人员填写“患者治疗服药卡”。县(区)级疾病预防控制中心每月对督导人员和患者督导访视一次,查看督导人员督导治疗执行情况和患者服药情况。 3. 药物不良反应的发现与处理:督导人员必须密切观察患者的症状和药物不良反应发生情况,出现中度及以上药物不良反应时,须及时督促患者到结核病定点医院检查处理,防止发生严重后果。 4. 督促患者按期随访复查:患者需按医生医嘱及时到结核病定点医院随访复查,督导人员应提前提醒并指导患者事先留痰。患者随访复查时将上月的“患者治疗服药卡”交给医生存留在门诊病历内,并作为填写病案记录的重要依据。 注 本指南参考文献按照改良哈佛体系著录 志谢 本指南得到了以下单位、项目和个人的大力支持,在此一并表示感谢!中华人民共和国国家卫生和计划生育委员会疾病预防控制局、中国疾病预防控制中心结核病预防控制中心、中国疾病预防控制中心结核病防治临床中心、同济大学附属上海市肺科医院、上海市结核病(肺)重点实验室、中国全球基金结核病项目(CHN-S10-G14-T)、“十二五”国家科技重大专项(2013ZX10003009)、同济大学附属上海市肺科医院结核病临床研究中心的医生(以姓氏笔画排序)(卫卫、马俊、王鹏、尹洪云、平静娜、史祥、刘轾彬、孙雯雯、李红、杨妍、何娅、邹丹凤、沈芸、张少俊、郝晓晖、姚岚、崔海燕、梁莉、葛燕萍、蒋瑞华、程丽平、楼海) 附件1 耐药结核病化学治疗指南(2015)编辑委员会组成名单 主 编 肖和平 副主编 屠德华 朱莉贞 王黎霞 编 委 (按照姓氏笔画排序) 万利亚 马 玙 马 艳 王撷秀 王黎霞 方 勇 成诗明 朱莉贞 朱桂林 刘一典 刘宇红 闫丽萍 李仁忠 李 琦 肖和平 沙 巍 初乃惠 张 青 陈明亭 范 琳 桂徐蔚 顾 瑾 高孟秋 高微微 唐神结 屠德华 蒋建英 端木宏谨 附件2 耐药结核病化学治疗指南(2015)英文缩写查询表 ADR (adverse drug reactions):药物不良反应;AIDS (acquired immunodeficiency syndrome):人类获得性免疫缺陷综合征(艾滋病);ALT (alanine aminotransferase):丙氨酸转氨酶(丙氨酸氨基转移酶);Am (amikacin):阿米卡星;Amx-Clv (amoxicillin-clavulanate):阿莫西林-克拉维酸钾;ART (antiretroviral therapy):抗逆转录病毒治疗;Bdq (bedaquiline):贝达喹啉;CCR (creatinine clearance rate):肌酐清除率;CDC (Centers for Disease Control and Prevention):疾病预防控制中心;Cfz (clofazimine):氯法齐明;Clr (clarithromycin):克拉霉素;Cm (capreomycin):卷曲霉素;CNS (central nervous system):中枢神经系统;Cs (cycloserine):环丝氨酸;CYP3A4 (cytochrome P450 3A4):细胞色素 P450 3A4;DILI(drug-induced liver injury):药物性肝损伤;Dlm (delamanid):德拉马尼;DOT (directly-observed therapy):直接面视督导下治疗;DOTS (directly observed therapy short course):现代结核病控制策略(为我国官方释义,非直接翻译);DR-TB (drug-resistant tuberculosis):耐药结核病;DST (drug susceptibility testing):药物敏感试验;DS-TB (drug-susceptible tuberculosis):药物敏感结核病;EMB(E)(ethambutol):乙胺丁醇;Eto (ethionamide):乙硫异烟胺;FQ (fluoroquinolone):氟喹诺酮类药物;Gfx (gatifloxacin):加替沙星;HBC(high-burden country):高负担国家;HIV (human immunodeficiency virus):人类获得性免疫缺陷病毒;INH(H)(isoniazid):异烟肼;Ipm-Cln (imipenem-cilastatin):亚胺培南-西司他丁;Km (kanamycin):卡那霉素;Lfx (levofloxacin):左氧氟沙星;Lzd (linezolid):利奈唑胺;MAC(Mycobacteriumavium-intracellularecomplex):鸟-胞分枝杆菌复合群;MDR (multidrug resistance):耐多药;MDR-TB (multidrug-resistant tuberculosis):耐多药结核病;Mfx (moxifloxacin):莫西沙星;MIC (minimum inhibitory concentration):最低抑菌浓度; NTM (non-tuberculous mycobacteria):非结核分枝杆菌;Mpm (meropenem):美罗培南;MR-TB (mono-resis-tant tuberculosis):单耐药结核病;MDR-TB(multidrug-resis-tant tuberculosis):耐多药结核病; NDR(natural drug resistantance:自然耐药(天然耐药);NTP(national TB control programme):国家结核病控制规划;Ofx (Ofloxacin):氧氟沙星;Pa (isoniazid aminosalicylate):对氨基水杨酸异烟肼;PAE(postantibiotic effect):抗生素后效应;PAS (P-ami-nosalicylic acid):对氨基水杨酸;PAS-Na (P-aminosalicylate sodium):对氨基水杨酸钠;PR-TB (poly-resistant tuberculosis):多耐药结核病;PI (protease inhibitor):蛋白酶抑制剂;PMDT (programmatic management of drug-resistant tuberculosis):耐药结核病规划管理;Pto (protionamide):丙硫异烟胺;PZA(Z)(pyrazinamide):吡嗪酰胺;QTcF(QT interval corrected for heart rate (Fridericia method)):QT间期矫正值(Fridericia法);RFP(R)(rifampicin):利福平;Rfb (rifabutin):利福布汀;Rft (rifapentine):利福喷丁;RR-TB (rifampicin-resistant tuberculosis):利福平耐药结核病;Sm(S)(streptomycin):链霉素;TB (tuberculosis):结核病; Thz (thioacetazone):氨硫脲;Trd (terizidone):特立齐酮;TSH (thyroid stimulating hormone):促甲状腺激素;ULN(upper limit of normal):正常值上限;Vm (viomycin):紫霉素;WHO(World Health Organization):世界卫生组织;XDR-TB(extensively drug-resistant tuberculosis):广泛耐药结核病。 [1] 申晓娜,赵雁林,肖和平,等.对氨基水杨酸异烟肼及异烟肼体外抗结核分枝杆菌活性分析.中华结核和呼吸杂志,2014,37(2):132-134. [2] 王前,宋媛媛,逢宇,等.耐氧氟沙星结核分枝杆菌对五种氟喹诺酮类药物交叉耐药的研究.中国防痨杂志,2014,36(6):453-457. [3] 杨华,胡忠义,沙巍,等.结核分枝杆菌对氧氟沙星耐药的体外诱导及稳定性研究.中华预防医学杂志,2014,48(4):318-323. [4] 常珊,付育红,李琦,等.结核分枝杆菌临床分离株对四种注射用抗结核药物耐药及交叉耐药分析.中国防痨杂志,2013,35(1):37-40. [5] 刘一典,桂徐蔚,景玲杰,等.耐多药结核分枝杆菌临床分离株30株对氟喹诺酮类及二线注射类抗结核药敏感性的分析.中华临床医师杂志(电子版),2013,7(4):1565-1568. [6] 唐神结.结核病临床诊治进展年度报告(2012).北京:人民卫生出版社,2013:79-85. [7] 姚岚,唐神结,孙华,等. 耐多药结核分枝杆菌对第5组抗结核药物的耐药性初步分析.同济大学学报(医学版),2013,34(4):111-115. [8] 赵冰,宋媛媛,逢宇,等.中国耐多药结核分枝杆菌二线抗结核药物敏感性分析.中国防痨杂志,2013,35(10): 831-834. [9] 中华医学会结核病学分会,中华结核和呼吸杂志编辑委员会. 抗结核药所致药物性肝损伤诊断与处理专家建议.中华结核和呼吸杂志,2013,36(10):732-736. [10] 高丽,肖和平,胡忠义,等. 耐多药结核分枝杆菌对利福布汀和利福平的交叉耐药性分析. 中华结核和呼吸杂志,2012, 35(5):333-335. [11] 郝晓晖,姚岚,唐神结,等.初治耐多药肺结核临床疗效及其转归队列分析.中华传染病杂志,2012,30(3):157-161. [12] 何佩贤,黎婉媚,康莉娟.321例耐多药结核病耐药情况分析.中国防痨杂志,2012,34(8):514-518. [13] 李玲,姚嵩,陈静. 安徽省192例HIV阳性结核病患者的治疗转归分析. 中国防痨杂志,2012,34(1):15-18. [14] 全国第五次结核病流行病学抽样调查技术指导组,全国第五次结核病流行病学抽样调查办公室. 2010年全国第五次结核病流行病学抽样调查报告.中国防痨杂志,2012,34(8):485-507. [15] 王怀冲,徐颖颖,张相彩,等.联合氯法齐明方案治疗耐多药肺结核的临床研究.中国临床药理学与治疗学,2012,17(11):1268-1271. [16] 谢安,肖和平.环丝氨酸在治疗耐多药结核病方面的应用.中华结核和呼吸杂志,2012, 35(12): 949-950. [17] 尹洪云,何娅,邹丹凤,等. 161例耐多药肺结核治疗随访结果.中国防痨杂志, 2012,34(2):110-114. [18] 赵恒敏,王卫华.抗耐多药结核病新药的研究进展.中国防痨杂志,2012,34(5):324-326. [19] 桂徐蔚,肖和平,胡忠义,等.氯法齐明对不同耐药类型结核分枝杆菌的体外抑菌活性研究.中华结核和呼吸杂志,2011,34(8): 579-581. [20] 刘一典,唐神结,张青,等.上海地区结核分枝杆菌分离株对一线和二线抗结核药物的耐药性分析.中华传染病杂志,2011,29(9):544-548. [21] 沙巍,王洁,胡忠义,等.痰噬菌体生物扩增法检测一线抗结核药物敏感性的临床应用研究.中华临床感染病杂志,2011,4(5): 271-274. [22] 唐神结,高文. 临床结核病学. 北京:人民卫生出版社,2011:191-200. [23] 唐神结,肖和平. 抗结核药物研究进展. 中华全科医师杂志,2011,10(11):814-816. [24] 唐神结,肖和平.广泛耐药结核病的现状与对策.中华医学杂志,2011,91(5):355-358. [25] 唐神结,张青,余金明,等.上海市结核病专科医院广泛耐药结核病的情况. 中华结核和呼吸杂志,2011,34(8): 637. [26] 肖和平. 耐药结核病化学治疗指南(2010年).北京:人民卫生出版社,2011. [27] 曹广云,肖和平,闫丽萍,等. 三种注射用抗结核药物对结核分枝杆菌的耐药情况分析.中国防痨杂志,2010,32(4): 227-230. [28] 方勇,肖和平,唐神结,等.抗结核药物致药物热的临床特征及处理措施.中华临床医师杂志(电子版),2010,4(11):2237-2240. [29] 唐神结,肖和平.利奈唑胺抗结核作用的研究及其最新进展. 中华临床医师杂志(电子版),2010,4(1):63-66. [30] 肖东楼,马玙,朱莉贞. 抗结核药品不良反应诊疗手册. 北京:人民卫生出版社,2010:14-62. [31] 肖和平.中国耐药结核病的流行现状与治疗对策.中华结核和呼吸杂志,2010,33(7): 481-482. [32] 闫丽萍,肖和平,郑瑞娟,等.结核分枝杆菌耐氧氟沙星临床分离株gyrA基因突变的研究. 中国感染与化学杂志,2010,10(1): 31-34. [33] 姚岚,唐神结,肖和平,等. 利奈唑胺治疗广泛耐药结核病的临床疗效观察. 中华临床医师杂志(电子版),2010,4(12):2435-2440. [34] 中国防痨协会.耐药结核病化学治疗指南(2009).中国防痨杂志,2010,32(4):181-198. [35] 楼海,肖和平,张青,等.148例耐多药和广泛耐药肺结核的临床特点.中国防痨杂志,2009,31(11):653-656. [36] 唐神结,肖和平,张青. 耐多药结核病化学治疗方案研究的新进展.中华结核和呼吸杂志,2009,32(8):617-620. [37] 唐神结,肖和平.耐药结核病的化学治疗药物及其研究进展.中华医学杂志,2009,89(44):3160-3162. [38] 唐神结.耐药结核病防治手册. 北京:人民卫生出版社,2009. [39] 肖和平,唐神结.二线抗结核药物的临床应用.中国防痨杂志,2009,31(10):612-616. [40] 熊晗晖,冯端浩,郑越,等.力克肺疾治疗难治复治多耐药肺结核的Meta 分析.中南药学,2009,7(9):688-692. [41] 闫丽萍,肖和平.住院肺结核患者耐氧氟沙星情况分析.中国防痨杂志,2009,31(8):477-480. [42] 汪复,张婴元.抗菌药物临床应用指南.北京:人民卫生出版社,2008:135-142. [43] 肖和平.耐多药结核病化疗药物的选择与方案的制定.中华结核和呼吸杂志,2006,29(8):517-519. [44] 朱莉贞,傅瑜,初乃惠,等. 利福类联合多种药物长疗程方案治疗耐多药肺结核.中华结核和呼吸杂志,2006,29(8):520-523. [45] 江明性.新编实用药物学.北京:科学出版社,2000:551-552. [46] Public Health Agency of Canada,The Lung Association,Canadian Thoracic Society.Canadian tuberculosis standards. 7th ed. Ottawa:Public Health Agency of Canada,The Lung Association,Canadian Thoracic Society,2014. [47] World Health Organization. Policy implementation package for new TB drug introduction. WHO/HTM/TB/2014.22.Geneva:World Health Organization, 2014. [48] World Health Organization.Companion handbook to the guidelines for the programmatic management of drug-resistant tuberculosis. WHO/HTM/TB/2014.11.Geneva: World Health Organization, 2014. [49] De Lorenzo S,Alffenaar JW,Sotgiu G,et al. Efficacy and safety of meropenem-clavulanate added to linezolid-containing regimens in the treatment of MDR-/XDR-TB. Eur Respir J,2013,41(6):1386-1392. [50] Dey T,Brigden G,Cox H,et al. Outcomes of clofazimine for the treatment of drug-resistant tuberculosis: a systematic review and meta-analysis. J Antimicrob Chemother,2013,68(2):284-293. [51] Dharmadhikari AS,Kabadi M,Gerety B,et al. Phase I, single-dose, dose-escalating study of inhaled dry powder capreomycin: a new approach to therapy of drug-resistant tuberculosis. Antimicrob Agents Chemother,2013,57(6):2613-2619. [52] Dooley KE, Obuku EA, Durakovic N, et al.World Health Organization group 5 drugs for the treatment of drug-resistant tuberculosis: unclear efficacy or untapped potential? J Infect Dis,2013,207(9):1352-1358. [53] Falzon D,Gandhi N,Migliori GB,et al. Resistance to fluoroquinolones and second-line injectable drugs: impact on multidrug-resistant TB outcomes. Eur Respir J,2013,42(1):156-168. [54] Hwang TJ,Wares DF,Jafarov A,et al. Safety of cycloserine and terizidone for the treatment of drug-resistant tuberculosis: a meta-analysis. Int J Tuberc Lung Dis,2013,17(10):1257-1266. [55] Jo KW,Ji WJ,Hong Y,et al. The efficacy of rifabutin for rifabutin-susceptible, multidrug-resistant tuberculosis. Respir Med,2013,107(2):292-297. [56] Koh WJ,Lee SH,Kang YA,et al. Comparison of levofloxacin versus moxifloxacin for multidrug-resistant tuberculosis. Am J Respir Crit Care Med,2013,188(7):858-864. [57] Kurbatova EV,Cavanaugh JS,Dalton T,et al. Epidemiology of pyrazinamide-resistant tuberculosis in the United States, 1999—2009.Clin Infect Dis,2013,57(8):1081-1093. [58] Prach LM,Pascopella L,Barry PM,et al. Rifampin monoresistant tuberculosis and HIV comorbidity in California, 1993—2008: a retrospective cohort study. AIDS,2013,27(16):2615-2622. [59] Zhang Q, Liu Y, Tang S,et al.Clinical benefit of delamanid (OPC-67683) in the treatment of multidrug-resistant tuberculosis patients in China. Cell Biochem Biophys,2013,67(3): 957-963. [60] Skripconoka V,Danilovits M,Pehme L,et al. Delamanid improves outcomes and reduces mortality in multidrug-resistant tuberculosis. Eur Respir J,2013,41(6):1393-1400. [61] World Health Organization. Definitions and reporting framework for tuberculosis - 2013 revision. WHO/HTM/TB/2013.2. Geneva: World Health Organization, 2013. [62] World Health Organization. Global tuberculosis report 2013. WHO/HTM/TB/2013.11. Geneva: World Health Organization, 2013. [63] Yan LP, Qin LH, Zhang Q, et al.Transmission of extensively drug-resistant and multidrug resistantMycobacteriumtuberculosisin families identified by genotyping. Chin Med J (Engl),2013,126(3):521-525. [64] Ahuja SD,Ashkin D,Avendano M,et al. Multidrug resistant pulmonary tuberculosis treatment regimens and patient outcomes: an individual patient data meta-analysis of 9 153 patients. PLoS Med,2012,9(8):e1001300. [65] Althomsons SP,Cegielski JP. Impact of second-line drug resistance on tuberculosis treatment outcomes in the United States: MDR-TB is bad enough. Int J Tuberc Lung Dis, 2012, 16(10): 1331-1334. [66] Amaral L. Thioridazine: an old neuroleptic effective against totally drug resisitant tuberculosis. Acta Med Port,2012,25(2):118-121. [67] Diacon AH, Dawson R, von Groote-Bidlingmaier F,et al. 14-day bactericidal activity of PA-824, bedaquiline, pyrazinamide, and moxifloxacin combinations:a randomised trial. Lancet,2012,380(9846):986-993. [68] Blöndal K,Viiklepp P,Gumundsson LJ,et al. Predictors of recurrence of multidrug-resistant and extensively drug-resis-tant tuberculosis. Int J Tuberc Lung Dis,2012,16(9):1228-1233. [69] Carroll MW, Lee M, Cai Y,et al. Frequency of adverse reactions to first- and second-line anti-tuberculosis chemotherapy in a Korean cohort. Int J Tuberc Lung Dis,2012,16(7):961-966. [70] Chang KC,Leung CC,Yew WW,et al. Pyrazinamide may improve fluoroquinolone-based treatment of multidrug-resistant tuberculosis. Antimicrob Agents Chemother,2012,56(11):5465-5475. [71] Cox H,Ford N. Linezolid for the treatment of complicated drug-resistant tuberculosis: a systematic review and meta-ana-lysis. Int J Tuberc Lung Dis,2012,16(4):447-454. [72] Curran A,Falcó V,Pahissa A,et al. Management of tuberculosis in HIV-infected patients. AIDS Rev,2012,14(4):231-246. [73] Decloedt EH,Maartens G,Smith P,et al. The safety, effectiveness and concentrations of adjusted lopinavir/ritonavir in HIV-infected adults on rifampicin-based antitubercular therapy. PLoS One,2012,7(3):e32173. [74] Diacon AH,Donald PR,Pym A,et al. Randomized pilot trial of eight weeks of bedaquiline (TMC207) treatment for multidrug-resistant tuberculosis: long-term outcome, tolerability, and effect on emergence of drug resistance. Antimicrob Agents Chemother,2012,56(6):3271-3276. [75] Gler MT,Podewils LJ,Munez N,et al. Impact of patient and program factors on default during treatment of multidrug-resistant tuberculosis. Int J Tuberc Lung Dis,2012,16(7):955-960. [76] Gler MT,Skripconoka V,Sanchez-Garavito E,et al. Delamanid for multidrug-resistant pulmonary tuberculosis. N Engl J Med,2012,366(23):2151-2160. [77] Harris T,Bardien S,Schaaf HS,et al. Aminoglycoside-induced hearing loss in HIV-positive and HIV-negative multidrug-resistant tuberculosis patients. S Afr Med J,2012,102(6 Pt 2);363-366. [78] Keshavjee S,Gelmanova IY,Shin SS,et al. Hepatotoxicity during treatment for multidrug-resistant tuberculosis: occurrence, management and outcome. Int J Tuberc Lung Dis,2012,16(5):596603. [79] Ahmad Khan F, Minion J, Al-Motairi A, et al. An updated systematic review and meta-analysis on the treatment of active tuberculosis in patients with HIV infection. Clin Infect Dis,2012,55(8):1154-1163. [80] Kim HJ,Kwak HK,Lee J,et al. Patterns of pncA mutations in drug-resistantMycobacteriumtuberculosisisolated from patients in South Korea. Int J Tuberc Lung Dis, 2012,16(1):98-103. [81] Koh WJ,Kang YR,Jeon K,et al. Daily 300 mg dose of linezolid for multidrug-resistant and extensively drug-resistant tuberculosis: updated analysis of 51 patients. J Antimicrob Chemo-ther,2012,67(6):1503-1507. [82] Kurbatova EV,Cavanaugh JS,Shah NS,et al. Rifampicin-resistantMycobacteriumtuberculosis:susceptibility to isoniazid and other anti-tuberculosis drugs. Int J Tuberc Lung Dis,2012,16(3):355-357. [83] Kurbatova EV,Taylor A,Gammino VM,et al. Predictors of poor outcomes among patients treated for multidrug-resistant tuberculosis at DOTS-plus projects.Tuberculosis (Edinb),2012,92(5):397-403. [84] Lee M,Lee J,Carroll MW, et al. Linezolid for treatment of chronic extensively drug-resistant tuberculosis. N Engl J Med,2012,367(16):1508-1518. [85] Manosuthi W,Mankatitham W,Lueangniyomkul A,et al. Time to initiate antiretroviral therapy between 4 weeks and 12 weeks of tuberculosis treatment in HIV-infected patients: results from the TIME study. J Acquir Immune Defic Syndr,2012,60(4):377-383. [86] Mitchison D, Davies G.The chemotherapy of tuberculosis: past, present and future. Int J Tuberc Lung Dis, 2012, 16(6):724-732. [87] Mukinda FK,Theron D,van der Spuy GD,et al. Rise in rifampicin-monoresistant tuberculosis in Western Cape, South Africa. Int J Tuberc Lung Dis,2012,16(2):196-202. [88] Oudijk JM,McIlleron H,Mulenga V,et al. Pharmacokinetics of nevirapine in HIV-infected children under 3 years on rifampicin-based antituberculosis treatment. AIDS,2012,26(12):1523-1528. [89] Palacios E,Franke M,Muoz M,et al. HIV-positive patients treated for multidrug-resistant tuberculosis: clinical outcomes in the HAART era. Int J Tuberc Lung Dis,2012,16(3):348-354. [90] Payen MC,De Wit S,Martin C,et al. Clinical use of the meropenem-clavulanate combination for extensively drug-resistant tuberculosis. Int J Tuberc Lung Dis,2012,16(4):558-560. [91] Pierre-Audigier C,Surcouf C,Cadet-Daniel V,et al. Fluoroquinolone and pyrazinamide resistance in multidrug-resistant tuberculosis. Int J Tuberc Lung Dis,2012,16(2):221-223, i-ii. [92] Ramkissoon S,Mwambi HG,Matthews AP. Modelling HIV and MTB co-infection including combined treatment strategies. PLoS One,2012,7(11):e49492. [93] Rey-Jurado E,Tudó G,Martínez JA,et al. Synergistic effect of two combinations of antituberculous drugs againstMycobacte-riumtuberculosis. Tuberculosis (Edinb),2012,92(3):260-263. [94] Rose PC,Hallbauer UM,Seddon JA,et al. Linezolid-containing regimens for the treatment of drug-resistant tuberculosis in South African children. Int J Tuberc Lung Dis,2012,16(12):1588-1593. [95] Satti H,Mafukidze A,Jooste PL,et al. High rate of hypothyroidism among patients treated for multidrug-resistant tuberculosis in Lesotho. Int J Tuberc Lung Dis,2012,16(4):468-472. [96] Satti H,McLaughlin MM,Hedt-Gauthier B,et al. Outcomes of multidrug-resistant tuberculosis treatment with early initiation of antiretroviral therapy for HIV co-infected patients in Leso-tho. PLoS One,2012,7(10):e46943. [97] Sotgiu G,Centis R,D’Ambrosio L,et al. Efficacy, safety and tolerability of linezolid containing regimens in treating MDR-TB and XDR-TB: systematic review and meta-analysis. Eur Respir J,2012,40(6):1430-1442. [98] Winston CA,Mitruka K. Treatment duration for patients with drug-resistant tuberculosis, United States. Emerg Infect Dis, 2012,18(7): 1201-1202. [99] World Health Organization. Global tuberculosis report 2012. WHO/HTM/TB/2012.6. Geneva: World Health Organization, 2012. [100] World Health Organization. WHO policy on collaborative TB/HIV activities:Guidelines for national programmes and other stakeholders. WHO/HTM/HIV/2012.1. Geneva:World Health Organization,2012. [101] Abdool Karim SS,Naidoo K,Grobler A, et al. Integration of antiretroviral therapy with tuberculosis treatment. N Engl J Med, 2011, 365(16):1492-1501. [102] Baghaei P,Tabarsi P,Dorriz D,et al. Adverse effects of multidrug-resistant tuberculosis treatment with a standardized regimen: a report from Iran. Am J Ther,2011,18(2):e29-34. [103] Bonnet M,Pardini M,Meacci F,et al. Treatment of tuberculosis in a region with high drug resistance: outcomes, drug resistance amplification and re-infection. PLoS One,2011,6(8):e23081. [104] Chang KC,Yew WW,Zhang Y. Pyrazinamide susceptibility testing inMycobacteriumtuberculosis: a systematic review with meta-analyses. Antimicrob Agents Chemother,2011,55(10):4499-4505. [105] da Silva PE,Von Groll A,Martin A,et al. Efflux as a mechanism for drug resistance inMycobacteriumtuberculosis. FEMS Immunol Med Microbiol,2011,63(1):1-9. [106] Dauby N,Muylle I,Mouchet F,et al. Meropenem/clavulanate and linezolid treatment for extensively drug-resistant tuberculosis. Pediatr Infect Dis J,2011, 30(9):812-813. [107] Dutta NK,Mazumdar K,Dastidar SG,et al. New patentable use of an old neuroleptic compound thioridazine to combat tuberculosis: a gene regulation perspective. Recent Pat Antiinfect Drug Discov,2011,6(2):128-138. [108] Falzon D,Jaramillo E,Schünemann HJ,et al. WHO guidelines for the programmatic management of drug-resistant tuberculosis: 2011 update. Eur Respir J,2011,38(3):516-528. [109] Garazzino S,Tovo PA. Clinical experience with linezolid in infants and children. J Antimicrob Chemother,2011,66 Suppl 4:iv23-iv41. [110] Havlir DV,Kendall MA,Ive P, et al. Timing of antiretroviral therapy for HIV-1 infection and tuberculosis. N Engl J Med,2011,365(16):1482-1491. [111] Isaakidis P,Cox HS,Varghese B,et al. Ambulatory multi-drug resistant tuberculosis treatment outcomes in a cohort of HIV-infected patients in a slum setting in Mumbai, India. PLoS One,2011,6(12):e28066. [112] Jacobson KR,Theron D,Victor TC,et al.Treatment outcomes of isoniazid-resistant tuberculosis patients, Western Cape Province, South Africa. Clin Infect Dis,2011,53(4):369-372. [113] Joseph P,Desai VB,Mohan NS,et al. Outcome of standardi-zed treatment for patients with MDR-TB from Tamil Nadu, India. Indian J Med Res,2011,133:529-534. [114] Lai CC,Tan CK,Huang YT,et al. Isoniazid-resistant tuberculosis, Taiwan, 2000—2010.Emerg Infect Dis,2011,17(9):1769-1770. [115] Lee J,Lee CH,Kim DK,et al. Retrospective comparison of levofloxacin and moxifloxacin on multidrug-resistant tuberculosis treatment outcomes. Korean J Intern Med,2011,26(2):153-159. [116] Liu CH,Li L,Chen Z,et al. Characteristics and treatment outcomes of patients with MDR and XDR tuberculosis in a TB referral hospital in Beijing: a 13-year experience. PLoS One,2011,6(4):e19399. [117] Pascopella L,Deriemer K,Watt JP,et al. When tuberculosis comes back: who develops recurrent tuberculosis in California? PLoS One,2011,6(11):e26541. [118] Sarkar S,Suresh MR. An overview of tuberculosis chemotherapy-a literature review. J Pharm Pharm Sci,2011,14(2):148-161. [119] Tangg SJ,Zhang Q,Zheng LH, et al. Efficacy and safety of linezolid in the treatment of extensively drug resistant tuberculosis. Jpn J Infect Dis,2011,64(6):509-512. [120] Shi W,Zhang X,Jiang X,et al. Pyrazinamide inhibits trans-translation inMycobacteriumtuberculosis. Science,2011,333(6049):1630-1632. [121] Sturdy A,Goodman A,José RJ,et al. Multidrug-resistant tuberculosis (MDR-TB) treatment in the UK: a study of injec-table use and toxicity in practice. J Antimicrob Chemother,2011,66(8):1815-1820. [122] Tabarsi P,Chitsaz E,Tabatabaei V,et al. Revised Category Ⅱ regimen as an alternative strategy for retreatment of Category Ⅰ regimen failure and irregular treatment cases. Am J Ther,2011,18(5):343-349. [123] Tang S,Zhang Q,Yu J,et al. Extensively drug-resistant tuberculosis at a tuberculosis specialist hospital in Shanghai, China: clinical characteristics and treatment outcomes. Scand J Infect Dis,2011,43(4):280-285. [124] Udwadia ZF,Sen T,Pinto LM. Safety and efficacy of thioridazine as salvage therapy in Indian patients with XDR-TB. Recent Pat Antiinfect Drug Discov,2011,6(2):88-91. [125] Veziris N,Truffot C,Mainardi JL,et al. Activity of carbape-nems combined with clavulanate against murine tuberculosis. Antimicrob Agents Chemother, 2011,55(6):2597-2600. [126] World Health Organization. Guidelines for the programmatic management of drug-resistant tuberculosis 2011 update. WHO/HTM/TB/2011.6. Geneva:World Health Organization, 2011. [127] World Health Organization. Rapid implementation of the Xpert MTB/RIF diagnostic test. WHO/HTM/TB/2011.2. Geneva:World Health Organization, 2011. [129] Alffenaar JW,van Altena R,Harmelink IM,et al. Comparison of the pharmacokinetics of two dosage regimens of line-zolid in multidrug-resistant and extensively drug-resistant tuberculosis patients. Clin Pharmacokinet,2010,49(8):559-565. [130] Amaral L,Boeree MJ,Gillespie SH,et al.Thioridazine cures extensively drug-resistant tuberculosis (XDR-TB) and the need for global trials is now! Int J Antimicrob Agents,2010,35(6):524-526. [131] Bloss E,Kuksa L,Holtz TH,et al. Adverse events related to multidrug-resistant tuberculosis treatment, Latvia, 2000—2004. Int J Tuberc Lung Dis,2010,14(3):275-281. [132] Caminero JA,Sotgiu G,Zumla A,et al. Best drug treatment for multidrug-resistant and extensively drug-resistant tuberculosis. Lancet Infect Dis,2010,10(9):621-629. [133] Dhillon J,Andries K,Phillips PP,et al. Bactericidal activity of the diarylquinoline TMC207 againstMycobacteriumtuberculosisoutside and within cells.Tuberculosis (Edinb),2010,90(5):301-305. [134] Gupta R,Lavollay M,Mainardi JL,et al. TheMycobacteriumtuberculosisprotein LdtMt2 is a nonclassical transpeptidase required for virulence and resistance to amoxicillin. Nat Med,2010,16(4):466-469. [135] Hsu HL,Bai KJ,Chiang YC,et al. Hepatitis associated with prothionamide for treatment of multidrug-resistant tuberculosis. J Formos Med Assoc,2010,109(12):923-927. [136] Jacobson KR,Tierney DB,Jeon CY,et al. Treatment outcomes among patients with extensively drug-resistant tuberculosis: systematic review and meta-analysis. Clin Infect Dis,2010,51(1):6-14. [137] Leung CC,Leung EC,Yew WW. Can some patients with multidrug-resistant tuberculosis be cured with shorter duration of chemotherapy?Am J Respir Crit Care Med,2010,182(12):1570. [138] British Thoracic Society Standards of Care Committee and Joint Tuberculosis Committee,Milburn H,Ashman N, et al. Guidelines for the prevention and management ofMycobacte-riumtuberculosisinfection and disease in adult patients with chronic kidney disease. Thorax,2010,65 (6):557-570. [139] Poissy J,Aubry A,Fernandez C,et al. Should moxifloxacin be used for the treatment of extensively drug-resistant tuberculosis? An answer from a murine model. Antimicrob Agents Chemother,2010,54(11):4765-4771. [140] Van Deun A,Maug AK,Salim MA,et al. Short, highly effective, and inexpensive standardized treatment of multidrug-resistant tuberculosis. Am J Respir Crit Care Med,2010,182(5):684-692. [141] World Health Organization. Antiretroviral therapy for HIV infection in adults and adolescents: recommendations for a public health approach. 2010 revision.WHO.Geneva:World Health Organization, 2010. [142] World Health Organization. Treatment of tuberculosis: guidelines. 4th ed. WHO/HTM/TB/2009.420. Geneva: World Health Organization,2010. [143] Chikamatsu K,Mizuno K,Yamada H,et al. Cross-resistance between rifampicin and rifabutin among multi-drug resistantMycobacteriumtuberculosisstrains [Article in Japanese]. Kekkaku,2009,84(9):631-633. [144] Diacon AH,Pym A,Grobusch M,et al. The diarylquinoline TMC207 for multidrug-resistant tuberculosis. N Engl J Med,2009,360(23):2397-2405. [145] Jenny-Avital ER,Joseph K. Rifamycin-resistantMycobacte-riumtuberculosisin the highly active antiretroviral therapy era: a report of 3 relapses with acquired rifampin resistance following alternate-day rifabutin and boosted protease inhibitor therapy. Clin Infect Dis,2009,48(10):1471-1474. [146] Orenstein EW, Basu S, Shah NS,et al. Treatment outcomes among patients with multidrug-resistant tuberculosis: systematic review and meta-analysis. Lancet Infect Dis,2009,9(3):153-161. [147] Richardson ET,Lin SY,Pinsky BA,et al. First documentation of isoniazid reversion inMycobacteriumtuberculosis. Int J Tuberc Lung Dis,2009, 13(11):1347-1354. [148] Sweetman SC. Martindale:the complete drug reference. 36th ed. London: Pharmaceutical Press,2009:207,248,347. [149] Nuermberger E,Tyagi S,Tasneen R,et al. Powerful bactericidaland sterilizing activity of a regimen containing PA-824, moxifloxacin, and pyrazinamide in a murine model of tuberculosis.Antimicrob Agents Chemother,2008,52(4):1522-1524. [150] Katiyar SK,Bihari S,Prakash S,et al. A randomised controlled trial of high-dose isoniazid adjuvant therapy for multidrug-resistant tuberculosis. Int J Tuberc Lung Dis,2008,12(2):139-145. [151] Koul A,Vranckx L,Dendouga N,et al. Diarylquinolines are bactericidal for dormant mycobacteria as a result of disturbed ATP homeostasis. J Biol Chem, 2008,283(37):25273-25280. [152] World Health Organization.Guidelines for the programmatic management of drug-resistant tuberculosis: emergency update 2008. WHO/HTM/TB/2008.402. Geneva:World Health Organization, 2008. (本文编辑:郭萌 薛爱华) 10.3969/j.issn.1000-6621.2015.05.001 100710 北京,中国防痨协会 肖和平,Email:xiaoheping_sars@163.com 2015-03-06)






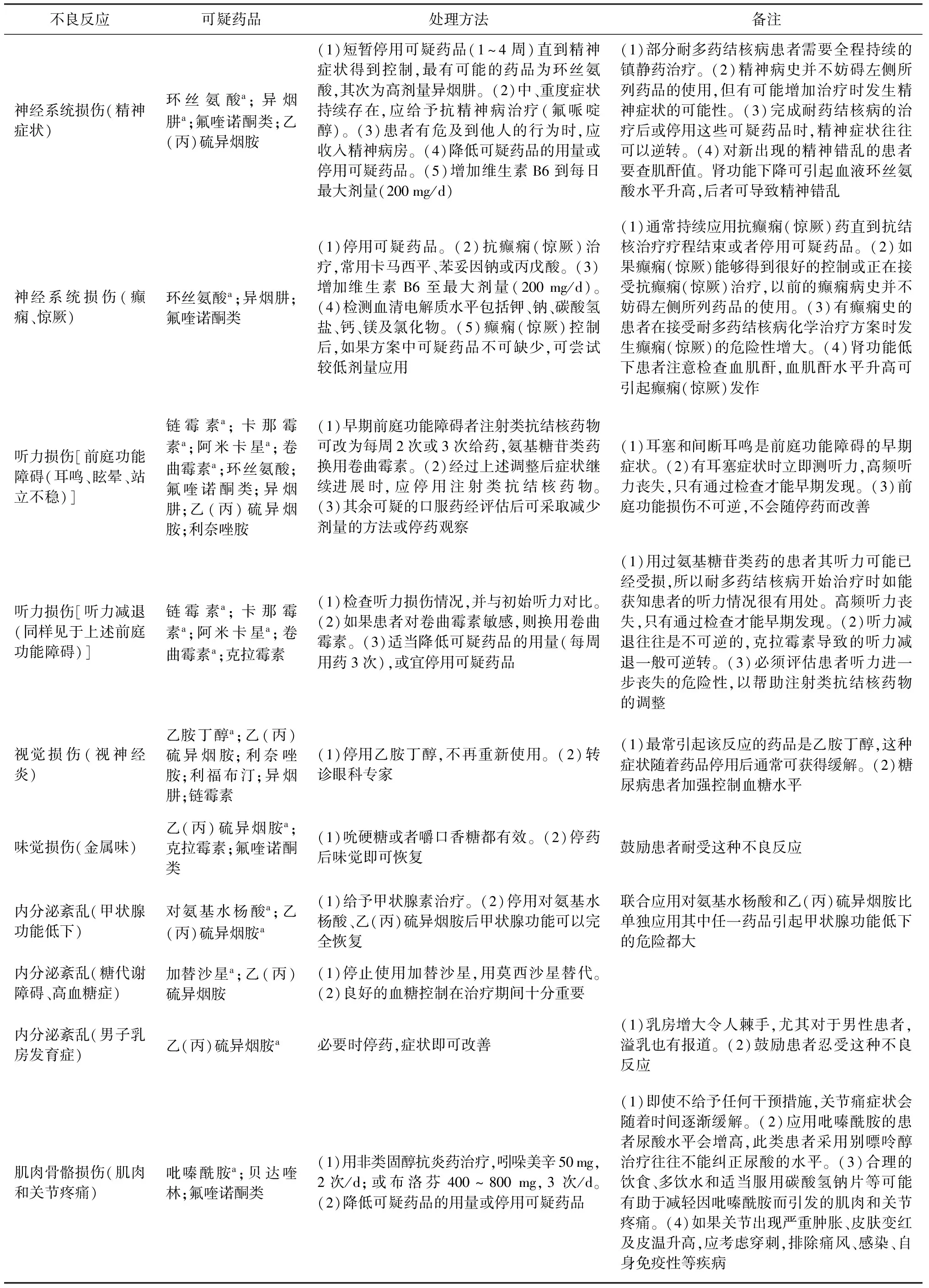


耐药结核病的化学治疗方案

耐药结核病化学治疗方案的调整
耐药结核病化学治疗的转归
耐药结核病患者化学治疗的管理
