季铵化壳聚糖胰岛素纳米粒的制备、处方优化及其初步药效学实验
2015-05-15王美玲崔黎丽第二军医大学药学院无机化学教研室基础部数理教研室海军医学系上海200433
苑 旺,王美玲,石 岩,崔黎丽(第二军医大学 .药学院无机化学教研室,.基础部数理教研室,.海军医学系,上海 200433)
・论著・
季铵化壳聚糖胰岛素纳米粒的制备、处方优化及其初步药效学实验
苑 旺a,王美玲b,石 岩c,崔黎丽a(第二军医大学 a.药学院无机化学教研室,b.基础部数理教研室,c.海军医学系,上海 200433)
目的采用正交设计试验优化载胰岛素季铵化壳聚糖纳米粒的处方工艺,并初步考察其降糖效果。方法 用离子交联法制备载胰岛素的季铵化壳聚糖纳米粒,用正交试验确定其最佳处方工艺。用透射电子显微镜观察纳米粒的表面形态;用粒径/Zeta电位仪测定纳米粒的粒径和Zeta电位;用高效液相色谱(HPLC)法测定纳米粒的包封率、载药量及体外释放情况。对糖尿病大鼠皮下注射给药,对其药效学进行初步考察。结果制得的纳米粒呈球形,分布均匀;平均粒径(63.26± 1.88)nm;Zeta电位(33.1±0.3)mV;包封率(37.92±2.11)%;载药量(5.42±0.3)%;24 h累计释放率63.83%。皮下注射给药8 h,糖尿病大鼠血糖较单纯注射胰岛素组下降平缓,且药效持久。结论优化后的载胰岛素的季铵化壳聚糖纳米粒形态较好、粒径较小,为研究胰岛素的新型给药途径奠定了基础。
胰岛素;纳米粒;离子交联法;正交设计
糖尿病是常见的内分泌系统代谢疾病。根据国际糖尿病联盟(IDF)公布的新版全球“糖尿病地图”可以看出,随着人们生活水平的提高,糖尿病的发病率逐年上升,糖尿病患者的治疗费用给社会经济带来巨大负担,糖尿病并发症对人类健康构成严重威胁[1]。我国已经是世界上糖尿病患病人数最多的国家。
胰岛素是一种具有降血糖作用的体内激素[2],注射胰岛素是临床上治疗糖尿病的重要手段之一,但是长期注射胰岛素会导致患者给药部位产生炎症,且常伴有低血糖等不良反应,给患者带来痛苦。经皮给药系统是一种无创给药方式,具有缓控释等优点,且皮肤内酶的活性较低,是胰岛素经皮给药的理想方式。但是,胰岛素属于大分子(分子量5 800)蛋白类药物,很难自然透过皮肤致密的角质层结构。因此,寻找一种合适的载体材料将胰岛素包载于纳米粒中,并与其他促渗方法结合,可以有效提高胰岛素的经皮吸收率。
壳聚糖是甲壳素脱乙酰基而得到的产物,是一种天然的聚阳离子多糖,具有黏膜吸附性、生物相容性、生物可降解性等特点,且已有报道壳聚糖具有促进药物经皮转运的作用。但是,壳聚糖水溶性较差,限制了其广泛应用,而季铵化壳聚糖较好地克服了壳聚糖的这一局限性,具有较好的水溶性,且保留了壳聚糖的优点,是一种较好的载体材料。
本研究以胰岛素为模型药物,季铵化壳聚糖为载体材料,三聚磷酸钠为交联剂,采用离子交联法制备载胰岛素的季铵化壳聚糖纳米粒(INS-NPs),对其进行处方优化及表征。并初步考察其降血糖效果,为胰岛素的经皮给药探寻新的思路和方法。
1 仪器与材料
1.1 仪器 高效液相色谱(HPLC)仪(LC-2010A,日本岛津公司);C18柱(250 mm×4.6 mm,5μm,迪马公司);FA2004B电子天平(上海精科天美科学仪器有限公司);JB-3型定时恒温磁力搅拌器(上海雷磁新泾仪器有限公司);高速离心机(上海安亭科学仪器厂);DL-120超声洗瓶器(浙江石浦海天电子仪器厂);Zetasizer nano ZS粒径/Zeta电位测定仪(英国MALVERN公司);血糖仪(One Touch○R U tra EasyTM,美国强生公司);JEM-1230透射电子显微镜(日本电子株式会社)。
1.2 材料 羟丙基三甲基氯化铵壳聚糖(南通绿神生物工程有限公司,取代度97.2%);猪胰岛素(徐州万邦制药有限公司);链脲佐菌素(美国Sigma公司);三聚磷酸钠、氢氧化钠、磷酸二氢钾、冰醋酸、磷酸、无水硫酸钠(分析纯,均购自国药集团化学试剂有限公司);乙腈、甲醇(高效液相纯,均购自国药集团化学试剂有限公司);雄性SD大鼠(220±10)g(第二军医大学实验动物中心)。
2 实验方法
2.1 INS-NPs的制备[4]以季铵化壳聚糖为载体材料,胰岛素为模型药,三聚磷酸钠为交联剂,采用离子交联法制备INS-NPs。分别配制一定浓度的季铵化壳聚糖醋酸溶液和一定浓度的三聚磷酸钠水溶液。将一定量的季铵化壳聚糖溶液与一定量的胰岛素溶液混合,磁力搅拌30 m in,滴加一定量的三聚磷酸钠溶液,继续搅拌30 min,即得。
2.2 INS-NPs的处方优化 按照L9(34)正交设计表,3个因素分别为季铵化壳聚糖浓度(A)、三聚磷酸钠浓度(B)、壳聚糖与三聚磷酸钠体积比(V∶V)(C),研究它们对胰岛素纳米粒的粒径和包封率的影响,各因素水平见表1。

表1 正交试验的因素与水平
采用综合评分法,粒径和包封率权重系数均为0.5,以包封率最大值和粒径最小值分别为100分对每一组数据进行综合评分,应用统计分析软件SPSS18.0对实验数据进行方差分析。
2.3 载药纳米粒的表征 按照最优处方和工艺,平行制备3批载胰岛素季铵化壳聚糖纳米粒,对纳米粒进行表征。
2.3.1 形态学考察 采用JEM-1230透射电子显微镜观察纳米粒的表面形态。
2.3.2 粒径和电位 纳米粒混悬液经0.45μm微孔滤膜过滤后,使用马尔文电位粒径仪测定纳米粒的粒径和Zeta电位。
2.4 载药纳米粒中胰岛素含量的测定
2.4.1 色谱条件 HPLC仪(岛津LC-2010AHT),C18色谱柱(250 mm×4.6 mm,5μm,迪马公司),流动相:0.2 mol/L无水硫酸钠溶液(pH=2.3)-乙腈(76∶24),检测波长:214 nm,流速:1 m l/min,柱温:30℃,进样量:10μl。
2.4.2 胰岛素标准曲线的绘制 精确配制500μg/m l胰岛素溶液作为储备液。分别精密吸取胰岛素储备液200、500、1 000、1 500、2 000、2 500、3 000μl于10 m l容量瓶中,用pH=7.4的PBS缓冲液稀释定容至刻度,即得系列浓度胰岛素溶液。按照“2.4.1”色谱条件进样,测定记录胰岛素峰面积,以胰岛素峰面积为纵坐标,胰岛素浓度为横坐标,线性回归,得到胰岛素定量标准曲线。
2.4.3 包封率的测定 取新鲜制备的纳米粒混悬液1 m l,高速离心机在转速12 000 r/min条件下离心30 m in,以分离未包裹的胰岛素,收集上清溶液。胰岛素含量用HPLC法测定,计算纳米粒包封率(entrapped efficiency,EE)和载药量:
EE(%)=(投入胰岛素总量-上清液中游离胰岛素量)/投入胰岛素总量×100%
2.5 胰岛素纳米粒的体外释放实验 取新鲜制备的胰岛素纳米粒混悬液,置于37℃恒温摇床中,以80 r/min速度振荡,于0、1、2、4、6、8、10、12和24 h取出,离心,取上清液,用HPLC法测定释放介质中胰岛素的含量,确定载胰岛素季铵化壳聚糖纳米粒的体外释放曲线。
2.6 降血糖作用
2.6.1 糖尿病大鼠模型的建立 SD雄性大鼠,体重(220±10)g,腹腔注射链脲佐菌素溶液(60 mg/kg),1周后于大鼠尾静脉采血,测定血糖含量,取连续2次测量血糖水平均≥18 mmol/L者,即为糖尿病大鼠模型。
2.6.2 实验分组 随机选取6只正常大鼠作为空白对照组(皮下注射PBS)。将“2.6.1”项下准备的糖尿病大鼠随机分为3组:实验对照组(皮下注射PBS)、胰岛素溶液组(皮下注射胰岛素)、纳米粒组(皮下注射纳米粒混悬液),每组6只,分别于0.5、1.0、1.5、3.0、4.5、6.0和8.0 h尾静脉采血,测定血糖含量。
3 实验结果
3.1 INS-NPs的处方优化 正交试验结果见表2。评分规则采用参考文献[5]进行评分。

表2 正交试验结果(n=3)
包封率:以9组试验最高包封率(EEmax)组为100分,最低包封率(EEmin)组为0分,其余各组依下式计算得分:包封率评分=100-100×(EEmax-包封率)/(EEmax-EEmin)。
粒径:以9组试验最大粒径(Dmax)组为0分,最小粒径(Dm in)组为100分,其余各组依下式计算得分:粒径评分=100×(粒径-Dm in)/(Dmax-Dm in)。
由表3结果显示,各因素作用大小依次为C>A>B。壳聚糖浓度(A)、三聚磷酸钠浓度(B)、壳聚糖与三聚磷酸钠体积比(V∶V)(C)对于胰岛素纳米粒的粒径和包封率均有显著影响(P<0.05)。最终确定优化水平组合为A2 B1 C2,即在壳聚糖浓度为5.0 mg/m l,三聚磷酸钠浓度为0.5 mg/m l,两者体积比为2∶1的条件下,制得的纳米粒最佳。

表3 方差分析结果
3.2 纳米粒的表征
3.2.1 形态学考察 采用透射电子显微镜观察纳米粒的表面形态。从图1可以看出,纳米粒呈球形,大小适中,分布均匀。

图1 JEM-1230透射电镜(×80 000)观察纳米粒形态
3.2.2 粒径和电位 INS-NPs的平均粒径为(63.26±1.88)nm,如图2所示。Zeta电位(33.1±0.3)mV。
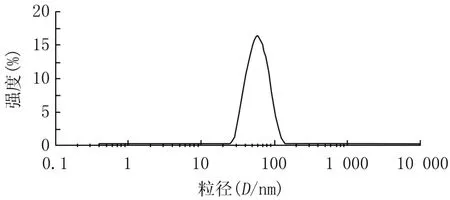
图2 胰岛素纳米粒的粒径分布
3.3 包封率的测定
3.3.1 标准曲线的绘制 按照“2.4.2”项下方法,以胰岛素峰面积(A)为纵坐标,胰岛素浓度(C)为横坐标,得到回归方程A=10 856 C-32 686,r=0.999 9,在10~150μg/m l的浓度区间内,线性关系较好(图3)。

图3 胰岛素定量的标准曲线
表4为胰岛素定量检测的日内、日间精密度结果。结果显示:日内精密度RSD<2%,日间精密度RSD<2%,符合药物分析日内精密度RSD<5%,日间精密度RSD<15%的要求。
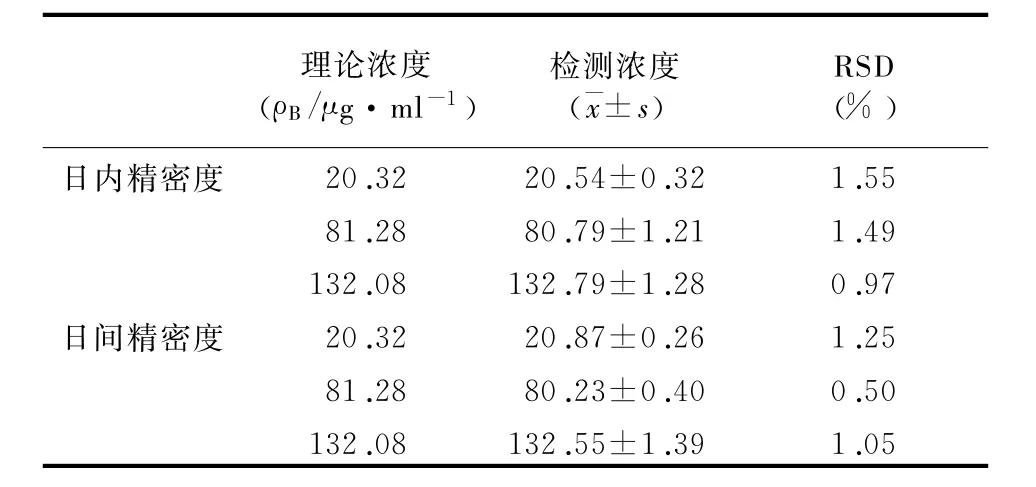
表4 胰岛素检测的日内和日间精密度(n=5)
3.3.2 包封率的测定 计算得到纳米粒的包封率为(37.92±2.11)%,载药量为(5.42±0.3)%。
3.4 胰岛素纳米粒的体外释放实验 由图4可以看出,纳米粒在前2 h释放率达到44.15%,24 h累计释放率63.83%。

图4 胰岛素纳米粒的体外释放曲线(n=3)
3.5 降糖实验 图5为糖尿病大鼠血糖浓度随时间变化曲线。结果显示,皮下注射给药后,实验对照组(PBS)大鼠的血糖值随着时间的推移变化不大,维持较高的血糖水平。胰岛素溶液组给药后,糖尿病大鼠血糖值迅速下降,并在1 h处出现极值,之后随着时间的推移,血糖水平逐渐回升。皮下注射胰岛素纳米粒组给药后,血糖值平缓下降,并随着时间推移,血糖水平维持在稳定水平。

图5 血糖浓度随时间的变化曲线
4 讨论
经皮给药方式给慢性病患者及需要反复给药的患者带来了便利,可以有效降低给药频率、改善患者依从性、维持血浆药物浓度稳定、避免肝脏首过效应、提高药物的生物利用度。因此,经皮给药是胰岛素给药的理想途径。将胰岛素包载于适当的载体材料中制备成纳米粒,可以有效改善经皮吸收率低这一问题。纳米粒具有包封率高、稳定性强以及体内特异性分布、缓控释等特点。因此,我们选用季铵化壳聚糖作为载体材料,三聚磷酸钠作为交联剂,采用离子交联法制备INS-NPs,并对其处方进行优化,筛选出粒径较小和包封率较高的纳米粒,为胰岛素的经皮转运奠定基础。采用正交设计试验和综合评分法,筛选得到季铵化壳聚糖浓度5.0 mg/m l、三聚磷酸钠浓度0.5 mg/m l、两者体积比2∶1为最佳处方。按照最佳处方制备出的纳米粒在体外释放实验中,2 h内释放率为44.12%,这可能是由于在纳米粒的制备过程中,部分胰岛素吸附在纳米粒表面,当纳米粒置于释放介质中时,胰岛素迅速溶解于介质中,因此产生突释现象;24 h累计释放率达63.83%,显示纳米粒对胰岛素溶液具有持续保护作用。考察其药效学结果显示,载胰岛素纳米粒可以很好地发挥降糖效果,与单纯注射胰岛素相比,显示出更加温和的药性。
综上所述,通过离子交联法制备的载胰岛素纳米粒具有较小的粒径,适合应用于经皮转运系统,且包封率较好,可有效发挥药效。在降糖实验中,糖尿病大鼠给药后2 h血糖迅速下降,达到正常血糖水平,之后大鼠血糖缓慢下降,并且长时间维持在正常血糖水平范围内,INS-NPs显示出较好的药效性能。这与载药纳米粒的体外释放度考察实验结果相吻合,这可能是由于在纳米粒制备过程中,部分胰岛素吸附在纳米粒表面,给药后迅速释放发挥药效,使糖尿病大鼠的血糖较快降至正常水平,之后持续缓慢释放,使血糖水平长时间稳定在正常范围。表明该法制备的纳米粒性质良好,可用于透皮吸收的研究,与其他促进药物经皮转运的手段相结合,将有效促进胰岛素经皮转运效率,这为胰岛素等大分子药物的经皮转运提出了新思路和新方法。
[1] UnwinN,GanD,Whiting D.The ID Fdiabetesatlas:providingevidence,raisingawareness and promotingaction[J].DiabetesResClinPract,2010,87(1):2-3.
[2] 韩丽娜,尹丽芳,赵月芳,等.胰岛素/维生素B12-透明质酸纳米粒的制备及口服给药体内外性质的评价[J].中山大学学报,2012,33(5):597-602.
[3] 欧 歌,廖德华,张 凯,等.采用离子交联法制备壳聚糖胰岛素纳米粒的研究进展[J].中南药学,2013,11(2):111-119.
[4] AvadiMR,Sadeghi AM,MohammadpourN,etal.Preparation and characterization of insulinnanoparticlesusingchitosan andarabicgumwithionicgelationmethod[J].Nanomedicine,2010,6(1):58-63.
[5] 曹 姗,胡凯莉,刘 梅,等.多西紫杉醇口服磷脂纳米粒的制备与处方优化[J].中成药,2013,35(9):1896-1900.
Preparation,formulation optim ization and prelim inary pharmacodynam ic experiment of insulin-loaded N-trimethyl chitosan nanoparticles
YUANWanga,WANG Meilingb,SH IYanc,CUILilia(a.Department of Inorganic Chemistry,School of Pharmacy;b.Department of Physics and Mathematics,College of Basic Medical Sciences;c.College of Naval Medicine,Second M ilitary Medical University,Shanghai200433,China)
ObjectiveTo prepare and optim ize insulin-loaded N-trimethyl chitosan nanoparticles via orthogonal design,and prelim inarily study the effects on blood glucose level.MethodsThe insulin-loaded N-trimethyl chitosan nanoparticles(INS-NPs)were prepared by ionic gelation,and the optimal proportionwas obtained with orthogonal design.The nanoparticles were characterized by transmission electronmicroscopy and zeta/sizer nano analyzer.The entrapmentefficiency of insulin-loaded nanoparticles and the in vitro releasing characteristicswere studied by HPLC.A preliminary pharmacodynamic study of the insulin-loaded nanoparticles was also carried out.ResultsThe INS-NPs exhibited narrow distribution.Themean diameter of INS-NPswas(63.26±1.88)nm,while the entrapment efficiency was(37.92±2.11)%.After 8 hours of subcutaneous injection of the INS-NPs,the blood glucose level in diabetic rats decreased to normal level and kept stable.ConclusionThe optimized insulin-loaded nanoparticles had homogeneous spherical shape,small size,and could be a new approach of administration for insulin.
insulin;nanoparticles;ionic gelation;orthogonal design
R943.44;R977.15
A
1006-0111(2015)04-0319-05
10.3969/j.issn.1006-0111.2015.04.008
2015-02-10
2015-06-02[本文编辑]顾文华
国家自然科学基金(No.51477175)
苑 旺,硕士研究生.E-mail:yuanwang1115@126.com
崔黎丽,本科,教授,硕士生导师.研究方向:物理药剂学.E-mail:cuilili39@hotmail.com
