奥沙利铂联合卡培他滨治疗晚期结肠癌40例
2015-05-02徐建民朱金元
徐建民,朱金元
(江苏省昆山市第一人民医院,江苏 苏州 215300)
结肠癌是最常见的恶性肿瘤,由于患者在诊断时多已处于晚期,化学治疗(简称化疗)成为最常规的治疗方法,临床需要寻找疗效好、不良反应少的化疗药物与治疗方案。笔者观察了奥沙利铂与卡培他滨联合应用对晚期结肠癌患者的疗效以及不良反应发生情况,现报道如下。
1 资料与方法
1.1 一般资料
选取2013年1月至2013年12月我院收治的晚期结肠癌患者80例,所有患者Karnofsky(KPS)评分≥60分,且化疗前心、肺、肝、肾等功能均正常,无化疗禁忌证。其中男56例,女24例;年龄37~75岁,平均(55.2±7.5岁);初治者 47例,复治者 33例;按病理类型分,腺癌60例,黏液腺癌8例,印戒细胞癌12例。将其随机均分为两组,各40例。两组患者性别、年龄、病理分型等资料比较,差异无统计学意义(P>0.05),具有可比性。
1.2 治疗方法
所有患者在化疗前均给予注射用盐酸雷莫司琼(商品名维意舒,湖南科伦制药有限公司,国药准字H20052678,规格为0.3mg)静脉滴注,用于止呕。对照组采用奥沙利铂联合5-氟尿嘧啶(5-FU)方案,第1天给予奥沙利铂注射液(商品名艾恒,江苏恒瑞医药股份有限公司,国药准字H 20050962,规格为每瓶0.1 g)130 mg /m2,静脉滴注 2 h,第 1,2,14 天给予氟尿嘧啶氯化钠注射液(商品名弗米特,山东齐都药业有限公司,国药准字H20020415,规格为250 mL∶氟尿嘧啶0.5 g与氯化钠2.25 g)1 000mg/m2静脉滴注24 h,均分别溶于5%葡萄糖注射液500mL,2周为1个疗程。试验组采用奥沙利铂联合卡培他滨方案,奥沙利铂药品规格型号、剂量和给药方式同对照组,同时每日给予卡培他滨片(商品名希罗达,上海罗氏制药有限公司,国药准字H20073024,规格为每片 0.5 g)2 500 mg/m2,分早晚 2 次饭后30 min口服,连续给药2周,停服1周,3周为1个疗程。
1.3 疗效判定标准
两组患者均经3个连续疗程后比较,参照世界卫生组织(WHO)制订的实体肿瘤疗效评价标准[1],将疗效分为完全缓解(CR)、部分缓解(PR)、稳定(SD)及进展(PD),总有效(RR)= CR+PR。不良反应参照WHO抗癌药物毒性分级标准,分为0~Ⅳ级。
1.4 统计学处理
使用SPSS 13.0软件进行统计学分析。计数资料行 χ2检验。P<0.05表示差异具有统计学意义。
2 结果
结果见表1和表2。两组均有部分患者出现不良反应,主要表现为感觉神经异常、口腔黏膜炎、白细胞减少、血小板减少、恶心呕吐、肝功能异常等。按照WHO抗癌药物毒性分级标准,本研究中患者出现的不良反应均为Ⅰ~Ⅱ级,无Ⅲ级及以上不良反应。
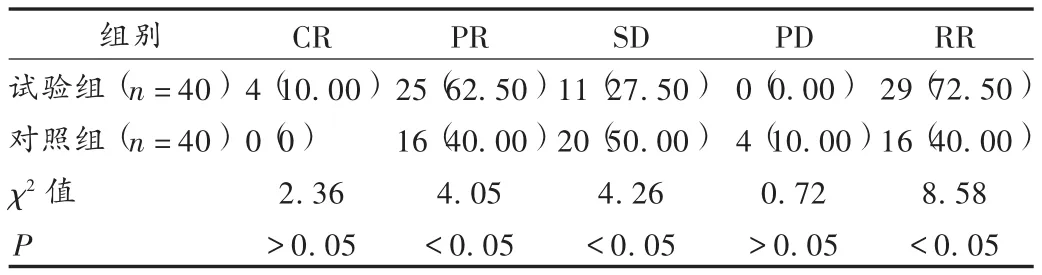
表1 两组患者临床疗效比较[例(%)]
3 讨论
结肠癌是一种威胁性极高的消化道恶性肿瘤,死亡率位居全世界第4,且目前发病率与死亡率仍呈上升趋势[2]。在发展中国家,受到环境、诊疗技术等方面的限制,80%以上的结肠癌患者确诊时已属晚期。目前,化疗仍是治疗结肠癌的主要手段,但复发率极高,复发后再次对该患者使用铂类药物,60%以上会产生耐药性[3],这也导致结肠癌 5 年整体生存率很低[4]。因此,克服化疗耐药性,寻找最佳靶向治疗结肠癌的方案,对于晚期以及复发性结肠癌的治疗具有非常重要的意义。

表2 两组患者不良反应发生情况比较[例(%)]
临床常规使用的化疗药物主要有铂类、5-FU及其衍生物和拓扑异构酶Ⅰ抑制剂。奥沙利铂属于第3代铂类化疗药物,能通过与肿瘤DNA共价结合,从而干扰肿瘤DNA复制,最终抑制肿瘤细胞增殖,促进其凋亡;其优势在于毒性较前两代铂类药物较小、水溶性高、抗瘤谱广、不良反应较轻等,且与顺铂耐药的肿瘤株无交叉耐药现象[5]。
卡培他滨是新一代口服氟尿嘧啶氟尿嘧啶类药物,它在经口服吸收后,可在肝脏内转化,在胸腺磷酸化酶(TP)的作用下转化为具有细胞毒性的5-FU,从而杀死细胞。由于肿瘤组织中TP活性通常较高,而正常组织中TP活性较低,因此正常组织受卡培他滨的影响就非常小,使药物的细胞毒作用具有一定的选择性和靶向性,并且降低了不良反应的发生[6]。
临床对肿瘤进行化疗时,考虑的因素除了疗效,毒性及副反应也是一个非常重要的影响因素[7]。因此,采用两种或多种药物综合治疗,可避免单一药物高服药剂量后带来的副反应强烈的影响,同时获得更好的治疗效果[8]。本试验结果显示,奥沙利铂与卡培他滨联合应用比奥沙利铂与5-氟尿嘧啶联合应用,显著提高晚期结肠癌的临床治疗效果,且不良反应出现较少,是一种安全、有效的治疗晚期结肠癌的化疗方案,为结肠癌临床治疗研究和药物应用提供了新思路。但仍需进一步对远期疗效和预后进行观察分析,以及对详细机制的探究。
参考文献:
[1]王吉林,唐洁婷,房静远.I-Ⅲ期结直肠癌患者围手术期肝脏局部化疗对术后肝转移及生率影响的Meta分析[J].中国癌症杂志,2010,20(8):615-616.
[2]Markowitz SD,BertagnolliMM.Molecular origins of cancer:Molecular basisof colorectal cancer[J].N Engl JMed,2009,361(1):2 449-2 460.
[3]陈永胜,丁璐璐,张永辉,等.江苏省启东市2001—2007年结直肠癌患者生存率分析[J]. 中国癌症杂志,2011,21(2):134-138.
[4]Voland C,Bord A,Péleraux A,et al.Repression of cell cycle-related proteins by oxaliplatin but not cisplatin in human colon cancer cells[J].Mol Cancer Ther,2006,5(9):2 149-2 157.
[5]郭东升,董柏年.卡培他滨联合奥沙利铂治疗恶性结、直肠肿瘤50例[J]. 中国药业,2012,21(7):52-53.
[6]章 峰.奥沙利铂联合卡培他滨治疗大肠癌120例[J].中国药业,2013,22(3):92-93.
[7]王运红.卡培他滨联合奥沙利铂治疗晚期结肠癌的疗效观察[J].海南医学院学报,2011,7(4):506-510.
[8]吴海静,张国楠.化疗的副反应及其防治[J].中国实用妇科与产科杂志,2008,24(9):667-669.
