HPLC法测定乳癖消结丸中丹参酮ⅡA、橙皮苷含量
2015-04-26张鹤,马宁
张 鹤,马 宁
(1.辽阳市食品药品检验所,辽宁 辽阳 111000;2.抚顺市中医院,辽宁 抚顺 113008)
HPLC法测定乳癖消结丸中丹参酮ⅡA、橙皮苷含量
张 鹤1,马 宁2
(1.辽阳市食品药品检验所,辽宁 辽阳 111000;2.抚顺市中医院,辽宁 抚顺 113008)
目的:建立乳癖消结丸中丹参酮ⅡA、橙皮苷高效液相含量测定方法。方法:色谱柱为Diamonsil C18(200mm×4.6mm,5μm),丹参酮ⅡA流动相:甲醇-水(75∶25),检测波长:270nm,流速:1mL/min,柱温:30℃;橙皮苷流动相为乙腈-0.2%磷酸溶液(21∶79),检测波长:284nm,流速:1mL/min,柱温:25℃。结果:丹参酮ⅡA进样量在0.040 3~0.403 2μg范围内与峰面积呈良好的线性关系,回归方程为:Y=3E+06X-38 932(r=0.999 7),平均回收率为96.4%,RSD为1.6%(n=6);橙皮苷进样量在0.115 7~0.694 2μg范围内与峰面积呈良好的线性关系,回归方程为:Y=787 926X-3 384.3(r=0.999 9),平均回收率为96.9%,RSD为0.9%(n=6)。结论:该方法可用于测定乳癖消结丸中丹参酮ⅡA及橙皮苷的含量,简便稳定、灵敏度高、重现性好,可作为有效控制该药物质量的参考指标。
乳癖消结丸;丹参酮ⅡA;橙皮苷;HPLC
乳癖消结丸为抚顺市中医院制剂,已用于临床多年,疗效确切,具有软坚散结、行气止痛的功效,主要用于治疗肝郁痰凝所致的乳腺内肿块、乳增生、乳癖、乳癌等症。该药物由丹参、青皮、牡蛎、鳖甲、穿山甲、川楝子、红花、青皮、延胡索、通草等十二味中药粉碎加炼蜜制成。目前,乳癖消结丸质量标准中仅有对丹参酮ⅡA及橙皮苷的TLC定性鉴别,且无含量测定标准,因此不能准确有效控制药品的质量。方中丹参活血调经、祛瘀止痛,青皮对于消除乳肿、乳核具有独特功效。本文对方中主药丹参及青皮中有效成分丹参酮ⅡA及橙皮苷有效成分进行含量测定[1-7],探讨更加准确、有效的药品质量控制方法,以保证药品质量稳定性,现具体报道如下。
1 仪器与试药
1.1 仪器
高效液相色谱仪LC-2010(日本岛津公司),LC-10AT vp输液泵;HS-3120型超声波清洗器,赛多利斯电子天平BP211-D。
1.2 试剂与试药
乳癖消结丸(辽阳市中医院制剂室,批号:20140306、20140521、20140615);丹参酮ⅡA对照品(批号:110766-200619,中国食品药品检定研究院),橙皮苷对照品(批号:110721-201316,含量95.3%,中国食品药品检定研究院)。甲醇、乙腈为色谱纯,水为二次蒸馏水。
2 方法与结果
2.1 丹参酮ⅡA含量测定
2.1.1 色谱条件 色谱柱为DiamonsilC18(200mm×4.6mm,5μm);流动相:甲醇-水(75∶25);检测波长:270nm;流速:1mL/min;柱温:30℃;进样量:10μL;理论塔板数按丹参酮ⅡA峰计算应不低于2 000。
2.1.2 溶液配制 ①对照品溶液制备。精密称取丹参酮ⅡA对照品适量,加甲醇制成0.2mg/mL的对照品储备液;精密量取对照品储备液2mL加甲醇定容至25mL容量瓶,制得16μg/mL的对照品溶液。
②供试品溶液制备。取本品适量,研细,精密称取1.0g,置具塞锥形瓶中,精密加入甲醇50mL,称重,冷浸2h,超声处理30min,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,作为供试品溶液。
③阴性对照溶液制备。取除丹参外的其他各味药材,按处方比例,粉碎,加炼蜜制成阴性对照样品,再按供试品溶液的制备方法制备阴性对照溶液。
2.1.3 系统适应性试验 对照品溶液、供试品溶液、阴性空白溶液各10μL,注入高效液相色谱仪测定。在上述色谱条件下,丹参酮ⅡA峰与其它色谱峰达到基线分离,阴性空白溶液无干扰。见图1。
2.1.4 线性范围考察 精密吸取“2.1.2”项对照品储备液0.5、1、2、3、4、5mL置于25mL棕色量瓶中,加甲醇稀释至刻度,分别制成4、8、16、24、32、40μg/mL的对照品溶液,各进样10μL。按上述色谱条件测定,记录色谱峰面积,以进样量(μg)为横坐标(X),色谱峰面积为纵坐标(Y),绘制标准曲线,结果表明进样量在0.040 3~0.403 2μg范围内线性关系良好,回归方程为:Y=3E+06X-38 932,r=0.999 7。
2.1.5 精密度试验考察 精密吸取对照品溶液10μL,注入液相色谱仪,连续进样6次,测定样品中丹参酮ⅡA色谱峰面积。测定结果RSD为0.92%,表明仪器精密度良好。
2.1.6 稳定性试验考察 精密吸取同一份供试品溶液,分别于配置后0、2、4、8、16、24h进样10μL,按“2.1.1”项色谱条件,测定样品中丹参酮ⅡA色谱峰面积。结果显示,RSD为0.87%,表明供试品溶液制备24h内稳定性良好。
2.1.7 重复性试验考察 取同一批次乳癖消结丸样品(批号:20140306)6份,按供试品溶液制备方法提取、制备,测定丹参酮ⅡA平均含量为0.42mg/g,RSD为1.0%。测定结果提示,该实验重复性良好。
2.1.8 加样回收率试验考察 取已知含量同一批号样品(批号:20140306)6份,每份约0.5g,精密称定,置具塞锥形瓶中,再分别精密加入0.224 0mg/mL(精密称取丹参酮ⅡA对照品11.20mg,加甲醇定容至50mL容量瓶)的丹参酮ⅡA对照品1mL,按“2.1.2”项方法配制供试品溶液,按“2.1.1”项色谱条件测定丹参酮ⅡA含量,计算回收率。结果显示,平均回收率为96.4%,RSD为1.6%(n=6)。见表1。

图1 丹参酮ⅡA HPLC色谱
2.1.9 样品测定 取3个不同批次样品,按供试品制备方法制备供试品溶液,按上述色谱条件,注入液相色谱仪,测定色谱峰面积。结果见表2。
2.2 橙皮苷含量测定
2.2.1 色谱条件 色谱柱为Diamonsil C18(200mm×4.6mm,5μm);流动相:乙腈-0.2%磷酸溶液(21∶79);检测波长:284nm;流速:1mL/min;柱温:25℃;进样量:10μL;理论塔板数按橙皮苷峰计算应不低于2 000。
2.2.2 溶液的配制 ①对照品溶液制备。精密称取橙皮苷对照品适量,加甲醇制成0.2mg/mL的对照品储备液;精密量取对照品储备液2mL加甲醇定容至25mL容量瓶中,制得40μg/mL对照品溶液。
②供试品溶液制备。取本品适量,研细,精密称取0.2g,置具塞锥形瓶中,精密加入甲醇25mL,称重,冷浸2h,超声处理1h,放冷,称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,作为供试品溶液。
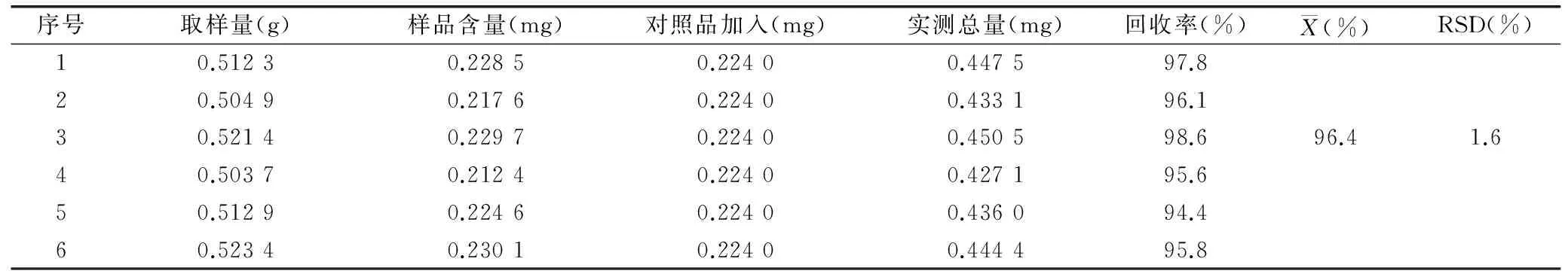
表1 丹参酮ⅡA加样回收率试验测定结果 (n=6)

表2 丹参酮ⅡA含量测定结果 (n=3,mg·g-1)
③阴性对照溶液制备。取除青皮外其他各味药材,按处方比例,粉碎加炼蜜制成阴性对照样品,按上述供试品溶液制备方法制成阴性对照溶液。
2.2.3 系统适应性试验 对照品溶液、供试品溶液、阴性空白溶液各10μL,注入高效液相色谱仪测定。在上述色谱条件下,橙皮苷峰与其他色谱峰达到基线分离,阴性空白溶液无干扰。见图2。

图2 橙皮苷 HPLC色谱
2.2.4 线性范围考察 精密吸取“2.2.2”项对照品储备液0.5、1、1.5、2、2.5、3mL置于10mL棕色量瓶中,加甲醇稀释至刻度,分别制成10、20、30、40、50、60μg/mL的对照品溶液,各进样10μL,按上述色谱条件测定,记录色谱峰面积,以进样量(μg)为横坐标(X),色谱峰面积为纵坐标(Y),绘制标准曲线,结果表明进样量在0.115 7~0.694 2μg范围内线性关系良好,回归方程为:Y=787 926X-3 384.3,r=0.999 9 。
2.2.5 精密度试验考察 精密吸取对照品溶液10μL,注入液相色谱仪,连续进样6次,测定样品中橙皮苷色谱峰面积。测定结果RSD为0.96%,表明仪器精密度良好。
2.2.6 稳定性试验考察 精密吸取同一份供试品溶液,分别于配置后0、2、4、8、16、24h进样10μL,按“2.2.1”项色谱条件,测定样品中橙皮苷色谱峰面积。测定结果RSD为0.92%,表明供试品溶液制备24h内稳定性良好。
2.2.7 重复性试验考察 取同一批次乳癖消结丸样品6份,按供试品溶液制备方法提取、制备、测定,橙皮苷平均含量为1.21mg/g ,RSD为1.10%。测定结果提示,该实验重复性良好。
2.2.8 加样回收率试验考察 取已知含量的同一批号样品(批号:20140306)6份,每份约0.1g,精密称定,置具塞锥形瓶中,分别精密加入0.604 2 mg/mL(精密称取橙皮苷对照品15.85mg,加甲醇定容至25mL)的橙皮苷对照品1mL,按“2.2.2”项方法配制供试品溶液,按“2.2.1”项色谱条件测定橙皮苷含量,计算回收率。结果显示,平均回收率为96.9%,RSD为0.9%(n=6)。见表3。
2.2.9 样品测定 取3个不同批次样品,按供试品制备方法制备供试品溶液,按上述色谱条件,注入液相色谱仪,测定色谱峰面积。结果见表4。
3 讨论
本实验对丹参酮ⅡA、橙皮苷成份冷浸后超声提取及直接超声提取方法进行考察,研究发现冷浸后超声提取含量较直接超声提取含量高,因此采用冷浸后超声提取。关于橙皮苷流动相的选择,比较不同比例的甲醇-磷酸和乙腈-磷酸溶液,研究发现甲醇-磷酸盐溶液会产生基线不稳,最终确定乙腈-磷酸溶液(21∶79)系统为流动相,该系统分离度和峰型均良好。
乳癖消结丸作为抚顺市中医院临床常用药,方中有效成分的含量可正面反映该制剂质量的优劣,因此应进行组方中药品成分含量的检测,更好地控制药物临床疗效及药品质量。
[1] 国家药典委员会.中华人民共和国药典[M].一部.北京:化学工业出版社,2010.
[2] 刘静,戴忠,王钢力,等.丹参活性成分及相关分离分析方法研究进展[J].中国实验方剂学杂志,2012,18(11):288-295
[3] 于百青,杨 敏,孙鹏云.高效液相色谱法测定心舒丸中丹参酮ⅡA含量[J].中国药业,2012,21(13):36-37.
[4] 吴德明,董茂臣,唐文君.高效液相色谱法测定乙肝扶正胶囊中丹参酮ⅡA的含量[J].黑龙江中医药,2012(2):49-50.
[5] 张瑞.HPLC法测定橘红片中橙皮苷和柚皮苷的含量[J].安徽医药,2013,17(3):401-402.
[6] 张维,张志云,礼彤,等.HPLC法同时测定冠脉康片中橙皮苷和芍药苷的含量 [J].辽宁中医药大学学报,2013,15(8):53-55.
[7] 刘玉春,张 静.HPLC同时测定橘红枇杷胶囊中橙皮苷、柚皮苷的含量[J].安徽医药,2013,17(12):2044-2045.
(责任编辑:李岚春)
Content Determination of TanshinoneⅡA and Hesperidin in Rupixiao Node Pills by HPLC method.
ZhanG He1, Ma Ning2
(1.Liaoyang Institute for Food and Drug Control, Liaoyang 111000,China;2.Fushun Hospital of Traditional Chinese Medicine,Fushun 113008,China)
Objective:To establish the content determination of tanshinoneⅡA and hesperidin in Rupixiao node pills by HPLC. Methods:The column was Diamonsil C18(200mm×4.6mm,μm), Tanshinone II A mobile phase was methanol-water (75∶25),detection wavelength was 270nm, flow rate was 1mL/min .The column temperature: 30 ℃. Hesperidin the mobile phase was 0.2% phosphoric acid solution (21∶79), detection wavelength was 284nm, flow rate was 1mL/min. The column temperature: 25℃.Results:Tanshinone IIA in 0.040 3μg~0.403 2μg showed a good linear relationship with the peak area range, The regression equation was: Y=3E+06X-38932(r=0.9997).The average recovery was 96.4%, with RSD of 1.6%(n=6). Hesperidin in 0.115 7~0.694 2μg showed a good linear relationship with the peak area range, The regression equation was: Y=787 926X -3 384.3(r=0.999 9).The average recovery was 96.9%, with RSD of 0.9%(n=6).Conclusion:The method was used to determine the content of nodes in Rupixiao pills of tanshinone A and hesperidin simple and stable, high sensitivity, good reproducibility, Can be used as reference for the effective control of the drug quality.
Rupixiao Node Pills; TanshinoneⅡA; Hesperidin; HPLC
2015-01-27
张鹤(1982-),女,辽宁省辽阳市食品药品检验所主管中药师,研究方向为中药检验及质量标准。E-mail:95137509@qq.com
R286.0
A
1673-2197(2015)12-0024-03
10.11954/ytctyy.201512010
