响应面法优化玉米芯预处理及酶解工艺的研究
2015-04-23杨盛茹侯丽芬丁长河马永生
杨盛茹,侯丽芬,丁长河,马永生
(1.河南牧业经济学院 食品系,河南 郑州 450044;2.郑州旅游职业学院,河南 郑州 450009;3.河南工业大学 粮油食品学院,河南 郑州 450001)
0 引言
第一代乙醇燃料由于以粮食作物为原料,被烙上“与人争食,与粮争地”的标签,现逐渐向以木质纤维素为生产原料的纤维素乙醇即第二代乙醇燃料发展[1].
在我国玉米是仅次于小麦的主要粮食作物,其种植面积居世界第二位[2],据中国国家统计局发布的数据显示,2014 年中国玉米产量为2.156 7 亿t,其加工副产物玉米芯年产量约为0.719 亿t.目前我国对玉米芯的加工使用比较少,大部分作为农家燃料直接被烧掉,造成环境污染和资源的极大浪费[3].
玉米芯主要由半纤维素、纤维素、木质素等构成,只有分解为可发酵性糖才可以转化为乙醇燃料.由于半纤维素、木质素对纤维素的包裹作用以及结晶纤维素本身复杂的结构特点,需对其进行一定的预处理以利于酶与底物反应,从而提高酶解速度和增加糖转化率[4].原料预处理工艺是木质纤维素原料资源利用最大化实现的关键,对整个生产的经济性有重大影响[5].研究证明,经石灰预处理的原料残渣中含有的大量氢氧化钙,与二氧化碳反应,生成的碳酸钙可用作饲料起到补钙的功效[6].
本研究利用氧化钙处理玉米芯,通过响应面法对预处理、酶解转化还原糖工艺进行优化,为玉米芯资源的开发利用提供依据,具有重要的生态效益和经济效益.
1 材料与方法
1.1 材料与试剂
玉米芯:无杂质、无霉变,产自郑州,晾晒干燥、粉碎过筛(直径4 mm)后存放备用.
氧化钙:分析纯,天津市科密欧化学试剂有限公司.
纤维素酶(10 000 U)、半纤维素酶(10 000 U):肇东日程酶制剂有限公司.
1.2 仪器与设备
旋转蒸发仪RE-52A:上海亚荣生化仪器厂;色谱柱:Waters Carbohydrate High Performance 4 μm×4.6 mm×250 mm;高效液相色谱:Waters 2695(配2420 蒸发光散射检测器和Empower Pro工作站).
1.3 试验方法
1.3.1 还原糖含量测定方法
酶解液中还原糖主要由葡萄糖、木糖组成,采用高效液相色谱(HPLC)法测定还原糖含量[7].
配制葡萄糖、木糖标准溶液,待测样品和标准溶液经过滤膜(0.22 μm)后用于HPLC 测定分析.
配制葡萄糖标准溶液:分别称取0.50 g、1.00 g、1.25 g、1.50 g 和2.00 g 葡萄糖于容量瓶(100 mL)中,加水定容.
配制木糖标准溶液:分别称取0.25 g、0.50 g、0.75 g、1.00 g 和1.25 g 木糖于容量瓶(100 mL)中,加水定容.
色谱分析操作参数如下.柱温:35 ℃;检测器温度:80 ℃;进样量:10 μL;流速:1.0 mL/min;氮气压力:25 PSI;流动相:乙腈/水,75/25(V/V).
1.3.2 氧化钙法预处理、酶解玉米芯工艺单因素试验
以氧化钙含量、浸泡时间、预处理时间、加酶量、酶解时间等进行单因素试验,确定影响玉米芯还原糖转化的适宜条件.
1.3.2.1 氧化钙含量的确定
称6 份玉米芯(4.00 g)于三角瓶(250 mL)中,按每克玉米芯依次添加0、25、50、75、100、125 mg氧化钙,分别加水(60 mL)混匀、45 ℃浸泡18 h、高温(121 ℃)处理1 h,然后调pH4.5,加入纤维素酶和半纤维素酶(固形物含量的5%,1∶1)于130 r/min、45 ℃的条件下水解72 h,以5 000 r/min 离心10 min,取上清液测还原糖含量.
1.3.2.2 浸泡时间的确定
称取6 份玉米芯(4.00 g)于三角瓶(250 mL)中,每克玉米芯添加100 mg 氧化钙,加水(60 mL)混匀、45 ℃分别浸泡0、6、12、18、24、30 h,高温(121 ℃)处理1 h,然后调pH4.5,加入纤维素酶和半纤维素酶(固形物含量的5%,1∶1)于130 r/min、45 ℃的条件下水解72 h,以5 000 r/min 离心10 min,取上清液测还原糖含量.
1.3.2.3 预处理时间的确定
称取6 份玉米芯(4.00 g)于三角瓶(250 mL)中,每克玉米芯添加100 mg 氧化钙,加水(60 mL)混匀、45 ℃浸泡18 h,高温(121 ℃)分别处理0、15、30、45、60、75 min,然后调pH4.5,加入纤维素酶和半纤维素酶(固形物含量的5%,1∶1)于130 r/min、45 ℃的条件下水解72 h,以5 000 r/min 离心10 min,取上清液测还原糖含量.
1.3.2.4 加酶量的确定
称取9 份玉米芯(4.00 g)于三角瓶(250 mL)中,每克玉米芯添加100 mg 氧化钙,加水(60 mL)混匀、45 ℃浸泡18 h、高温(121 ℃)处理1 h,然后调pH4.5,分别以固形物含量的1%、2%、3%、4%、5%、6%、7%、8%、9%加入纤维素酶和半纤维素酶(1∶1),于130 r/min、45 ℃的条件下水解72 h,以5 000 r/min 离心10 min,取上清液测还原糖含量.
1.3.2.5 酶解时间的确定
称取8 份玉米芯(4.00 g)于三角瓶(250 mL)中,每克玉米芯添加100 mg 氧化钙,加水(60 mL)混匀、45 ℃浸泡18 h、高温(121 ℃)处理1 h,后调pH4.5,加入纤维素酶和半纤维素酶(固形物含量的5%,1∶1)于130 r/min、45 ℃的条件下分别水解12、24、36、48、60、72、84、96 h,以5 000 r/min 离心10 min,取上清液测还原糖含量.
1.3.3 预处理、酶解工艺的响应面试验设计
在单因素试验的基础上,应用Design-Expert 7.0 软件,以还原糖转化量为响应值,通过响应面曲面分析[8],对玉米芯预处理、酶解工艺条件进行优化.
2 结果与讨论
2.1 氧化钙法预处理、酶解玉米芯工艺单因素试验结果分析
2.1.1 氧化钙含量对还原糖转化量的影响(图1)

图1 氧化钙含量对葡萄糖和木糖转化量的影响Fig.1 Effect of calcium oxide content on the conversion amount of glucose and xylose
从图1 可以看出,氧化钙加入量为0 mg/g 时,酶解液中葡萄糖和木糖含量最低;随着氧化钙加入量逐渐增大,葡萄糖、木糖转化量均明显增加,分别在氧化钙含量为75 mg/g、50 mg/g 时达到最大值,之后均有降低趋势.稀碱溶液中木质素和其他成分之间发生酯键皂化作用[9],降低纤维素结晶度,增加原料多孔性,利于后续酶解,但加入氧化钙量过高,产物还原糖的积累对纤维素酶、半纤维素酶有抑制作用[10],也会造成二者转化量降低.考虑总还原糖转化量,试验中选定氧化钙加入量为50 mg/g.
2.1.2 浸泡时间对还原糖转化量的影响(图2)

图2 浸泡时间对葡萄糖和木糖转化量的影响Fig.2 Effect of maceration time on the conversion amount of glucose and xylose
由图2 可知,在一定时间范围内,原料中还原糖降解量增加,酶解液中木糖、葡萄糖含量随浸泡时间延长而增大,当浸泡时间大于18 h 时总还原糖转化量并无显著增加,葡萄糖含量维持在130 mg/g 左右,木糖含量维持在115 mg/g 左右,所以选定浸泡时间为18 h.
2.1.3 预处理时间对还原糖转化量的影响(图3)
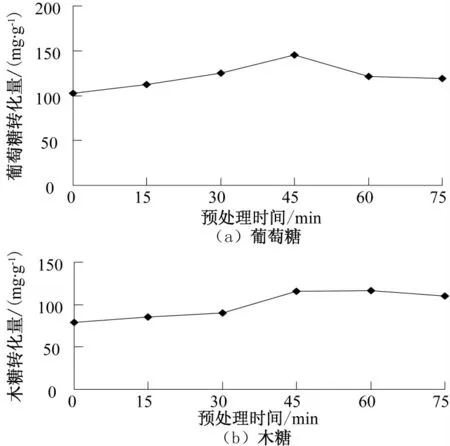
图3 预处理时间对葡萄糖和木糖转化量的影响Fig.3 Effect of pretreatment time on the conversion amount of glucose and xylose
从图3 可以看出,高温下处理玉米芯,其酶解液中葡萄糖和木糖的含量随着处理时间延长均呈现出先升高后降低的趋势,处理45 min 时木糖转化量接近于最大值,葡萄糖达到最大值145.6 mg/g.由于121 ℃下处理时间较长,糖类被分解为其他物质使得总还原糖含量降低[11],所以试验中确定预处理45 min.
2.1.4 加酶量对还原糖转化量的影响(图4)

图4 加酶量对葡萄糖和木糖转化量的影响Fig.4 Effect of enzyme dosages on the conversion amount of glucose and xylose
由图4 可知,加酶量不同,酶解液中葡萄糖、木糖含量均有显著变化.当加酶量低于7%时增加加酶量,二者都呈现明显上升趋势,其中葡萄糖含量增加尤为明显.当加酶量高于7%时,可能是纤维素酶、半纤维素酶与底物逐渐结合[12],还原糖转化量增加平缓.由于酶用量增加会增大生产成本,试验中选定加酶量为7%.
2.1.5 酶解时间对还原糖转化量的影响(图5)
从图5 可以看出,酶解时间较短时,酶解液中葡萄糖、木糖含量均随酶解进行逐渐增加,二者分别在60 h、72 h 时达到最大值,此后由于分解略有降低.考虑总还原糖转化量,选定酶解时间72 h.
2.2 响应面试验结果
在单因素试验的基础上,选取氧化钙含量、加酶量和酶解时间设计三因素三水平的响应面试验,试验方案及结果见表1、表2.

表1 响应面试验设计因素与水平Table 1 Factors and levels of response surface design
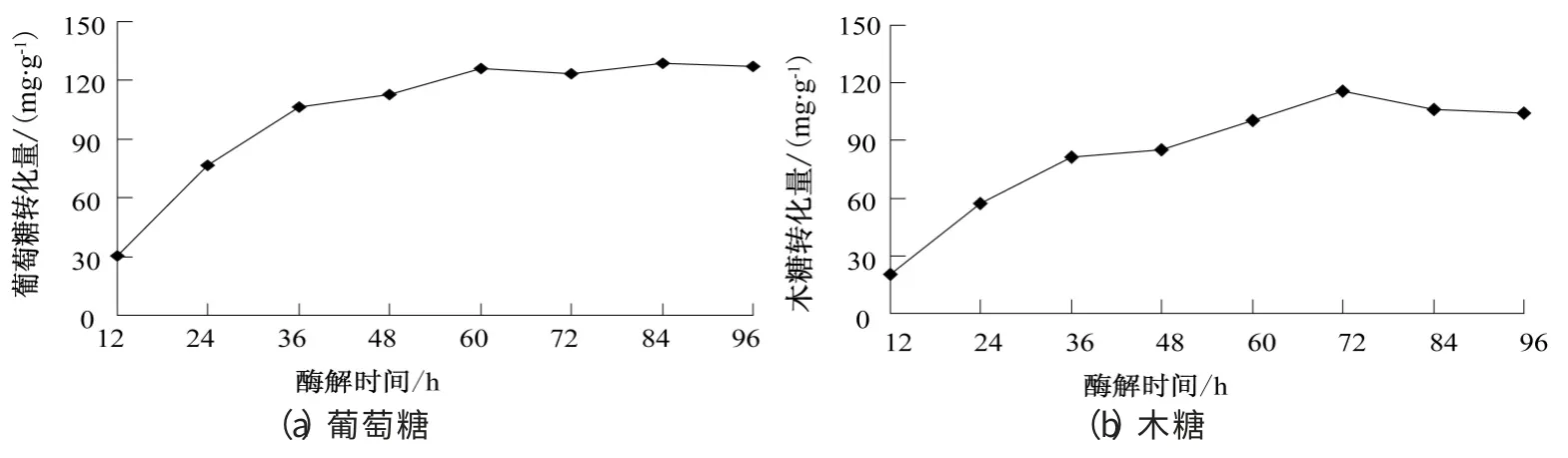
图5 酶解时间对葡萄糖和木糖转化量的影响Fig.5 Effect of enzymatic hydration time on the conversion amount of glucose and xylose

表2 响应面试验设计与结果Table 2 Experimental Design and results of response surface analysis
将表2 的数据通过软件Design-Expert 7.0 进行分析,结果见表3.从表3 可知,加酶量(Prob>F)<0.05,酶解时间(Prob>F)<0.05,二者对还原糖转化量影响显著.以酶解液中总还原糖转化量为响应值,各因素经回归拟合得到回归方程:
还原糖转化量=364.65 +9.67A +14.25B +18.30C-51.26A2-2.20B2-9.14C2+6.60AB-31.44AC-1.13BC.
根据方差分析结果,模型F 值58.18,其Prob>F=0.000 2,此值<0.05,极其显著.差拟项检验Prob>F=0.166 3,此值>0.05,不显著.R2(决定系数)=0.990 0.表明此模型充分拟合试验数据[13],此回归方程是玉米芯中还原糖转化各参数的合适数学模型,可用此方程确定玉米芯中还原糖转化的最佳预处理、酶解工艺.
根据回归方程做出了氧化钙含量、加酶量、酶解时间3 个试验因子的响应面分析图,图6 是响应值还原糖转化量对3 个试验因子所构成的三维空间的曲面图,可直观地看出各参数之间的相互作用和最佳参数.由图6 可看出,因素交互作用对还原糖转化量的影响,曲线越陡峭表明此因素对还原糖转化量影响越大,对应响应值的相应变化.其中酶解时间对总还原糖转化量影响最大,加酶量次之,酶解时间与氧化钙含量间的交互作用有一定的显著性,与表3 方差分析结果一致,酶解时间、加酶量和酶解时间与氧化钙含量的交互作用三者对应的Prob>F 值均小于0.05,都达到显著水平.

表3 方差分析Table 3 Variance analysis

图6 两因素交互作用对还原糖转化量的响应面和等高线Fig.6 Response surface and contour plots for the effect of operating parameters on the conversion amount of glucose and xylose
回归模型预测的预处理、酶解玉米芯转化还原糖的最佳工艺为氧化钙含量50.20 mg/g、加酶量8.00%、酶解时间80.36 h,还原糖转化量理论值为384.18 mg/g.将工艺条件修正为氧化钙含量50 mg/g、加酶量8%、酶解时间80 h 进行验证试验,还原糖转化量为385.85 mg/g,与理论值基本一致,证明工艺参数合理可靠,具有实用价值.
3 结论
碱处理是一种有效、实用的化学方法,其中石灰因价格低廉成为研究碱处理法和实际应用中的常用物质.以玉米芯为原料,在单因素试验基础上,采用响应面法对预处理、酶解工艺优化,拟合了氧化钙含量、加酶量、酶解时间这3 个因素对还原糖转化量的回归模型,分析研究因素显著性和交互作用强弱,得出还原糖转化的最佳工艺条件:氧化钙含量50 mg/g,浸泡时间18 h,121 ℃处理45 min,加酶量8%,酶解时间80 h,还原糖转化量为385.85 mg/g,为进一步研究玉米芯中还原糖提供了研究基础.
[1]Velmurugan Rajendran,Muthukumar Karuppan.Sono-assisted enzymatic saccharification of sugarcane bagasse for bioethanol production [J].Biochemical Engineering Journal,2012,63:1 -9.
[2]田亚红,常丽新,王丽萍,等.玉米秸秆、玉米芯发酵生产乙醇的研究[J].食品研究与开发,2014,35(3):47-50.
[3]姚笛,叶曼曼,李琳,等.响应面法优化玉米芯中低聚木糖的酶法提取工艺[J].中国粮油学报,2014,29(11):14-18.
[4]潘裕清,张宏嘉,邱学良,等.草酸预浸连续汽爆玉米芯制备木糖的模拟与中试研究[J].过程工程学报,2014,14(4):643-648.
[5]黄加军,杜金宝,闫莉,等.纤维素酒精预处理技术进展[J].酿酒,2013,40(4):23-26.
[6]曹春梅,闫贵龙.石灰处理秸秆的适宜剂量优选[J].中国草食动物,2005,25(4):35-37.
[7]杨俊,刘江生,蔡继宝,等.高效液相色谱-蒸发光散射法测定烟草中的水溶性糖[J].分析化学研究简报,2005,33:1596-1598.
[8]Kramar A,Turk S,Vrecer F.Statistical opti -mization of diclofenac sustained release pellets coated with polymethacrylic films[J].Int J Pharm,2003,256:43-52.
[9]严青,仲兆平,张茜芸.采用酸K 超声波强化碱预处理稻秆和玉米芯[J].东南大学学报:自然科学版,2013,43(1):105-109.
[10]Andric P,Meyer A S,Jensen P A,et al.Reactor design for minimizing product inhibition during enzymatic lignocelluloses hydrolysis:I.Significance and mechanism of cellobiose and glucose inhibition on cellulolytic enzymes[J].Biotechnology Advances,2010,28(3):308-324.
[11]Gould J M.Studies on the mechanism of alkaline peroxide deliainfication of agricultural residues[J].Biotechnology and Bioengineering,1985,27:225-231.
[12]Walker L P,Wilson D B.Enzymatic hydrolysis of cellulose:a overview [J].Bioresource Technology,1991,36(1):3-14.
[13]SIN H N,YUSOF S,HAMID N S A,et al.Optimization of hot water extraction for sap -odilla juice using response surface methodology[J].J Food Eng,2006,75(3):352-358.
