西黄胶囊辅助乳腺癌患者全程化疗的临床研究
2015-04-21张杰张颖孟惠彦李航杨帅姚天张风华
张杰 张颖 孟惠彦 李航 杨帅 姚天 张风华
乳腺癌是严重威胁女性健康的常见的恶性肿瘤之一。目前,乳腺癌的治疗主要是以手术为主,联合化学治疗、放射治疗、分子靶向治疗及中医中药治疗等的综合治疗,然而化学药物治疗所带来的毒副反应较大,使患者体力状况明显下降,导致患者的依从性降低,对于临床疗效造成负面影响,而且严重影响患者的生存质量[1]。近年来,文献报道中药抗肿瘤的基础研究及临床研究逐渐增多,机制及优势逐渐被人们认识[2]。针对乳腺癌患者辅助治疗的西黄丸是源于清代王洪绪的《外科证治全生集》,曾记载是古代治疗“乳岩”的重要方剂[3];而西黄胶囊是在西黄丸祖方的基础上经现代工艺将西黄丸中乳香和没药通过β-环糊精包埋技术处理后制成,因此对胃肠道刺激减轻,增加了抗肿瘤疗效。目前,国内关于西黄胶囊辅助乳腺癌患者全程化疗疗效的报道较少。本研究是一项临床前瞻性研究,旨在评价西黄胶囊辅助乳腺癌患者全程化疗的临床疗效。
1 资料与方法
1.1 病例选择
所有病例来源于2012年9月至2014年8月河北省人民医院普外一科收治的90 例经术后病理证实的乳腺癌患者,按随机数字表法分为治疗组和对照组,治疗组45 例(浸润性导管癌35 例;浸润性小叶癌10 例),年龄31 ~69 岁,平均年龄50.6 岁;Ⅰ期11 例,Ⅱ期25 例,ⅢA 期9 例。对照组45 例(浸润性导管癌34 例;浸润性小叶癌11 例)中,年龄29 ~68 岁,平均年龄50.2 岁;Ⅰ期14 例,Ⅱ期22 例,ⅢA 期9 例。(所有分期均依据2014 版乳腺癌NCCN 指南)。
1.2 治疗方法
对照组及治疗组均应用AC ×4→T ×4(吡柔比星+环磷酰胺→多西他赛)方案化疗,具体用药方案如下:前4 周期:注射用环磷酰胺(Cyclophosphamide for Injection 江苏恒瑞医药,批号H32020875)600 mg/m2静脉滴注;注射用吡柔比星注射液(Pirarubicin Hydrochloride for Injection 深圳万乐药业,批号H10930105)25 ~40 mg/m2静脉滴注。于化疗第1 天使用,21 天为1 周期,共进行4 次。患者于化疗药物静点前均给予托烷司琼注射液5 mg 静脉注射预防呕吐,给予地塞米松注射液5 mg 静脉注射防止过敏。序贯后4 周期:多西他赛(Docetaxel for Injection 江苏恒瑞医药,批号H20020543)75 mg/m2静脉滴注,在给予多西他赛滴注前1 天服用地塞米松片16 mg,连用3 天,同样静点化疗药前给予托烷司琼注射液5 mg 静脉注射预防呕吐,给予地塞米松注射液5 mg 静脉注射防止过敏。静点多西他赛时,给予心电监护,尤其是首次静脉注射,防止过敏性反应发生。21 天为1个周期,共4 个周期。而治疗组在化疗当天开始应用西黄胶囊(江苏万邦医药,批号Z61020121),8 粒/次,2 次/天。
1.3 纳入标准
(1)患者均经术后病理诊断证实;(2)乳腺癌分期为ⅠA 期~IIIA 期者(仅T3N1M0,无需术前新辅助化疗者);(3)能够耐受化疗;(4)预计生存期大于6个月;(5)年龄18 ~70 岁。
1.4 排除标准
(1)未能完成8 周期化疗者;(2)化疗期间曾服用其它中药或中成药时间大于1 周者;(3)年龄小于18 岁或大于70 岁者;(4)合并有重要脏器功能障碍者,如肝、肾、心脏等器官衰竭者;(5)无明确病理学诊断者;(6)合并严重的糖尿病、自身免疫性疾病等;(7)合并严重精神疾病及精神失常者。(8)Ⅲ期及Ⅳ期中需要术前新辅助化疗的患者。
1.5 疗效及不良反应标准
1.5.1 体力状况 以卡劳夫斯基(Kanorfsky)评分为标准评定。治疗后较治疗前增加10 分以上者为提高,减少10 分以上者为下降,介于两者之间为稳定[4]。
1.5.2 生活质量 生活质量以FACT-B(Functiond Assessment of Cancer Therapy-Breast)评估。该量表从以下几个方面进行测定:身体状况、社会/家庭状况,情感状况,功能状况等,每个指标均采用5 级评分法:根本不、有一点、有些、相当、非常;正向条目直接记0 ~4 分,各条目相加得分越高,说明生活质量越好[5]。
1.5.3 化疗毒副反应 采用WHO 抗癌化疗毒性反应分度标准。治疗期间患者主要发生的毒副反应主要为白细胞减少、贫血、血小板减少、以及恶心呕吐等胃肠道反应,以及肝脏转氨酶升高以及心肌酶异常变化。
1.6 统计方法
所得数据均采用统计学软件SPSS 13.0 进行分析处理,表示体力状况的计数资料采用百分比表示;组间比较采用χ2检验。表示生活质量评分的计量资料采用±s表示,组间比较采用配对t 检验;表示化疗副反应情况的计数资料用秩转换的非参数检验。检验水准α=0.05。
2 结果
2.1 体力状况
治疗组提高、稳定和下降分别为17.8%(8/45)、60%(27/45)和22.2% (10/45);对照组分别为4.5%(2/45)、53.3%(24/45)和42.2%(19/45)。经统计学处理有显著差异(P =0.037),与对照组相比,治疗组体力状况明显改善。
2.2 生活质量
治疗组化疗期间加用西黄胶囊各方面情况明显好转,治疗前后身体状况(P =0.009)、情感状况(P =0.007)、社会/家庭状况(P =0.013)、功能状况(P=0.046)经统计学处理均有显著性差异(P <0.05);而对照组单纯化疗后各方面情况下降,其中身体状况(P = 0.028)、社会/家庭状况(P =0.044)、情感状况(P = 0.042)、功能状况(P =0.006)经统计学处理有显著性差异(P <0.05),说明乳腺癌患者全程化疗期间同时服用西黄胶囊可明显改善患者的生活质量。
表1 两组治疗前后生活质量对比情况(±s,n=45)
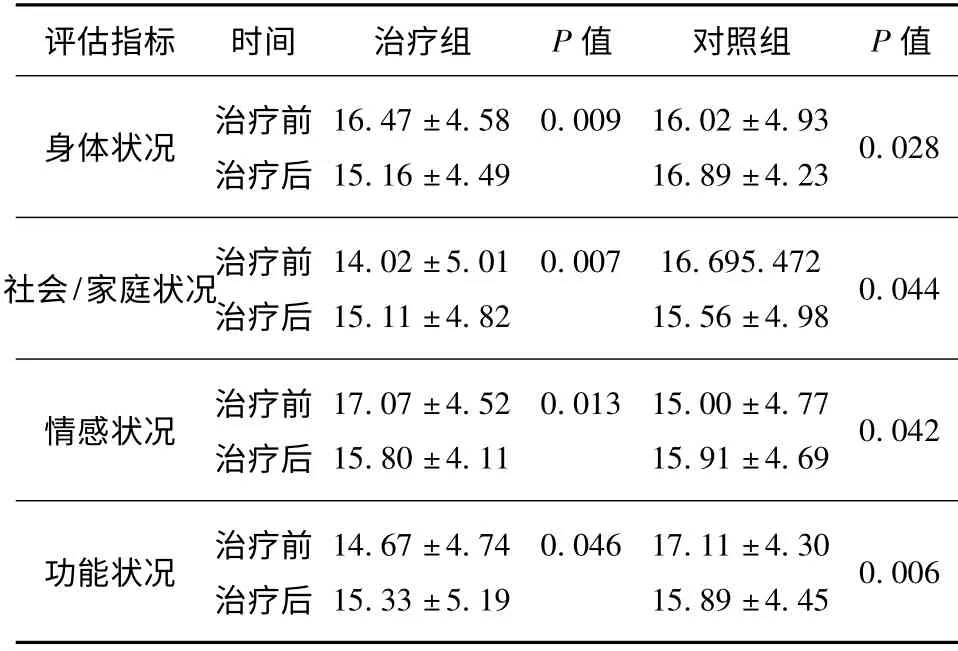
表1 两组治疗前后生活质量对比情况(±s,n=45)
评估指标 时间 治疗组 P 值 对照组 P值身体状况 治疗前治疗后16.47 ±4.58 15.16 ±4.49 0.009 16.02 ±4.93 16.89 ±4.23 0.028社会/家庭状况治疗前治疗后14.02 ±5.01 15.11 ±4.82 0.007 16.695.472 15.56 ±4.98 0.044情感状况 治疗前治疗后17.07 ±4.52 15.80 ±4.11 0.013 15.00 ±4.77 15.91 ±4.69 0.042功能状况 治疗前治疗后14.67 ±4.74 15.33 ±5.19 0.046 17.11 ±4.30 15.89 ±4.45 0.006
2.3 西黄胶囊对于化疗毒副反应作用的结果
化疗后治疗组与对照组的血红蛋白含量变化有统计学差异(P =0.002,P <0.05)。化疗后两组的血小板含量变化无统计学差异(P =0.081,P>0.05)。白细胞含量变化有统计学差异(P =0.049,P <0.05)。化疗后胃肠道反应持续时间组间比较,差异具有统计学意义(P =0.038,P <0.05)。根据以上结果,加用西黄胶囊可以明显减轻乳癌患者化疗造成的贫血,白细胞减少,但对于血小板的减少则无明显作用;同时服用西黄胶囊还可以显著缩短化疗药物造成的恶心、呕吐等消化道反应持续时间。对于肝脏转氨酶升高以及心肌酶异常变化则无明显影响。

表2 两组患者治疗前后毒副反应对比情况(n=45)
3 讨论
西黄丸又称犀黄丸,是由牛黄、麝香、乳香和没药为原料制成的中成药。牛黄有清热解毒、化痰散结的功效。麝香有活血散结、通经活络作用。二药合用,相得益彰,故化痰、解毒、散结效著。加之乳香、没药有活血散瘀、消肿生机、止痛的作用[6]。故西黄胶囊抗肿瘤的机制是清热解毒与活血化瘀相结合,对于因情志抑郁史,致气与痰结、肝气郁滞、经络不通而致的“乳岩”有效[7]。既往一些基础研究表明了西黄丸中的各种成分的抗肿瘤作用,以现代医学的实验研究从深层次揭示了其抗肿瘤作用机制。例如:汪世元等[8]发现体外培育牛黄能使人肝母细胞瘤HepG2 细胞膜皱缩、核碎裂,最终形成凋亡小体,认为牛黄具有诱导肿瘤细胞凋亡的作用。孟照华等[9]研究表明麝香实验组小鼠的癌瘤小、质量轻、小鼠生存期延长,证实其抑瘤作用。该实验结果初步证明麝香可提高荷瘤小鼠非特异性免疫功能。张勇等[10]用乳香提取物作用于HL-60细胞株,结果表明,该提取物不但在一定浓度范围内可抑制体外细胞株增殖,而且能下调血管内皮生长因子的表达及蛋白分泌。没药主要成分为树脂、树胶和挥发油中β-榄香烯对多种肿瘤细胞的增殖均有抑制作用[11]。
目前,中医药主要作为恶性肿瘤化疗的辅助治疗,目的在于尽可能有效改善化疗期间患者的体力状况及减轻毒副反应,提高患者的生活质量[12]。西黄胶囊是在西黄丸的基础上经现代工艺改造后的成药,国内有关西黄胶囊辅助乳腺癌患者全程化疗的前瞻性研究较少。洪日等[1]在将西黄丸用于中晚期乳腺癌治疗中,随访发现接受西黄丸辅助治疗的治疗组KPS 评分较未接受西黄丸治疗的对照组显著升高,患者体力状况显著改善。治疗组病灶稳定率显著升高。证实了西黄丸在中晚期乳腺癌患者中的治疗作用。肖琅等[13]在肺癌放化疗时加用西黄胶囊,结果表明治疗组在临床症状、生存期、生活质量方面改善明显高于对照组。同样彭明娥等[14]证实西黄胶囊可显著改善大肠癌患者的生活生存质量。笔者的研究表明,化疗加用西黄胶囊治疗组生活质量各方面情况明显改善;同时治疗组中因化疗造成的贫血、白细胞减少均较对照组明显减轻;并且可以显著缩短化疗药物造成的恶心、呕吐等消化道反应时间。这与西黄胶囊应用于其他类型肿瘤临床研究结果相一致,充分证实了西黄胶囊作为辅助治疗的抗肿瘤效应。当然,笔者的研究尚需要进一步延长随访时间,以评估西黄胶囊对于乳腺癌化疗患者的远期疗效。
综上所述,本研究表明乳腺癌患者全程化疗期间联合西黄胶囊可以显著改善患者的体力状况、生活质量及减轻化疗造成的毒副反应,值得临床推广、应用。
[1]洪日,吴永强,吴越.西黄丸辅助治疗中晚期乳腺癌的疗效观察[J].中国中药杂志,2014,39(6):1120-1122.
[2]程樱,张立.中药抗肿瘤机制及药物研究进展[J].中国药业,2013,22(17):103-104.
[3]陈信义,王婧,张雅月,等.西黄丸药效学研究及治疗肿瘤特点分析[J].中华中医药杂志,2010,25(3):409-412.
[4]贾文娟,田菲,邢秀玲.西黄丸联合唑来磷酸注射液治疗乳腺癌骨转移癌的临床研究[J].世界科学技术-中医药现代化,2009,11(3):450-453.
[5]万崇华,张冬梅,汤学良,等.乳腺癌患者生命质量测定量表(FACT-B)中文版的修订[J].中国心理卫生杂志,2003,17(5):298-300.
[6]金娟,李志鸿.西黄丸联合化疗治疗乳腺癌30 例[J].中华中医药杂志,2010,25(5):715.
[7]辛天星,谢晓冬.从中医体质学对乳腺癌病因病机的探讨[J].实用中医内科杂志,2011,25(7):49.
[8]汪世元,陈孝平,蔡红娇,等.体外培育牛黄诱导人肝癌HepG2 细胞凋亡的实验研究[J].华中科技大学学报:医学版,2005,34(6):754-756.
[9]孟照华,单礼成,曾家修,等.皮下埋藏麝香对BALB/2 纯系小鼠恶性肿瘤生长影响的实验研究[J].中国肿瘤临床,1998,25(11):834-836.
[10]张勇,齐振华,李乐赛,等.乳香提取物对HL-60 细胞株VEGF分泌及其Flt-1 受体表达的影响[J].湖南师范大学学报:医学版,2011,8(2):16-18.
[11]高天慧,段芳龄,刘明月,等.β-榄香烯和NDV 共修饰对脂质体瘤苗的免疫增强作用[J].中国现代药物应用,2012,6(2):9-10.
[12]周和超,陈兴贵,王镇南,等.西黄胶囊对乳腺癌术后放疗患者免疫功能及生存质量的影响[J].中国实用医药,2014,9(20):10-11.
[13]肖琅,李琦,阎萍.西黄胶囊增强肺癌放化疗作用的临床疗效的观察[J].陕西中医,2012,33(2):226.
[14]彭明娥,马 速.西黄胶囊治疗大肠癌46 例[J].天津药学,2007,19(6):34-36.
