活性白土-Bi2WO6的制备及其光催化氧化脱硫的研究
2015-04-19高晓明宜沛沛付峰李稳宏
高晓明, 宜沛沛, 付峰, 李稳宏
(1.延安大学化学与化工学院, 陕西省化学反应工程重点实验室, 陕西 延安 716000;2. 西北大学化工学院,陕西 西安 710069)
活性白土-Bi2WO6的制备及其光催化氧化脱硫的研究
高晓明1, 宜沛沛1, 付峰1, 李稳宏2
(1.延安大学化学与化工学院, 陕西省化学反应工程重点实验室, 陕西 延安 716000;2. 西北大学化工学院,陕西 西安 710069)
采用水热法合成了纳米Bi2WO6粉末,将其负载于活性白土上,制得负载性可见光催化剂活性白土-Bi2WO6,并对其进行X射线衍射、扫描电镜、紫外-可见光谱和孔径分析等表征手段对其结构性质进行了表征。结果显示:负载白土后,没有改变Bi2WO6的晶相,晶型较完整,延伸了Bi2WO6的可见光吸收范围,吸收边带轻微红移;制备的活性白土-Bi2WO6为扁平纳米片堆积组装的三维花球状结构,比表面积较大,能有效地吸附有机物分子;低温氮吸附表明活性白土-Bi2WO6的孔半径主要分布在10 nm和40 nm附近。在液相反应体系中,研究了活性白土-Bi2WO6氧化脱除FCC汽油中特征硫化物噻吩的效果,结果表明:在催化剂加入量为1.0 mg/L、氧化剂用量为1.0 mL/L、400 W金卤灯光照3.0 h条件下,活性白土-Bi2WO6对模拟汽油的脱硫率可达到94%。
活性白土-钨酸铋 可见光 脱硫 噻吩
汽油中含有的有机硫化物燃烧以后产生的SOx,严重影响着人类的生存环境。为此,人们采用多种方法来实现汽油的脱硫,如吸附法、微生物法、转化抽提法等[1]。其中噻吩类有机化合物存在空间位阻效应,性质稳定,很难脱除[2-5],因此,脱除噻吩类有机硫化物成为汽油脱硫技术的开发重点。近年来,光催化氧化技术作为一种新兴的污染治理技术得到了国内外学者的广泛关注[6-7]。其中,Bi2WO6作为一种可见光诱导的新型催化剂,具有无毒、反应速度快、降解效率高、无二次污染等优点,得到了广泛的研究[9-11]。但在应用过程中,还不能解决Bi2WO6粉末存在的比表面积小、易凝聚、易失活、利用率低、分离回收困难等问题[8-9]。为此,人们采用了多种手段对Bi2WO6进行改性,得到了较好的效果[10-12]。这些研究为Bi2WO6的修饰改性奠定了一定的基础,但尚缺乏对制备条件与结构、形貌和性能之间关系的系统研究;另外,这些研究都是基于甲基橙、罗丹明和苯酚的降解为目的的,将改性Bi2WO6应用于燃料油脱硫技术中却鲜有报道。
笔者以提高Bi2WO6的光催化活性为目的,采用水热法合成了Bi2WO6,以活性白土为载体,制备了活性白土负载型Bi2WO6光催化剂,通过XRD、UV-Vis、SEM、孔径及比表面积分析等手段对催化剂进行表征分析;以模拟汽油的脱硫率为研究目标噻吩,研究了光催化氧化工艺条件对活性白土-Bi2WO6的脱硫性能的影响。
1 实 验
1.1 活性白土-Bi2WO6的制备
称取一定量的硝酸铋和一定量钨酸钠固体,溶于适量的去离子水中,超声均化30 min后,调节pH至6.0。将溶液转移到聚四氟乙烯水热反应罐中,置于反应釜中,密封后放入烘箱中,在140 ℃水热反应24 h。冷却至室温,抽滤,得到淡黄色沉淀。反复用蒸馏水洗涤沉淀,置于干燥箱中80 ℃恒温烘干,研细,制得Bi2WO6试样,备用。
称取一定量的Bi2WO6试样和一定量活性白土于坩埚中,加5 mL蒸馏水,25 ℃水浴静置12h,用滴定管吸去上层清夜,将沉淀放入烘箱在80 ℃烘干4 h,然后放入马弗炉中于140 ℃煅烧3 h,得到活性白土-Bi2WO6试样,负载率为4.88%。
1.2 试样的表征
试样的结构分析用日本SHIMADZU公司的XRD-7000型全自动X射线衍射仪测定,CuKα射线源,管压40 kV,管流100 mA,扫描范围20°~80°。试样的紫外-可见光漫反射吸收光谱用日本SHIMADZU公司的UV-2550型紫外-可见分光光度仪测定,BaSO4为参考,测量范围200~800 nm。试样的形貌及微孔结构在日本HITACHI的TM3000上测定。试样的比表面积和等温线在北京金埃谱的V-Sorb2800P全自动比表面积及孔径分析仪上采用静态法测定。
1.3 光催化氧化脱硫试验方法
脱硫反应在50 mL石英试管中进行,可见光光源为400 W金卤灯。室温下,加入定量噻吩于正辛烷配成一定初始浓度的模拟汽油,待噻吩充分溶解并浓度稳定后,取30 mL模型化合物,加入一定量的活性白土-Bi2WO6、H2O2,在光化学反应仪上用可见光照射进行光催化反应,反应试管与光源垂直放置,距离为8 cm。反应完全后,用乙腈溶剂萃取硫生成物。用微库仑分析仪测定脱硫前后模拟汽油中硫含量的变化。
2 结果与讨论
2.1 试样的XRD表征
一般认为,光催化材料的结晶度和比表面积是影响光催化活性的两个重要因素。图1是用水热法所得的不同催化剂的XRD谱。由图1可知:试样在2θ=28.3°,32.8°,47°,55.6°,58.4°,68.5°,75.7°,78.1°处均出现了明显、尖锐的衍射峰,与Bi2WO6的标准卡(卡片号 JCPDF No.39-0256)符合的很好,结果表明白土的负载没有改变Bi2WO6的晶型。
经测定,Bi2WO6和活性白土-Bi2WO6的BET比表面积分别为8.9 m2/g和24.5。可见,负载活性白土以后,比表面积增大了近3倍。说明性白土的负载虽然没有改变Bi2WO6的晶型结构,但增大了其比表面积,这样可以有效吸附有机污染物,提高光催化降解能力。
2.2 试样的UV-Vis表征
Bi2WO6和活性白土-Bi2WO6试样的UV-Vis吸收光谱如图2所示。
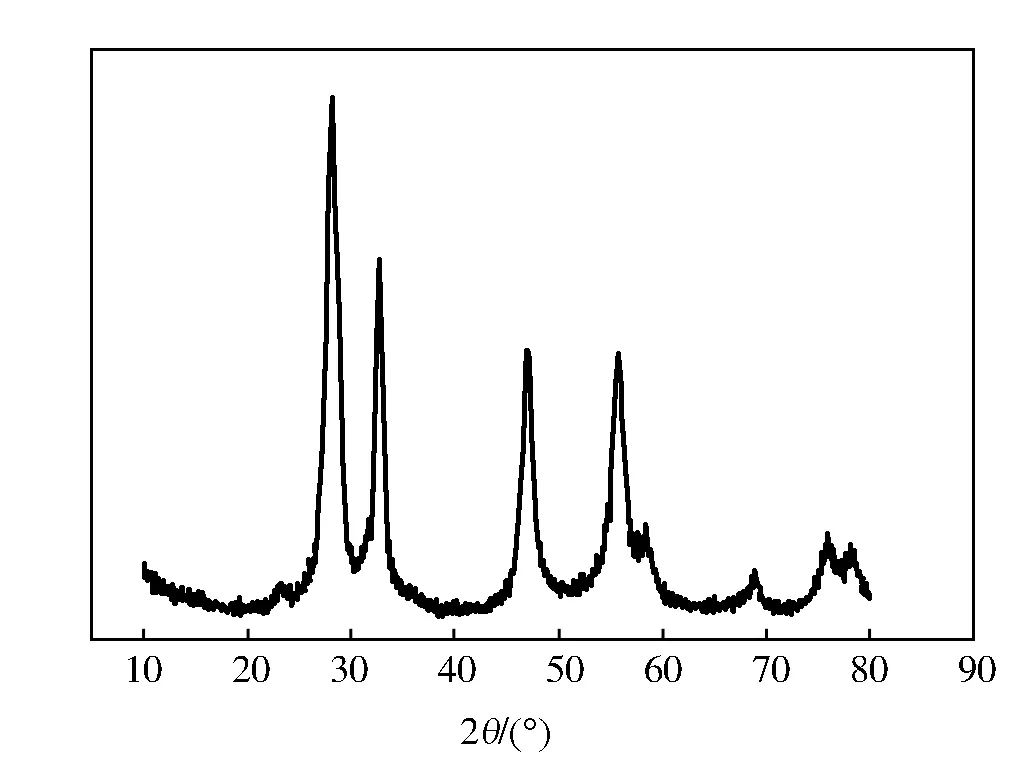
图1 活性白土-Bi2WO6的XRD谱

图2 试样的UV-Vis谱a-活性白土-Bi2WO6;b-Bi2WO6
从图2可以看出:Bi2WO6和活性白土-Bi2WO6试样从紫外区到部分可见光区对光线都有不同程度的吸收,吸收强度都存在从紫外区到可见光区的急剧下降。这说明二者光谱的吸收是由半导体材料的带间跃迁造成的,二者在可见光区的吸收是由Bi2WO6半导体材料的能带结构决定的。W5d轨道形成的导带和Bi6S和O2p轨道杂化形成的价带构成了Bi2WO6半导体材料的能带结构,Bi2WO6半导体材料对光的吸收带是由电子从Bi6S和O2p所形成的杂化轨道向W5d轨道跃迁产生的,由于Bi6S和O2p轨道的杂化,使Bi2WO6半导体材料的价带电位升高,禁带宽度减小,因此在可见光区有吸收。
半导体材料的光催化活性主要取决于光催化剂的能带禁宽的大小,能带禁宽越小,半导体的吸收边界就越向长波区域移动,即向可见光方向移动,使其可见光利用程度提高[13]。由图2可见,活性白土-Bi2WO6相对纯的Bi2WO6,试样的吸收边界出现了红移,对可见光的利用率增强。
由半导体材料的吸收边界可估算各产物的能带禁宽,估算公式为:Eg=1 240/λ0[14],其中:Eg表示半导体材料的能带禁宽,λ0表示半导体材料的吸收边界延长线与横轴交点处的波长值。根据公式估算出性白土-Bi2WO6的能带禁宽为2.7 eV,与波长小于400 nm的紫外光(3.1 eV)相比,性白土-Bi2WO6具有良好的可见光催化活性。
2.3 活性白土-Bi2WO6试样的形貌分析
图3是活性白土-Bi2WO6试样的SEM照片。由图3可知,活性白土-Bi2WO6主要以松散的聚集体形态存在,这些聚集体为三维花球状结构,直径为2~3 μm,是由许多较大的扁平纳米片堆积组装形成的,纳米片长约100~200 nm,分散较均匀。这种花球状结构活性白土-Bi2WO6的生成是晶体成核过程与生长过程共同作用产生的结果。由于三维花球状结构的活性白土-Bi2WO6是由扁物分子的传输提供有用的通道,从而大大提高它的光催化活性,另外由于三维花球状的特殊结构使活性白土-Bi2WO6的比表面积增大,从而能有效地吸附有机物分子,使其光催化效率得到提高。

图3 活性白土-Bi2WO6试样的SEM照片
2.4 试样的孔径物理吸附分析
图4为Bi2WO6和活性白土-Bi2WO6在-196 ℃对氮气的吸附等温线,内嵌图为其孔径分布。根据IUPAC分类,图4中所示的二种试样的吸附-脱附等温线均为Ⅳ型等温线,可见Bi2WO6和活性白土-Bi2WO6试样的表面有填充孔。
图4中,在低p/p0区,吸附-脱附等温曲线向上微凸,并且两条等温曲线重合;在较高p/p0区,氮气在Bi2WO6和活性白土-Bi2WO6试样的表面发生毛细管凝聚,吸附-脱附等温线迅速上升。由于氮气在Bi2WO6和活性白土-Bi2WO6试样的表面发生毛细管凝聚,表现在吸附-脱附等温线上为脱附等温线的滞后于吸附等温线,即在吸附时达到的等温曲线与脱附时得到的等温曲线不重合,吸附等温线在脱附等温线的下方,形成吸附滞后。由图4(a)可见,活性白土-Bi2WO6试样的滞后环起始位置处的相对压力p/p0=0.8,内嵌图中孔径分布主要集中在10 nm和40 nm左右。相对压力p/p0=0.8时,对应的孔半径为5.27 nm,吸附膜厚度为0.998 nm,实际孔直径为10.54 nm。当相对压力p/p0>0.8时,活性白土-Bi2WO6试样对氮气的吸附量急剧增加,吸附-脱附等温线陡然增加,说明此时活性白土-Bi2WO6试样中相对压力p/p0>0.8时的孔发生吸附,而且这种孔的数目占绝对优势。而Bi2WO6试样的吸附等温线(图4(b))相对于活性白土-Bi2WO6试样,滞后环起始位置右移,即滞后环起始位置处的p/p0减小,由图中的内嵌图可发现孔径分布的最大值右移,说明Bi2WO6试样中的大孔数量减少。
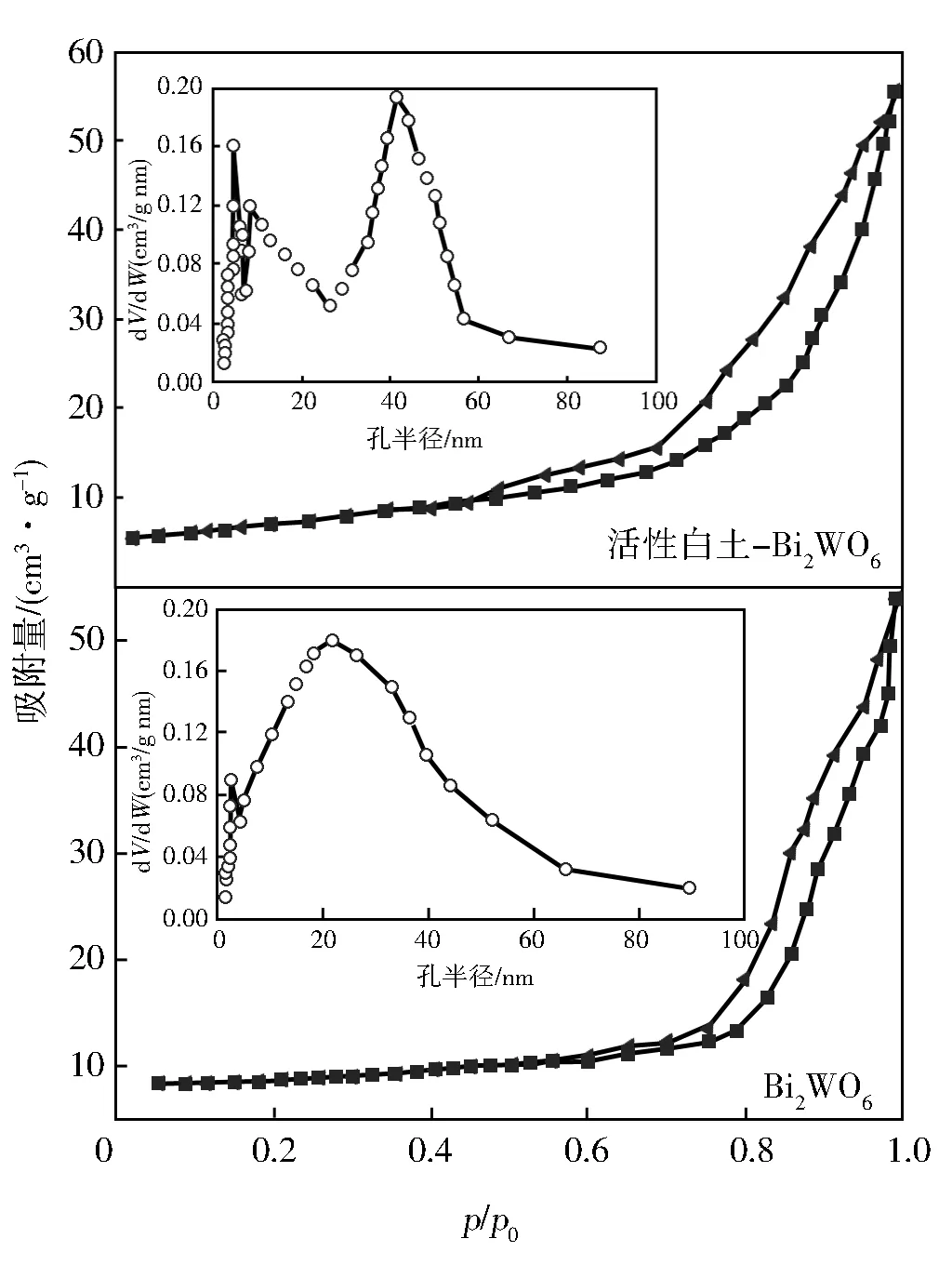
图4 试样对氮气的吸附等温线和孔径分布(内嵌图)
2.5 活性白土-Bi2WO6催化脱硫工艺
2.5.1 催化剂的类型对光催化脱硫效果的影响
在模拟汽油中加入1.0 mg/L的Bi2WO6和活性白土-Bi2WO6,1.0 mL/L H2O2,400 W金卤灯下光照2 h,考察Bi2WO6和活性白土-Bi2WO6对脱硫率的影响,如图5所示。
由图5可以看出,当不加入任何催化剂时,光照反应2 h后,脱硫率为44.3%,这说明H2O2受光照激发后,产生·OH自由基,该自由基是一种强氧化剂,可以将噻吩氧化分解,因此,在光照和H2O2存在情况下,对噻吩也有一定的降解作用;当加入Bi2WO6时,光照反应2 h后,脱硫率为75.3%,这是由于在Bi2WO6光催化氧化降解反应体系中,可见光照射Bi2WO6后,Bi2WO6吸收一定波长的光子产生光生电子和空穴,光生空穴移向表面,与吸附的噻吩发生氧化反应,或与H2O分子作用生成·OH自由基,进而氧化噻吩,而光生电子则被溶氧捕获,最终生成·OH自由基参与氧化反应;同时H2O2受光激发产生·OH自由基,并与噻吩发生光化学氧化反应;这两种作用共同促进了脱硫的完成。然而,在反应体系中加入活性白土-Bi2WO6时,脱硫率增大到93.14%,这是由于Bi2WO6负载活性白土以后,比表面积大大增大,一方面,比表面积的增大显著提高了噻吩的吸附量,从而提高了噻吩被降解的几率;另一方面,比表面积的增大使光催化反应所需的活性中心位增多,可以较大程度的吸附光子和噻吩分子,有利于噻吩的光催化氧化降解。从图5也可以看出随着时间的延长,不同催化剂对模拟汽油的脱硫率逐渐升高,前90 min脱硫率增加的速度比较快,后90min脱硫率增加的速度比较平缓,几乎都在180 min时脱硫过程完成。

图5 不同催化剂对脱硫率的影响
2.5.2 催化剂加入量对脱硫率的影响
在模拟汽油中加入1.0 mL/L H2O2,在400 W金卤灯下光照不同时间,考察活性白土-Bi2WO6加入量对脱硫率的影响,如图6所示。
催化反应主要在光可穿透的催化剂表面上进行,其活性高低既与电子-空穴对的产生量及复合速度有关,又与催化剂表面吸收光量子的数量及与光降解对象的吸附率有关[15]。从图6可以看出,当催化剂的加入量由0.6 mg/L增大到1.0 mg/L时,脱硫率呈上升趋势。这是由于在一定范围内,光催化剂量不足时,活性位少且容易被有机污染物占据,因而催化活性不高。随着催化剂剂量的增加,活性位增多,光利用率增加,且适量的催化剂能有效吸收光量子,并增加对噻吩的吸附,导致其向光反应活性中心扩散,使可见光催化活性迅速提高[16];但超过一定范围,光催化脱硫速率反而下降,这是由于反应体系中,活性白土-Bi2WO6的加入量过多时,会减弱溶液的透光性,增强光的散射作用,降低了活性白土-Bi2WO6对光的吸收效率,从而使脱硫效率降低。
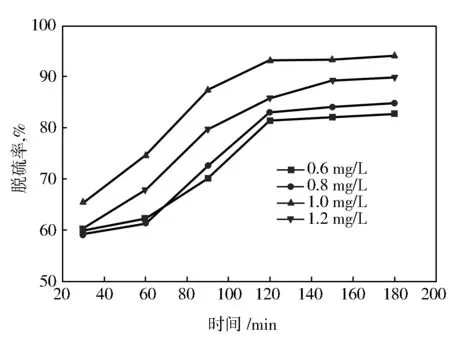
图6 活性白土-Bi2WO6加入量对脱硫率的影响
2.5.3 氧化剂加入量对脱硫率的影响
在模拟汽油中加入1.0 mg/L活性白土-Bi2WO6,在400 W金卤灯下光照不同时间,考察氧化剂的用量对脱硫率的影响,如图7所示。

图7 氧化剂加入量对脱硫率的影响
由图7可以看出,随着过氧化氢用量的增加,脱硫率明显增加。过氧化氢在光催化反应过程中,获得电子产生自由基·OH,产生的自由基·OH与噻吩发生自由基链反应,达到含硫化合物的光降解,可见过氧化氢在光催化反应体系中的浓度至关重要,增加氧化剂的量,可提高·OH的产生速率,有利于含硫化合物的光降解[23]。当过氧化氢加入量为1.0 mL/L时,脱硫率达到最大。随着过氧化氢加入量的进一步提高,脱硫率随之下降,这可能因为过量的过氧化氢经过光照产生的气体量较大,阻碍了反应物在活性白土-Bi2WO6表面的吸附,减少了反应机率,从而对·OH起了消除作用;另外,过量的过氧化氢会对反应体系造成污染,使脱硫率下降。
2.6 催化剂的寿命与稳定性
将1.0 mg/L活性白土-Bi2WO6加入模拟汽油中,在氧化剂用量为0.1 mL/mL,400 W金卤灯下光照180 min的条件下连续使用3次,脱硫率依次为93.14%,91.30%,90.56%。由此可见,回收的催化剂虽然活性有所下降,但仍具有较高的降解率。其活性下降的原因可能是在循环使用的过程中催化剂颗粒发生了团聚或者回收过程中超细级的活性组分产生了损耗。
3 结 论
制备的可见光催化剂活性白土-Bi2WO6结晶度较好,晶型完整;活性白土-Bi2WO6为扁平纳米片堆积组装的三维花球状结构,该结构有较大的比表面积,能有效地吸附有机物分子;白土的负载延伸了Bi2WO6的可见光吸收范围,吸收边带轻微红移。光催化脱硫实验表明,催化剂加入量为1.0 mg/L,氧化剂用量为1.0 mL/L,400 W金卤灯光照3.0 h,活性白土-Bi2WO6对模拟汽油的脱硫率可达到94%。
该研究为材料化学与环境科学提供了新的研究内容,为合成表面结构特殊且具有光催化性能的复合材料提供了新的思路,同时也为复合材料光催化治理燃料油中的硫化物提供借鉴意义。
[1] Li Huaming, Jiang Xue, Zhu Wenshuai, et al. Deep oxidative desulfurization of fuel oils catalyzed by decatungstates in the ionic liquid of [Bmim]PF6[J/OL]. Industial & Engingeering Chemistry Ressearch, 2009, 48(19): 9034-9039[2009-09-02] .http://pubs.acs.org/doi/abs/10.1021/ie900754f.
[2] 陈兰菊, 郭绍辉, 赵地顺. 催化裂化汽油中特征硫化物噻吩的催化氧化脱硫[J/OL]. 化工学报,2007, 58(3): 652-655[2006-04-10]. http://www.cjcu.jlu.edu.cn/CN/abstract/abstract12396.shtml.
[3] Wang Bo,Zhu Jianpeng,Ma Hongzhu.Desulfurization from thiophene by/ZrO2catalytic oxidation at room temperature and atmospheric pressure[J/OL]. Journal of Hazardous Materials, 2009, 164(1): 256-264[2008-08-13]. http://www.sciencedirect.com/science/article/pii/S0304389408011965.
[4] 赵地顺, 刘翠微,马四国. FCC汽油模型化合物光催化氧化脱硫的研究[J/OL].高等学校化学学报, 2006, 27(4):692-696[2006-04-10]. http://www.cjcu.jlu.edu.cn/CN/abstract/abstract12396.shtml.
[5] Robertson J, Bandosz T J. Removal of dibenzothiophene from tetradecane using catalytic photoxidationon TiO2/hectorite thin films layered catalyst[J/OL]. Journal of Colloid and Interface Science, 2006, 299(1):125-135[2006-04-05]. http://www.sciencedirect.com/science/article/pii/S00219797060 01068.
[6] Na Ping, Zhao Baolin, Gu Linyuan, et al. Deep desulfurization of model gasoline over photoirradiated titanium-pillared montmorillonite[J/OL]. Journal of Physics and Chemistry of Solids, 2009, 70(12): 1465-1470[2009-08-15]. http://www.sciencedirect.com/science/article/pii/S0022369709002200.
[7] Yan Xumin, Mei Ping, Lei Jiaheng, et al. Synthesis and characterization of mesoporous phosphotungstic acid/TiO2 nanocomposite as a novel oxidative desulfurization catalyst[J/OL]. Journal of Molecular Catalysis A: Chemical, 2009, 304 (1/2): 52-57[2009-01-21]. http://www.sciencedirect.com/science/article/pii/S1381116909000351.
[8] Sun Songmei, Wang Wenzhong, Zhang Ling. Efficient contaminant removal by Bi2WO6films with nanoleaflike structures through a photoelectrocatalytic process[J/OL]. Journal of Physical Chemistry C, 2012, 116(36): 19413-19418[2012-08-15]. http://pubs.acs.org/doi/abs/10.1021/jp306332x.
[9] Bhattacharya C, Lee H C, Allen J. Bard. Rapid screening by scanning electrochemical microscopy (SECM) of dopants for Bi2WO6improved photocatalytic water oxidation with Zn doping[J/OL]. Journal of Physical Chemistry C, 2013, 117(19): 9633-9640[2013-04-10]. http://pubs.acs.org/doi/abs/10.1021/jp308629q.
[10] Xu Jiehui, Wang Wenzhong, Shang Meng, et al. Efficient visible light induced degradation of organic contaminants by Bi2WO6film on SiO2modified reticular substrate[J/OL]. Applied Catalysis B: Environmental, 2010, 93(3-4): 227-232[2009-10-01]. http://www.sciencedirect.com/science/article/pii/S0926337309003877.
[11] Chen Yilin, Cao Xiaoxin, Kuang Jidong, et al. The gas-phase photocatalytic mineralization of benzene over visible-light-driven Bi2WO6@C microspheres[J/OL]. Catalysis Communications, 2010, 12(4): 247-250[2010-09-27]. http://www.sciencedirect.com/science /article/pii/S 1566736 710002888.
[12] Zhang Zhijie, Wang Wenzhong, Wang Lu, et al. Enhancement of visible-light photocatalysis by coupling with narrow-band-gap semiconductor: A case study on Bi2S3/Bi2WO6[J/OL]. ACS Applied Material Interfaces, 2012, 4(2): 593-597[2012-01-16] .http://pubs.acs.org/doi/abs/10.1021/am2017199.
[13] He Dongqing, Wang Lingling, Xu Dandan, et al. Investigation of photocatalytic activities over Bi2WO6/ZnWO4composite under UV light and its photoinduced charge transfer properties[J/OL]. ACS Applied Material Interfaces, 2011, 3(8): 3167-3171[2011-07-11]. http://pubs.acs.org/doi/abs/10.1021/am200664y.
[14] Duan Fang, Zheng Yan, Chen Mingqing. Flowerlike PtCl4/Bi2WO6composite photocatalyst with enhanced visible-light-induced photocatalytic activity[J/OL]. Applied Surface Science, 2011, 257(6): 1972-1978[2010-09-21].http://www.sciencedirect.com/science/article/pii/S0169433210012699.
[15] Konstantinou I K, Albanis T A. TiO2-assisted photocatalytic degradation of azo dyes in aqueous solution: kinetic and mechanistic investigations: A review[J/OL]. Applied Catalysis B: Environmental, 2004, 49(1):1-14[2004-02-07]. http://www.sciencedirect.com/science/article/pii/S 0926337303 005411.
[16] Agustina T E, Ang H M, Vareek V K. A review of synergistic effect of photocatalysis and ozonation on wastewater treatment[J/OL]. Journal of Photochemistry and Photobiology C, 2005, 6(4):264-273[2006-03-03] . http://www.sciencedirect.com/science/article/pii/S1389556706000050.
PREPARATION OF ACTIVATED CLAY-Bi2WO6AND ITS APPLICATION IN THE PHOTOCATALYTIC OXIDATIVE DESULFURIZATION
Gao Xiaoming1, Yi Peipei1, Fu Feng1, Li Wenhong2
(1.CollegeofChemistryandChemicalEngineering,ShaanxiKeyLaboratoryofChemicalReactionEngineering,Yan’anUniversity,Yan’an716000,Shaanxi,China;2.CollegeofChemicalEngineering,NorthwestUniversity,Xi’an710069,Shaanxi,China)
The Bi2WO6was prepared by hydrothermal synthesis method, which was loaded on the activated caly to make the activated clay-Bi2WO6. The activated clay-Bi2WO6was characterized by X-ray diffraction, scanning electron microscopy, UV-Vis absorption spectroscopy, and N2adsorption. The characterized results indicated that the doping clay did not change the crystal phase of Bi2WO6.The morphology and microstructure of activated clay-Bi2WO6was 3D flower spherical structure, and had a complicated surface morphology and the size of micro-porosity was large. The activated clay-Bi2WO6had a significant red-shift in the absorption band in the visible region, and the absorption intensity increased greatly for the doped catalyst. The N2adsorption results revealed that the pore size of the activated clay-Bi2WO6mostly distribute in 10 nm and 40 nm. The desulfurization ability of the activated clay-Bi2WO6was researched by photocatalytic oxidation of thiophene in visible light. The results showed that the desulfurization rate could achieve 94% when the amount of oxidant was 1.0 mL/L, catalyst dosage was 1.0 mg/L, and illumination time was 3 h in 400 W metal halide lamp.
activated clay-bismuth tungstate; visible light; desulfurization; thiophene
2014-04-16;修改稿收到日期:2014-12-09。
高晓明(1979-),博士,主要从事催化材料和能源化工方面的研究工作。E-mail:dawn1026@163.com。
陕西省科技厅项目(2014K10-04);延安市科技局项目(2012kg-09);陕西省教育厅项目(2013JK0689);延安大学自然科学基金项目(YDQ2013-17)。
TQ426.64
A
