多囊卵巢综合征患者夫精人工授精前预处理的价值研究*
2015-04-19吴成勇杨满林梅蔡敏生
吴成勇 杨满 林梅 蔡敏生
多囊卵巢综合征( polycystic ovary syndrome,PCOS)是常见的妇科内分泌疾病,也是引起女性不孕的主要疾病之一,主要表现为月经紊乱、稀发排卵[1]。多数患者可以通过促排卵指导受孕,但仍然有部分患者对促排卵药物不敏感,不能产生成熟卵子,或虽然有成熟卵子,但卵子质量差,难以受孕,受孕后流产率也明显高于正常女性[2]。考虑与多囊卵巢综合征患者出现内分泌紊乱和代谢异常相关。本研究通过对多囊卵巢综合征患者夫精人工授精前药物预处理,以期改善患者的内分泌与代谢异常状态,提高促排卵药物的敏感性,改善患者的妊娠结局,现报告如下。
1 资料与方法
1.1 一般资料 选取2012年1月-2013年12月在本院行夫精人工授精的患者100例,所有患者均进行相关检查,符合多囊卵巢综合征的诊断标准,均签署知情同意书[3]。按照患者预处理治疗意愿分为观察组和对照组。观察组50例,年龄21~34岁,平均(27.81±5.47)岁,体质量指数(BMI)23.76~29.35 kg/m2,平均(26.59±4.57)kg/m2;对照组年龄22~37岁,平均(28.91±7.02)岁,体质量指数(BMI)21.47~30.56 kg/m2,平均(27.62±5.38)kg/m2,两组患者年龄、体质量指数等一般资料比较差异无统计学意义(P>0.05),具有可比性。
1.2 方法 观察组:预处理前:月经第2~3 d测定性激素水平。预处理:月经第5 d开始:口服炔雌醇环丙孕酮片,1片/d,口服21 d(1周期)停药,月经来潮的第5 d重复炔雌醇环丙孕酮片治疗,连续口服3周期。预处理后:月经第2~3 d复查性激素水平,月经第5 d阴道B超检查双侧卵巢及子宫(有无卵巢囊肿),无异常则给予氯米芬片50~100 mg口服,口服5 d,月经周期第10~11天开始阴道B超监测卵泡发育,根据卵泡发育速度和卵泡大小,考虑肌注尿促性素75~150单位,当卵泡直径≥18 mm时肌注人绒毛膜促性腺激素5000~10 000 U,注射后24~48 h行夫精人工授精术。对照组:不进行预处理治疗,月经第2~3天测定性激素水平后直接进行促排卵治疗和夫精人工授精术,具体方案同观察组。两组患者在夫精人工授精术后第2天阴道B超检查排卵,排卵后口服黄体酮胶丸200 mg/d,或地屈孕酮片20 mg/d。
1.3 观察指标
1.3.1 性激素测定 早晨8时空腹抽取肘部静脉血5 mL,以3000 r/min转速离心5 min,吸取血清,采用罗氏cobase411电化学发光仪测定黄体生成素(LH)、促卵泡激素(FSH)、睾酮(T)、性激素结合球蛋白(SHBG)、雌二醇(E2)水平。 并 计 算 出 LH/FSH比 值、FAI值。FAI=T(ng/mL)×347/SHBG(nmol/L)。
1.3.2 卵泡监测及妊娠判断 阴道B超检测卵泡直径大小,注射HCG日子宫内膜厚度。成熟卵泡消失,盆腔后穹隆出现积液暗区表示已排卵。排卵后14 d进行尿早早孕测定确定生化妊娠,排卵后30 d阴道B超显示宫腔内有妊娠囊,确定临床妊娠。
1.3.3 妊娠结局追踪 定期返院复查妊娠情况,并定期产科产检,了解妊娠情况,记录流产率,过度刺激综合征(OHSS)、妊娠期高血压(PIH)、妊娠期糖尿病(GDM)等并发症发生率。
1.4 统计学处理 采用SPSS 13.0统计学软件对数据进行处理,计量资料以(x-±s)表示,比较采用t检验,计数资料用频数或率(%)表示,比较采用 字2检验,以P<0.05表示差异具有统计学意义。
2 结果
2.1 观察组治疗前与治疗后及对照组性激素水平的比较 观察组患者治疗后LH、LH/FSH、T和SHBG水平均降低,明显低于治疗前和对照组,比较差异均有统计学意义(P<0.05)。见表1。
2.2 两组患者夫精人工授精具体情况的比较 观察组内膜厚度(HCG日)明显高于对照组,卵泡数明显少于对照组,比较差异均有统计学意义(P<0.05);而两组E2(HCG日)和HMG总用量比较,差异均无统计学意义(P>0.05)。见表2。
表1 观察组治疗前与治疗后及对照组性激素水平的比较(±s)
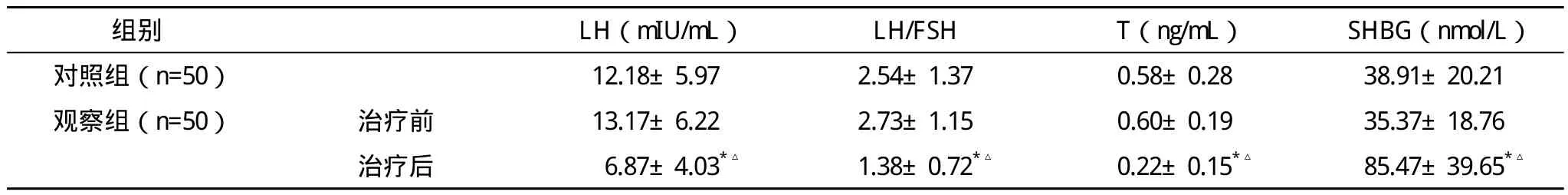
表1 观察组治疗前与治疗后及对照组性激素水平的比较(±s)
*与治疗前比较,P<0.05;△与对照组比较,P<0.05
组别 LH(mIU/mL)LH/FSH T(ng/mL)SHBG(nmol/L)对照组(n=50)12.18±5.97 2.54±1.37 0.58±0.28 38.91±20.21观察组(n=50)治疗前 13.17±6.22 2.73±1.15 0.60±0.19 35.37±18.76治疗后 6.87±4.03*△ 1.38±0.72*△ 0.22±0.15*△ 85.47±39.65*△
表2 两组患者夫精人工授精具体情况的比较(±s)

表2 两组患者夫精人工授精具体情况的比较(±s)
组别 内膜厚度(mm)E2(pg/mL)HMG用量(U)卵泡数(个)对照组(n=50)7.58±5.36 489.45±126.74 10.59±5.25 3.86±2.05观察组(n=50)9.85±4.28 519.35±198.31 9.36±4.87 1.75±1.29 t值 2.340 0.898 1.215 6.159 P值 <0.05 >0.05 >0.05 <0.01
2.3 两组患者妊娠情况的比较 观察组排卵周期数、临床妊娠率明显高于对照组,比较差异有统计学意义(P<0.05);观察组流产率低于对照组,比较差异有统计学意义(P<0.05)。见表3。
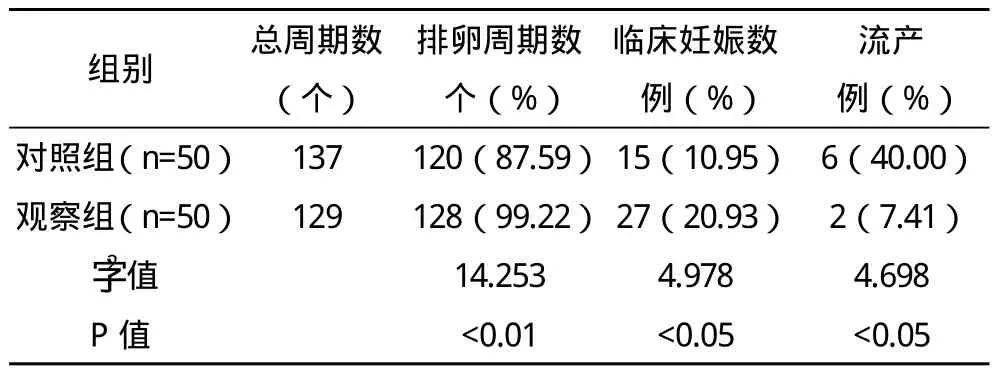
表3 两组患者妊娠情况的比较
2.4 两组患者并发症的比较 观察组并发症发生率明显高于对照组,比较差异有统计学意义(P<0.01)。见表4。

表4 两组患者妊娠期并发症的比较 例(%)
3 讨论
夫精人工授精技术是治疗男方少弱畸精症、女方排卵功能障碍如PCOS的辅助生殖技术之一。精子和卵子的质量、女方年龄、人工授精时机的把握与夫精人工授精技术的临床妊娠率密切相关[4]。PCOS患者由于内分泌异常(高LH水平、高雄激素血症),以及代谢功能障碍(高胰岛素血症),导致卵泡发育障碍,稀发排卵甚至不排卵,或者卵子质量差,严重影响着妊娠结局[5]。因此,对PCOS患者的预处理治疗,改善患者的内分泌状态,纠正代谢功能异常,提高卵子质量,提高女性临床妊娠率是临床学者的重要研究内容。
3.1 预处理改善多囊卵巢综合征患者的内分泌状态 达英-35通用名为炔雌醇环丙孕酮片,主要成分为炔雌醇和环丙孕酮。人体血液循环中,T主要与SHBG结合,仅有少许T分子呈游离状态,发挥着雄激素样作用。炔雌醇可通过促进SHBG蛋白的合成,间接降低血液循环中游离T水平。同时,还可以抑制LH分子的合成,抑制T分子的合成与释放。环丙孕酮本身具有很强的抗雄激素作用,它在外周靶器官中竞争性结合雄激素受体,抑制雄激素的作用。同时,它通过下丘脑-垂体-卵巢轴反馈性抑制LH分泌,抑制T分子的合成与释放[6]。如上所述,炔雌醇环丙孕酮片可通过多种途径,降低LH水平,改善高雄激素状态,从而改善异常的内分泌状态。二甲双胍为糖尿病患者的一线药物,它可以抑制肝糖原的合成,提高周围靶器官对胰岛素的敏感性,改善高胰岛素状态。同时,它可以抑制肝脏P450酶的活性,促进SHBG合成,降低循环中的游离雄激素水平[7]。炔雌醇环丙孕酮片联合二甲双胍预处理治疗PCOS患者,可以通过不同机制改善内分泌状态,改善卵子发育的内环境,提高卵子的质量,改善妊娠结局。
3.2 预处理对卵子质量及妊娠的影响 有学者研究发现,PCOS患者的卵子质量差,临床妊娠率低,且容易流产,体外受精-胚胎移植技术治疗后,卵子回收率、卵子的质量和发育成优势胚胎的能力低于正常妇女,这些均考虑与PCOS患者的卵泡内环境出现改变有关[8-9]。Stephen等[10]研究认为,PCOS患者的卵子暴露在高LH和高雄激素的环境中,卵泡的颗粒细胞分裂和凋亡出现异常,改变了卵子发育的内环境,从而影响了卵子的生长成熟。本研究发现,虽然对照组卵泡数为(3.86±2.05)个,多于观察组的(1.75±1.29)个,但临床妊娠率显著低于观察组,流产率显著高于观察组。这表明,通过对PCOS患者的预处理,改善了患者异常的内分泌状态和代谢状态,卵子生长发育的微环境恢复正常,卵子的质量得到了明显提高,因此临床妊娠率相应提高,流产率明显下降。
3.3 预处理降低妊娠期并发症的风险 PCOS患者由于高雄激素、高LH水平的影响,卵巢内出现了大量小卵泡,大量的小卵泡发育导致体内E2的水平上升,刺激血管内皮因子产生,使血管通透性增加,从而导致OHSS的发生。本研究发现,预处理后,PCOS患者仅有1例出现OHSS,且症状较轻,患者无腹腔积液及血液浓缩现象,嘱高蛋白饮食后,症状自然缓解。而对照组出现4例OHSS,其中1例因症状较重,出现胸腹腔积液,予住院放腹水治疗,补充白蛋白等对症治疗后好转。但本研究中,两组患者OHSS的发生率比较差异无统计学意义,可能与标本数少有关。
Smirnakis等[11]研究发现出现GDM的患者血清SHBG明显减少,考虑SHBG减少是导致GDM的原因之一,在早孕期非空腹状态下测定SHBG水平是预测将来发生GDM的可靠指标。本研究发现预处理后PCOS患者SHBG水平明显升高,GDM发生率仅为3.70%。这表明预处理后,PCOS的SHBG水平升高,从而降低了GDM的发病风险。研究认为,高胰岛素血症和胰岛素抵抗可通过刺激交感神经系统,促使钠水潴留,血管平滑肌增生,血管阻力增加等的发生,从而引起妊娠期血压升高,导致PIH的发生[12]。因此,PCOS患者的代谢异常,出现高胰岛素血症和胰岛素抵抗,容易导致PIH的发生。本研究发现,观察组的GDM和PIH的发生率均小于对照组,但两组比较差异均无统计学差异,可能与样本数少有关。本研究通过对总的妊娠期并发症的风险分析,观察组并发症发生率明显小于对照组,表明通过预处理,可以显著减少PCOS患者妊娠期并发症的发生。
综上所述,对PCOS患者夫精人工授精前给予炔雌醇环丙孕酮片联合二甲双胍预处理治疗,可以改善患者的内分泌和代谢异常状态,提高卵子质量及临床妊娠率,降低流产率,降低妊娠期并发症的发生,值得临床中推广应用。
[1]刘明慧,刘英,王树玉,等.控制性超排卵治疗对多囊卵巢综合征患者卵母细胞质量的影响[J].中国优生与遗传,2014,22(1):97-99.
[2] Chen Z J,Shi Y.Polycystic ovary syndrome[J].Front Med China,2010,4(3):280-284.
[3] Rotterdam ESHRE/ASRM-Sponsored PCOS Consensus Workshop Group.Rivised 2003 consensus on diagnostic criteria and long tem health risked related to polycystic ovary syndrom[J].Fertil Steril,2004,81(1):19-25.
[4] Dong F L,Sun Y P,Su Y C,et al.Relationship between processed total motile sperm count of husband or donor semen and pregnancy outcome following intrauterine insemination[J].Syst Biol Reprod Med,2011,57(5):251-255.
[5] Lathi R B,Dahan M H,Reynolds-May M F,et al.The role of serum testosterone in early pregnancy outcome:a comparison in women with and without polycystic ovary syndrome[J].J Obstet Gynaecol Can,2014,36(9):811-816.
[6] Kahraman K,Sükür Y E,Atabekoğlu C S,et al.Comparison of two oral contraceptive forms containing cyproterone acetate and drospirenone in the treatment of patients with polycystic ovary syndrome:a randomized clinical trial[J].Arch Gynecol Obstet,2014,290(2):321-328.
[7] Ito-Yamaguchi A,Suganuma R,Kumagami A,et al.Effects of metformin on endocrine,metabolic milieus and endometrial expression of androgen receptor in patients with polycystic ovary syndrome[J].Gynecol Endocrinol,2014,19(1):1-4.
[8]张文杰,冯玉昆,王珏,等.卵泡液中Leptin与体外受精-胚胎移植结局的关系[J].中国优生与遗传杂志,2006,14(7):106-107.
[9] Ostanin A A,Aizikovich B I,Aizikovich I V,et al.Role of cytokines in the regulation of reproductive function[J].Bull Exp Biol Med,2007,143(1):75-79.
[10] Stephen F,Ruth R,Kate H.Gonadotrophin regimens and oocyte quality in women with polycystic ovaries[J].RBM online,2002,6(2):181-184.
[11] Smimakis K V,Plati A,Wolf M,et al.Predicting gestational diabetes:choosing the optimal early serum marker[J].Am J Obstet Gynecol,2007,196(4):410-416.
[12] Boomsma C M,Eijkemans M J,Hughes E G,et al.A meta analysis of pregnancy outcomes in women with polycystic ovary syndrome[J].Hum Reprod Update,2006,12(6):673-683.
