进展期胃癌患者D2根治手术后S-1单药或联合奥沙利铂辅助化疗方案的疗效对比研究
2015-04-14李定云凌亚非赖家骏翁伟明胡志伟李治国
李定云,张 涛,凌亚非,赖家骏,翁伟明,胡志伟,李治国
(粤北人民医院胃肠外科,广东 韶关 512026)
进展期胃癌患者D2根治手术后S-1单药或联合奥沙利铂辅助化疗方案的疗效对比研究
李定云,张 涛,凌亚非,赖家骏,翁伟明,胡志伟,李治国
(粤北人民医院胃肠外科,广东 韶关 512026)
目的 研究国产替吉奥胶囊(S-1)单药与联合奥沙利铂辅助化疗方案在进展期胃癌患者D2根治手术后的疗效和安全性。方法选择D2根治手术后进展期胃癌患者100例,采用隐匿数字随机法分为两组,每组50例,A组给予S-1单药化疗;B组患者给予S-1联合奥沙利铂化疗,记录化疗期间毒副反应,所有患者随访3~36个月,记录患者1年、2年、3年总生存率、无复发生存率。结果A组1年、2年、3年生存率分别为100.00%、100.00%、83.67%,无瘤生存率分别为100.00%、81.63%、67.35%,B组三年总生存率分别为100.00%、100.00%、95.83%,无瘤生存率分别为100.00%、91.67%、81.25%,两组1年、2年总生存率与1年无瘤生存率比较,差异均无统计学意义(P>0.05),但B组3年总生存率,2年、3年无瘤生存率明显高于A组,差异均有统计学意义(P<0.05)。A组3年复发转移率为32.65%,明显低于B组,B组消化道毒副反应、血液学毒性发生率高于A组,差异均有统计学意义(P<0.05)。结论两种辅助化疗方案均可延长进展期胃癌患者术后无瘤生存期和总生存期,联合治疗效果更佳,但也会增加毒副反应发生率,因此在方案的选择上应根据患者的耐受性加以选择。
进展期胃癌;D2根治术;替吉奥胶囊;奥沙利铂;化疗;比较
东北亚地区是全世界胃癌最高发的地区之一[1]。近年来,随着环境污染、食品污染日益严重,我国恶性肿瘤发病率和死亡率在不断攀升,胃癌作为我国发病率和死亡率最高的恶性疾病之一,临床检出率也在逐年增加[2]。目前,手术是胃癌治疗的主要有效手段,但术后观察结果显示,有近一半的患者术后出现复发转移,D2根治术虽然扩大了淋巴结清扫范围,减少了进展期胃癌患者术后肿瘤相关死亡的发生,但进展期胃癌患者的5年生存率仍维持在较低的水平,与日本等医学发达国家比较仍存在较大差距[3]。为了减少患者肿瘤相关死亡的发生,延长无瘤生存期和总生存期,术后的辅助化疗是其有效手段之一。本研究比较了国产S-1单药与联合奥沙利铂两种辅助化疗的疗效,为进展期胃癌术后的治疗提供参考,现报道如下:
1 资料与方法
1.1 一般资料 选取我院2010年8月至2011年8月D2根治手术后进展期胃癌患者100例,男性63例,女性37例,年龄31~64岁,平均(42.3±11.3)岁;预计研究时间为24个月。按日本胃癌研究会TNM分期[4],其中Ⅱ期38例,Ⅲa期42例,Ⅲb期20例;根治性全胃切除32例,根治性胃大部切除68例,清扫淋巴结17~23枚,平均(20.3±3.3)枚,术后病理学诊断均为R0切除。采用隐匿数字随机法分为两组,每组50例,A组给予S-1单药化疗;B组患者给予S-1联合奥沙利铂化疗。两组患者在年龄、性别、TNM分期、手术类型、切除范围、淋巴结清扫个数等方面比较差异均无统计学意义(P>0.05),具有可比性。
1.2 纳入及排除标准 本次研究经院伦理委员会批准,所有患者知情同意并签署知情同意书后实施。纳入标准:①年龄18~70岁,经病理组织学证实的Ⅱ期、Ⅲ期进展期胃癌患者,ECOG评分0~2分;②符合腹腔镜胃癌适应证和禁忌证,均行腹腔镜胃癌根治术;③血流动力学指标正常;白细胞(WBC)>4.0×109/L,血小板>100×109/L,胆红素<1.5倍正常参考值上限,谷草转氨酶和谷丙转氨酶肌酐<2.5倍正常参考值上限;④心脏功能良好;⑤无不可控制的良性疾病如肺部、肾脏、肝脏、感染等。排除标准:①半年内有心脑血管意外发作患者;②不可控制的高血压、冠心病患者,对本次研究药物过敏,妊娠或哺乳期及研究期间有生育要求者;③伴腹膜、肝脏或远处转移患者;④细胞学检查腹水中发现肿瘤细胞患者;⑤治疗前及治疗过程中参加其他研究项目的患者。
1.3 治疗方法
1.3.1 A组给药方法 S-1(鲁南制药集团山东新时代药业有限公司)40~60 mg,2次/d,第1~14天连续给药;3周为1个周期,至术后1年,共16个周期。研究过程中根据不良反应事件发生的等级进行适量的调整,Ⅰ级毒性反应无需减量或中止,Ⅱ~Ⅳ级毒性反应则按标准进行减量或终止治疗,本组患者中1例因毒副反应不能耐受于第5周期中止治疗。
1.3.2 B组给药方法 奥沙利铂(江苏恒瑞医药股份有限公司)100 mg/m2静脉滴注第1天给药;S-1 40~60 mg2次/d,第1~14天连续给药;3周为一个周期,共6个周期。联合化疗结束后以S-1单药40~60 mg,2次/d,第1~14天连续给药,维持治疗至术1年,共10个周期,毒副反应处理同A组,本组患者中2例因毒副反应不能耐受分别于第3、4周期中止治疗。
1.4 观察指标 本研究的肿瘤疗效评估为终点事件的发生(包括肿瘤复发/转移/死亡),复发转移的诊断以影像学检查(CT、MRI、PET-CT、X-Ray、B超)、内镜检查和/或组织学、细胞学的客观证据。治疗过程中毒副反应根据NCI毒性分级标准进行评价[5]。
1.5 统计学方法 数据采用SPSS13.0统计学处理,计量资料以均数±标准差(±s)表示,组间比较采用t检验,计数资料采用χ2检验,用Logistic回归分析对总生存率及无复发生存率进行探索性分析,变量用Kaplan-Meier方法进行估计,提供中位事件发生时间和可信区间,计算中位时间的95%双侧可信区间(CI),根据可能出现的异质性因素进行亚组分析,以χ2检验各研究的异质性。以P<0.05为差异有统计学意义。
2 结果
2.1 两组胃癌患者生存期比较 两组1年、2年总生存率与1年无瘤生存率比较差异均无统计学意义(P>0.05),但B组3年总生存率明显高于A组,2年、3年无瘤生存率明显高于A组,差异均具有统计学意义(P<0.05)。经显著性检验显示结果差异有统计学意义(P<0.05)。异质性检查中没有异质性(P>0.05),95%CI在可信区间,见表1~4。
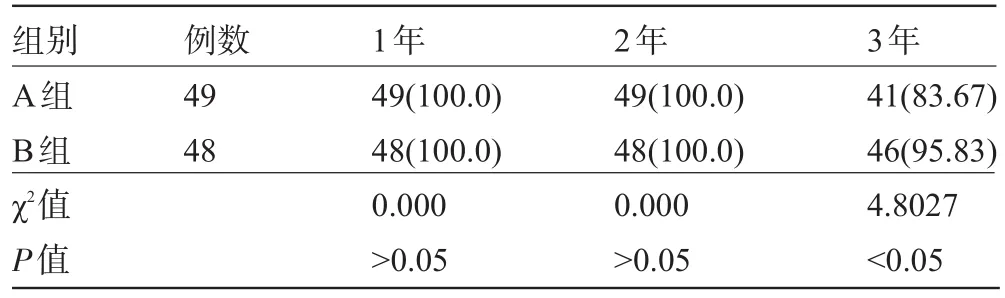
表1 两组胃癌患者1年、2年、3年总生存情况比较[例(%)]
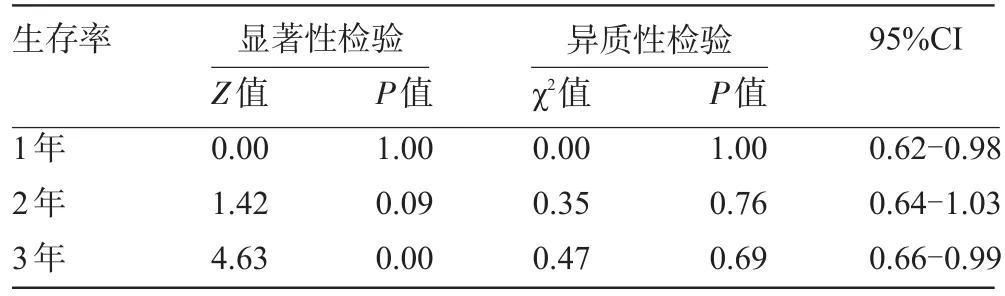
表2 总生存率Logistic回归分析
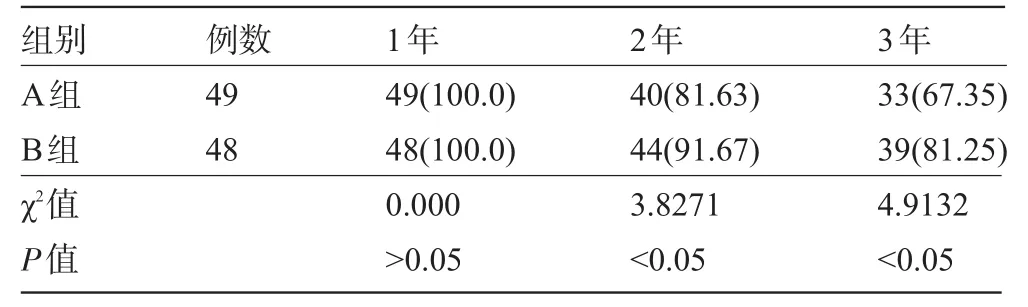
表3 两组胃癌患者1年、2年、3年无瘤生存情况比较[例(%)]
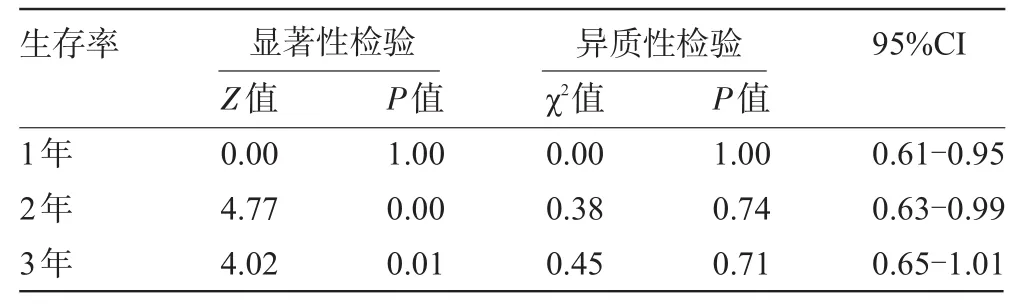
表4 无瘤生存率Logistic回归分析
2.2 复发转移情况比较 A组3年复发转移16例,复发转移率为32.65%;B组3年复发转移9例,复发转移率为50.00%;差异具有统计学意义(χ2= 4.9132,P<0.05),见表5。

表5 两组胃癌患者3年复发转移情况比较[例(%)]
2.3 毒副反应比较 B组消化道毒副反应、血液学毒性发生率均高于A组,差异具有统计学意义(P<0.05),见表6。
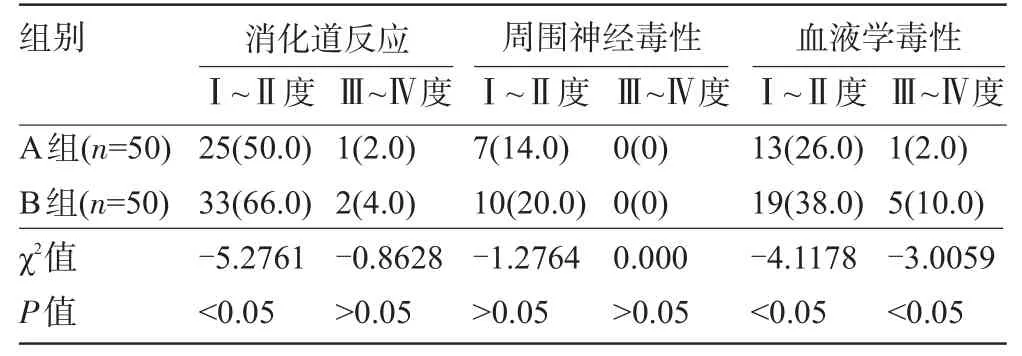
表6 两组胃癌患者主要毒副反应比较[例(%)]
3 讨论
进展期胃癌是指癌组织已侵胃壁肌层、浆膜层,与病灶大小、是否伴转移无关[6]。D2根治手术是进展期胃癌中国版指南推荐的手术治疗NCCN的标准术式[7],也是患者获得治愈的唯一途径。但从术后患者的远期疗效观察显示,日本在2009年胃癌根治性切除率为91.9%,患者5年生存率达到50%。而在我国,胃癌患者根治术后5年生存率仅为30%,与日本相比还存在较大的差距。原因之一是我国的医疗技术水平还落后于日本等国家,另一个主要原因是我国胃癌患者在明确诊断时,约90%为进展期,其中Ⅲb、Ⅲc、Ⅳ期患者所占比例超过50%,而在日本,胃癌患者就诊早,Ⅰ期胃癌居多。同时由于我国目前缺乏有效的胃癌根治术后控制转移和复发的治疗措施,因此,部分进展期胃癌患者,特别是Ⅲb分期以上的患者,术中虽然达到R0切除,其远期疗效仍不乐观,5年生存率一直未得到明显的提高。
目前我国胃癌学者已经基本达成共识,大多数进展期胃癌患者靠根治手术无法达到生物学意义上的根治[8]。因此,在提高诊断水平、提高早期诊断率的基础上,探讨进一步提高进展期胃癌患者的远期疗效的治疗方法对患者具有重要意义。近年来联合治疗方法不断应用于肿瘤的治疗中对延长患者的生存期有一定的作用。S-1是一种新型口服复合抗肿瘤药物,是以替加氟为主体,与吉美嘧啶、奥替拉西钾按(1:0.4:1)mol比值组成的[9]。药理作用是阻止氟尿嘧啶活化物降解,特异性抑制肠道黏膜细胞内乳清酸核糖转移酶,阻断5-FU的磷酸化,具有半衰期长、抗肿瘤活性强、胃肠道反应小、口服给药方便等优点。但进口S-1费用较高,国内能承受S-1治疗费用的患者较少。国产S-1在国内首先由鲁南制药集团山东新时代药业有限公司研发上市,并进行了相关二期临床试验,取得了较好的效果。陈颖等[10]选择30例局部进展期胃癌患者,于术前应用国产S-1辅助化疗,并与同期单纯手术治疗的患者进行对照结果显示,化疗组一年生存率达明显高于对照组,提示国产S-1辅助化疗可提高近期疗效。本研究对100例患者进行了对照研究,将国产S-1单药联合奥沙利铂辅助化疗方案应用于进展期胃癌患者D2根治术后,联合化疗旨在发挥两种药物的协同作用,进一步延长生存期,从应用效果显示,两组3年总生存率达83.67%和95.83%,高于国内平均水平,无瘤生存率分别为67.35%、81.25%,提示联合辅助化疗是进展期胃癌患者根治术后的有效手段。但副反应观察结果显示,联合化疗较单药化疗会增加消化道毒副反应、血液学毒性的发生率,因此,在术后化疗方案的选择上应视患者耐受情况而定。
随着医疗科学技术的不断发展,联合治疗已逐渐成为慢性疾病治疗的发展方向,积极研究和改进胃癌综合治疗方法,发挥各种治疗手段的优势使众多患者获益是医疗工作者追求的目标。国产S-1价格优惠,而且是医保药物,术后1年的治疗费用能为我国大多数居民所能承担,同时本研究结果中总生存率和无瘤生存率均经异质性检查无异质性,提示两组在临床试验中差异无统计学意义,提示S-1用于进展期胃癌术后辅助化疗在临床上值得推广应用。但因本研究只局限于单中心报道,入组对象尚有限,且术后随访时间较短,S-1单药或联合奥沙利柏治疗进展期胃癌远期疗效尚有待于更大样本的多中心随机对照研究进一步明确。
[1]樊翠珍,初玉平,戴 红,等.卡培他滨联合奥沙利铂与替吉奥联合奥沙利铂治疗进展期胃癌的对比研究[J].临床肿瘤学杂志, 2011,16(8):725-727.
[2]马晴晴,曲颜丽,唐 勇.替吉奥或奥沙利铂联合紫杉醇脂质体治疗进展期胃癌的临床分析[J].中国肿瘤临床,2014,41(3): 200-203.
[3]刘 林,杨新辉,王海江,等.多西他赛联合奥沙利铂及替吉奥治疗进展期胃癌的疗效及对围手术期影响[J].中国肿瘤临床,2013, 40(13):788-791.
[4]傅国平,王 薇,裘哲君,等.替吉奥联合奥沙利铂或顺铂治疗进展期胃癌的临观察[J].中国癌症杂志,2012,22(4):291-294.
[5]段训凰,徐 欢,龚敏勇,等.替吉奥胶囊联合奥沙利铂治疗进展期胃癌的临床研究[J].江西医药,2014,4:286-288.
[6]尹良伟,马海英,张春妹,等.替吉奥分别联合奥沙利铂、多西他赛与顺铂治疗进展期胃癌的比较研究[J].现代中西医结合杂志, 2012,21(24):2628-2630.
[7]宋金成,张 弦,张 阳,等.替吉奥联合奥沙利铂与改良FOLFOX6方案一线治疗进展期胃癌的随机对照研究[J].实用临床医药杂志,2013,17(3):63-65.
[8]邵 华,孙 威,李 岩,等.替吉奥胶囊联合奥沙利铂与FOLFOX4方案对晚期胃癌疗效的对比研究[J].现代肿瘤医学,2013, 21(6):1273-1276.
[9]Koizumi W,Takiuchi H,Yamada Y,et al.PhaseⅡstudy of ox-aliplatin plus S-l as first-line treatment for advanced gastric cancer (G-SOX study)[J].Ann Oneol,2010,21(5):1001-1005.
[10]陈 颖,邵 俊,邓周峰,等.S-1新辅助化疗联合手术治疗30例局部进展期胃癌的临床观察[J].现代肿瘤医学,2013,12(21): 2746-2749.
Comparative study of curative effect of S-1 monotherapy or S-1 and oxaliplatin combination chemotherapy for patients with advanced gastric cancer after D2 radical operation.
LI Ding-yun,ZHANG Tao,LING Ya-fei,LAI Jia-jun,WENG Wei-ming,HU Zhi-wei,LI Zhi-guo.
Department of Gastrointestinal Surgery,Yuebei People's Hospital, Shaoguan 512026,Guangdong,CHINA
ObjectiveTo study the efficacy and safety of S-1 monotherapy or S-1 and oxaliplatin combination chemotherapy for patients with advanced gastric cancer after D2 radical operation.MethodsOne hundred patients with advanced gastric cancer after D2 radical operation were selected and randomly divided into two groups, with 50 cases in each group.Group A received S-1 monotherapy,while group B was treated by S-1 combined with oxaliplatin chemotherapy.The adverse reactions of chemotherapy period were recorded.All patients were followed up for 3~36 months.The 1-year,2-year and 3-year overall survival rates were recorded,as well as the recurrence free survival rate.ResultsThe 1-year,2-year and 3-year overall survival rates were 100.00%,100.00%,83.67%in group A and 100.00%,100.00%,95.83%in group B,respectively.Tumor-free survival rates were 100.00%,81.63%, 67.35%in group A and 100.00%,91.67%,81.25%in group B.The two groups showed no statistically significant difference in 1-and 2-year overall survival rates,1-year tumor-free survival rate(P>0.05),but the 3-year overall survival rate,2-and 3-year tumor-free survival rate in group B were significantly higher than those in group A(P<0.05).The 3-year recurrence/transfer rate was 32.65%in group A,significantly lower than that of group B.The incidence of gastrointestinal toxicity,hematologic toxicity in group B were significantly higher than those in group A(P<0.05).ConclusionThe two therapies can both prolong the tumor-free survival and overall survival for patients with advanced gastric cancer after D2 radical operation.The combined treatment has better efficacy but results in higher adverse reactions rate.Therefore,the therapies should be selected based on the tolerance of patients.
Advanced gastric cancer;D2 radical operation;S-1;Oxaliplatin;Chemotherapy;Comparison
R735.2
A
1003—6350(2015)06—0812—04
10.3969/j.issn.1003-6350.2015.06.0291
2014-09-21)
2012年韶关市医药卫生科研计划项目(编号:Y12147)
李定云。E-mail:ldy152138@163.com
