消石利尿化瘀法降低高尿酸血症大鼠血清尿酸及其机理的研究
2015-03-21王林元黄银峰王丽丽李艳霞
王 淳 王林元 郑 媛 黄银峰 王丽丽 李艳霞
(1 北京中医药大学基础医学院,北京,100029; 2 北京中医药大学中药学院,北京,100029)
实验研究
消石利尿化瘀法降低高尿酸血症大鼠血清尿酸及其机理的研究
王 淳1王林元2郑 媛1黄银峰1王丽丽1李艳霞1
(1 北京中医药大学基础医学院,北京,100029; 2 北京中医药大学中药学院,北京,100029)
目的:研究以消石利尿化瘀法为指导创制的中药复方对高血酸血症大鼠血清尿酸的影响,并对其作用机理进行探讨。方法:雄性Wistar大鼠随机分为空白组、模型组、痛风定胶囊组、苯溴马隆组及中药复方组(6.07 g/kg、3.03 g/kg)共6组。除空白组外,其余各组以腺嘌呤和乙胺丁醇灌胃,同时各给药组灌胃给予相应的药物;空白组和模型组给予等体积蒸馏水,连续10 d。末次给药后,取血,分离血清,以紫外分光光度法测定大鼠血清尿酸(UA)、尿素氮(BUN)的含量及黄嘌呤氧化酶(XOD)的活性;用放射免疫分析法测定大鼠血清中尿酸盐转运蛋白(UAT)、有机阴离子转运蛋白(OAT)的含量。结果:中药复方高、中剂量组大鼠血清UA含量较模型组均降低(P<0.05,P<0.01);中药复方高剂量组大鼠血清XOD活性与模型组比较,明显降低(P<0.01);中药复方中剂量组大鼠血清BUN含量较模型组显著降低(P<0.05);中药复方高剂量组大鼠血清UAT含量与模型组比较,明显升高(P<0.01);中药复方高、中剂量组大鼠血清OAT含量与模型组比较,均明显升高(P<0.01)。结论:以消石利尿化瘀法创制的中药复方能降低高尿酸血症大鼠血清尿酸含量;其降尿酸机理可能与抑制XOD活性、减少尿酸生成,以及保护肾功能、增加UAT、OAT的含量、促进尿酸分泌与排泄有关。
高尿酸血症;UA;UAT;OAT;消石利尿化瘀法
高尿酸血症是痛风发病的生化基础,属于难治性疾病。2003年邵继红[1]等在南京的调查显示:高尿酸血症患病率(男女合计)已达13.3%,与欧美地区2%~18%的水平持平;痛风患病率达1.33%。随着生活水平的日益提升,饮食结构的逐渐改变,高尿酸血症和痛风的发病率呈日趋上升趋势。中医药治疗痛风有悠久的历史,积累了丰富的临床经验,有一定的优势。课题组根据前期研究,针对高尿酸血症属于湿热、浊瘀互阻的基本病机特点,针对尿酸盐结晶属于结石的客观事实,结合临床用药经验,确立以消石化瘀利尿法论治高尿酸血症,拟定中药复方,前期研究已经证实了其对高尿酸血症小鼠有降低血清尿酸的作用[2],为进一步确证其作用并探讨机制,我们以高尿酸血症大鼠模型进行研究。
1 材料与方法
1.1 药物 中药复方(由金钱草、土茯苓、粉防己、黄柏、萆薢、三七、川牛膝、赤芍、青风藤等组成):北京中医药大学基础医学院临床中药室制备;苯溴马隆/立加利仙:江苏昆山龙灯瑞迪制药有限公司,批号:1010342;痛风定胶囊:成都中汇制药有限公司,批号:100703。
1.2 试剂 腺嘌呤,北京奥博星生物技术有限责任公司,批号:20101205;盐酸乙胺丁醇片,杭州民生药业集团有限公司,批号:T10F541;尿酸试剂盒,南京建成生物工程研究所,批号:20100605;UAT ELISA试剂盒,Adlitteram Diagnostic Laboratorie产品,批号:RT10370;OAT ELISA试剂盒,Adlitteram Diagnostic Laboratorie产品,批号:RT10370。
1.3 动物 清洁级健康雄性Wistar大鼠60只,体重(200±10)g,由中国医学科学院实验动物研究所提供,动物合格证号:SCXK(京)2013-0001。
1.4 仪器 TGL-16A台式高速冷冻离心机,长沙平凡仪器仪表有限公司;SK-1快速混匀器,江苏国华仪器厂;752紫外光栅分光光度计,上海精密科学仪器有限公司;恒温水浴锅,北京长风仪器仪表公司;酶标仪,Thermo MULTISKAN MK3。
1.5 方法
1.5.1 动物分组及给药方法[3]取雄性Wistar大鼠70只,随机分为空白组、模型组、苯溴马隆组(benzbromarone)、痛风定胶囊组(TFD)及中药复方高、中、低剂量组共7组,每组10只。除空白组外,其余各组以腺嘌呤100 mg/kg及乙胺丁醇250 mg/kg灌胃,连续10 d。同时各给药组灌胃给予相应的药物,痛风定胶囊组剂量为0.56 g·kg-1·d-1(相当于成人临床用量的7倍);苯溴马隆组剂量为10 mg·kg-1·d-1(相当于成人临床用量的7倍);中药复方高、低剂量组剂量按生药计,分别为6.07 g/kg、3.03 g/kg、1.52 g/kg(分别相当于成人每日用量的14倍、7倍、3.5倍);空白组和模型组给予等体积蒸馏水,连续10 d。
1.5.2 观察指标 末次给药后2 h,各组动物水合氯醛麻醉后,腹主动脉取血,分离血清,采用生化法按说明书测定大鼠血清UA、BUN含量及XOD活性;以放射免疫分析法测定血清UAT、OAT含量。
2 结果
实验结果表明:模型组大鼠血清UA含量较空白组显著升高(P<0.01);苯溴马隆组及中药复方中剂量组大鼠血清UA含量均较模型组显著降低(P<0.01)。中药复方高剂量组大鼠血清UA含量较模型组亦降低,差异有统计学意义(P<0.05)。
模型组大鼠血清XOD活性较空白组显著升高(P<0.01);中药复方高剂量组大鼠血清XOD活力单位与模型组比较,明显降低(P<0.01)。但各治疗组大鼠血清XOD活力单位与空白组比较,均显著升高(P<0.01)。
模型组大鼠血清BUN含量较空白组显著升高(P<0.01);中药复方中剂量组大鼠血清BUN含量较模型组显著降低(P<0.05)。其余各治疗组大鼠血清BUN含量较模型组亦降低,但没有统计学意义(P>0.05)。
酶联免疫测定结果表明:模型组大鼠血清UAT较空白组明显降低(P<0.01)。苯溴马隆组及中药复方高剂量组大鼠血清UAT含量均较模型组显著升高(P<0.01)。
模型组大鼠血清OAT较空白组大鼠明显降低(P<0.01)。苯溴马隆组、痛风定组及中药复方高、中剂量组大鼠血清OAT含量均较模型组显著升高(P<0.01)。

表1 中药复方对高尿酸血症大鼠模型血清UA、XOD、BUN的影响
注:与空白组比较,*P<0.05;**P<0.01;与模型组比较,ΔP<0.05;ΔΔP<0.01。
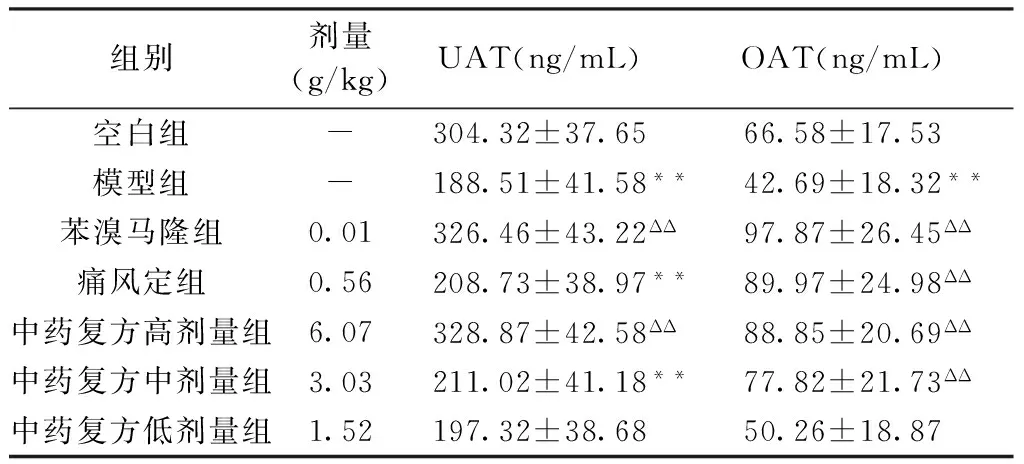
表2 中药复方对高尿酸血症大鼠模型血清UAT、
注:与空白组比较,*P<0.05;**P<0.01;与模型组比较,ΔP<0.05;ΔΔP<0.01。
3 讨论
高尿酸血症是痛风发生的重要生化基础。小鼠雌雄个体及同性别个体之间血清尿酸正常值差异较大,作为一种疾病动物模型,个体之间差异过大[4],则实验结果的准确性会受到影响。因此,本实验建立高尿酸血症大鼠模型进行研究,结合临床发病的实际情况,痛风患者男女比例为20∶1,故实验中所用动物均为雄性大鼠。
黄嘌呤氧化酶(XOD)能催化黄嘌呤和次黄嘌呤的氧化进而生成尿酸,并产生过氧化物自由基。尿酸浓度过高会导致高尿酸血症,并可引起痛风的发作。自由基涉及到炎性反应、动脉硬化、癌症和衰老等病理过程[5]。XOD能明显促进动脉粥样硬化斑块中平滑肌细胞(SMC)的增殖;平滑肌细胞是动脉粥样硬化(AS)斑块中的主要细胞,它的增殖在AS形成过程中具有十分重要的意义,而氧自由基可以促进血管平滑肌细胞增殖进而诱发AS[6]。因此,减少体内尿酸和过氧化氢的方法之一是降低人体内XOD的活性。
一个对6 403例患者的调查发现,血清尿酸是肾脏疾病进展的独立危险因素,其危险性甚至高于蛋白尿[7]。临床上痛风患者约20%左右有慢性进展的肾脏病变[8],而尸体解剖证实痛风患者有肾脏病变者高达100%[9]。因此,痛风病中出现最早,而且又能危及患者生命的是痛风性肾病[10]。BUN是反映肾脏功能的客观指标。患有肾脏疾病时,尿酸盐清除受损,血尿酸盐水平呈升高倾向。
人尿酸盐转运蛋白(hUAT),为电压敏感性的尿酸转运蛋白。广泛表达于各种组织,主要表达于上皮源性细胞,其中在肾脏表达最丰富,为贯穿细胞膜的高度选择性离子通道[11-12]。hUAT是尿酸由细胞内到细胞外的关键转运体,进入肾近端小管的尿酸盐50%由其介导分泌到细胞外,排出体外[13]。研究者提出hUAT作为将尿酸盐分泌至肾近曲小管腔的产电通道,其基因变异可限制细胞内尿酸盐的外流从而影响肾脏尿酸的分泌,因此可能成为导致疾病的始动的细胞内改变。同时由于hUAT的mRNA在肠道表达较为丰富,肠道中hUAT可能发挥与在肾脏相似的分泌功能[14]。因此认为hUAT在调节全身尿酸盐的稳态中起重要作用。有机阴离子转运体(OAT)有2种蛋白,OAT1和OAT3;OAT1主要表达于近曲小管的基底膜,参与对氨基马尿酸(PAH)转运,有学者提出在尿酸盐分泌的第一步,即将尿酸盐从管周间隙摄取入肾小管细胞这一过程中OAT1起重要作用;OAT1的缺陷会引起血尿酸水平的升高,hOAT1基因突变可能与家族性青年性痛风性肾病(Familial Juvenile Gouty Nephropathy,FJGN)有关[15]。hOAT3基因表达于肝脏、肾脏、脑及眼组织,在近端肾小管的各段均有表达。Erdman等[16]研究发现,hOAT3是一个有机阴离子/二羧酸盐转运子,可能参与肾脏尿酸盐的转运,但具体作用机制目前还不清楚,因其位于肾小管的基底膜,推测其可能参与管周细胞摄取尿酸盐,从而有利于尿酸盐的分泌,或者与基底膜的尿酸盐排入管周毛细血管及随后的尿酸盐重吸收有关。
中医学认为,高尿酸血症患者多有先天禀赋异常,或素体脾胃虚弱,或年迈脏腑功能逐渐衰退,若加之饮食不节,沉溺酒酪,嗜啖膏粱厚味,长此以往,致脾失健运、升清降浊无权,水谷不归正化,湿浊随之而酿生,留滞脏腑而发病。湿热浊毒外注皮肉关节可致痛风性关节炎、痛风石的形成;湿热浊邪久蕴,化热入血,血中湿热浊毒稽留,可致痛风性肾病的发生,而发石淋、尿血。总之,湿热浊毒郁积日久,阻滞络脉,遂致瘀成,湿热浊瘀互结,是导致本病发生的根本。基于尿酸钠盐的结石属性,基于90%的高尿酸血症是由尿酸排泄减少所引起的客观事实[17],基于瘀浊稽留的基本病机,确立消石利尿化瘀法,消石利尿以促进尿酸盐的代谢、排泄,活血化瘀以消肿止痛、保护机体,创制中药复方进行论治。方中金钱草消石化坚散结,清热利尿,解毒消肿;土茯苓、粉防己、黄柏、萆薢、川牛膝同用以清热除湿、利尿泻浊;三七、赤芍相伍有化瘀定痛、活血消肿之功;青风藤通络止痛、利尿消肿。其中黄柏、牛膝、防己、土茯苓等为治疗痛风常用的核心药物[18]。全方共奏消石化坚散结,利尿除湿泻浊、化瘀通脉止痛之功。
研究显示,对于不同方法造成的高尿酸血症动物模型,以消石利尿化瘀法论治,均能有效降低血清尿酸含量[2],为治疗高尿酸血症提供最基础的药效支撑;能降低高尿酸血症大鼠模型血清的XOD活性,说明消石化瘀利尿法可能通过抑制XOD活性,减少尿酸的生成,达到降低血清尿酸和防治痛风的作用;同时,也可能通过抑制XOD活性而对预防和治疗高尿酸血症的并发症发挥积极、重要的作用;对高尿酸血症模型所表现的血清BUN升高有显著的降低作用,说明消石利尿化瘀法可改善肾脏功能,对预防痛风性肾病有积极意义;还可以通过保护肾脏功能而利于尿酸的排泄,形成良性循环。该方促进尿酸排泄的机制可能与促进UAT、OAT的表达有关。
综上所述,以消石利尿化瘀法指导组方论治高尿酸血症,辨证用药与辨病用药相结合,传统中医理论与现代医学及药理研究成果相结合,“消石”可促进尿酸代谢,抑制尿酸盐结晶;“利尿”促进尿酸排泄;“化瘀通脉”可消散瘀浊、保护机体;标本兼治。既有理论依据,又取得了实验研究所奠定的药效基础,可对临床论治高尿酸血症提供借鉴。
[1]李剑,田慧,李春霖,等.老年男性高尿酸血症与心血管危险因素[J].中国医刊,2011,46(10):33.
[2]王淳,高学敏,张建军.苓丹痛风康胶囊抗痛风作用的实验研究[J].中华中医药杂志,2008,23(8):742-744.
[3]张慧敏,艾辉,王娱.高尿酸血症与冠心病患者性别关系的研究[J].中国医药,2013,8(8):1048-1050.
[4]陈光亮,朱立然,那莎,等.萆薢总皂苷对大鼠慢性高尿酸血症和肾小管尿酸转运体1表达的影响[J].中国中药杂志,2013,38(14):2348.
[5]Halliwell B,Gutteridge JM,Cross CE.Free radicals,antioxidants,and human diseases:where are we now?[J].Lab.Clin.Med,1992,119(6):598-620.
[6]Nishio E,Watanabe Y.The involvement of reaction oxygen species and arachidonic acid in a adrenoceptor.Induced-smooth muscle cell proliferation and migration[J].British Journal of Pharmacology,1997,84:113-121.
[7]Johnson RJ,Kang DH,Feig D,et al.Is there a pathogenetic role for uric acid in hypertension and cardiovascular and renal disease[J].Hypertension,2003,41(6):1183.
[8]董德长.内科各系统疾病与肾脏[M].北京:人民卫生出版社,1996:197.
[9]叶任高,刘冠贤.临床肾脏病学[M].北京:人民卫生出版社,1997:123.
[10]张开富.痛风临床防治指南[M].北京:人民军医出版社,2006:82.
[11]Leal-Pinto E,Tao W,Rappaport J,et al.Molecular cloning and functional reconstitution of a urate transporter/channel[J].J Biol Chem,1997,272:617.
[12]Leal-Pinto E,Cohen BE,Lipkowitz MS,et al.Functional analysis and molecular model of the human urate transporter/channel,hUAT[J].Am J Physiol Renal Physiol,2002,283(1):150.
[13]Lipkowitz MS,Leal-Pinto E,Cohen BE,et al.Galectin9 is the sugarregulated urate transporter/ channel UAT[J].Glycoconj J,2004,19:491.
[14]Hyink DP,Rappoport JZ,Wilson PD,et al.Expression of the urate transporter/channel is developmentally regulated in human kidneys[J].Am J Physiol Renal Physiol,2001,281:875.
[15]Ichida K,Hosoyamada M,Kimura H,et al.Urate transport via human PAH transporter hOAT1 and its gene structure[J].Kidney Int,2003,63:143-155.
[16]Erdman AR,Mangravte LM,Urban TJ,et al.The human organic anion transporter 3(OAT3;SLC22A8):genetic variation and functional genomics[J].Am J Physiol Renal Physiol,2006,290:905.
[17]叶任高.内科学[M].5版,北京:人民卫生出版社,2006:877.
[18]吕毅斌,李立,王志飞,等.中药治疗类风湿性关节炎、痛风及骨性关节炎用药规律研究[J].世界科学技术-中医药现代化,2010,12(5):833-836.
(2014-11-25收稿 责任编辑:王明)
Research on the Effect and Mechanism of “Expelling Stone, Diuresis and Removing Stasis” Method on Reducing UA in Serum of Hyperuricemia Rats
Wang Chun1, Wang Linyuan2, Zheng Yuan1,Huang Yinfeng1, Wang Lili1, Li Yanxia1
(1SchoolofBasicMedicalsciencesBUCM,Beijing100029,China;2SchoolofChineseMateriaMedicaBUCM,Beijing100029,China)
Objective:To investigate the effect and mechanism of Chinese herbal compounds prescription, which based on the traditional therapeutics of “expelling stone, diuresis and removing stasis”, on uric acid (UA) in rats with hyperuricemia. Methods: Male Wistar rats were randomly divided into normal group, model group, Tongfengding Capsules group, Benzbromarone group and Chinese herbal compounds prescription group(TFK) in two doses of 6.07 g·kg-1and 3.03 g·kg-1. In addition to the normal group, the rest were offered with Ademine and the Ethambutol for 10 days. While the appropriate drugs administered to the rats of the administration group, the normal group and the model group were given by gavage distilled water for 10 days. Then blood was collected, UA, BUN content and XOD activity in serum were determined by ultraviolet-visible spectroscopy while UAT、OAT content in serum were detected by radiommunoassay. Results: Compared with the model group, the concentration of UA in high-dose and middle-dose Chinese herbal compounds prescription group significantly decreased in serum(P<0.05,P<0.01). The level of XOD activity of high-dose group significantly decreased as compared to the model group (P<0.01). The BUN content of middle-dose group was decreased in serum compared to the model group (P<0.05). The UAT content of high-dose group compared to the model group was significantly increased (P<0.01). The content of OAT in high-dose and middle-dose group was significantly increased in serum compared to the model group (P<0.01). Conclusion: The Chinese herbal compounds prescription which based on the traditional therapeutics of “expelling stone, diuresis and remove stasis” decreased the uric acid content in hyperuricemia model rats. The mechanism may be related to the relieving effect of the activation of XOD, reducing generation of uric acid, protecting renal function, increasing of UAT and OAT content and promoting excretion of uric acid.
Hyperuricemia; UA; UAT; OAT; Expelling stone; Diuresis and removing stasis
国家自然科学基金面上项目(81273632)——基于P38-NF-κB-MCP-1路径的消石利尿化瘀法保护高尿酸血症大鼠血管内皮功能的研究,负责人:王淳
王林元,副教授,主要研究方向:中药产业化应用;王淳,副教授,主要研究方向:中医药防治痛风,E-mail:wangyl@bucm.edu.cn
R259;R285.5
A
10.3969/j.issn.1673-7202.2015.03.022
