木质素光降解机理研究进展
2015-03-21于海霞方崇荣于文吉
于海霞 方崇荣 于文吉
(1.中国林业科学研究院,北京 100091;2.浙江省林产品质量检测站,浙江省森林资源生物与化学利用重点实验室,浙江 杭州 310023)
木质素光降解机理研究进展
于海霞1,2方崇荣2于文吉1
(1.中国林业科学研究院,北京 100091;2.浙江省林产品质量检测站,浙江省森林资源生物与化学利用重点实验室,浙江 杭州 310023)
从木质素模型及原本木质素2个方面综述木质素光降解的研究现状。木质素模型研究表明,光降解是典型的自由基反应,主要通过游离酚途径、羰游基途径和苯甲酰甲基芳醚途径反应,苯氧自由基是光化学反应的重要中间产物。木质素光降解是个氧化过程,伴随着碳的氧化态升高、非共轭羰基减少、共轭羰基增加,大分子木质素发生解聚,最终形成对醌、邻醌等发色基团及苯甲酸、苯甲醛等可溶性小分子酚类化合物,木质素含量明显降低。木质素光化学反应的机理研究中,木质素模型和原本木质素存在一定差距,分子和细胞水平上的深入研究将是未来的发展方向。
木质素;光降解;苯氧自由基;共轭羰基;解聚
木质素是自然界中仅次于纤维素的生物多聚体,和半纤维素一起充填细胞壁起加固粘结作用,广泛存在于草本植物和木本植物中[1]。木质素具有芳香族特性,含有大量苯环和双键,构成了竹、木质材料表面多种多样的颜色,但同时这些基团造成了木质素的光不稳定性,如纸张或纸浆的黄化,其首要原因就是木质素的光降解。困扰户外用竹、木质材料使用寿命的表面光劣化,其原因也主要归咎于木质素的光不稳定性[2]。因此,阐明木质素的光降解机理对防护技术的开发十分重要。
近年来,国际上许多学者从木质素模型及原本木质素2个方面对木质素的降解机理进行了深入研究,取得了许多进展。为了深入木材加工基本理论的研究,促进木质复合材料工业发展,本文综述了木质素的光化学反应机理方面的研究进展。
1 木质素光化学反应影响因素研究
木质素光降解反应受内因和外因影响,内因主要与木质素本身的结构、官能团、联结方式、键能及其吸光特性等有关,而外因包括光、热、水、氧等,这里主要综述光源的影响。
1.1 木质素颜色的主要来源
木质素是具有芳香族特性的、非结晶性的三维空间结构的高聚物,其基本结构单元是苯基丙烷,并含有羟基、羰基、乙烯基等官能团,这些官能团与苯环形成共轭体系。随着共轭度的增加,其吸光特性会发生变化,可吸收部分红色可见光。对比大多数竹、木材组分的UV吸收系数,木质素占80%~95%[3]。原本木质素中最主要的发色基团是各种环共轭乙烯基团,如肉桂酸(苯丙烯醇)和肉桂醛基团,以及羰基结构,如α-羰基和醌[4]。
1.2 光源与光化学反应
经过大气层的吸收,照射在地球上的光最短波长为295 nm,紫外光(295~400 nm)占太阳光总辐照度的6.8%,而木质素中大多数碳-氧基团的光离解其波长都分布在295~400 nm[2]。一般饱和有机化合物结构以单键联结,在 200~1 000 nm 范围内光波不产生吸收高峰,但是当分子中具有共轭双键结构时,因π电子活动性大,所需要的激发能量小,吸收光波的波长较长(图1),有可能使吸收光谱从紫外光区转移到可见光区,而显出颜色。
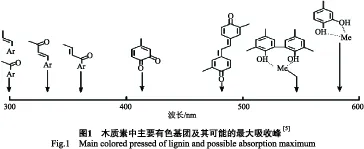
2 木质素模型光降解研究
木质素是由3种苯基丙烷单元组成的分子量为几千到几万的高分子混合物,由于木质素本身结构的复杂性,自20世纪60—70年代以来主要采用模型物来研究其光降解机理。早期研究主要从木质素基本骨架苯丙烷侧链的羰基或芳香环共轭双键对光能吸收开始。
2.1 游离酚途径
光化学反应可分为2大类:一是直接光辐射反应,二是激活的光氧化反应。对于苯酚而言,这2种反应途径都存在,主要取决于辐射波长。在300 nm以上,自由酚羟基团中的氢原子可以通过激发单态氧[6-7]、氧基自由基如羟基自由基或氢过氧化物自由基[2],或激发的羰基[8]等进行消去反应(图2~3),单态氧在氧淬灭或光诱发三重态环共轭乙烯结构中形成。如果有单态氧参与,活跃的羰基和酚基团不需要直接接触来发生反应[9]。在300 nm波长以下UV/VIS辐射游离酚可直接发生光解反应[10]。这个途径被称为游离酚途径,即通过苯酚上氢原子消去、激活结构或者直接光降解产生苯氧自由基。
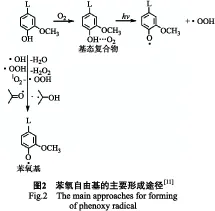

2.2 苯甲酰甲基芳基醚途径
木质素羰基类中比较特殊的类型就是苯甲酰芳基醚(2-芳基醚-1-苯基丙酮),其是木质素单元的侧链兼有α羰基和β-O-4连接的单元。苯甲酰芳基醚在液体和固体木质素模型中被广泛研究[12]。这种结构一经激发,会产生β-醚键均裂,形成苯甲酰甲基-苯氧基成对自由基(图4),这就是著名的苯甲酰甲基芳醚途径。Castellan等[13]用α-羰基-β-芳醚型结构二聚体和四聚体模拟化合物进行辐射试验,发现降解主要是分子内的β-O-C键,形成苯酰甲基和愈创木基二甲基等。最初苯甲酰甲基自由基的脱氢导致酮的形成,新形成的酮扮演光敏剂作用,导致进一步反应。进一步充当光敏剂或经历Cα-Cβ断裂,最初形成的自由基对可重新组合生成原始的β-O-4连接或其他类型的内部连接β-5。这些形式的重组反应在固体和液体木质素模型中都有发生[14]。苯甲酰甲基芳基醚断裂可能引发木质素的解聚及新的苯酚基形成,解聚(平均分子量降低)反应在一定程度上抵消了由于最初形成自由基的重组反应,形成新的β-5连接(图4)。
2.3 羰游基(乙烯酮)途径
苯氧基自由基和β-O-4键断裂产生的木质素解聚的反应机理可能是羰游基自由基途径[15](图5)。

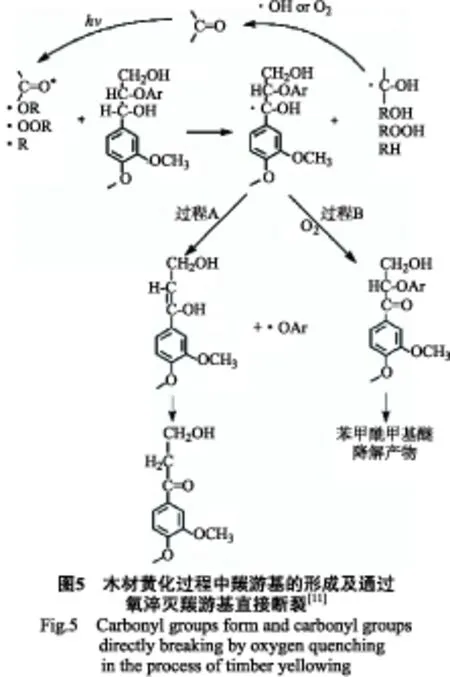
这个途径涉及最常见的木质素连接键,即芳基甘油β-芳基醚键,在软木木质素中占35%的侧链、典型阔叶材占45%的侧链的连接类型[16]。这些醚键的断裂可以解释为分子量的大量降解而不是苯甲酰甲基芳基键的断裂。芳基-酯键的断裂均由紫外光波辐射所致,而光还原发生脱氢反应则是由可见光波辐射所致。羰基一旦激发就被氧(单态氧和基态羰基)淬灭,经过Cα-Cβ断裂(Norrish I型反应)(图5),或者消去一个氢原子形成羰游基,羰基就可以作为光化学反应催化剂的角色,因为由消氢反应生成的羰游基可以与氧或者羟基自由基发生反应[17]而产生羰基。对于a羰基,这将最终导致端部结构为对羟基苯甲醛和对羟基苯甲酸等的形成[14],这是木质素模型中常见的光产物。尽管木质素中α羰基含量很少,但这种基团在光老化过程中确实起到很重要的作用。
3 有色物质的形成研究
最初解释光变色初期的黄色产物的产生途径为苯氧自由基直接形成的醌、醌甲基化合物和环己二烯酮[18],根据照射过程中甲氧基含量的减少[18-19]认为有邻醌形成。基于有氧存在情况下木质素模型化合物辐射后产生的产物模式,Lin等[20]提出苯氧自由基形成邻醌和对醌,他们提议的机理见图6。邻醌在氧和不同共振形式的稳定的苯氧自由基作用下形成,邻醌的形成是由于氧或氢自由基与芳环C3位置处反应,并伴随着甲氧基减少。对醌产物可能在芳环1位反应后产生,产生于侧链置换(图6)[11]。
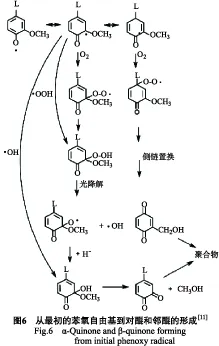
综上所述,木质素的结构复杂,其有色物质的形成研究结果总结如下:
1) 木质素光化学反应主要是自由基反应,从酚羟基中很容易生成苯氧自由基,苯氧自由基是木质素光降解中的主要中间产物。
2) 与α羰基相邻的C-C键经过Norrish I型反应被光离解,而与α羰基相邻的醚键化合物不能有效的进行Norrish I型反应。
3) α羰基在木质素的光降解中起到光敏剂的作用。
4) 苯氧自由基在光照下与氧作用诱发木质素中愈创木基的脱甲基过程,从而产生邻醌型结构,醌的形成是木质素变色的主要原因。
5) 木质素光降解过程中伴随着甲氧基的减少、木质素含量的降低及有色物质的形成。
6) 光降解过程中伴随着苯氧自由基形成木质素大分子的解聚及有色物质的形成。
由于天然木质素的复杂性,采用模型化合物是研究光降解机理的有效手段。但通常采用溶液型低分子量的木质素模型化合物,其对氧气的供应、溶液的选择自由基中间体的寿命等都存在不同,不能完全代表高分子量固态及与碳水化合物和其他木质素单体共同存在的原本木质素。近年来,随着户外用竹木质材料的开发利用,对竹木质材料直接进行人工光辐射来模拟户外自然老化进程,并采用先进仪器进行老化分析的研究开始增多。
4 原本木质素光降解机理研究
4.1 自由基的形成
自由基又称游离基,因具有不成对电子所以活泼性极强。木材并不含有固有的自由基,可为很好的吸光体,很容易与波长等于或短于可见光的电磁辐射相互作用,从而产生各种自由基。Hon等[21]提出苯氧自由基是木质素降解过程中最主要的中间产物,这些产物迅速与氧作用或和脱甲基化形成对醌结构。Kamoun等[22]采用ESR研究辐射(Pinusradista)松木质素光降解证实了苯氧自由基的存在。
4.2 木质素的氧化
自由基具有强氧化性,导致木质素光化学反应过程中碳氧比的增加。XPS测试结果表明[7],竹材表面光劣化处理后O元素含量及氧碳比(O/C)明显增加。Wang等[23]采用XPS分析发现,毛竹(Phyllostachyspubescens)材表面光降解后O/C明显增加,C1(C-C)含量减少,C2(C-O)含量增加,C3(C=O)和C4(O-C=O)含量增加明显,C的氧化态显著升高。
在光照初期,材料表面生成各种氧化态,反应激烈而变化大;随变化的深入,各种氧化态在相互竞争中,不稳定的结构逐渐让位于稳定结构,主要表现为C=O双键向C-O单键过渡,从而表现为光化学反应趋于缓和,量子产率下降。通过光电子能谱(ESCA)观察表面的氧含量增加,表明表面已经产生严重的氧化,产生新的发色基团,如羰基、羧酸和醌类物质[24]。
4.3 共轭羰基减少及非共轭羰基增加
光化学反应伴随共轭羰基的减少和非共轭羰基的生成,Wang等[23]采用红外光谱对毛竹进行光老化分析,发现木质素芳环峰 1 512 cm-1显著减少,与此同时 1 735 cm-1处的羰基增加明显,说明有新的羰基生成,羰基的增加是木质素氧化的结果。Krishna等[24]以氙灯模拟太阳光对松木(Pinusspp.)和橡胶木(Hereabrasiliensis)进行加速老化试验的研究发现,由于木质素结构发生变化,在 1 506 cm-1波数处的强度迅速下降,在试验50 h后几乎消失,并指出木材的降解速率可以通过木质素的降解速率和羰基的生成速率来推算。Muller和Seiner[25]指出,非共轭的脂肪族羰基在木质素降解过程中随着光照时间的延长,含量不断增加,而且增加的速度约为木质素降解速度的2倍。
4.4 芳环减少及木质素含量降低
因醌类化合物是不饱和环状二酮(环己二烯二酮),已不是芳香环,不具有芳香性,因此,木材发生光降解后生成的醌类化合物与原来存在于木质素中的芳香族化合物对光波的吸收产生了差异,从宏观上就形成了木材的变色[26]。光化学反应伴随着木质素的解聚、木质素含量降低及甲氧基的减少[23]。
4.5 木质素光化学反应产物
4.5.1醌类物质 Willian[2]总结了前人的研究认为,醌为木质素光化学反应的主要基团。主要分邻醌和对醌,苯氧自由基与氧作用可诱发木质素中愈疮木基的脱甲基反应,产生邻醌型结构。醌的形成过程伴随着芳香族结构的减少和共轭羰基的增加,且邻醌含量在光照初期即达到最大值,可推断辐照初期邻醌的快速形成是继有色但非醌类结构(富含共轭羰基)形成之后产生的[14-27]。对醌产物是在芳环1位发生侧链置换而产生[11],老化初期表面的迅速黄化现象就是由对醌的形成而引起的[8]。醌基团在光诱导黄变过程中形成,但其自身也具有光敏性,除了显示颜色,还可以催化其他光化学反应形成醌类或非醌类型的有色物质[28-29]。邻醌和对醌分别是红色和黄色物质,是木质素的主要发色结构。对醌结构除极少数缩合单元外,多数以单体形式溶出,而邻醌则以不溶出的形式保留在木质素大分子中,构成木质素颜色的首要来源[6]。木质素光化反应形成的醌型结构是导致木质素和木质材料变色的主要发色基团。
4.5.2水溶性小分子产物的形成 光降解材分解产物中除气体和水之外,主要是各种有机酸、香草醛、丁香醛及一些分子量较大的聚合物片段(聚合物片断,或醇、醛、酮、酸),这些分解物是可流失的[30]。光降解的主要产物有4-羰基- 3 甲氧基甲醛、3-二甲氧基苯甲醛、乙酰化愈疮木醇、松柏醛等酚类物质[9]。Koch等[31]对榉木(Fagussylvatioa)紫外光照射后表面层用甲醇-水进行加速萃取高效液相色谱测定,研究结果认为,儿茶酸和2,6-二甲基苯醌是导致变色的主要原因。
此外,木质素是由3种苯基丙烷单元组成的空间结构的混合物,不同结构单元对光的敏感性存在差异。Krishna等[32]在对针阔叶林老化速度的比较中发现,阔叶材的老化速度要比针叶材快,阔叶材中的紫丁香基丙烷结构对光的敏感性比愈疮木基丙烷弱。Colom等[33]研究认为,愈创木基核比紫丁香基对光降解更为敏感。
从分析技术和研究内容上看,20世纪70—80年代多采用化学分析光电子能谱(ESCA)、电子自旋共振(ESR)等技术侧重从自由基及单态氧的参与方面进行研究[6-8, 21],且采用木质素模型的研究较多。20世纪90年代以来,X射线光电子能谱(XPS)及红外光谱(FTIR)[23,34-35]分析技术被广为采用,主要从碳氧比、碳化学键链接及木质素官能团变化的角度进行分析[23,36]。2000年以来,色谱技术开始应用于降解产物的研究[31]。
5 结 语
迄今为止,木质素光老化的研究已取得一定的进展,尤其是在木质素模型的研究上,对老化机理已形成一些共识。但木质素模型与原本木质素的存在条件有一定的差距,基于原本木质素的结构和存在的复杂性,目前多采用间接手段进行研究。在分子和细胞水平上进行深入细致的研究及定量分析是今后研究的重点。
[1] 尹思慈.木材学[M].北京:中国林业出版社,1996.
[2] Williams R S. Handbook of Wood Chemistry and Wood Composites[M]. Madison: USDA, 2005.
[3] Kuo M L, Hu N. Ultrastructural changes of photodegradation of wood surfaces exposed to UV[J]. Holzforschung, 1991, 45(5): 347-353.
[4] Hon D N-S, Glasser W. On possible chromophoric structures in wood and pulp:a survey of the present state of knowledge[J]. Technol Eng,1979,12(2):159-179.
[5] Gratzl J S. Lichtinduzierte vergilbung von zellstoffen-ursachen und verhütung[J]. Papier, 1985, 39(10A): 14-23.
[6] Matsuura T, Yoshimura N, Nishinaga A, et al. Phtoinduced reactions-LVI:participation of singlet Oxygen in the Hydrogen abstraction from a phenol in the photosensutuzed oxygenation[J]. Tetrahedron, 1972, 28(19): 4933-4938.
[7] Brunow G, Sivonen M. The yellowing of lignin.Part II.The participation of Oxygen in the photodehydrogenation of lignin model compounds[J]. Paperija Puu, 1975, 57(4a): 215-220.
[8] Gellerstedt G G J, Pettersson E L. The reaction of lignin.Part 2.The oxidative degradation of aromatic rings[J]. Svensk Papperstidn, 1977, 80(1): 15-21.
[9] Fischer K B M, Koch H. Photo-induced yellowing of high yield pulps[J]. Holzforschung,1995,49(3):203-210.
[10] Kringstad K P, Lin S Y. Mechanism in the yellowing of high-yield pulps by light.Structure and reactivity of free radical intermidiates in the photodegradation of lignin[J]. Tappi, 1970, 53(12): 2296-2301.
[11] Paulsson M, Parkas J. Review light induced yellowing of lignocellulosic pulps-Mechanisms and preventive method[J]. BioResources, 2012, 7(4): 5995-6040.
[12] Vanucci C, Fornier D P, Bouas-Laurent H, et al. Photodegradation of lignin:a photophysical and photochemiscal study of a nonphenolic α-carbonyl β-O-4 lignin model dimer,3,4-dimethoxy-α-(2′-methoxy-phenoxy)acetophenone[J]. J Photochem Photobio A, 1988, 41(2): 251-265.
[13] Castellan A, Colombo N C. Photodegradation of lignin:a photochemical study of a phenolicα-carbonyl β-O-4 lignin model dimer 4-hydroxy-3-methoxy-α-(2′-methoxylphenoxy)-acetophenone[J]. Holzforschung, 1989, 43(3): 179-185.
[14] Argyropoulos D S, Sun Y. Photochemically induced solid-state degradation condensation and rearrangement reactions in lignin model compounds and milled wood lignin[J]. Photochemistry and Photobiology, 1996, 64(3): 510-517.
[15] Schmidt J A, Heitner C. Light-induced yellowing of mechanical and ultra-high yield pulps.Part 2.Radical-induced cleavage of etherified guaiacylglycerol-β-arylether groups is the main degradative pathway[J]. Journal of Wood Chemistry and Technology, 1993, 13(3): 309-325.
[16] Brunow G, Lundquist K. Functional Groups and Bonding Patterns in Lignin (Including the Lignin-Carbonhydrate Complexes)[M]. New York: CRC Press, 2010: 267-299.
[17] Francis R C,Omori S. Photostabilization of thermomechanical pulps by alkylation and borohydride reduction[J]. Tappi Journal, 1991, 74(12):127-133.
[18] Leary G J.The yellowing of wood by light:Part II[J].Tappi,1968,51(6):257-260.
[19] Leary G J.Photochemical production of quinoid structures in wood[J]. Nature,1968, 217(5129): 672-673.
[20] Lin Y,Kringstad K. Some reactions in the photoinduced discoloration of lignin[J]. Norsk Skogind, 1971, 25(9): 252-256.
[21] Hon D N-S, Chang S T. Surface degradation of wood by ultraviolet light[J]. Journal of Polymer Science: Polymer Chemistry Edition , 1984,22(9):2227-2241.
[22] Kamoun C, Merlin A, Deglise X, et al. Electron paramagnetic resonance spectroscopy study of photodegradation of lignins extracted and isolated from pinus radiate wood[J]. Annals of Forest Sci, 1999, 56(7): 563-578.
[23] Wang X Q, Ren H Q. Surface deterioration of moso bamboo (Phyllostachyspubescens) induced by exposure to artificial sunlight[J]. Journal of Wood Science,2009,55(1):47-52.
[24] Pandey K K. Study of the effect of photo-irradiation on the surface chemistry of wood[J]. Polymer Degradation and Stability, 2005, 90(1): 9-20.
[25] Mueller U, Steiner M. Colour stabilisation of wood composites using polyethylene glycol and melamine resin[J]. European Journal of Wood and Wood Products, 2010, 68(4): 435-443.
[26] Andrady A L, Hamid S H, Hu X, et al. Effects of increased solar ultraviolet radiation on materials[J]. Journal of Photochemistry and Photobiology B-Biology, 1998, 46(1/3): 96-103.
[27] Hirashima H, Sumimoto M. A basic chromophore and lecucochromophore in mechanical pulps:Possible repetition of photochemiscal reduction-oxidation-reduction[J]. Tappi Journal, 1994, 77(1): 146-154.
[28] Neumann M G, Machado A E. The role of Oxygen in the photodegradation of lignin in solution[J]. Journal of Photochemistry and Photobiology B-Biology, 1989, 3(4): 473-481.
[29] Lennholm H,Rosenqvist M, Ek M, et al. Photoyellowing of groundwood pulps[J]. Nordic Pulp & Paper Research Journal, 1994, 9(1): 10-15.

(责任编辑 曹 龙)
Research Progress on Lignin Photo Degradation Mechanism
YU Hai-xia1,2,FANG Chong-rong2,YU Wen-ji1
(1.Chinese Academy of Forestry, Beijing 100091, China;2.Zhejiang Provincial Key Laboratory of Biological and Chemical Utilization of Forest Resources, Zhejiang Forestry Product Testing Station, Hangzhou Zhejiang 310023, China)
The paper summarized current studies concerning phododegradation of lignin model and natural lignin. The results of lignin model studies showed that lignin photodegradation was a typical free radical reaction, and hydroxyl radical, carbonyl groups and phenacyl aryl ether cleavage were the main type of reaction. Moreover, phenoxy radical was very important intermediate product. Lignin photodegradation is an oxidation and degradation process, during which carbon′s oxidation state raised, conjugated carbonyl increased and non-conjugated carbonyl decreased, followed by high molecular lignin depolomerizing to some extent, α-quinone and β-quinone were main reason contribute to the discolor, there were soluble small molecular product such as benzoic acid and benzaldehyde. In the end, the paper pointed out the key problem of the current study and the development direction.
lignin;photo degradation;phenoxy radical;conjugated carbonyl;depolymerization
2014-06-30
国家自然科学基金项目(31470591)资助。
于文吉(1962—),男,博士,博士生导师,研究员。研究方向:竹、木基复合材研究。Email:yuwenji@caf.ac.cn。
10.11929/j.issn.2095-1914.2015.01.020
S718.42
A
2095-1914(2015)01-0104-07
第1作者:于海霞(1976—),女,博士生,高级工程师。研究方向:竹、木制品检测与科研。Email:ivyyhx@126.com。
