两个含2-(2-吡啶基)苯并咪唑的镍(Π)配合物的合成、晶体结构及表征
2015-03-20瞿志荣
范 艳,瞿志荣
(杭州师范大学有机硅化学及材料技术教育部重点实验室,浙江 杭州311121)
近年来,过渡金属配合物是配位化学研究的重要领域,也是无机化学研究的前沿领域之一[1-2].金属-有机配合物不仅有无机物的性能,又能表现出有机物的特性,因此,新型的配合物由于其潜在的功能在分子吸附、离子交换、荧光、导电性、磁性、生物医药、光学特性、气体储存和多相催化等方面的应用引起了人们广泛的关注[3-6].苯并咪唑配体以及它们的衍生物代表的杂环化合物是一类重要的有机金属配合物,在许多领域,如高性能复合材料、电子化学品、金属防腐、感光材料、生物、医药、催化呈现独特的性能,并具有广泛的应用前景[7-8].选择合适的配体以及金属离子有助于构筑新型的多功能配位化合物,2-(2-吡啶基)苯并咪唑含3个N 原子,具有多个配位点,可以通过氢键、π…π堆积及C—H…π等非共价作用力自组装成多种具有单核或双核的新颖多功能配合物.
本文用氯化镍、2-(2-吡啶基)苯并咪唑通过自然挥发法合成了配合物[Ni(PBIm)2Cl2H2O]·(C2H5OH)(H2O)1;用氯化镍,2-(2-吡啶基)苯并咪唑,邻苯二甲酸通过水热法合成了[Ni(PBIm)Cl2(CH3CH2OH)]22.X 射线单晶衍射结果表明:配合物1属于三斜晶系,Pī空间群,是以镍原子为中心构筑的六配位的新型配合物;配合物2属于单斜晶系,P21/c空间群,是以镍原子为中心的通过氯桥键自组装成的双核新型配合物.并对其荧光及热稳定性进行了表征,配合物1与配合物2相比较,后者的热稳定性高且荧光强度大.
1 实验部分
1.1 试剂和仪器
实验中所用试剂均为市售分析纯,没有进一步提纯.2-(2-吡啶基)苯并咪唑参照文献[9]合成.荧光发射光谱采用的是Hitachi公司的F-2500荧光光谱仪,热重分析使用的是NETZSCH 公司的TG209C热重分析仪,氮气氛围,氮气流量20 m L/min,升温速率10 ℃/min,温度从室温升至800 ℃.
1.2 配合物的合成
1.2.1 配合物[Ni(PBIm)2Cl2H2O]·(C2H5OH)(H2O)1的合成
称取0.0475 g的NiCl2·6H2O(0.2 mmol),0.039 g的2-(2′-吡啶基)苯并咪唑(PBIm)(0.2 mmol)溶于10 m L 95%的乙醇,滴加两滴5×10-5mol/L的盐酸溶液.混合物在回流条件下搅拌12 h,溶液变浑浊,过滤,滤液静置于室温条件下缓慢挥发析出深绿色晶体,收集到0.06 g的晶体(产率为69.4%).在显微镜下挑选出合适的晶体进行X-Ray晶体结构的测定.
1.2.2 配合物[Ni(PBIm)Cl2(CH3CH2OH)]22的合成
称取0.0475 g的NiCl2·6H2O(0.2 mmol),0.039 g的2-(2-吡啶基)苯并咪唑(PBIm)(0.2 mmol)0.030 g的邻苯二甲酸(0.2 mmol)溶于10 m L 95%的乙醇.然后将此混合物转入25 m L具有聚四氟乙烯内衬的不锈钢反应釜中,密封,恒温130 ℃,反应3 d后停止加热,待反应釜在烘箱中自然冷却到室温后取出,在反应釜底部得到绿色块状晶体.
1.3 晶体结构的测定
晶体结构的测定使用Bruker Smart ApexΠDUO X 射线单晶衍射仪.在296 K 条件下挑选合适尺寸的晶体收集衍射数据,用辐射MoKα射线(λ=0.071073 nm),在设定的2θ范围内收集衍射数据,全部数据通过SADABS[10]程序进行经验吸收校正.晶体结构用SHELXS-97 软件由直接法解出,精修采用SHELXL-97.所有非氢原子的坐标及各向异性温度因子用全矩阵最小二乘法进行修正.除水上的氢原子外,其余氢原子均为理论加氢,通过差值Fourier合成得到.主要的晶体数据列于表1.主要的键长和键角列于表2—表4.

表1 配合物1和2的主要晶体学参数Tab.1 Crystallographic data and refinement parameters for complexes 1 and 2

续表
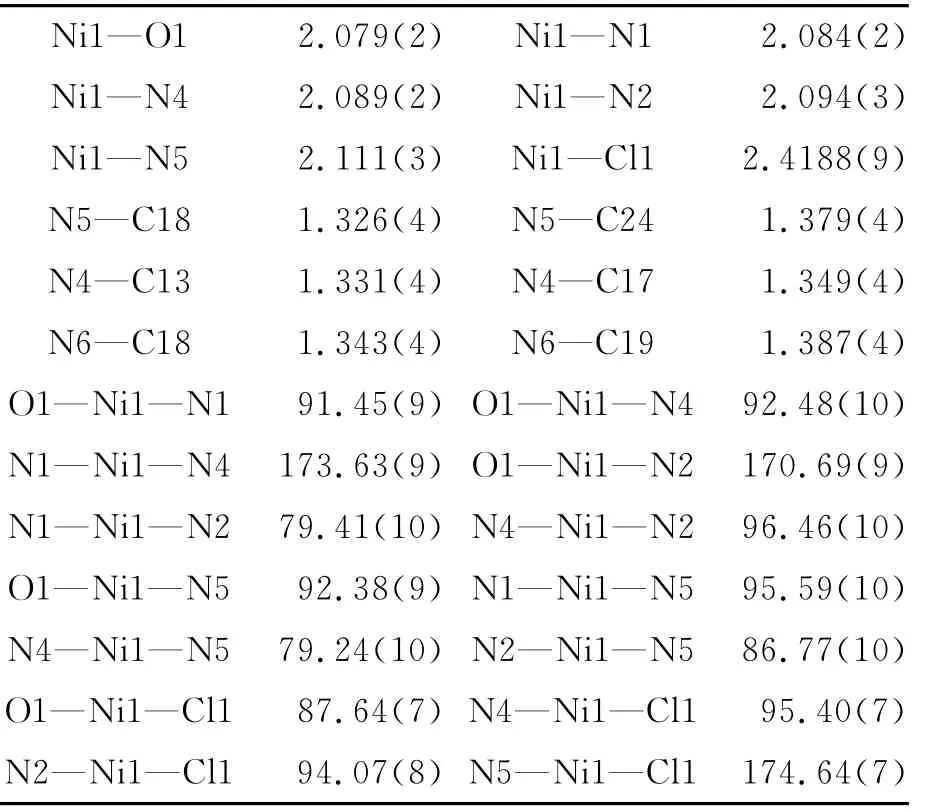
表2 配合物1的主要键长和键角数据Tab.2 Selected bond lengths(Å)and angles(°)for the complex 1
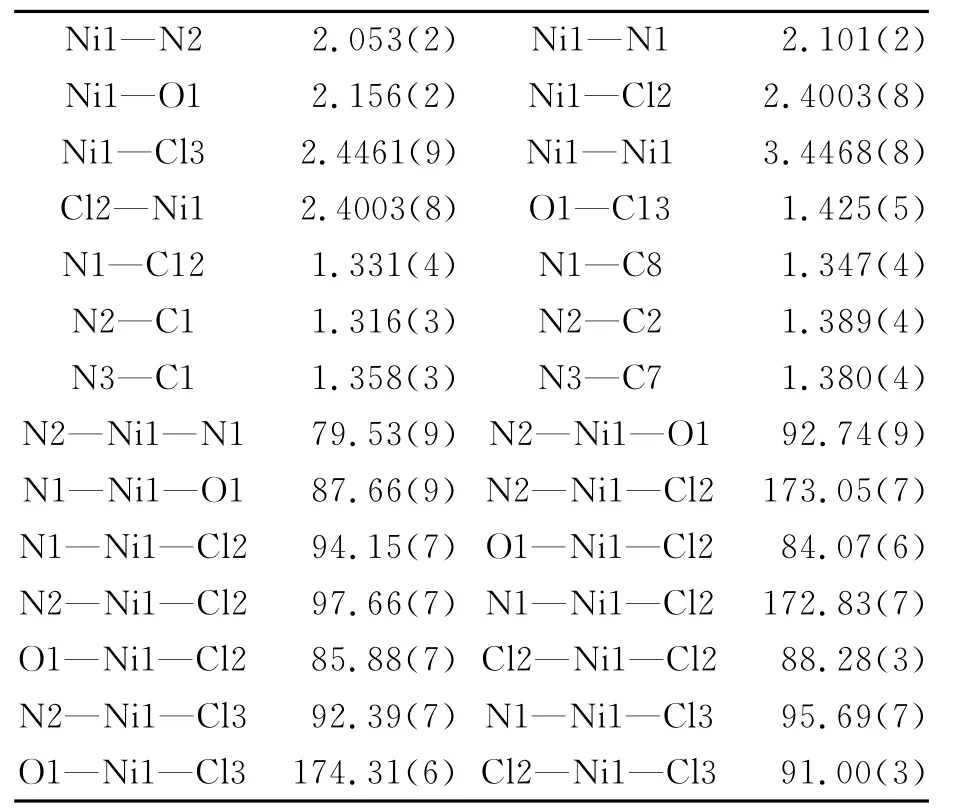
表3 配合物2的主要键长和键角数据Tab.3 Selected bond lengths(Å)and angles(°)for the complex 2
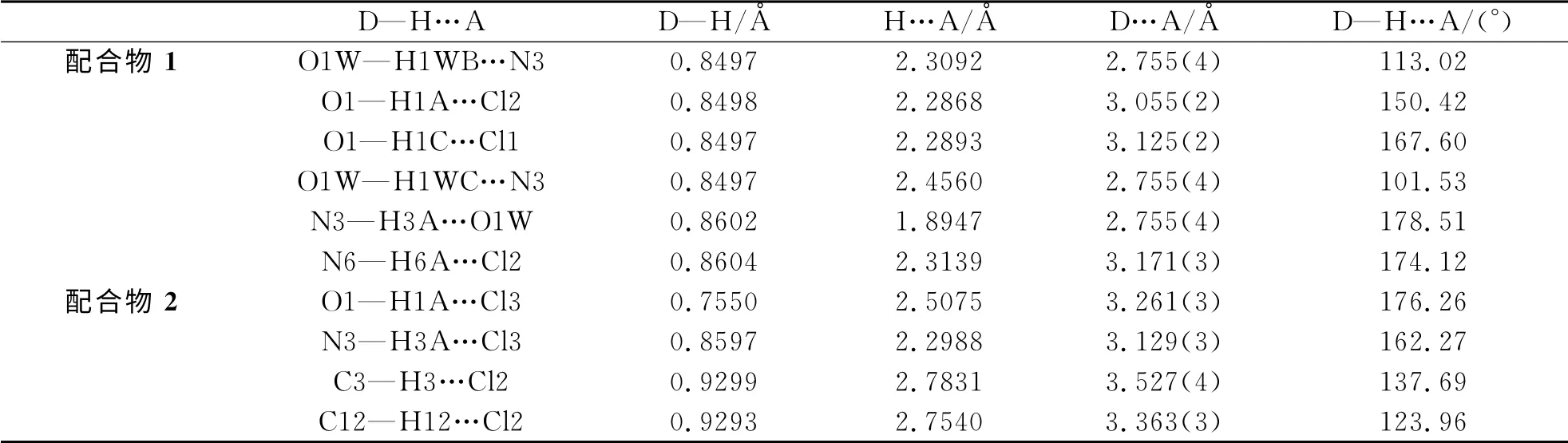
表4 配合物1和2的主要的氢键键长和键角Tab.4 Hydrogen bond lengths(Å)and angles(°)for the complexes 1 and 2
2 结果与讨论
2.1 晶体结构
2.1.1 配合物1的晶体结构

图1 配合物1的晶体结构图Fig.1 Molecular structure of complex 1
配合物1是由六配位的中心原子Ni和分别来自2个苯并咪唑环和吡啶环的4个N 原子、一个来自水分子的氧原子、一个来自氯化镍本身的氯原子配位,构成以Ni原子为中心的稍微扭曲的八面体结构.其晶体结构见图1.其中N4、N5、N1和Cl1形成以镍原子为中心的八面体底面,O1和N2位于该底面的上下两侧,O1—Ni1—N2的键角为170.69(9)°,其主要的键长键角见表2.配体PBIm 在没受到配位金属离子干扰时,单个配体中吡啶环与苯并咪唑环形成的二面角为13.7°,而在配合物[Ni(PBIm)2](Cl)2(H2O)2(Et OH)中,因配位效应的影响它们之间的二面角为3.9°,几乎在同一个平面上,而两配体之间的二面角为68.6°,由以上因素可以看出配合物1构成扭曲八面体结构.
配合物1中存在4种典型的分子间氢键,配位水中的氧原子与2个氯原子结合形成的氢键,键长O1—H1A…Cl2:2.2868Å,O1—H1C…Cl1:2.2893Å,键角分别为150.42°和167.60°(对称操作码:1.1-x,1-y,1-z;2.1-x,2-y,1-z);配位水中的氧原子跟配体中的氮原子之间,键长O1W—H1WB…N3:2.3092Å,O1W—H1WC…N3:2.4560Å,键角分别为113.02°和101.53°(对称操作码:x,y,1+z);配体中的N 原子与游离的氯离子之间,键长N6—H6A…Cl2:2.3139Å,键角为174.12°;配体中的氮原子与游离的水中的氧原子之间,键长N3—H3A…O1W:1.8947Å,键角几乎接近180°(对称操作码:x,y,-1+z).这几种氢键的作用存在使得分子之间形成一维的链状结构(图2).

图2 配合物1的一维链状结构Fig.2 1D chain structure of complex 1
2.1.2 配合物2的晶体结构

图3 配合物2的晶体结构图Fig.3 Molecular structure of complex 2
配合物2是由NiCl2·6 H2O 和配体在酸性条件下水热法得到的.它是由五配位的中心镍原子,来自配体中的2个氮原子,NiCl2·6 H2O 中的2个氯原子,和1个配位乙醇中的氧原子构成的一个多面体结构(图3).配合物2是由2个氯原子形成的氯桥键连接成的双核结构,结构中存在两种氢键:一种是配位乙醇中的氧原子与氯原子之间形成的分子内氢键,键长O1—H1A…Cl3:2.5075Å,键角为176.26°(对称操作码:-x,1-y,1-z);另一种是配体中的氮原子与氯原子之间形成的分子间的氢键,键长N3—H3A…Cl3:2.2988Å,键角为162.27°(对称操作码:1-x,1-y,1-z).通过这些氢键的作用,分子之间构成了一维的链状结构(图4).另外,分子间还存在一种弱的非典型氢键C—H…Cl,这种氢键的存在加固了配合物的稳定性.

图4 配合物2的一维链状结构Fig.4 1D chain structure of complex 2
2.2 配合物的热稳定性研究
配合物1和2在室温到800℃温度范围内的热重曲线如图5所示.配合物1在82.5~102℃,质量损失约11.06%,与失去一个水分子和一个乙醇分子相应的理论失重值10.29%相吻合.随着温度的升高,在300~550℃,配合物发生剧烈分解,失重约40.23%.配合物2在220℃以下几乎没有分解,当温度升高到251 ℃时,质量损失约11.95%,与失去一个乙醇分子相应的理论失重值11.86%相吻合.当温度升高到373.2 ℃时,配体开始发生分解.
由热重分析图可以看出,配合物2比配合物1的热稳定性强,配合物2在220 ℃以下几乎不发生分解.导致这种差异的原因主要是配合物1是溶液法合成的,配合物2是水热法合成的,一般溶液法得到动力学稳定的产物,而水热合成得到热力学稳定的产物,因此配合物2比配合物1稳定(因为它们具有结构多样性、组分类似),二者合成时都是酸性环境.
2.3 配合物的荧光光谱
配合物1、2和配体在DMSO 溶液中的荧光光谱如图6所示,分别在最大激发波长下λ=323 nm,λ=322 nm 和λ=312 nm,可能是由于配体分子的π-π*跃迁导致的,配合物1的发射峰位于364 nm,配合物2的发射峰位于378 nm,与配体的发射峰λ=369 nm 相比较,配合物2发生红移现象,且荧光明显增强,由于金属离子的配位,使得配合物的刚性增加,荧光发光性能也就越好[11].而配合物1则是荧光淬灭.导致这种差异现象的原因主要应该是配合物1中有配位与结晶水,结晶水有不同作用,在有些化合物中能增强荧光,但大部分情况下是减弱荧光:也可能是由于金属离子不同的配位方式以及配合物中不同强度的氢键作用[12]产生的.

图5 配合物1和2的热重图Fig.5 Thermogravimetric analysis diagram of complexes 1 and 2

图6 配合物1,2和配体在DMSO 溶液中的荧光光谱Fig.6 Flourescence of complexes 1,2 and the ligand in DMSO solution
3 结论
本文用相同的原料氯化镍与2-(2-吡啶基)苯并咪唑在不同的酸性条件下分别通过自然挥发法和水热法合成了两种配合物,通过分子间氢键自组装成了两种新颖的一维链状的金属配合物.并用单晶衍射确定了结构,同时我们还对其热稳定性及荧光性质进行表征,结果表明配合物2的热稳定性高且荧光强度相对较大.所以配合物2可以作很好的潜在的荧光材料应用于光电材料领域.
[1]李海鹏,朱有兰.配位化学的地位和发展趋势[J].广东工业大学学报,1996,13(2):52-62.
[2]项斯芬,姚光庆.中级无机化学[M].北京:北京大学出版社,2003.
[3]朱莉,于贤勇,龙云飞,等.2-苯并咪唑吡啶镍配合物的合成﹑晶体结构及与DNA 相互作用的共振散射光谱研究[J].无机化学学报,2009,67(2):139-144.
[4]Jesse L C,Omar M.Strategies for hydrogen storage in metal-organic frameworks[J].Angew Chem Int Ed,2005,44(30):4670-4679.
[5]Janiak C.Clathrates and coordination polymers:new dimensions in poly(azolyl)borate chemistry with poly-(triazolyl)-and-(tetrazolyl)-borate ligands[J].J Chem Soc Chem Commun,1994,4(79):545-547.
[6]Singh H,Chawla A S,Kapoor V K,etal.Medicinal chemistry of tetrazoles[J].Prog Med Chem,1980,17(4):151-183.
[7]Jiang H,Liu H Y,Ma J F,etal.Infinite chains constructed from flexible bis(benzimidazole)-based ligands[J].Polyhedron,2008,27(12):2595-1550.
[8]Liu H Y,Wu H,Ma J F,etal.Syntheses,structures,and photoluminescence of Zinc(II)coordination polymers based on carboxylates and flexible Bis-[(pyridyl)-benzimidazole]ligands[J].Crystal Growth Design,2010,10(11):4795-4805.
[9]Lu J,Ge H G,Bai Y J.Solvent-free synthesis of 2-substituted benzimidazoles under microwave-irradiation using PPA as a catalyst[J].Chin J Org Chem,2002,22(10):782-784.
[10]Scheldrick G M.SADABS[M].Göttingen:University of Göttingen,1996.
[11]Thompson L,Legendziewicz J,Cybinska J,etal.Structure,photophysics and magnetism of a europium mixed complex,Eu(HFAA)bipy·H2O,in the solid state and solution[J].J Alloys and Compounds,2002,341(1/2):312-322.
[12]Muthu S,Ni Z,Vittal J J.Photoluminescent coordination polymers of d10metals with 4-4’-dipyridylsulfide(dps)[J].Inorganica Chimica Acta,2005,358(3):596-605.
