纳米氧化亚铜薄膜的制备及光电性能研究
2015-03-15胥桂萍
胥桂萍,邱 黎
(江汉大学 光电化学材料与器件教育部重点实验室,化学与环境工程学院,湖北 武汉 430056)
纳米氧化亚铜薄膜的制备及光电性能研究
胥桂萍,邱 黎
(江汉大学 光电化学材料与器件教育部重点实验室,化学与环境工程学院,湖北 武汉 430056)
采用水热法制备n型和p型Cu2O薄膜,并采用电化学法制备p型Cu2O薄膜。通过X-射线衍射(XRD)、扫描电子显微镜(SEM)等方法对Cu2O薄膜进行表征,研究了p型Cu2O薄膜的光电性能。实验结果表明:在弱酸性溶液中,用水热法制备的Cu2O薄膜导电类型为n型;在碱性溶液中,Cu2O薄膜导电类型为p型;电化学法制备的p型Cu2O为立方型晶体。
纳米氧化亚铜薄膜;水热法;电化学法;光电性能
0 引言
纳米氧化亚铜(Cu2O)是新型的可被可见光激发的p型半导体材料,Cu2O薄膜比Cu2O粉体在电学和光学属性方面表现更好,然而到目前为止,人们对粉末状Cu2O的研究却比薄膜Cu2O的研究多得多。
笔者对Cu2O的研究主要集中在光电应用方面,Cu2O材料的形貌和晶体结构对其光电性质影响很大,因此制备各种形貌的Cu2O材料具有重要的意义。已报道的制备方法有化学沉积法[1]、溶胶凝胶法[2]、水热法[3]、反应溅射法[4]、多元醇法[5]、微乳法[6]、电化学法[7-8]等,其中电化学法对纳米Cu2O晶型有较强选择性,可通过电流、电压等条件控制其形态、尺寸。
本研究采用水热法以乙酸铜为原料,在不同pH值下制备Cu2O薄膜。采用电化学法以硫酸铜和乳酸的混合液为电解液在碱性条件下制备Cu2O薄膜。通过扫描电子显微镜(SEM),X-射线衍射(XRD)等方法对所制备样品结构和形貌进行分析;通过开路电压测试方法对样品的光电性能进行表征。
1 实验
1.1 实验药品及仪器
主要试剂有:乙酸铜,乳酸,氢氧化钠,氯化钾,碳酸氢钾,硫酸钠,盐酸,氨水,醋酸,苯并三唑,无水乙醇,丙酮,铜片(纯度99.98%)。
主要仪器有:85-1恒温磁力搅拌器,常州国华电器有限公司;BS200S-WEI型电子分析天平,北京赛多利斯天平有限公司;XQ350W氙灯,上海蓝晟电子有限公司;RAR2273电化学工作站,美国普林斯顿公司;SB-5200D超声波清洗器,宁波新芝生物科技股份有限公司;DZF-1型(6050B)真空干燥箱,上海福玛实验设备有限公司;GC-2014气相色谱仪,日本岛津;Y-2000型X-射线衍射仪(XRD);JOEL-6700F型扫描电子显微镜(SEM)。
1.2 水热法制备n型和p型纳米Cu2O薄膜
1.2.1 铜片基底的清洗 将铜片修剪成2 cm×6 cm大小,先用浓盐酸浸泡30 min,取出并用大量清水冲洗,再用二次去离子水冲洗。依次浸泡在蒸馏水、丙酮、无水乙醇中各以超声波清洗10 min。取出后用电吹风吹干备用。
1.2.2 制备 将处理后的铜片分别浸没到盛有60 mL的10-3M醋酸铜水溶液的高压釜中,用醋酸和氨水调节pH值,使得pH值依次为4、5、9、10、11,高压釜的反应温度为160℃,反应时间为8 h。
1.3 电化学法制备纳米Cu2O薄膜
1.3.1 铜片基底的清洗 清洗方法同1.2.1。
1.3.2 制备 取0.4 M CuSO4+3 M乳酸60 mL于100 mL烧杯,用4 M NaOH调节pH值,使得pH值依次为9、10、12,配得电解液。在烧杯上盖一个硬纸片,分别将处理好的铜片、铂电极、Ag/AgCl饱和KCl电极固定在纸片上。将三电极连接RAR2273电化学工作站,加热电解液使温度升至60℃开始电解,反应时间为1 h,控制电压为-0.1 V。待反应完毕后,取出铜片,用蒸馏水洗涤。干燥后放入质量分数为1‰的乙醇苯丙三唑(BTA)中浸泡2 h,取出后干燥待用。
1.4 样品的表征
用Y-2000型X-射线衍射仪(XRD)对样品进行成分分析;用JOEL-6700F型扫描电子显微镜(SEM)观测所制样品的整体形貌;用电化学工作站RAR 2273对样品的电化学性能进行测试,测试过程中采用三电极工作体系:以制备的Cu/Cu2O薄膜样品作为工作电极,以Pt为对电极,以参比电极为Ag/AgCl饱和KCl电极,以0.1 M的Na2SO4溶液作为电解液。
2 结果与讨论
2.1 XRD分析
图1~图4是以水热法和电化学法在不同pH值时制备Cu2O薄膜的XRD图谱。由于制备Cu2O薄膜时以铜片为基底,在其表面只附着很薄的一层Cu2O薄膜,因此XRD图谱中金属铜的峰很强,Cu2O的峰基本上被掩盖,分析图1到图3中2θ值为43.05°、50.45°和73.46°处的衍射峰分别对应于金属铜的(220)、(200)和(311)晶面,而在29.78°、36.56°、42.39°和62.51°处的微弱衍射峰则对应于立方晶型Cu2O的(110)、(111)、(200)和(220)晶面。对于水热法的XRD图,图2中Cu2O在(110)和(200)晶面衍射峰消失,说明溶液的酸碱性可以影响Cu2O的取向度。可以判断,采用水热法确实在Cu基底表面得到了一层Cu2O薄膜。在酸性条件下Cu2O薄膜生长情况较好,在强碱性条件下较难生成Cu2O薄膜。比较图2和图3可知,用电化学法制备的Cu2O薄膜在立方晶型Cu2O的(110)、(111)和(220)晶面生长情况较好。
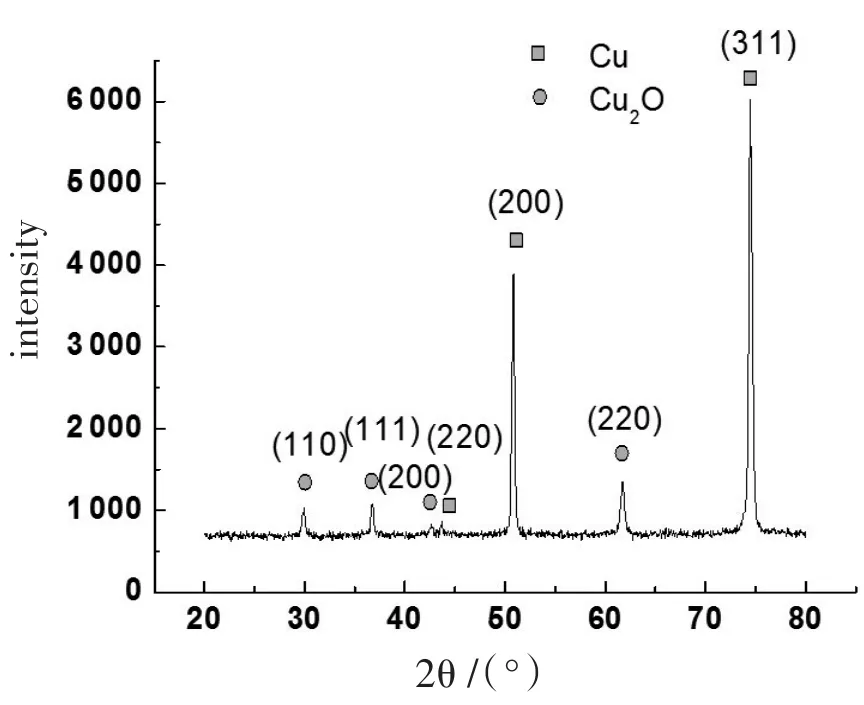
图1 水热法制备Cu2O薄膜的XDR图谱(pH=5)Fig.1 XRD pattern of Cu2O film prepared with hydrothermal method with pH=5
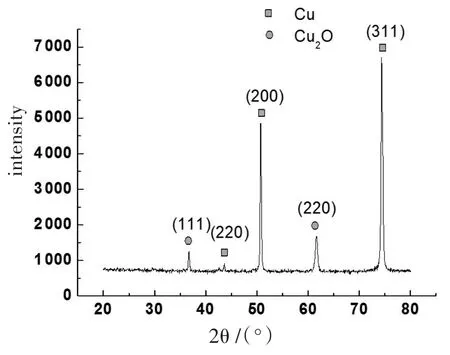
图2 水热法制备Cu2O薄膜的XRD图谱(pH=10)Fig.2 XRD pattern of Cu2O film prepared with hydrothermal method with pH=10
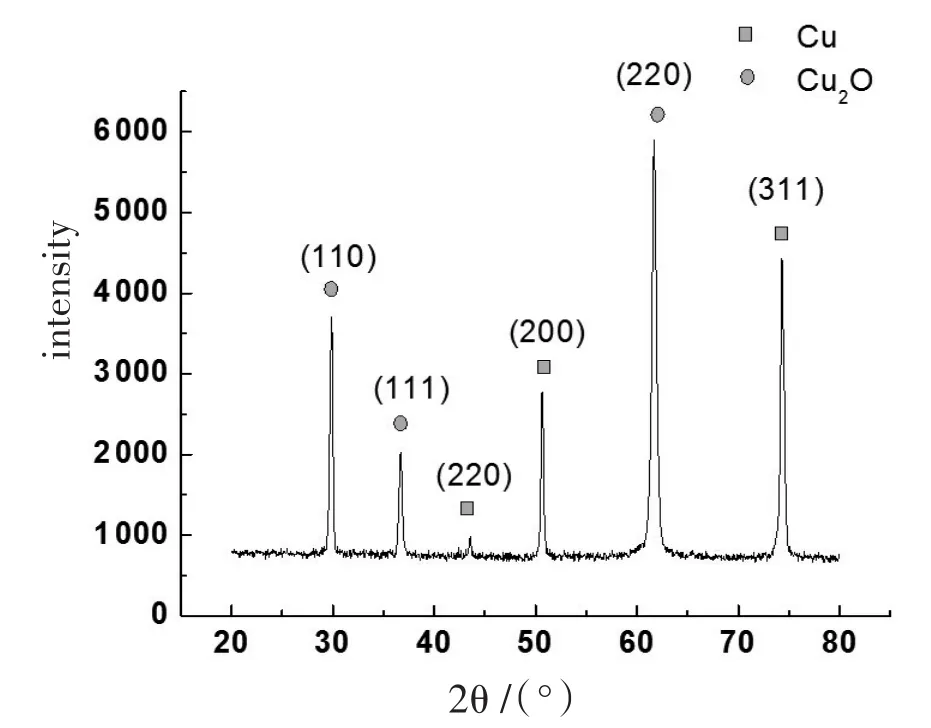
图3 电化学法制备Cu2O薄膜的XDR图谱(pH=10)Fig.3 XRD pattern of Cu2O film prepared with electrochemical method with pH=10

图4 电化学法制备Cu2O薄膜的XDR图谱(pH=12)Fig.4 XRD pattern of Cu2O film prepared with electrochemical method with pH=12
图5和图6是以水热法在不同pH值时制备Cu2O薄膜的SEM图谱。从图5和图6可看出,在酸性条件下制备的Cu2O薄膜由不规则粒状结构组成,粒子表面粗糙;在碱性条件下制备的Cu2O薄膜由立方体结构组成,粒子表面光滑平整。
图7和图8是以电化学法在不同pH值时制备Cu2O薄膜的SEM图谱。从图7和图8可看出,电化学法制备的Cu2O薄膜是立方体结构,且pH值越大得到的Cu2O薄膜表面纳米结构越精细,棱面越完整,其尺寸更加细小。
2.2 两种Cu2O薄膜的p型和n型特性表征
由于Cu2O是一种非理想配比的具有内部缺陷的半导体氧化物,通常是通过脉冲光开启瞬间电极电势突变的方向来判断半导体的类型。在酸性环境下,溶液中Cu+浓度较高而OH-的浓度很低,可能生成铜和氧的原子配比大于2(理想配比为2∶1)的具有氧缺陷的n型半导体Cu2O。在碱性环境下,溶液中的OH-浓度相对较大,可能生成铜和氧的原子配比小于2的具有铜缺陷的p型半导体Cu2O。
图9和图10是n型和p型Cu2O薄膜在脉冲可见光照射下的开路光电压曲线图。由图9可知,在脉冲光开启的瞬间,酸性环境下制得的Cu2O薄膜的电势向较低电位方向突变,产生一个负偏压,呈现了n型半导体的特性。由图10可知,在脉冲光开启的瞬间,碱性环境下制备的Cu2O薄膜的电势向较高电位方向突变,产生一个正偏压,体现了p型半导体的特性。由此可见,采用水热法制备Cu2O薄膜在酸性条件下生成了n型半导体Cu2O,在碱性条件下生成了p型半导体Cu2O。

图5 水热法制备Cu2O薄膜的SEM图谱(pH=5)Fig.5 SEM image of Cu2O film prepared with hydrothermal method with pH=5

图6 水热法制备Cu2O薄膜的SEM图谱(pH=10)Fig.6 SEM image of Cu2O film prepared with hydrothermal method with pH=10

图7 电化学法制备Cu2O薄膜的SEM图谱(pH=10)Fig.7 SEM image of Cu2O film prepared with electrochemical method with pH=10

图8 电化学法制备Cu2O薄膜的SEM图谱(pH=12)Fig.8 SEM image of Cu2O film prepared with electrochemical method with pH=12

图9 水热法制备Cu2O薄膜的开路光电压曲线图(pH=4)Fig.9 Curve of open circuit photovoltage of Cu2O film prepared with hydrothermal method pH=4
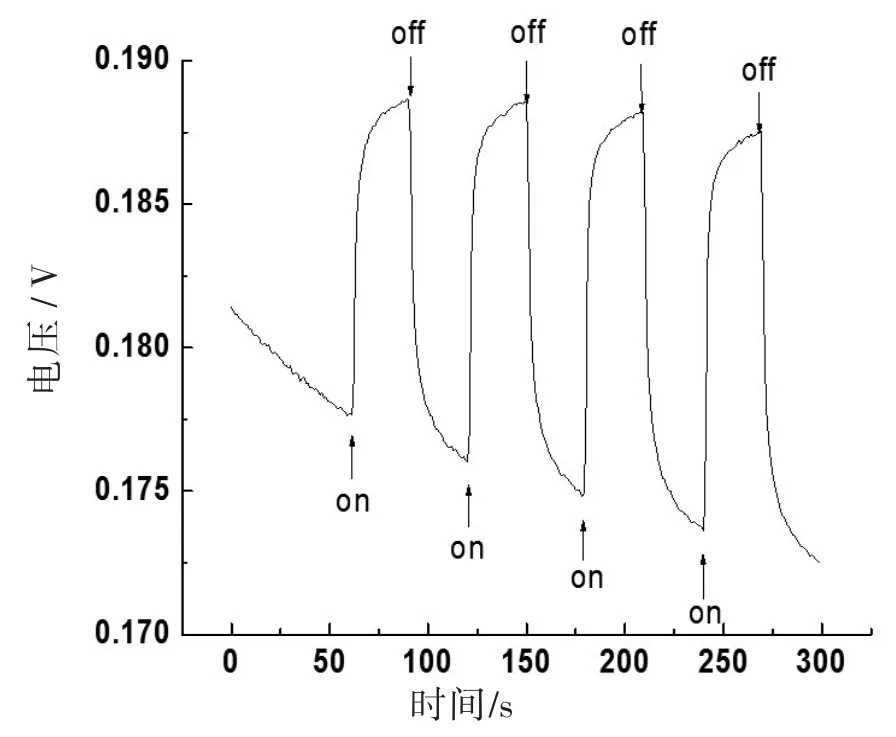
图10 水热法制备Cu2O薄膜的开路光电压曲线图(pH=9)Fig.10 Curve of open circuit photovoltage of Cu2O film prepared with hydrothermal method pH=9
3 结语
采用水热法在不同pH环境下制备Cu2O薄膜,并对其进行XRD和SEM分析及开路电路测试光电压。酸性条件下生成的Cu2O为n型,碱性条件下生成的为p型半导体。采用电化学法在碱性条件下分别控制电流和电压制备Cu2O薄膜,电化学法制备的Cu2O薄膜是立方体结构,且pH值越大得到的Cu2O薄膜表面纳米结构更加精细,棱面更加完整,尺寸更加细小。
(References)
[1]刘明辉,张丽莎,贾志勇,等.化学沉淀法制备氧化亚铜薄膜[J].华中师范大学学报:自然科学版,2006,40(1):75-78.
[2]乔振亮,马铁成.溶胶-凝胶法制备氧化亚铜薄膜及其工艺条件[J].大连轻工业学院学报,2004,23(1):4-9.
[3]刘晓璐,安太成,陈江耀,等.不同水热温度下Cu2O的制备及其可见光催化活性研究[J].功能材料,2009,40(增刊):595-597.
[4]AKIMOTO K,ISHIZUKA S,YANAGITA M,et al.Thin film deposition of Cu2O and application for solar cells[J].Solar Energy,2006,80(6):715-722.
[5]马丽丽,余颖,黄文娅,等.多元醇法制备Cu2O/CNTs复合材料的研究[J].化学学报,2005,63(18):1641-1645.
[6]秦明娜,葛忠学,郑晓东.微乳法制备纳米材料的研究进展[J].化工时代,2008,22(7):50-53.
[7]汪志勇,曾庆学,崔舜,等.电化学法制备氧化亚铜的研究[J].化学研究,2001,12(1):29-32.
[8]胡飞,江毅,梁建.p型Cu2O半导体薄膜的电化学沉积研究[J].人工晶体学报,2009,38(4):952-956.
(责任编辑:叶 冰)
Preparation of Nano-Cuprous Oxide Film and Its Photoelectric Properties
XU Guiping,QIU Li
(Key Laboratory of Optoelectronic Chemical Materials and Devices,Ministry of Education,School of Chemistry and Environmental Engineering,Jianghan University,Wuhan 430056,Hubei,China)
The n-type and p-type Cu2O films were prepared with hydrothermal method and p-type Cu2O films were prepared with electrochemical method.With X-ray diffraction(XRD),scanning electron microscopy(SEM)and other tests,these p-type Cu2O thin films were characterized and studied in photoelectric properties.The experimental results showed that:in weak acid solution,the conductivitive Cu2O films prepared by hydrothermal were n-type,in alkaline solution,the films were p-type;while the conductivitive Cu2O films prepared by electrochemical method were p-type which were cubic crystal.
nano-cuprous oxide film;hydrothermal method;electrochemical method;photoelectric properties
O484
:A
:1673-0143(2015)06-0485-05
10.16389/j.cnki.cn42-1737/n.2015.06.001
2015-09-17
湖北省教育厅科学技术研究计划指导性项目(B20123407)
胥桂萍(1968—),女,副教授,硕士,研究方向:化工及环保领域基础与应用。
