纳米氧化亚铜的溶剂热合成和对亚甲基蓝的催化降解
2014-08-06谢光勇刘公毅张爱清
谢光勇,李 龙,刘公毅,张爱清
(中南民族大学 催化材料科学国家民委-教育部共建暨湖北省重点实验室,武汉 430074)
随着水环境污染问题的日益严重,传统的污水处理方法耗资大、处理速度慢、净化不彻底、有再次污染等,急需寻求更经济有效的消除环境污染的新技术方法.光催化降解有机污染物是一种节能环保的污染治理手段[1],开发新型高效、可见光利用效率高的纳米半导体光催化剂,成为半导体光催化氧化法治理环境污染问题的关键技术.纳米氧化亚铜是一种新型的半导体光催化剂[2,3],除大量应用于石油化工催化和船舶防污涂料外,还具有许多新性能,如在甲醇燃料电池中体现的阳极催化、太阳能电池中的可见光催化、可见光下分解水产氢和降解有机废水的光催化等.制备氧化亚铜方法常用化学沉积法[4]、电化学法[5]、辐照法[6,7]等,本文以五水硝酸铜为原料,乙醇水溶液为溶剂和还原剂,溶剂热法[8]合成了纳米铜和氧化亚铜,水的加入可有效控制纳米铜和氧化亚铜的合成,制备方法简便、高效、环保和可控,所制备的纳米氧化亚铜具有光催化降解亚甲基蓝的性能.
1 实验部分
1.1 试剂和仪器
硝酸铜[Cu(NO3)2·5H2O]、无水乙醇、亚甲基蓝、双氧水(分析纯, 国药集团化学试剂有限公司). X射线衍射仪(Bruker Advanced D8,德国),透射电子显微镜(FEI Tecnai G20,美国),紫外可见光分光光度计(TU-1901型,北京普析通用仪器有限责任公司).
1.2 纳米铜和氧化亚铜的制备
称取五水硝酸铜1.0 g置于烧杯中,加入4.0 mL 蒸馏水,搅拌至完全溶解,倒入25.0 mL 的反应釜中,再加入14.0 mL 无水乙醇,混合均匀,密封反应釜并置于马弗炉中恒温48 h,冷却至室温后,取出减压抽滤,于真空干燥箱内60 ℃下干燥10 h,不同的水热反应温度可分别得到纳米铜和氧化亚铜颗粒.
1.3 催化降解亚甲基蓝
配制一定浓度的亚甲基蓝溶液200 mL,加入一定量的氧化亚铜,搅拌后离心,取上层清液于660 nm波长处测零时刻吸光度(记为A0). 滴加一定量的H2O2后在太阳光照下反应并计时,每隔一定时间取样,测t时刻的吸光度(记为At),计算亚甲基蓝在光催化反应中的降解率,降解率(%)=(A0-At)/ A0×100%. 其中A0、At分别为亚甲基蓝降解前、后在其最大吸收波长处的吸光度值.由于亚甲基蓝溶液浓度与其吸光度呈线性关系,故考察其降解率, 可体现其降解效果,衡量光催化反应的能力.
2 结果与讨论
2.1 反应条件对溶剂热反应产物的影响
2.1.1 反应温度的影响
溶剂热反应温度对产物的影响较大,通过不同的溶剂热反应温度可控合成不同的产物.以Cu(NO3)2为原料,乙醇为溶剂和还原剂,加入少量水,改变反应温度,进行溶剂热反应48 h,所得产物XRD图如图1所示.
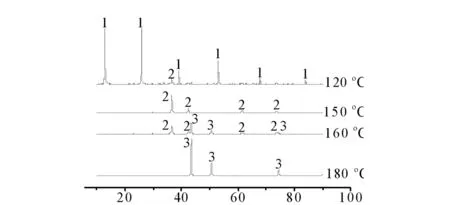
2θ/(°)1) Cu2(NO3)2(OH)2 ; 2) Cu2O; 3) Cu图1 不同温度下产物的XRD 图Fig.1 XRD patterns of products at different temperatures
由图1可见, 120℃ 时产物主要为碱式硝酸铜, 150℃ 时,产物为纯的氧化亚铜,升温至160℃ 时,部分氧化亚铜被还原成铜,产物为铜和氧化亚铜的混合物,到180℃ 时产物彻底还原成铜.故通过溶剂热反应,以乙醇为溶剂和还原剂,加入少量的蒸馏水,控制反应温度,即可使硝酸铜可控还原为铜和氧化亚铜.
反应温度为150℃和180℃下产物形貌的TEM表征结果见图2.由图2可见, 150℃时,产物纯的Cu2O是5~6nm左右的球形颗粒,分布较均匀. 180℃时,原料彻底还原为铜,约为50nm的球形颗粒. 故该方法提供了一种简便、高效、环保和可控地制备小尺寸的纳米级的Cu2O的方法.
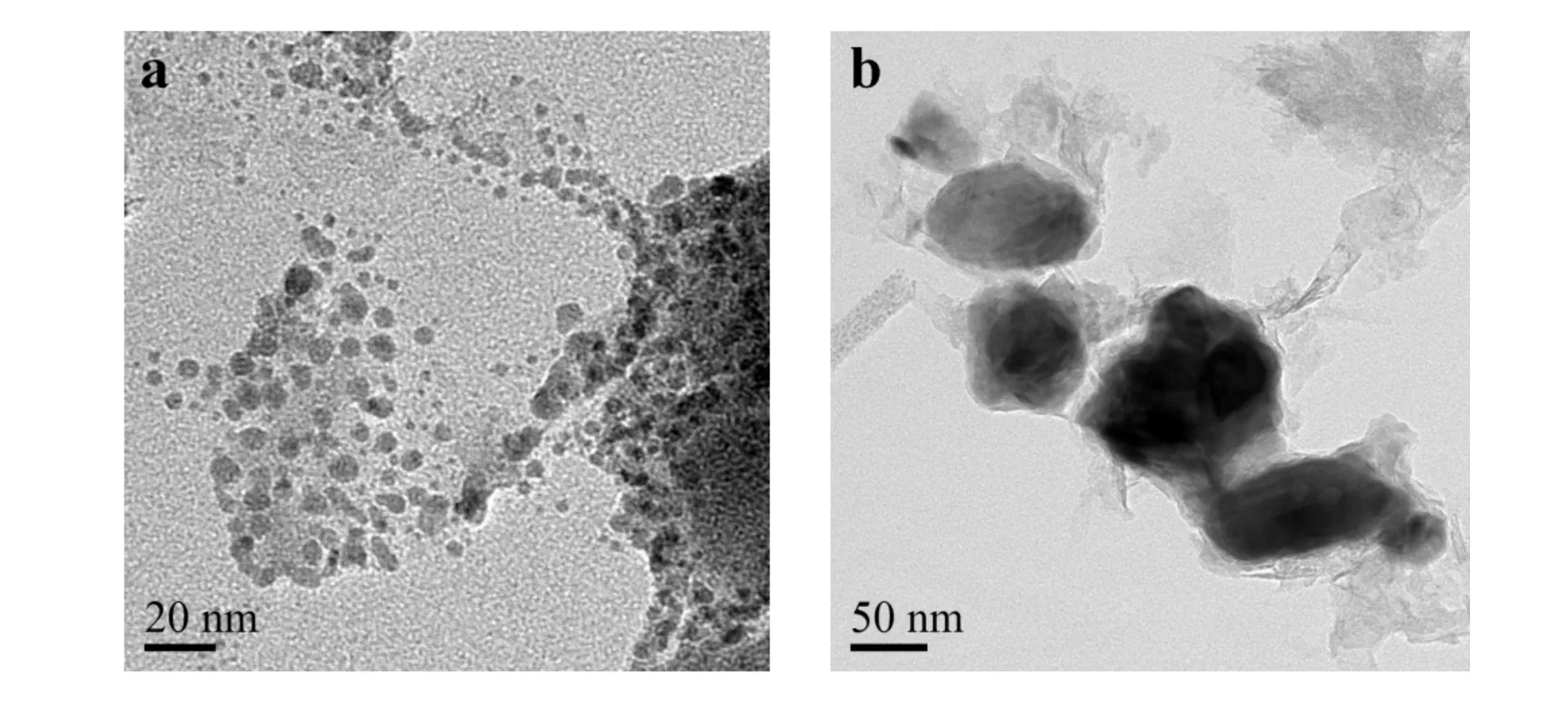
a) 150℃; b) 180℃图2 不同温度下产物的TEM 图Fig.2 TEM images of products at different temperatures
2.1.2 溶剂的影响
水在溶剂热反应可控制备铜和氧化亚铜中起着非常重要的作用. 以无水乙醇为反应溶剂,不加水,其他反应条件同上,所得产物的XRD谱图如图3所示. 由图3可知,不加入蒸馏水,150℃ 时,产物为碱式硝酸铜、氧化亚铜和铜的混合物,产物成分复杂不单一. 温度升至180℃ 时,产物仍是氧化亚铜和铜的混合物,成分也不单一,可见溶剂热法制备氧化亚铜的反应中,蒸馏水起重要作用.有蒸馏水时,产物成分单一可控性能较好.无水时反应产物成分复杂,可控性能差,不利于得到较纯的产物.

2θ/(°)1) Cu2(NO3)2(OH)2; 2) Cu2O; 3) Cu图3 无水时不同温度下产物的 XRD 图 Fig.3 XRD patterns of products without water at different temperatures
由以上结果,推测可能的反应机理为:
2Cu(NO3)2+2H2O→Cu2(NO3)2(OH)2+2HNO3,
Cu2(NO3)2(OH)2+2C2H5OH→Cu2O+
2CH3COOH+2NO+3H2O,
Cu2O+C2H5OH→2Cu+CH3CHO+H2O.
故水在该溶剂热反应中作用非常重要,不仅是反应的溶剂,也作为反应物参与了反应.
2.2 纳米氧化亚铜对亚甲基蓝的催化降解
以所制纳米氧化亚铜为催化剂,在H2O2条件下,对亚甲基蓝的光催化降解性能进行了研究.发现氧化亚铜和H2O2对亚甲基蓝的降解均有重要作用,不加氧化亚铜或H2O2几乎不能使亚甲基蓝发生降解.
2.2.1 氧化亚铜用量的影响
取 0.0010 g/L 的亚甲基蓝溶液 200 mL 于250 mL的圆底烧瓶中,分别加0.1、0.2、0.3 g氧化亚铜后搅拌,离心取样,测量初始的吸光度A0.然后加入4 mL 的H2O2在光照射条件下进行催化降解,间隔一定时间取样后测量样品溶液的吸光度At,计算降解率,结果如图4. 由图4可知,在氧化亚铜和H2O2作用下,亚甲基蓝能有效发生光催化降解,2h即可使降解率达90%以上;随着氧化亚铜用量的增加,降解速率和降解率有所增加,但当氧化亚铜增加到一定量后,降解速率和降解率几乎不变.

图4 氧化亚铜用量对降解率的影响Fig.4 Effect of Cu2O usage on degradation rate of methylene blue
2.2.2 双氧水用量的影响
双氧水的用量对亚甲基蓝的光催化降解也有影响,固定氧化亚铜的用量为0.20 g,不同双氧水的用量对亚甲基蓝光降解的影响如图5所示. 由图5可知,氧化亚铜的用量不变时,降解速率和降解率会随着双氧水的含量增加而增加.

图5 双氧水用量对亚甲基蓝降解率的影响Fig.5 Effect of H2O2 usage on degradation rate of methylene blue
3 结语
以五水硝酸铜为原料,乙醇和水为溶剂和还原剂,通过控制反应温度,用溶剂热法可控制备了纳米氧化亚铜和纳米铜;水的加入可极大地提高溶剂热反应的可控性和所得产物的选择性. 150℃时可以获得约5~6 nm的氧化亚铜, 180℃时可获得约50 nm的球形纳米铜.在H2O2的共同作用下,所制备的纳米氧化亚铜能高效光催化降解亚甲基蓝,2h即可使降解率达90%以上.
参 考 文 献
[1] 翟纪伟, 高荣杰, 张雅栋. Cu2O光催化降解海水中苯酚的研究[J]. 海洋环境科学, 2011, 30(2): 227-233.
[2] 洪啸吟, 冯汉保. 涂料化学[M]. 北京: 科学出版社, 1997: 278.
[3] 司徒杰. 化工产品手册无机化工产品[M].北京:化学工业出版社, 1999: 721.
[4] Zhu H,Chen Q,Niu H,et al. Growth of cuprite nano-cubes under acidic conditions[J]. Chinese J of Inorg Chem,2004,20(10): 1172-1176.
[5] Zhou Y,Switzer J. Effect of bath temperature on the phase composition and microstructure of galvanostatic electrodeposited cuprous oxide films [J]. Chin J Mater Res,1996,10(5): 512-516.
[6] Zhu Y,Qian Y,Zhang N,et al. Preparation and characte-rization of nanocrystalline powders of cuprous oxide by using γ-radiation[J].Mater Res Bull,1994,29(4): 377-383.
[7] 陈祖耀,朱玉瑞,陈文明,等. 紫外射线辐照制备Cu2O 超细粉及其宏观动力学[J]. 金属学报,1997,33(3): 330-335.
[8] Chen S J,Chen X T,Xue Z,et al. Solvothermal pre-paration of Cu2O crystalline particles[J]. J Cryst Growth,2002,246(1/2): 169-175.
