腹腔镜辅助与开腹胃癌根治术的中期疗效比较
2015-03-10高金辉李建国蔡铭智蔡丽生洪建明林小雷
高金辉 李建国 蔡铭智 蔡丽生 洪建明 林小雷
(福建医科大学附属漳州市医院普外二科,漳州 363000)
·临床论著·
腹腔镜辅助与开腹胃癌根治术的中期疗效比较
高金辉 李建国*蔡铭智 蔡丽生 洪建明 林小雷
(福建医科大学附属漳州市医院普外二科,漳州 363000)
目的 探讨腹腔镜辅助胃癌根治术与开腹胃癌根治术的中期疗效。 方法 比较2005年6月~2011年1月我科同组人员行腹腔镜辅助与开腹胃癌D2根治术,其中腹腔镜辅助胃癌根治术46例(腹腔镜组),开腹胃癌根治术54例(开腹组),比较2组胃癌根治术后肿瘤局部复发、远处转移、生存率等中期疗效。 结果 腹腔镜组与开腹组局部复发率分别为10.9%(5/46)、7.4%(4/54),无统计学差异(χ2=0.364,P=0.546);远处转移率分别为6.5%(3/46)、5.6%(3/54),差异无显著性意义(χ2=0.000,P=1.000)。2组生存率无显著性差异(χ2=1.386,P=0.239)。 结论 腹腔镜组辅助与开腹胃癌根治术在生存率、术后局部复发和远处转移等中期疗效方面无显著性差异。
胃癌; 腹腔镜; 开腹手术; 中期疗效
自1994年日本Kitano等[1]首次完成腹腔镜辅助下胃大部切除术治疗胃癌以来,腹腔镜辅助下胃癌根治术已经有20年发展,得到越来越多的国内外专家认可,但腹腔镜辅助胃癌根治术的中期疗效,特别是进展期胃癌的中期疗效报道不多。本文回顾性比较我院2005年6月~2011年1月腹腔镜辅助与开腹胃癌D2根治术,旨在探讨2种术式的中期疗效是否存在差异。
1 临床资料与方法
1.1 一般资料
病例选择标准:①术前胃镜病理检查证实胃癌,一般情况能够耐受手术;②无远处转移;③肿瘤直径<10 cm,浆膜层受侵面积<10 cm2;④无淋巴结转移灶融合并包绕重要血管;⑤患者知情同意。病例排除标准: ①伴有肝、肺、盆腔、腹膜种植等远处转移; ②未行D2 淋巴结清扫;③腹腔镜中转开腹。根据患者意愿选择腹腔镜手术或开腹手术。2组患者性别、年龄、TNM分期、肿瘤组织学分类、肿瘤部位、肿瘤浸润深度、淋巴结清扫数目无显著性差异(P>0.05),有可比性,见表1。
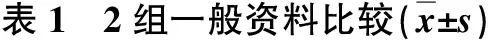

组别年龄(岁)性别男女肿瘤大小(cm)组织分型(例)浸润深度腺癌印戒细胞癌T1T2T3T4腹腔镜组(n=46)56.2±3.731155.3±2.1379581419开腹组(n=54)55.1±4.533216.1±2.34014781524t(χ2)值t=1.320χ2=0.425t=1.803χ2=0.567χ2=0.311P值0.09490.5140.0740.4510.958组别临床分期肿瘤部位术后化疗Ⅰ期Ⅱ期Ⅲ期胃窦胃角胃体、胃底、贲门有无腹腔镜组(n=46)1317161814143016开腹组(n=54)1620181819172925t(χ2)值χ2=0.031χ2=0.411χ2=1.361P值0.9840.8140.243
1.2 方法
1.2.1 腹腔镜辅助下根治性远端胃切除术(选择肿瘤位于胃窦、胃角的患者) 静吸复合全麻,仰卧位,头高20°,双侧下肢分开约30°。经脐部建立气腹,压力12 mm Hg(1 mm Hg=0.133 kPa),置入trocar和10 mm 30°腹腔镜。左、右腹直肌旁各建立2个操作孔,左侧操作孔置入超声刀。提起胃大弯侧,分离剔除大网膜、横结肠系膜前叶及全胰腺被膜,至胰腺上沿。向左侧分离至脾脏下极水平,分离显露胃网膜左血管,并于根部用钛夹及止血夹夹闭。沿胃大弯侧分离,左上分离至脾胃韧带,靠近脾脏切断并结扎胃网膜左血管及胃短血管1支,清除第4sb组淋巴脂肪组织。向右分离胃网膜,显露右血管根部,用钛夹及止血夹夹闭、切断。往右下分离至幽门下3 cm,显露胃十二指肠动脉,清除第6组淋巴结脂肪组织;将胃体顶向前方,于胃后方分离清扫第8组淋巴脂肪组织,胃左静脉于根部上止血夹后用超声刀切断。裸化胃左动脉,清除7、9组淋巴组织,根部用钛夹及止血夹夹闭,再用超声刀切断。沿脾动脉旁分离至脾门处,清扫10、11p、11d淋巴结。把肝脏向上拉开,高位离断肝胃韧带,左上分离至食管下段,清除食管旁及第1组淋巴脂肪,继续向上分离胃后壁,分离至贲门部小弯侧与食管下端相通。至此分离结束。关闭气腹,于上腹正中做4~5 cm切口进腹,行毕Ⅰ式吻合或Roux-en-Y吻合,检查吻合口无张力,无狭窄,逐层关腹。重新建立气腹,腹腔镜检查无出血,充分止血、冲洗腹腔,吸净腹腔积液。于左侧操作孔置1根引流管于肝下,缝合固定于皮肤。
1.2.2 腹腔镜辅助下根治性全胃切除术(选择肿瘤位于胃底、胃体、贲门的患者) 在远端胃癌清扫的范围上,在左肾前筋膜前的疏松间隙内分离,沿脾动脉表面清扫No.11 d组淋巴结至脾门部。取左高右低位暴露胃脾韧带,贴近脾门清扫至贲门左侧,清扫No.2、No.4sa组淋巴结。淋巴结清扫完毕后,于上腹部切开4~5 cm长切口进腹,行改良Roux-en-Y吻合或标准Roux-en-Y吻合。于脾窝及吻合口下方各放置1根橡胶引流管。
1.2.3 传统开腹手术均按照胃癌D2根治术规范手术[2]。
1.3 随访
术后每半年复查一次,复查内容:体格检查、胃镜检查、肝胆胰脾彩超、上下腹部MRI及胸部CT检查。随访方式:电话回访、信件回访、门诊复查及住院病历等。期间可疑复发、转移病例均经过经胃镜活检病理、腹部MRI、腹部彩超或肺部CT等至少一项证实。
1.4 观察指标
局部复发率,远处转移率,生存率。
1.5 统计处理

2 结果
随访时间6~72个月,中位随访时间37个月,无失访病例,其中随访生存超过36个月腹腔镜组34例,开腹组39例,随访生存超过60个月腹腔镜组30例,开腹组34例。
2.1 清扫淋巴结
腹腔镜组清扫淋巴结数目与开腹组差异无显著性,2组全胃切除淋巴结差异无显著性,远端胃切除淋巴结虽有统计学差异,但无临床意义,见表2。
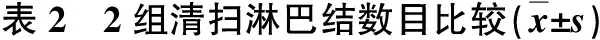

组别淋巴结全胃切除淋巴结远端胃切除淋巴结腹腔镜组25.6±4.6(n=46)27.4±3.6(n=14)24.1±2.6(n=32)开腹组26.8±4.2(n=54)28.6±3.2(n=17)25.3±2.3(n=37)t值-1.3630.9822.034P值 0.1760.2530.046
2.2 局部复发、远处转移和生存率的比较
腹腔镜组局部复发5例,复发率10.9%(5/46):术后1~36个月复发3例,其中1例吻合口复发,1例5组淋巴结位置复发,1例6组淋巴结位置复发;术后36~60个月复发2例,1例吻合口复发,1例脾门淋巴结复发。开腹组局部复发4例,局部复发率7.4%(4/54):术后1~36个月复发2例,其中1例吻合口复发,1例5组淋巴结位置复发;术后36~60个月复发2例,其中1例12组淋巴结位置复发,1例脾门淋巴结复发。2组复发率无显著性差异(P>0.05),见表3。

表3 2组局部复发、远处转移率比较
2组发生远处转移均为3例,转移率分别为6.5%(3/46)、5.6%(3/54),2组转移率无显著性差异。腹腔镜组术后1~36个月1例肝脏转移,术后36~60个月转移2例(盆腔转移1例,双肺转移1例)。开腹组术后1~36个月转移2例(肝脏转移1例,盆腔转移1例),术后36~60个月1例全身多发转移。2组远处转移率无统计学差异,见表3。2组生存率比较无统计学差异(χ2=1.386,P=0.239),见图1。

图1 2组生存率比较的Kaplan-Meier图
3 讨论
腹腔镜辅助胃癌根治术要取得良好的远期疗效,必须遵循胃癌手术的原则,必须做到[3]:①完整切除肿瘤及浸润的周围组织;②手术操作过程避免接触肿瘤操作;③切缘阴性;④彻底清扫各组淋巴结。只有这样才能取得与开腹手术相当的远期疗效。
腹腔镜具有放大及二维成像甚至3D成像效果,手术视野清楚,抓持少量组织就可以很好地进行暴露及操作,相对于开腹手术,接触及挤压肿瘤组织的几率较少,做到对肿瘤非接触。同时因腹腔有放大作用,可以具有较好的整体观,分清层次,做到整块切除肿瘤及浸润的周围组织。腹腔镜手术腹部切口较小,在取出标本时可以在切口放置保护器防止切口的种植转移,田夫等[4]报道切口及腹腔内用5-FU溶液冲洗、浸泡可以减少腹腔内及切口的种植转移。腹腔镜胃癌手术同时也能保证切缘阴性,顾钧等[5]报道132例根治性远端胃切除术,腹腔镜组正常组织切缘为(6.7±0.5)cm,开腹组正常组织切缘(6.3±0.7)cm,2组无统计学差异。Poviello等[6]统计47例腹腔镜胃癌手术标本的切缘均为阴性。本研究腹腔镜组所有切缘阴性,腹腔镜组正常组织切缘(5.8±0.7)cm,开腹组正常组织切缘(6.4±0.3)cm,说明腹腔镜胃癌手术可以保证切缘阴性。
胃癌术后远期疗效的关键是手术是否能彻底清扫各组淋巴结,做到胃癌D2根治术,彻底清扫淋巴结主要是体现在清扫淋巴结数目。腹腔镜视野广阔,具有更好的解剖层次,同时超声刀刀背具有隔热作用,损伤周围组织程度轻,可以对血管进行脉络化,彻底清扫血管周围脂肪组织及淋巴结,做到对血管进行根部结扎,彻底清扫胃周围淋巴结,这点比开腹手术更具优势。第5版国际抗癌联盟和美国癌症联合会(UICC和AJCC)规定清扫的各站淋巴结数目要>15枚。黄昌明等[7]比较506例腹腔镜胃癌根治术与同期428例开腹胃癌根治手术清扫的各站淋巴结数目,腹腔镜组清扫淋巴结(29.1±10.4)枚,与开腹胃癌根治术(28.3±10.7)枚无显著差异,在各组清扫的淋巴结数目上,腹腔镜组在第7、8组清扫的淋巴结数目明显多于传统开腹组,其余各组别淋巴结清扫数目与传统开腹组相当。本研究腹腔镜组清扫淋巴结(25.6±4.6)枚,开腹组清扫淋巴结数(26.8±4.2)枚,2组无显著性差异(t=-1.363,P=0.176),表明腹腔镜辅助胃癌根治术在淋巴结清扫上符合规定的清扫淋巴结数目。
因此,腹腔镜胃癌根治术很好地遵循胃癌手术的原则,能够取得良好的远期疗效。Shuang等[8]对同期进行腹腔镜与传统开腹手术治疗进展期胃癌进行50个月随访,2组患者术后生存率无统计学差异。叶再生等[9]对160例腹腔镜胃癌D2根治术与同期180例开腹胃癌D2根治术进行随访,随访时间3~60个月,中位时间19个月,3年累积生存率无显著性差异。本研究腹腔镜组生存率、局部复发率、远处转移率与开腹组相当(P>0.05),说明腹腔镜胃癌手术能与开腹胃癌手术取得相当的远期疗效。
腹腔镜手术中CO2气腹中可能引起肿瘤细胞飘逸而引起腹壁、trocar、切口位置的种植转移,即“烟囱效应”[10]。同时,气腹可能导致腹膜结构改变,腹膜局部免疫功能下降,肿瘤细胞可能更容易种植、生长。另外,腹腔镜胃癌手术难度大,需要团队熟练的配合,目前也还没有手术操作规范,这些是腹腔镜胃癌根治术需要解决的问题,需要我们努力研究及改进。
腹腔镜手术已被第2版日本《胃癌治疗指南》接受为早期胃癌的标准手术方式之一,但进展期胃癌缺乏多中心、大宗病例的长期随访数据,远期疗效尚不完全明确,欧美及我国的一些专家认为进展期胃癌侵犯浆膜层的面积≤10 cm2的患者可以选择腹腔镜胃癌D2根治术进行手术治疗[11,12],希望通过我们的努力能使腹腔镜胃癌根治术成为胃癌手术的标准术式。
1 Kitano S, Iso Y, Moriyama M,et al. Laparoscopic-assisted BillrothⅠgastrectomy. Surg Laparosc Endosc,1994,4(2):146-148.
2 邹寿椿.胃、十二指肠肿瘤.见:张启瑜,主编.钱礼腹部外科学.第1版.北京:人民卫生出版社,2006.250-258.
3 余佩武.腹腔镜胃癌根治术的原则与评价.中国普外基础与临床杂志,2009,16(1):1-5.
4 田 夫,邓 清,胡小苗,等.腹腔镜辅助下胃癌根治术21例报告.中国微创外科杂志,2012,12(3):217-219.
5 顾 钧,崔 龙,沈定丰.胃癌D3淋巴结清扫术的临床价值.中国现代手术学杂志,2008,12(1):9-12.
6 Roviello F, Pedrazzani C, Marrelli D, et al.Super-extended (D3) lymphadenectomy in advanced gastric cancer.J Cancer Surg,2010,36(5):439-446.
7 黄昌明,林建贤,郑朝辉,等.腹腔镜辅助胃癌根治术淋巴结清扫效果的临床对照研究.中华外科杂志,2011,49(3):200-203.
8 Shuang J, Qi S, Zheng J, et al. A case-control study of laparoscopy-assisted and open distal gastrectomy for advanced gastric cancer. J Gastrointest Surg,2011,15(1):57-62.
9 叶再生,应敏刚,陈路川,等.腹腔镜与开腹行胃癌D2根治术的对照研究及中期随访报告.中国微创外科杂志,2013,13(11):977-981.
10 Tseng LN, Berends FJ, Wittieh P, et al. Port-site metastases, impact of local issue trauma and gas leakage. Surg Endosc,1998,12(12):1377-1380.
11 黄昌明,林建贤.腹腔镜胃癌根治术合理应用及疗效评价.中国实用外科杂志,2011,31(8):672-674.
12 汤黎明,钱 峻,朱 杰,等.腹腔镜胃癌D2根治术在进展期胃癌中的应用探讨.中国微创外科杂志,2008,8(12):1079-1081.
(修回日期:2014-11-03)
(责任编辑:李贺琼)
Comparison of Medium-term Curative Effectiveness Between Laparoscopic Assisted and Open Radical Gastrectomy
GaoJinhui,LiJianguo,CaiMingzhi,etal.
DepartmentofGeneralSurgeryII,ZhangzhouMunicipalHospitalAffiliatedtoFujianMedicalUniversity,Zhangzhou363000,China
Correspondingauthor:LiJianguo,E-mail:jjxln649@163.com
Objective To explore the medium-term curative effectiveness of laparoscopic-assisted and open radical distal gastrectomy. Methods A total of 100 patients underwent either laparoscopic D2 gastrectomy (n=46, laparoscopic group) or open D2 gastrectomy (n=54, open group) by the same staffs in our department from June 2005 to January 2011. The medium-term curative effectiveness was compared between the two groups, including local recurrence, distant metastasis, and survival rates. Results The local recurrence rate in the laparoscopic group and the open group were 10.9% (5/46) and 7.4% (4/54), respectively, without significant difference (χ2=0.364,P=0.546).There was no distinct difference in the distant metastasis rate between the two groups[6.5%(3/46) vs 5.6%(3/54),χ2=0.000,P=1.000]. The survival rate in the laparoscopic group and the open group had no significant difference (χ2=1.386,P=0.239). Conclusion The local recurrence, distant metastasis, and survival rate after operation show no significant differences between laparoscopic and open gastrectomy.
Gastric cancer; Laparoscopy; Open surgery; Medium-term efficacy
R735.2
A
1009-6604(2015)07-0597-04
10.3969/j.issn.1009-6604.2015.07.005
2014-04-04)
* 通讯作者,E-mail:jjxln649@163.com
