某院2014年在用药品说明书与非处方药说明书范本对比分析
2015-03-09苏芬丽广州中医药大学第一附属医院药学部广州510405
熊 芬,苏芬丽,孙 旭,涂 星(广州中医药大学第一附属医院药学部,广州 510405)
药品说明书是指药品生产企业印刷并提供的包含药理学、毒理学、药效学等安全性、有效性、重要科学数据和结论,用以指导临床正确使用药品的技术性资料[1]。各国都有相应的法律对药品说明书的格式和内容加以约束和规范[2-3]。但由于我国目前一些“双跨”品种[经国家食品药品监督管理总局(CFDA)批准,既可作为处方药又可作为非处方药(OTC)]、一品多规、多生产厂家等问题的存在,药品说明书仍存在少标、漏标、标注内容不详等现象[4-7]。美国FDA确定了OTC说明书在患者安全用药方面的重要作用,出台了《企业指南:OTC 说明书理解力研究指导原则草案》[8];我国也根据相关研究开展了部分OTC 说明书的修改,但关注和监管力度仍不够,许多OTC 说明书与国家规范范本存在差异,特别是对特殊人群禁用、慎用的差异会给医师和患者选药带来困惑,也可能给医患关系留下隐患。本文通过对比2014年某院的在用药品说明书与CFDA 网站公布的OTC 说明书范本之间的差异,对其可能引起的风险进行归纳与分析,为加强说明书管理、减少临床用药的安全隐患提供参考。
1 资料与方法
1.1 资料来源
该院在用1 324 个药品说明书,从药房所拆药品包装获得;OTC说明书范本以CFDA网站公布的OTC(化学药和中成药)说明书范本为准。
1.2 方法
以该院在用药品的通用名、剂型和规格,与CFDA网站公布的OTC目录匹对,筛选出属于OTC的药物。将该院正在使用的OTC说明书和CFDA网站公布的OTC说明书范本进行比对,对存在的差异按照用药风险分为“可忽略”“一般”“重要”和“警惕”4 个层次,并对说明书差异率、差异风险程度分布比例和差异内容进行分析讨论。划分标准见表1。

表1 说明书差异风险程度划分标准Tab 1 Classification criteria of instruction difference risk
2 结果
2.1 在用药品和OTC匹配情况
有108个西药、136个中成药,合计244个品种在CFDA公布的OTC之列;其中,属于“双跨”品种的为62个(占25.4%)。
2.2 说明书差异率
进一步对244 个品种的说明书进行核对,与CFDA 网站OTC说明书范本内容一致的只有165个(西药70个,中成药95个);内容存在差异的有79 个(西药38 个,中成药41 个),占32.38%,具体见表2、表3。

表2 某院在用药品说明书与OTC说明书范本比较结果Tab 2 Comparison between hospital-acquired drug instructions and OTC model instructions
2.3 说明书差异风险程度评估
药品说明书的差异风险按照表1 的标准进行评估。如双氯芬酸二乙胺乳胶剂,说明书【禁忌】项为妊娠期末3 个月禁用;而CFDA 网站上公布的OTC 说明书范本【禁忌】项为妊娠期妇女禁用。这两种来源的说明书之间的差异,属于“禁忌项不一致”,按照表1,安全风险属于“警惕”级别。79种存在差异的药品说明书,其差异安全风险评估分布见表4。
2.4 风险层次为“警惕”和“重要”的说明书差异内容分析
风险层次为“警惕”和“重要”的说明书差异与患者的用药安全息息相关,笔者将此两种差异涉及的内容进行了整理,具体分布见表5。
由表5可见,在“警惕”风险层次中,差异主要表现为“特殊疾病禁用”和“妊娠妇女禁用”表述不一致,分别占43.48%和39.13%。此项目涉及到特殊人群、特别是孕妇用药的安全,也是医疗纠纷的高发点,不容忽视。
在“重要”风险层次中,“药物适应证限制”不一致占50.00%,其中涉及到的3个品种均为中成药,分别是川百止痒洗剂、保妇康栓和抗病毒口服液;其OTC 说明书范本【注意事项】均标注了相关注意事项,而在用品种说明书却未标注。如川百止痒洗剂,其OTC 说明书范本【注意事项】标明“因糖尿病、肾病、肝病、肿瘤等疾病引起的皮肤瘙痒,不属本品适用范围”,而该院在用药品说明书中却未标注。说明书“适应证限制”的标注缺失,会误导医师选择不适宜的药品,导致治疗失败。

表3 说明书有差异的药品列表Tab 3 List of drugs with differences in instructions
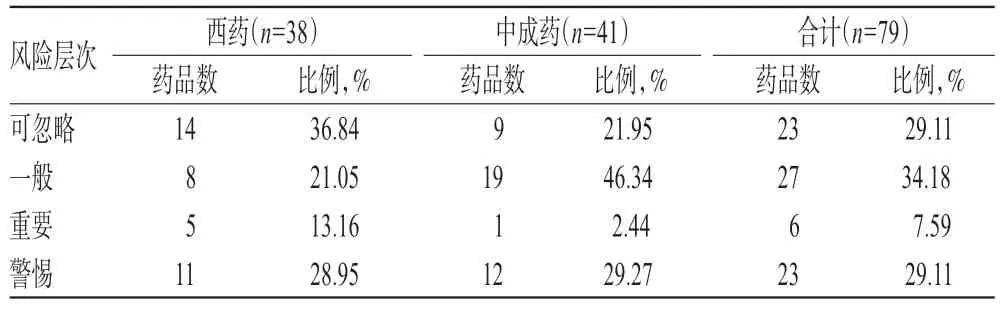
表4 说明书差异风险评估分布Tab 4 Distribution of the differences risk assessment of instruction
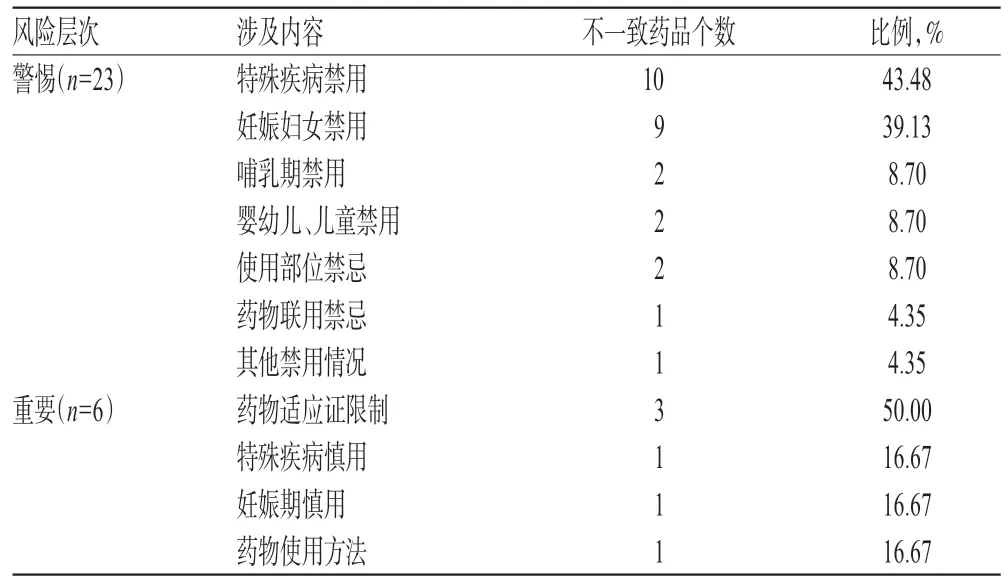
表5 说明书差异内容分布Tab 5 Content distribution of differences of instruction
3 讨论与建议
从统计结果可以看出,对于同一通用名称、相同规格的药品,32.38%的在用药品说明书与CFDA 网站公布的OTC 说明书范本不一致。其中,涉及到用药安全风险差异的占36.70%(“重要”风险层次占7.59%,“警惕”风险层次占29.11%)。说明书的表述不一致,给医师处方或患者自行选药带来了困惑和风险,特别是归于“警惕”和“重要”层次的说明书差异,涉及到特殊病理、生理人群的禁用、慎用限制,或药物联用之间的禁忌,更需要有统一、科学、规范的指导,否则极易引发用药安全事故或医疗纠纷。如清开灵颗粒为“双跨”品种,医院在用药品说明书上标示为【禁忌】尚不明确;而OTC 说明书范本标示为【禁忌】孕妇禁用。两份说明书出自同一生产厂家,这给医师为妊娠患者处方该药时带来了风险。
出现说明书不一致可能有如下原因:(1)我国上市的西药大多为仿制药,因此生产厂家在拟订说明书时可能参考了不同来源的文献资料,如引用的是国外不同厂家生产的同一成分药品的说明书、美国FDA颁布的药物妊娠危险性等级表、发表于不同时间的文献专著等,造成说明书中的“禁忌”和“注意事项”等信息不一致。(2)药品说明书是发生医疗纠纷时判定责任归属的重要法律依据之一,因此一部分生产厂家为了规避风险,对于妊娠妇女等特殊人群用药使用了更谨慎的语言来标注,如在临床上还没有基于孕妇的用药安全研究资料时,一律写“孕妇禁用”[9]。(3)药品说明书更新不及时。笔者在核对说明书时发现,很多药品说明书的核准日期仍为2006、2007年,已有多年未更新,而关于该药的安全性评估已有了新进展,部分生产厂家的说明书并未将这些进展体现出来。这种更新滞后的情况在说明书的“注意事项”“不良反应”“药物相互作用”等项目中尤为突出。
当医院在用药品说明书与CFDA网站上公布的说明书范本出现差异时,该以哪一份为标准?这是每一位药学工作者都必须面临的现实问题。引申开来,当同一个通用名不同生产厂家的说明书、重要的用药安全信息存在不一致时该如何取舍,也是我们经常面临的难题。由国家中医药管理局医政司、中华中医药学会临床药理专业委员会组织编写的《中药注射剂临床应用指南》指出:“凡是同一品种,若有的生产企业产品说明书安全性项目是‘尚不明确’,有的企业产品说明书安全性项目已具体明确,医疗机构应采用后者,并按说明书使用[10]”。鉴于此,从保障用药安全、减少医疗纠纷的角度来说,药学工作者应参考更严格的说明书指导临床用药,这样更能保障用药安全。
在我国药品说明书的标准上,一直存在“国产药不如进口药、中药不如西药”的现象[11]。药品监管部门需进一步加强说明书的规范化管理,出台细化的政策法规,提供统一、具体的说明书规范和标准,督促生产厂家严谨制订和及时修订说明书,提高其准确性,减少信息滞后性,从而确保临床安全、合理用药[9]。
[1]唐春燕,陈大建,曾立威,等.药品说明书在药品风险管理中的地位与作用[J].医药导报,2008,27(7):869.
[2]国家药品监督管理局.中华人民共和国药品管理法[S].北京:法律出版社,2003:22.
[3]张小鹏,孙德文,张新平.我国非处方药说明书的研究进展[J].医学与社会,2011,24(8):50.
[4]李玉衡,肖小川.新版化学药品说明书内容表达仍错误百出[J].首都医药,2007,14(6):22.
[5]刘敏豪,邬倩倩.我院药品说明书现状调查及其相关风险分析[J].中国药房,2012,23(17):1 619.
[6]张欣悦,孙成春,谢继青,等.33份抗肿瘤药类注射剂药品说明书的调查分析[J].中国药房,2014,25(1):91.
[7]Saito M,Hirata-Koizumi M,Urano T,et al.A literature search on pharmacokinetic drug interactions of statins and analysis of how such interactions are reflected in package inserts in Japan[J].J Clin Pharm Ther,2005,30(1):21.
[8]U.S Food and Drug Administration.Draft guidance for industry on label comprehension studies for nonprescription drug products;availability[EB/OL].(2009-07-30)[2014-12-01].http://www.regulation.gov/#!documentDetail;D=FDA-2009-D-0181-0001.
[9]黄咖雯.259 份抗高血压说明书中妊娠妇女用药信息调查分析[J].中国医院药学杂志,2014,34(12):1 027.
[10]任德全,张佰礼.中药注射剂临床应用指南[M].北京:人民卫生出版社,2011:98.
[11]张建平.中药注射剂说明书中的警示缺陷[J].中国医院药学杂志,2014,34(8):664.
