五味子提取过程中5-羟甲基糠醛的变化规律及影响因素研究
2015-03-09慕升君李德坤杨悦武余伯阳叶正良鞠爱春中国药科大学中药学院南京0009天津天士力之骄药业有限公司天津30040
李 越,慕升君,李德坤,杨悦武,余伯阳,叶正良,鞠爱春#(.中国药科大学中药学院,南京 0009;.天津天士力之骄药业有限公司,天津 30040)
五味子(Schisandra chinensis)系常用的滋补性中药,是木兰科多年生落叶木质藤本植物五味子[Schisandra chinensis(Turcz.)Baill.]的干燥成熟果实,因其具有甘、酸、辛、苦、咸五味,故名五味子[1-2],又名五梅子、玄及、会及、山花椒等[3]。五味子主产于黑龙江、吉林、辽宁等地,习称“北五味子”,具有收敛固涩、益气生津、补肾宁心的功效,主要用于治疗久嗽虚喘、梦遗滑精、遗尿尿频、久泻不止、自汗、盗汗、津伤口渴、短气脉虚、内热消渴、心悸失眠等症[1,4]。
5-羟甲基糠醛(5-hydroxymethylfurfural,简称5-HMF),是由葡萄糖等单糖化合物在高温或弱酸性等条件下脱水生成的一种具有呋喃环结构的醛类化合物,是麦拉德反应的典型产物之一[5-7]。目前对于5-HMF 的药理作用仍存在争议,有文献表述该化合物对人体内脏和横纹肌有损害[8],有神经毒性,可与人体蛋白质结合产生积蓄中毒,故在2010 年版《中国药典》(二部)中明确规定了5-HMF和相关物质在含葡萄糖注射液中的限量[9]。虽然近几年也有研究表明,5-HMF具有改变血液流变学、抗心肌缺血、抗氧化等对人体有益的作用[10-11],但目前还是将其认为是一种在药材或制剂中应控制其限量的化合物。五味子作为常用药材,其提取方法多为水提醇沉,但由于五味子中含有糖类和酸等成分,在水提醇沉的过程中不可避免地会产生5-HMF。由于目前对五味子提取过程中5-HMF含量的监控较少,为了更好地控制五味子提取物中5-HMF的含量,笔者对五味子提取过程中5-HMF 的含量进行了监控,探明五味子提取过程中5-HMF 的含量变化规律,并根据变化规律中5-HMF含量变化明显的过程研究其影响因素。
1 材料
1.1 仪器
1100 型高效液相色谱仪(美国安捷伦公司);AL204 型万分之一天平、XS105型十万分之一天平(瑞士梅特勒-托利多仪器有限公司);R-215型旋转蒸发仪(瑞士Buchi公司);SHB-Ⅲ型循环水式多用真空泵(郑州长城科工贸有限公司);ZDHW型调温电热套(北京中兴伟业仪器有限公司);ALPHA 1-4 LSC型冻干机(德国Christ 冻干机有限公司);真空减压干燥箱(天津市天宇实验仪器有限公司);WK-200B 型高速药物粉碎机(青州市精诚机械有限公司);KQ5200 型超声波清洗器(昆山市超声波仪器有限公司);L-550型低速自动平衡离心机(长沙湘仪离心仪器有限公司)。
1.2 药材、药品与试剂
五味子药材(天津天士力之骄药业有限公司,产地:辽宁,批号:20121201,经中国药科大学余伯阳教授鉴定为真品);5-HMF 对照品(中国食品药品检定研究院,批号:111626-201308,纯度:98.3%);甲醇、醋酸均为色谱纯,水为实验室自制超纯水,其他试剂均为分析纯。
2 方法与结果
2.1 五味子提取过程中5-HMF的监控
2.1.1 五味子提取过程及取样点设置 取五味子药材(L1)经纯化水煎煮3次,得三煎合并液(L2);减压浓缩得一次浓缩液(L3);加乙醇调节醇度为75%,冷置过滤得一次醇沉液(L4);减压浓缩得二次浓缩液(L5);加乙醇调节醇度为85%,冷置过滤得二次醇沉液(L6);加氢氧化钠溶液,调节pH 为7,冷置过滤得调碱后滤液(L7);减压回收乙醇得三次浓缩液(L8);L8浓缩液减压干燥得五味子提取物(L9)。其中L1~L9为取样点。
2.1.2 供试品溶液的制备(1)测定五味子药材(L1)中5-HMF的供试品溶液制备:取五味子药材粉末(过60目筛)约1.00 g,精密称定,置于离心管中,加入甲醇12 ml,冰浴超声(功率为200 W)提取,每次25 min,共提取4 次,离心,过滤,合并提取液,置于50 ml量瓶中,用甲醇加至刻度,摇匀,0.45 μm滤膜滤过,取续滤液作为供试品溶液。(2)测定五味子提取过程药液(L2~L8)中5-HMF的供试品溶液制备:精密量取五味子提取过程药液适量,用水稀释定容至适当体积,0.45 μm滤膜滤过,取续滤液作为供试品溶液。(3)测定五味子提取物(L9)中5-HMF的供试品溶液制备:精密称定五味子提取物0.1 g,置于50 ml量瓶中,加水溶解,定容,摇匀,0.45 μm滤膜滤过,取续滤液作为供试品溶液。
2.1.3 对照品溶液的制备 精密称取5-HMF对照品9.03 mg,置于25 ml 量瓶中,用水溶解,定容得0.361 2 mg/ml 的对照品贮备液;再取1 ml 贮备液定容至25 ml,得0.014 4 mg/ml 的对照品溶液。
2.1.4 色谱条件及方法学考察(1)五味子药材中5-HMF 含量的测定:色谱柱为Diamonsil C18(2)(250 mm×4.6 mm,5 μm);流动相为甲醇-0.5%醋酸水溶液(15∶85),等度洗脱,流速为1 ml/min;检测波长为284 nm;柱温为30 ℃;进样量为10 μl;外标法定量。经方法学考察,线性回归方程为y(峰面积)=55 810x(质量浓度)+1.092 1(r=0.999 9),线性范围为1.14~18.21 μg/ml;精密度试验测得5-HMF 峰面积的RSD 为0.21%(n=5);稳定性试验在10 h 内测得5-HMF 峰面积的RSD 为0.98%(n=5);重复性试验测得同一份样品5-HMF 含量的RSD为1.97%(n=5);加样回收率试验测定了3组不同质量浓度共9 份样品,结果平均加样回收率为100.06%(RSD=1.00%,n=3)。(2)五味子提取过程药液和提取物中5-HMF测定色谱条件:色谱柱为Diamonsil C18(2)(250 mm×4.6 mm,5 μm);流动相为甲醇-水(5∶95),等度洗脱,流速为1 ml/min;检测波长为284 nm;柱温为30 ℃;进样量为10 μl;外标法定量。经方法学考察,线性回归方程为y=7.1×107x-2 520.1(r=0.999 9),线性范围为0.90~36.1 μg/ml;精密度试验测得5-HMF 峰面积的RSD 为1.67%(n=5);稳定性试验在10 h 内测得5-HMF 峰面积的RSD 为1.58%(n=5);重复性试验测得同一份样品5-HMF 含量的RSD 为1.81%(n=5);加样回收率试验测定了3组不同质量浓度的9份样品,结果平均加样回收率为101.61%(RSD=0.97%,n=3)。
2.1.5 含量测定结果 共提取3批五味子药材,每个监控点取样平行测定3次,5-HMF的含量均折算为生药中的含量。测定结果见表1,含量变化趋势见图1。
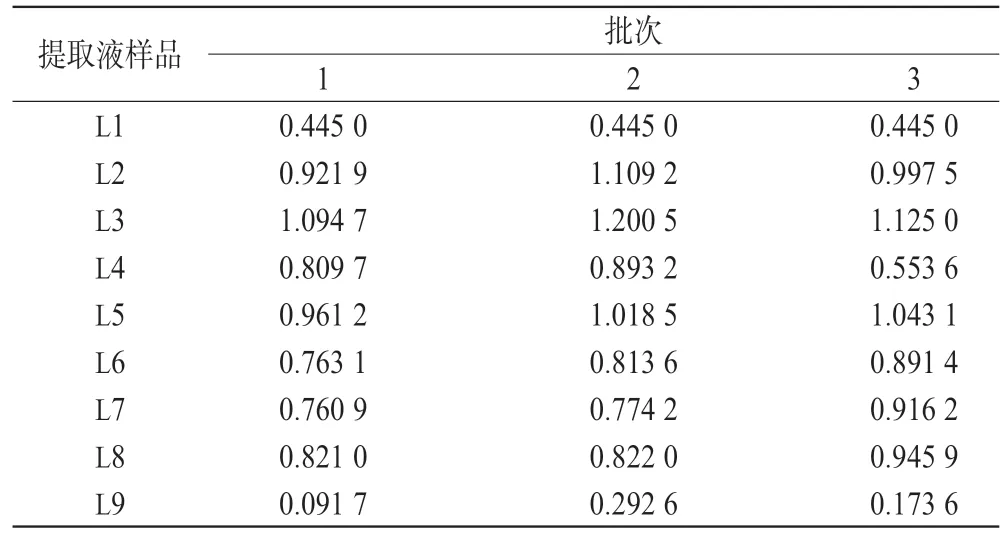
表1 3批五味子提取过程中各提取液中5-HMF的含量(g/kg)Tab 1 The contents of 5-HMF in the extracts in the extraction process of 3 batches of Schisandra chinensis(g/kg)
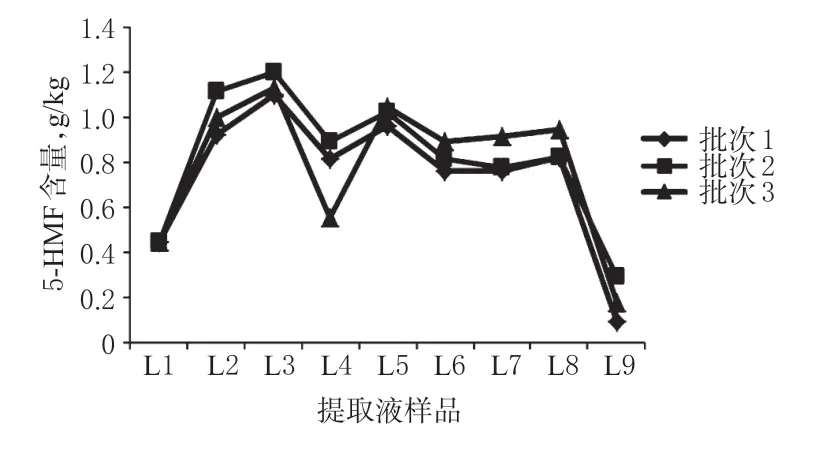
图1 3批五味子提取过程中5-HMF的含量变化趋势图Fig 1 The content variation trend of 5-HMF in the extraction process of 3 batches of Schisandra chinensis
由表1 和图1 可以看出,3 批五味子提取过程中5-HMF 的含量变化趋势一致:药材煎煮的过程中均产生大量5-HMF,浓缩时5-HMF含量均比前一监控点升高,醇沉时5-HMF含量均比前一监控点降低,调碱时5-HMF的含量基本不变,三次浓缩液(L8)减压干燥为提取物时5-HMF的含量明显下降。
2.2 温度和时间对五味子三次浓缩液(L8)干燥为提取物过程中5-HMF含量的影响
由上述试验结果发现,五味子三次浓缩液减压干燥至提取物的过程(见图1)中5-HMF的含量下降最明显,为了探明此过程中温度和时间对5-HMF 含量的影响,在不同温度下减压干燥五味子三次浓缩液,并在不同的时间点取样,测定5-HMF的含量;同时用同一批样品进行冷冻干燥,比较冷冻干燥和减压干燥所得的五味子提取物中5-HMF含量的差异。
2.2.1 供试品溶液的制备 减压干燥供试品溶液的制备:分别取400 μl五味子三次浓缩液置于西林瓶中,精密称定加样前后西林瓶的质量,在设定的温度下减压干燥,待温度达到设定值及真空表读数稳定后开始计时。当含水量达到12%左右时停止试验,每隔6 h 取1 次样,将取出的样品冷却后用甲醇溶解,定容至10 ml,摇匀,稀释5 倍后用0.45 μm 滤膜滤过,取续滤液作为供试品溶液。共设置5 个温度即50、55、60、65、70 ℃,每次试验保持相同的真空度。
冷冻干燥供试品溶液的制备:分别取400 μl稀释4倍的五味子三次浓缩液置于西林瓶中,精密称定加样前后西林瓶的质量,冻干。冻干完成后将样品用甲醇溶解,定容至10 ml,摇匀,0.45 μm滤膜滤过,取续滤液作为供试品溶液。
2.2.2 对照品溶液的制备 同“2.1.3”项下方法。
2.2.3 色谱条件 同“2.1.4”中五味子提取过程药液和提取物中5-HMF测定色谱条件。
2.2.4 5-HMF 含量测定结果 5-HMF 的含量以5-HMF 占样品干质量的含量计算。经水分测定得知五味子三次浓缩液干质量百分比为19.4%。五味子三次浓缩液在不同温度下减压干燥不同时间、冻干后5-HMF 的含量测定结果见表2,不同温度下减压干燥不同时间5-HMF含量变化见图2。
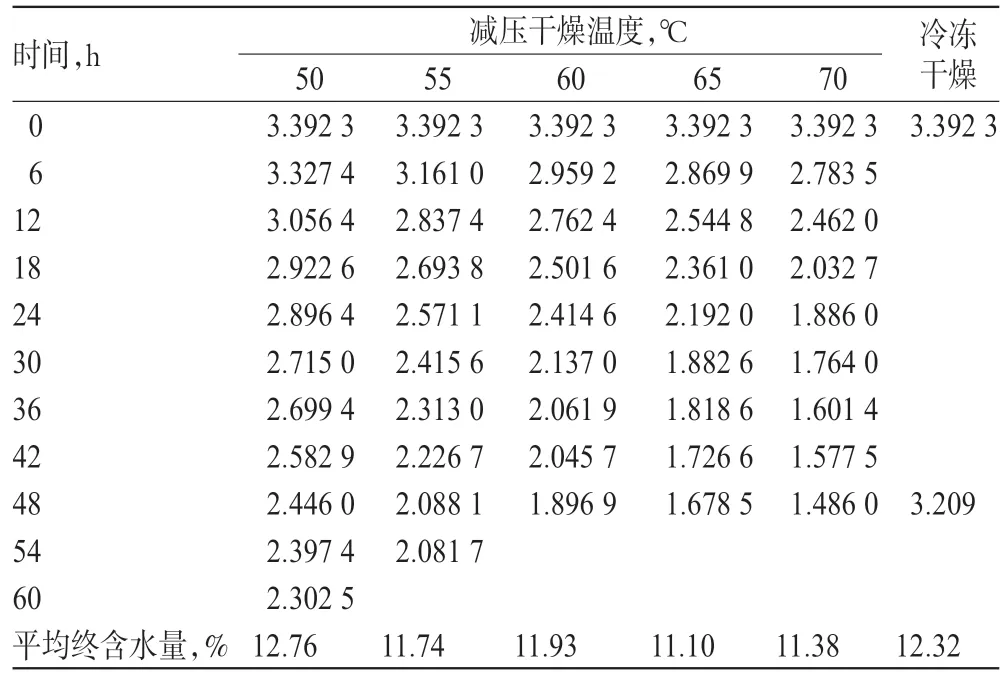
表2 五味子三次浓缩液在不同温度下减压干燥不同时间、冻干后5-HMF的含量(n=3,mg/g)Tab 2 The contents of 5-HMF in S.chinensis extracts by 3 times of concentrate at different time points after vacuum drying at different temperatures and after freeze-drying(n=3,mg/g)
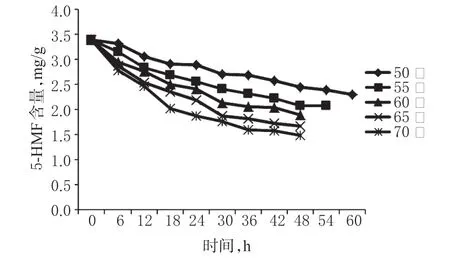
图2 五味子三次浓缩液在不同温度下减压干燥不同时间后5-HMF的含量变化Fig 2 The content variation of 5-HMF in S.chinensis extracts by 3 times of concentrate at different time points after vacuum drying at different temperatures
由表2 和图2 可以看出,真空度一定时,在相同温度下减压干燥,5-HMF的含量随减压干燥时间延长而逐渐下降;干燥相同时间时,5-HMF的含量随温度升高而降低;减压干燥至含水量接近时,随温度的升高,5-HMF 的含量降低,减压干燥所需时间缩短;冷冻干燥五味子提取液对5-HMF 含量的降低程度明显低于减压干燥法。
3 讨论
本试验中五味子药材、提取液及提取物中5-HMF 的含量测定所用的检测方法均经笔者试验得出,且经过方法学验证。由于5-HMF主要是由葡萄糖等单糖化合物在高温或弱酸性等条件下产生,温度对5-HMF的含量影响较大,故为了测定五味子药材中5-HMF 含量的真实值,避免加热提取的影响而采用了甲醇冰浴超声提取;但是在生产过程中通常采用水提醇沉的方法提取,所以药材和提取液(物)中物质基础可能有所不同。因此在本文中测定不同样品中的5-HMF含量时采用了不同的色谱条件。
分析五味子提取过程中5-HMF 含量变化趋势的原因:由文献[5-6,10]可知,影响5-HMF生成的主要因素有糖、温度和pH,且5-HMF 性质不稳定,可以发生聚合或分解反应。另外笔者经过试验验证发现,5-HMF可随水分蒸发或升华:通过旋蒸五味子三次浓缩液,检测蒸出液,发现其中含有5-HMF,表明5-HMF 会随水分蒸发;通过对五味子提取物的减压升华试验发现升华物中含有少量5-HMF,表明5-HMF 可以升华。五味子在煎煮和浓缩过程中5-HMF的含量增加是因为煎煮和浓缩时温度较高,且五味子中含有较多的有机酸[12],pH 为酸性,利于5-HMF 的生成,此时5-HMF 的生成量远大于随水分蒸发、升华等的去除量。醇沉时5-HMF 含量降低是因为此时温度较低,不利于产生5-HMF,而部分5-HMF此时会被包埋在沉淀物中而除去。加碱调节pH为中性时,5-HMF的含量变化不大,这是因为调碱的中性环境不具备糖类产生5-HMF的条件,且在此过程中不存在5-HMF 因蒸发、升华等被除去的现象。减压干燥后的提取物中5-HMF 的含量明显降低,是由于减压干燥的过程中pH 为中性,5-HMF 的生成较少,而温度较高,5-HMF随水分蒸发、升华等去除较多。
减压干燥所用样品为3批五味子三次浓缩液的合并液,合并后搅拌均匀,每次用完后冷冻保存,下次试验时,放至室温融化,分装于西林瓶中进行相应试验;冷冻干燥所用样品为减压干燥所用五味子三次浓缩液的稀释液。所有样品均来源于同一批五味子的三次浓缩液,避免了不同样品引起的干扰。
五味子三次浓缩液减压干燥时5-HMF的含量随温度的升高和干燥时间的延长而降低,这可能是由于干燥过程中pH为中性,不利于产生5-HMF,而5-HMF 会因随水分蒸发、升华等除去,温度的升高和干燥时间的延长利于5-HMF 发生这些反应。冷冻干燥对5-HMF 含量的降低效果不如减压干燥,可能是因为冻干时温度较低,不利于5-HMF的去除。
减压干燥时由于不同温度及不同时间点的样品含水量不同,为了准确比较其中5-HMF 的含量,应先测定样品的水分,最后折合成干质量进行分析比较。每个取样点取3 份样品平行测定,5-HMF 含量的RSD 均在2.0%以内,表明结果重复性好,具有代表性。
上述试验结果提示,可以适当采用较高的温度减压干燥五味子三次浓缩液,从而得到5-HMF 含量更低的五味子提取物,进而提高五味子提取物的质量。本次试验中70 ℃减压干燥五味子三次浓缩液时5-HMF含量最低,但是考虑到70 ℃温度过高会导致提取物产生糊味,所以笔者认为65 Ⅹ减压干燥效果最好。
[1]国家药典委员会.中华人民共和国药典:一部[S].2010年版.北京:中国医药科技出版社,2010:61-62.
[2]程振玉,杨英杰.五味子木脂素提取工艺研究新进展[J].吉林化工学院学报,2013,30(1):18.
[3]薛梅,周静.五味子多糖的提取及含量测定[J].陕西中医,2003,24(3):267.
[4]王森,张建国.五味子的研究概况及开发前景[J].经济林研究,2003,21(4):126.
[5]Bakhiya N,Monien B,Frank H,et al.Renal organic anion transporters OAT1 and OAT3 mediate the cellular accumulation of 5-sulfooxymethylfurfural,a reactive,nephrotoxic metabolite of the Maillard product 5-hydroxymethylfurfural[J].Biochem Pharmacol,2009,78(4):414.
[6]Fallico B,Arena E,Zappala M.Degradation of 5-hydroxymethylfurfural in honey[J].Journal of Food Science,2008,73(9):625.
[7]张轶,杨丽娟,王倩倩,等.5-羟甲基糠醛与牛血清白蛋白相互作用的光谱特性研究[J].中国药房,2011,22(33):3 095.
[8]何伍,凌霄.含葡萄糖注射液中5-羟甲基糠醛限度的检测方法[J].中国医药工业杂志,2008,39(1):47.
[9]国家药典委员会.中华人民共和国药典:二部[S].2010年版.北京:中国医药科技出版社,2010:928.
[10]傅紫琴,王明艳,蔡宝昌.5-羟甲基糠醛(5-HMF)在中药中的研究现状探讨[J].中华中医药学刊,2008,26(3):508.
[11]刘月新,潘雪,邹茜,等.探讨5-羟甲基糠醛在中药及复方中的存在意义[J].中国现代药物应用,2013,7(15):3.
[12]罗家洪,庄艳.五味子化学成分及生理活性研究进展[J].临床合理用药杂志,2012,5(10):174.
