左旋多巴/盐酸苄丝肼复方药物树脂制备
2015-03-07朱宇涵师双双黄鸿飞刘宏飞
刘 玮,丁 慧,朱宇涵,师双双,黄鸿飞,高 丽,刘宏飞*
·药学研究·
左旋多巴/盐酸苄丝肼复方药物树脂制备
刘 玮1,丁 慧2,朱宇涵2,师双双2,黄鸿飞2,高 丽2,刘宏飞2*
目的 制备左旋多巴/盐酸苄丝肼复方药物树脂并对影响因素进行考察。方法 采用静态法制备药物树脂复合物,对制备过程中的影响因素进行探究。采用高效液相色谱法,分别建立药物和药物树脂的稳定性考察方法。结果 影响因素研究表明,药物树脂的制备受药物浓度、温度和溶剂浓度的影响。色谱图显示,左旋多巴和盐酸苄丝肼在一定条件下出现降解峰,而左旋多巴树脂和盐酸苄丝肼树脂均无降解。结论 药物树脂有一定的缓释效果。采用药物树脂技术后,能明显提高药物的稳定性。
左旋多巴;盐酸苄丝肼;离子交换树脂;稳定性
0 引言
左旋多巴透过血脑屏障进入脑内,经多巴脱羧酶转化成多巴胺,增加大脑纹状体中多巴胺含量,从而成为目前最有效的治疗帕金森病(PD)的药物,被誉为PD药物治疗的“金标准”[1]。但是左旋多巴吸收后,只有1%透过血脑屏障进入脑内。为减少其外周不良反应,可同时配伍服用多巴脱羧酶抑制剂盐酸苄丝肼,可减少外周多巴胺的生成,使左旋多巴较大量地进入脑内,转化为多巴胺而生效。左旋多巴和盐酸苄丝肼都含有2~3个酚羟基,非常不稳定,放置在空气中,易氧化分解,在水溶液中更不稳定,在空气中露光放置,迅速变黄。左旋多巴在碱性范围,尤其当pH>8.5时,几乎瞬时分解。
离子交换树脂分子结构中的解离酸性或碱性基团可以通过离子键与荷正电或荷负电药物结合形成聚合物盐,供口服或其他非注射途径给药,稳定释药速度、提高生物利用度等[2-3],是国内外研究的热点领域,有力地推动了制剂学的发展[4]。
由于左旋多巴和盐酸苄丝肼均可离子化溶解,有望采用离子交换树脂技术研制液体缓释混悬剂。并且如制备成药物树脂混悬液,则由于大部分药物存在于树脂内部,能够明显提高稳定性[5]。本研究制备了左旋多巴/盐酸苄丝肼复方药物树脂,并进行了体外含量测定及溶出实验,为进一步制备液体缓释混悬液进行前期研究。
1 试药与仪器
左旋多巴(随州市红旗化工有限公司);盐酸苄丝肼(随州市红旗化工有限公司);强酸性阳离子交换树脂Amberlite IRP69(德国Rohm & Hass公司美国dow);UV-2401PC紫外可见光分光光度计(上海欣茂仪器有限公司);电子天平(德国 Sartorius);高效液相色谱仪(日本岛津)。
2 实验方法
2.1 药物树脂复合物的制备[6-7]
2.1.1 离子交换树脂的预处理 热水清洗树脂至洗涤水不带褐色为止。再以乙醇或其他溶剂浸泡以除去吸附的少量有机物质。将树脂于水中浸泡0.5 h后,装柱,以1 mol/L HCl冲洗至pH=0,然后用水冲洗至中性,再以1 mol/L NaOH冲洗至pH=14,然后用水洗至中性,再以1 mol/L HCl冲洗至pH=0,然后用水反复洗至中性,干燥备用。

2.2 药物树脂制备的影响因素考察
2.2.1 左旋多巴树脂制备影响因素考察 温度影响:取100 mg树脂加至100 mL浓度为0.5 mg/mL的左旋多巴(溶解在0.001 mol/L HCl溶液)溶液中,分别在25、30、35 ℃下磁力搅拌,以药物浓度对时间作图。药物浓度影响:取100 mg树脂,分别加至100 mL 浓度为0.3、0.5、0.7 mg/mL的左旋多巴(溶解在0.001 mol/L HCl溶液)溶液中,在20 ℃下磁力搅拌,以药物浓度对时间作图。盐酸溶液浓度的影响:取100 mg树脂加至100 mL浓度为0.5 mg/mL的左旋多巴溶液(溶解在0.001、0.005、0.01 mol/L HCl溶液)中,在20 ℃下磁力搅拌,以药物浓度对时间作图。
2.2.2 盐酸苄丝肼树脂制备影响因素考察 药物浓度的影响:取100 mg树脂分别加至100 mL浓度为0.3、0.5、0.7 mg/mL的盐酸苄丝肼溶液中,在15 ℃下磁力搅拌,以药物浓度对时间作图。温度的影响:取100 mg树脂加入100 mL浓度为0.5 mg/mL的盐酸苄丝肼溶液中,在15、20、25 ℃下磁力搅拌。取样100 min,测其吸光度A。以药物浓度对时间作图。
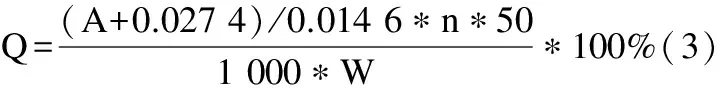
2.4 药物树脂的释放试验 按照释放度测定法(中国药典2010年版二部附录XD第一法),以0.15 mol/L NaCl溶液50 mL为释放介质,转速为50 r/min,温度37 ℃。依法操作,每10 min取样,测其吸光度A,及时补加同温度、同体积的相应介质,以释药百分率对时间作图。
以0.15 mol/L NaCl溶液100 mL为释放介质,转速为50 r/min,温度37 ℃。依法操作,分别于1、2、4、6、8、10、15、20 min取样,测其吸光度A,及时补加同温度、同体积的相应介质,以释药百分率对时间作图。
2.5 药物树脂的稳定性考察
2.5.1 左旋多巴的稳定性试验[11]分别在酸性、碱性、氧化条件下,对左旋多巴原料药和左旋多巴树脂进行稳定性考察。使用C18色谱柱,甲醇-水(2.5∶97.5)为流动相,检测波长280 nm,柱温30 ℃,流速1 mL/min,对左旋多巴进行检查。氧化破坏:取0.1 mg/mL左旋多巴溶液10 mL,加入30% H2O25滴,放置3 h。氧化破坏空白对照:取水10 mL,滴加30% H2O25滴,即得。碱破坏:取左旋多巴2 mg,置量瓶中,加入1 mol/L NaOH至10 mL,放置3 h,加入1 mol/L HCl 10 mL。酸破坏:取左旋多巴2 mg,置量瓶中,加入1 mol/L HCl至10 mL,放置3 h,加入1 mol/L NaOH 10 mL。酸碱破坏空白对照:取1 mol/L HCl 5 mL和1 mol/L NaOH 5 mL摇匀即得。
2.5.2 盐酸苄丝肼的稳定性试验 分别在碱性、光照、高温条件下,对左旋多巴原料药和左旋多巴树脂进行稳定性考察。使用C18色谱柱,以三氟醋酸-甲醇-水(1∶20∶1 000)为流动相,检测波长为220 nm,对盐酸苄丝肼进行检查[12]。碱破坏:取盐酸苄丝肼3 mg,置量瓶中,加入1 mol/L NaOH至10 mL,放置20 h,次日加入1 mol/L HCl 10 mL。光破坏:取0.3 mg/mL盐酸苄丝肼溶液10 mL,置于紫外灯下光照20 h。热破坏:取0.3 mg/mL盐酸苄丝肼溶液10 mL,置于60 ℃水浴锅加热1 h。
3 结果
3.1 药物树脂制备的影响因素
3.1.1 左旋多巴树脂制备影响因素考察 温度影响结果见图1、表1,温度升高,载药量增加,药物利用率增加。
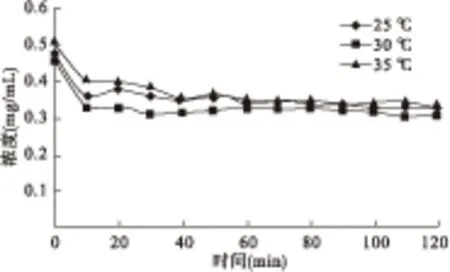
图1 温度对静态离子交换的影响

T(℃)253035Q∞0.15420.15480.1794E(%)3233.535.2
药物浓度影响结果见图2、表2,随着药物浓度增加,载药量略有增加,药物利用率下降。
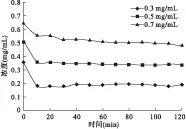
图2 药物浓度对静态离子交换的影响
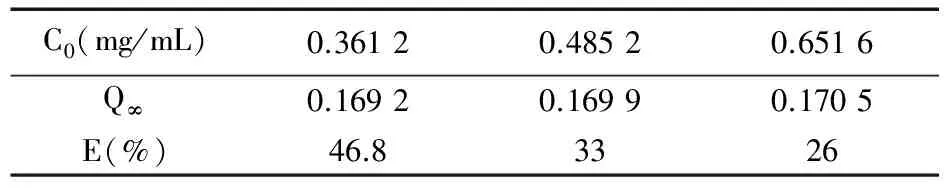
C0(mg/mL)0.36120.48520.6516Q∞0.16920.16990.1705E(%)46.83326
盐酸溶液浓度的影响结果见图3、表3,盐酸溶液浓度增加,载药量增加,药物利用率增加。

图3 盐酸溶液浓度对静态离子交换的影响

盐酸浓度(mol/L)0.0010.0050.01Q∞0.16990.18100.2431E(%)3338.845.7
3.1.2 盐酸苄丝肼树脂制备影响因素考察 药物浓度的影响结果见图4、表4,随着药物浓度增加,载药量增加,药物利用率下降。
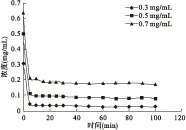
图4 药物浓度对静态离子交换的影响

C0(mg/mL)0.31600.50140.6375Q∞0.29300.42080.4676E(%)92.7283.9373.35
温度的影响结果见图5、表5,温度升高,载药量减小,药物利用率减小。
3.2 药物树脂的含量测定 计算得左旋多巴药物树脂Q=17.45%,盐酸苄丝肼药物树脂Q=13.763%,则左旋多巴药物树脂含量为17.45 mg(左旋多巴)/100 mg(药物树脂)。盐酸苄丝肼药物树脂含量为13.763 mg(盐酸苄丝肼)/100 mg(药物树脂)。
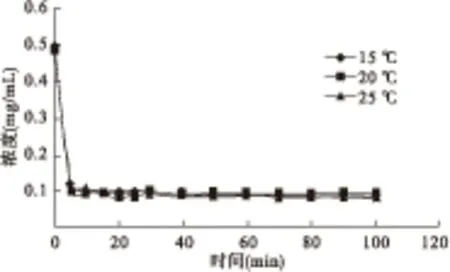
图5 温度对静态离子交换的影响
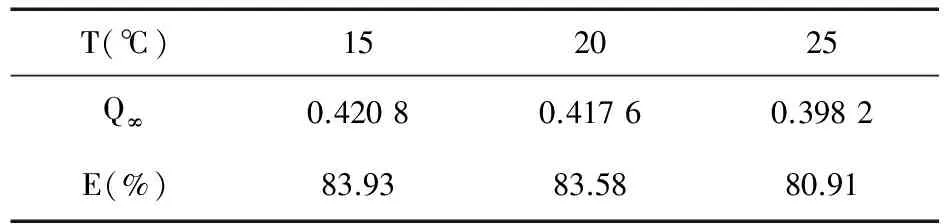
T(℃)152025Q∞0.42080.41760.3982E(%)83.9383.5880.91
3.3 药物树脂的释放试验 药物树脂有一定缓释效果,但其释药较快,不能达到理想的缓释效果。还需要在树脂外用合适的阻滞材料包衣以获得更好的缓释效果。见图6、图7。
3.4 药物树脂的稳定性考察
3.4.1 左旋多巴的稳定性试验 见图8。由左旋多巴原料药和左旋多巴树脂的色谱图看出,左旋多巴在酸性、碱性、氧化条件下均有降解峰,而左旋多巴树脂无降解峰。故左旋多巴树脂比左旋多巴原料药稳定。
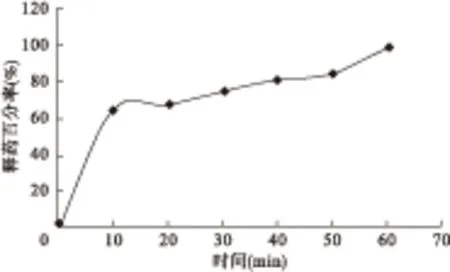
图6 左旋多巴树脂释药曲线

图7 盐酸苄丝肼树脂释药曲线

图8 左旋多巴溶液色谱图
3.4.2 盐酸苄丝肼的稳定性试验 见图9。由盐酸苄丝肼原料药和盐酸苄丝肼树脂的色谱图看出,盐酸苄丝肼在碱性、光照、高温条件下均有降解峰,而盐酸苄丝肼树脂均无降解峰。故盐酸苄丝肼树脂比盐酸苄丝肼原料药稳定。
以上结果表明,采用药物树脂技术后,能明显提高药物的稳定性,从而为制备药物树脂缓释混悬液奠定了良好的基础。分析原因:形成药物树脂复合物后,大部分药物存在于药物树脂内部,与外界形成了隔离,从而保护药物免受外界降解。
4 讨论
对静态离子交换而言,制备的最佳工艺应具备载药量高、药物利用率高的特点。由药物树脂制备影响因素结果中可以看出,药物溶液浓度、反应温度和采用的盐酸溶液浓度均对制备有明显的影响。对于左旋多巴,随着药物浓度增加,载药量增加,药物利用率下降。但由结果可知当浓度从0.3 mg/mL增至0.7 mg/mL时,载药量只有轻微上升,但药物利用率下降较大,表明0.3 mg/mL时,已近似达到饱和载药量,故应选择适中浓度的药物溶液进行制备。温度升高,载药量增加,药物利用率增加,所以应采用较高温度;盐酸溶液浓度增加,载药量增加,药物利用率增加,所以应采用较高浓度的盐酸溶液,但不能过高,以防氢离子与药物竞争进入树脂。
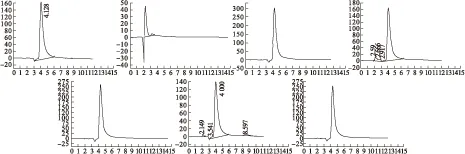
图9 盐酸苄丝肼溶液色谱图
对于盐酸苄丝肼,随着药物浓度增加,载药量增加,药物利用率下降。综合考虑载药量和药物利用率,应选择适中浓度的药物溶液进行制备。温度升高,载药量减小,药物利用率减小。故应尽可能选择较低温度。
左旋多巴和盐酸苄丝肼药物树脂体外释放度考察结果显示,药物树脂释药较快,这表明单纯依靠药物树脂不能获得足够的缓释效果,如需制备缓释混悬剂,则需要进一步的包衣操作。
由盐酸苄丝肼原料药和盐酸苄丝肼树脂的色谱图看出,盐酸苄丝肼在碱性、光照、高温条件下均有降解峰,而盐酸苄丝肼树脂均无降解峰。故盐酸苄丝肼树脂比盐酸苄丝肼原料药稳定。以上结果表明,采用药物树脂技术后,能明显提高药物的稳定性,从而为制备药物树脂缓释混悬液奠定了良好的基础。分析原因:形成药物树脂复合物后,大部分药物存在于药物树脂内部,与外界形成了隔离,从而保护药物免受外界降解。
[1] 董宝平.左旋多巴与帕金森氏病[J].化学教育杂志,2004,25(6):8-10.
[2] 李文秀,马英丽.离子交换树脂在药物制剂中的应用[J].中国新技术新产品,2010,13:19.
[3] Kikuchi S,Takayama K.Multivariate statistical approach to optimizing sustained-release tablet formulations containing diltiazem hydrochloride as a model highly water-soluble drug[J].Int J Pharm,2010,386(1):149-155.
[4] 李伟男,南洋,杨德强,等.离子交换树脂在中药制剂中的应用[J].中医药学报,2011,39(3):101-102.
[5] Lee JH,Choi G,Oh YJ,et al.A nanohybrid system for taste masking of sildenafil[J].Int J Nanomedicine,2012,7:1635-1649.
[6] Jeong SH,Park K.Drug loading and release properties of ion-exchange resin complexes as a drug delivery matrix[J].Int J Pharm,2008,361(1):26-32.
[7] Xie YP,Jing KJ,Lu YH.Kinetics,equilibrium and thermodynamic studies of l-tryptophan adsorptionusing a cation exchange resin[J].Chemical Engineering Journal,2011,171(3):1227-1233.
[8] Kim JI,Cho SM,Cui JH,et al.In vitro and in vivo correlation of disintegration and bitter tastemasking using orally disintegrating tablet containing ion exchange resin-drug complex[J].Int J Pharm,2013,455(1):31-39.
[9] Hu Q,Meng Y.Kinetics and equilibrium adsorption studies of dimethylamine (DMA) onto ion-exchange resin[J].J Hazard Mater,2011,185(2):677-681.
[10]Liu HF,Pan WS,Ke P,et al.Preparation and evaluation of a novel gastric mucoadhesive sustained-release acyclovir microsphere[J].Drug Dev Ind Pharm,2010,36(9):1098-1105.
[11]赵雷.高效液相色谱法测定左旋多巴片的有关物质[J].中国当代医药,2011,18(2):43-44.
[12]熊婧,袁猛.盐酸苄丝肼有关物质检查方法改进及杂质鉴定[J].药物分析杂志,2014,34(11):2035-2040.
Preparation of levodopa/benserazide hydrochloride compound drug resins
LIU Wei1,DING Hui2,ZHU Yu-han2,SHI Shuang-shuang2,HUANG Hong-fei2,GAO Li2,LIU Hong-fei2*
(1.Department of Pharmacy,Affiliated Hospital of Jiangsu University,Jiangsu 212001,China;2.Department of Pharmacy,Jiangsu University,Jiangsu 212013,China)
Objective To prepare the levodopa (L-dopa)/benserazide hydrochloride compound drug resins and to investigate the influence factors (temperature,drug concentration,particle size,efflux speed).Methods The drug resins were made by bath method and affecting factors during the process of preparation were studied.Studies on the stabilities of drugs and drug resins were carried out by HPLC.Results The preparation of drug resins was influenced by particle size of resins,drug concentration,reaction temperature and solvent concentration.In certain conditions,the degradation peaks were found in the chromatograms of L-dopa and benserazide hydrochloride,and the drug resins were not degraded.Conclusion The drug resin technology can greatly improve the stability of the drug and the drug resin has certain sustained-release effects.
L-dopa;Benserazide hydrochloride;Ion exchange resin;Stability
2015-03-24
1.江苏大学附属医院药剂科,江苏 212001;2.江苏大学药学院,江苏 212013
2015年江苏省大学生实践创新训练计划
10.14053/j.cnki.ppcr.201511020
*通信作者
