毛冬青胶囊对大鼠体内细胞色素P450代谢活性的影响*
2015-03-06赵文珠居文政臧雨馨孙冰婷谈恒山蒋志涛
赵文珠,居文政,2**,臧雨馨,孙冰婷,谈恒山,蒋志涛
1南京中医药大学药学院,南京 210029;2南京中医药大学附属医院临床药理科,南京 210029;3南京军区总医院,南京 210002;4张家港市中医医院,张家港 215600
毛冬青胶囊对大鼠体内细胞色素P450代谢活性的影响*
赵文珠1,居文政1,2**,臧雨馨1,孙冰婷1,谈恒山3,蒋志涛4
1南京中医药大学药学院,南京 210029;2南京中医药大学附属医院临床药理科,南京 210029;3南京军区总医院,南京 210002;4张家港市中医医院,张家港 215600
目的:采用Cocktail探针药物法研究毛冬青胶囊对大鼠CYP1A2、CYP3A2、CYP2C6、CYP2D1、CYP2D2和CYP2E1体内代谢活性的影响。方法:分别以茶碱、咪达唑仑、甲苯磺丁脲、奥美拉唑、右美沙芬和氯唑沙宗作为探针底物,将大鼠随机分为3组:空白对照组、毛冬青的低剂量组和高剂量组。低、高剂量组每日分别灌胃给予毛冬青胶囊1.8、3.6 g·kg-1,空白对照组每日给予与低剂量组等体积的生理盐水,各组均为1次/天,连续14 d。各组分别于第15天给予Cocktail探针药物,于给药前、后不同时间点取血,用LC-MS/MS检测各探针药物的血药浓度,计算药代动力学参数。结果:茶碱低剂量组cmax、AUC0-t有极显著差异(P≤0.01);甲苯磺丁脲高剂量组和氯唑沙宗低剂量组AUC0-t有显著差异(P≤0.05);其他无统计学差异。结论:毛冬青胶囊对大鼠体内CYP2C6和CYP1A2有强诱导作用,对CYP2E1有中强诱导作用,其他亚型基本无影响。
Cocktail探针法;CYP1A2;CYP3A2;CYP2C6;CYP2D1;CYP2D2;CYP2E1;毛冬青胶囊
毛冬青为冬青科(Aquifoliaceae)冬青属植物毛冬青(Ilex pubescens Hook.et Arn.)的干燥根,主产于我国广东、广西、福建、江西等地,性寒,味苦、涩,入心、肝经,富含黄酮、香豆素及三萜皂苷等多种化学成分。毛冬青具有清热解毒、活血通络功效,临床用于冠心病、心绞痛及脉管炎等疾病的治疗[1]。临床上毛冬青胶囊与其他药物联合使用时,容易产生药物相互作用,据统计,药物相互作用约40%是由药物代谢引起[2]。药物对代谢酶的诱导或抑制,影响药物代谢过程,其中细胞色素P450氧化酶系(cy-tochromap450s,CYP)起主导作用。本实验选择茶碱、甲苯磺丁脲、奥美拉唑、右美沙芬、氯唑沙宗和咪达唑仑作为 CYP1A2、CYP2C6、CYP2C11、CYP2D2、CYP2E1和CYP3A2的特异性探针药物,同时测定毛冬青胶囊对CYP450酶6种主要亚型酶活性的影响。
1 材料
1.1 药品与试剂
毛冬青胶囊(规格0.45 g/粒,批号130804,广东和平药业有限公司生产);咪达唑仑注射液(规格10 mg/mL/支,批号20130922,江苏恩华药业股份有限公司生产);奥美拉唑肠溶胶囊(规格20 mg/粒,批号060120932,石药集团欧意药业有限公司生产);咪达唑仑对照品(批号171250-200401)、奥美拉唑对照品(批号100367-201104)、吡罗昔康对照品(批号100177-200603)、替硝唑对照品 (批号100336-200402),均为中国药品生物制品检定所提供;甲苯磺丁脲、氯唑沙宗、茶碱、右美沙芬对照品(批号依次为:017K1025、017K1385、T1633、097K11348),均购自美国Sigma公司;肝素钠注射液(规格1.25万U/2 mL/支,批号110818,常州千红生化制药股份有限公司)。实验用水为超纯水;除甲醇、乙腈为色谱纯,其余均为分析纯。
1.2 仪器
液质联用仪Waters Quattro Micro;色谱工作站Masslynx 4.0;电子天平Sartorius CPA225D;微型旋涡混合仪WH-2;Micro-17R型冷冻离心机;Drict-Q5型超纯水机;KQ3200型超声波清洗器。
1.3 动物
大鼠24只,雌雄各半,体重(250±20)g,由江苏省中医院药理实验室提供,合格证号为scxk-(苏)2014-0001。
2 方 法
2.1 溶液配制及动物给药方法
2.1.1 毛冬青溶液的配制 称取毛冬青胶囊内容物11.25 g,研磨均匀,50 mL生理盐水边加边研,直至全部溶解,即得浓度为0.225g·mL-1的毛冬青溶液。
2.1.2 动物给药方法 24只大鼠随机分为3组:空白对照组、实验低剂量组和实验高剂量组,每组8只。低、高剂量组每日分别灌胃给予毛冬青溶液2 mL、4 mL。空白对照组每日给予与实验组等体积的生理盐水。各组均为每日一次,连续14 d。第15天各组大鼠均灌胃给予Cocktail探针药物溶液 (茶碱33.8 mg·kg-1、甲苯磺丁脲24.6 mg·kg-1、奥美拉唑43 mg·kg-1、右美沙芬33.8 mg·kg-1、氯唑沙宗33.8 mg· kg-1、咪达唑仑19.2 mg·kg-1)。分别于给药前及给药后 5、10、20、40 min和 1、1.5、2、2.5、3、5、8、12、24 h眼眶取血0.3 mL至肝素化离心管中,3000 r·min-1离心10 min,分离血浆,于-20℃冰箱冷冻待测。
2.2 色谱条件
色谱柱:Agilent Zorbax SB-C18(2.1 mm×150 mm,5 μm);保护柱:Agilent Eclipase XDB2-C8(2.1 mm× 12.5 mm,5 μm);流动相:乙腈-(0.1%甲酸-4 mmol· L-1甲酸铵)=75∶25;流速:0.2 mL·min-1;进样量:5 μL。
2.3 质谱条件
离子化方式:电喷雾(ESI),正负离子同时检测,多反应监测。检测电压:3.5 kV,离子源温度:120℃,脱溶剂温度:350℃,脱溶剂气体流速:450 L·h-1。各分析物的检测离子、质核比、锥孔电压、碰撞能量见表1。
2.4 混合标准溶液及质控溶液的配制
2.4.1 混合标准溶液的配制 精密称取茶碱、咪达唑仑、甲苯磺丁脲、奥美拉唑、右美沙芬、氯唑沙宗各对照品适量,乙腈溶解并定容,即得各对照品储备液,浓度分别为:1.113、1.00、1.172、1.407、1.151、1.171 mg·mL-1。另精密吸取各对照品储备液适量,用75%的乙腈配制混合标准溶液,并倍比稀释为7个不同浓度的混合标准溶液,于4℃冰箱冷藏备用。
2.4.2 质控溶液的配制 精密吸取各对照品储备液适量,用75%的乙腈依次配制高、中、低3种不同质量浓度的质控溶液,于4℃冰箱冷藏备用。
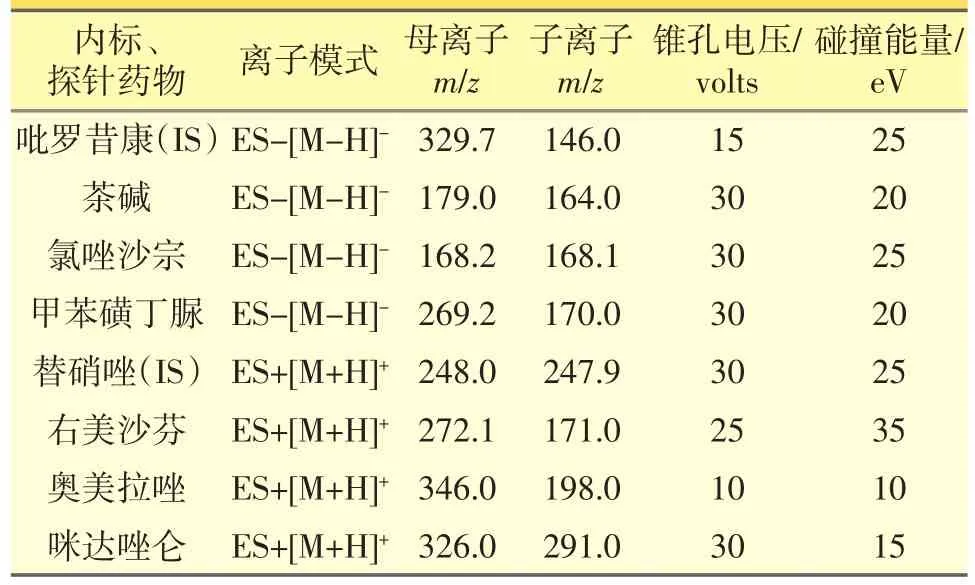
表1 内标和探针药物的质谱参数
2.4.3 内标溶液的配制 精密称取替硝唑、吡罗昔康各对照品适量,分别置于10 mL量瓶中,用甲醇定容至刻度,摇匀即得各对照品储备液。另精密吸取各对照品储备液适量于同一10 mL量瓶中,以75%的乙腈定容至刻度,摇匀,即得替硝唑和吡罗昔康混合内标溶液,浓度分别为10.21、26.79 μg·mL-1,于4℃冰箱冷藏备用。
2.5 血浆样品处理方法
精密吸取含药血浆样品50 μL,依次加入内标工作液 (替硝唑10.21 μg·mL-1和吡罗昔康26.79 μg·mL-1)10 μL、75%的乙腈10 μL,涡旋30 s,再加入乙酸乙酯400 μL,涡旋3 min,12000 r·min-1离心10 min。吸取上清液350 μL,氮气流吹干(40℃)。50 μL 75%的乙腈复溶,12000 r·min-1离心5 min,吸取上清液5 μL,进样分析。
2.6 标准曲线的制作
精密吸取空白血浆50 μL,依次加入不同浓度标准混合工作液10 μL、内标工作液(替硝唑10.21 μg· mL-1和吡罗昔康26.79 μg·mL-1)10 μL,涡旋30 s,再加入乙酸乙酯400 μL,涡旋3 min,12000 r·min-1离心10min。吸取上清液350μL,氮气流吹干(40℃)。以 75%的乙腈 50 μL复溶,12000 r·min-1离心 5 min,吸取上清液,进样分析。
2.7 数据处理
药动学参数采用DAS 1.0软件计算,用SPSS 11.5统计给药前后各探针药动学参数的差异,采用单因素方差分析。P<0.05表示差异有统计学意义。
3 结 果
3.1 色谱行为
在上述色谱条件下,替硝唑、吡罗昔康、咪达唑仑、奥美拉唑、右美沙芬、甲苯磺丁脲、氯唑沙宗及茶碱的保留时间依次为:2.07、2.62、3.28、2.27、3.01、2.49、2.36、1.99 min。结果表明,各分析物间分离良好,且无血中内源性杂质干扰,基线平稳(见图1)。该测定方法特异性好,能准确测定血浆中6个探针药物的浓度,且重现性好。
3.2 标准曲线制备
取空白血浆50 μL,加混合标准溶液10 μL、混合内标10 μL,按照大鼠空白“血浆样品处理方法”操作,分别计算各成分的峰面积与相应内标的峰面积的比值为Y,以比值Y对探针药物的浓度C作线性回归,得回归方程,见表2。

表2 6种探针药物回归方程与线性关系
3.3 精密度及准确度
取空白血浆50 μL,分别加入高、中、低三个浓度质控标准液10 μL,每个浓度平行5份,按“血浆样品处理方法”操作,进样分析,根据随行标准曲线计算各分析物浓度,日内重复测定5次,日间平行测定3天。结果(见表3)日内、日间精密度均小于10%,准确度在86%~100%。

表3 6种探针的精密度与准确度
3.4 提取回收率[3]
取大鼠空白血浆50 μL,配制高、中、低3个不同浓度含药血浆质控样品,按“血浆样品处理方法”处理样品,记录分析物峰面积Ax。另以流动相配制相同进样浓度的含药溶液,记录分析物峰面积As,提取回收率R(%)=Ax/As×100%×(8/7)。结果表明:咪达唑仑、奥美拉唑、右美沙芬、甲苯磺丁脲、氯唑沙宗、茶碱、替硝唑和吡罗昔康的提取回收率依次为 79.91%~87.13%、80.46%~90.88%、84.72%~96.54%、76.59%~97.68%、87.47%~93.87%、90.82%~97.09%、78.61%、74.79%。
3.5 基质效应[4]
取大鼠空白血浆,加乙酸乙酯,涡旋,离心,获得空白血浆洗脱液若干。分别精密吸取高、中、低质控工作液各10 μL,向其中分别依次加入内标工作液10 μL、空白血浆洗脱液30 μL,涡旋混匀,进样分析。每个浓度平行3个样本。记录各探针药物同一浓度的和所有浓度内标药物的
分别精密吸取高、中、低质控工作液各10 μL,向其中分别依次加入内标工作液10 μL、乙腈30μL,涡旋混匀,进样分析。每个浓度平行3个样本。记录各探针药物同一浓度的和所有浓度内标药物的

结果表明:咪达唑仑、奥美拉唑、右美沙芬、甲苯磺丁脲、氯唑沙宗、茶碱、替硝唑和吡罗昔康的介质效应分别为88.14%~89.77%、88.60%~91.09%、87.65%~89.96%、88.40%~89.92%、88.87%~90.16%、88.20%~91.33%、90.52%、90.31%。
3.6 稳定性试验
考察6种探针药物的标准品及含药血浆在不同条件下保存的稳定性。标准品在4℃冰箱保存2个月以上仍稳定,含药血浆置于-20℃冰箱冷冻保存一个月及反复冻融3次均稳定,血浆样品室温避光保存24 h稳定。
3.7 药动学参数
3.7.1 6种探针药物的药-时曲线图 大鼠连续给予不同剂量毛冬青胶囊14天后灌胃Cocktail探针药物与空白对照组直接灌胃Cocktail探针药物,按血浆样品处理方法操作,得6种探针药物的药-时曲线图,见图2。
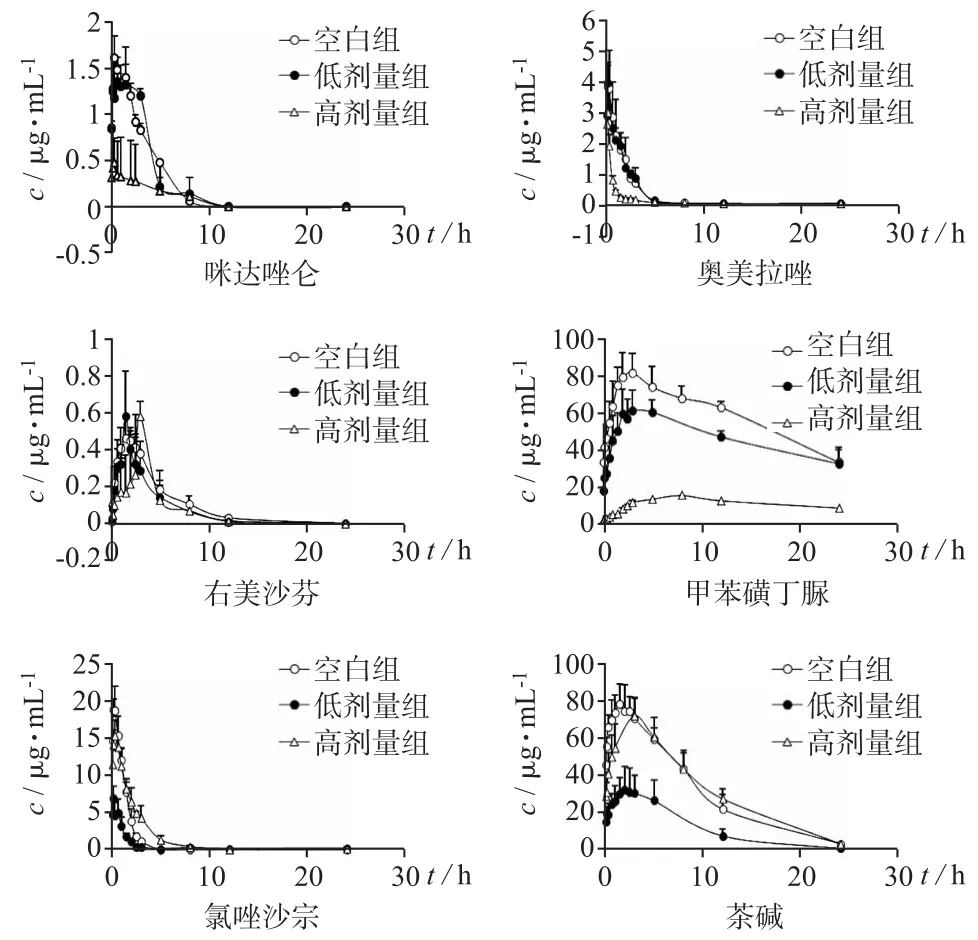
图2 6种探针药物的药-时曲线图
3.7.2 各组大鼠的药动学数据 采用DAS 1.0软件处理各组大鼠药动学数据,结果如下:奥美拉唑和右美沙芬符合一室模型(W=1),茶碱、氯唑沙宗、甲苯磺丁脲符合一室模型(W=1/CC),咪达唑仑符合二室模型 (W=1)。6种探针药物的最大血药浓度(cmax)、药时曲线下面积(AUC)、半衰期(t1/2)、表观分布容积(Vd/F)、总清除率(CL/F)、达峰时间(tmax)等参数,见表4。
由表4可知,咪达唑仑:高剂量组与空白组间t1/2存在显著差异(P≤0.05);甲苯磺丁脲:高剂量和空白组对比,cmax(P≤0.01)和AUC(P≤0.05)存在显著差异,低、高剂量组对比,cmax存在显著差异 (P≤0.05);氯唑沙宗:低、高剂量组间AUC存在显著差异(P≤0.05);茶碱:低剂量组与空白、高剂量组间AUC及cmax均存在显著差异(P≤0.01)。
4 讨 论
细胞色素P450酶系是一组由结构和功能相关的超家族基因编码的含铁血红素同工酶,CYP1A2、CYP2C9、CYP2C19、CYP2D6、CYP2E1和 CYP3A4是其主要亚型,参与体内大多数药物代谢[5]。大鼠的2C6[6-7]、2D1[7]、2D2[7]、3A2[6,8]分别对应人的 2C9[9]、2C19、2D6、3A4[7,10-11]。应用Cocktail法首先需排除联合使用探针底物间是否存在体内的代谢性相互作用;其次必须确保每种探针底物选择性地作用于某一种酶[12-13]。本实验采用空白对照的方法,排除了眼眶取血刺激对试验大鼠代谢可能造成的影响。并参考文献[11,14],排除了实验所选6种探针底物潜在的体内代谢性相互作用,实验设计基本符合Cocktail法的条件。
实验初期分别考察了甲醇、乙腈、甲酸、甲酸铵和乙酸铵在不同配比及用量时,对分析物色谱峰的影响,发现75%乙腈和0.1%甲酸-4 mmol·L-1甲酸铵为流动相,比例为75∶25时响应及峰形最佳。
由表4可知,连续给予毛冬青胶囊14天后,甲苯磺丁脲:与空白组对比,低剂量组AUC降低约18%,无统计学差异,高剂量组cmax和AUC依次降低约81%、79%,存在极显著差异(P≤0.01);与低剂量组对比,高剂量组cmax降低约80%,存在显著差异(P≤0.05)。氯唑沙宗:与低剂量组对比,高剂量组AUC升高约2.48倍,存在显著差异 (P≤0.05);空白、高剂量组比较,MRT存在极显著差异 (P≤0.01),其余参数无统计学差异。茶碱:低剂量组与空白组对比,tmax升高约1.29倍,cmax和AUC依次降低约52%、67%,统计学显示cmax和AUC存在极显著差异(P≤0.01);高剂量组与低剂量组对比,cmax升高约88%,AUC升高约3.06倍,存在极显著差异(P≤0.01)。咪达唑仑:与空白组对比,低剂量组t1/2β和tmax升高,AUC降低40%,无统计学差异(P>0.05),高剂量组t1/2β升高,cmax降低67%、AUC降低70%,统计分析结果表明,t1/2β存在显著差异(P≤0.05),其他参数无显著差异(P>0.05),这与咪达唑仑高剂量组的药-时曲线图不符,产生原因可能与雌雄大鼠个体间差异较大有关。另外,有文献报道[15]咪达唑仑个体间变异较大。奥美拉唑:高剂量组对比空白组,AUC降低约74%,无统计学差异。右美沙芬:与空白组对比,低、高剂量组t1/2α、tmax、cmax升高,AUC降低,无统计学差异。
表4 毛冬青胶囊不同给药组,各探针药主要药动力学参数(±s,n=8)

表4 毛冬青胶囊不同给药组,各探针药主要药动力学参数(±s,n=8)
经单因素方差分析,三组间两两对比,与空白组对比结果标记为:*P≤0.05、**P≤0.01;与低剂量组对比结果标记为:△P≤0.05、△△P≤0.01。
探针参数空白组低剂量组高剂量组探针参数空白组低剂量组高剂量组t1/2β/h 1.67±0.63 4.03±1.72 3.76±1.49*t1/2β/h 10.32±5.16 13.52±7.16 9.16±6.99 tmax/h 0.87±0.83 3.3±2.68 0.34±0.32 tmax/h 2.75±0.48 4.14±2.90 2.75±0.29 Vd/F,L·kg-115.85±3.65 14.95±10.53 175.36±165.58 Vd/F,L·kg-10.31±0.16 0.17±0.04 0.79±0.20咪达唑仑CL/F,L·h-1·kg-119.87±3.59 19.13±15.65 18.41±17.19 CL/F,L·h-1·kg-10.03±0.01 0.03±0.01 0.06±0.02 cmax,mg·L-12.10±1.67 1.82±1.58 0.69±0.54 cmax,mg·L-187.46±35.30 79.76±20.08 16.30±1.04**△AUC0-t,mg·L-1·h 9.64±8.30 5.78±5.32 2.87±2.11 AUC0-t,mg·L-1·h 1321.98±679.90 1086.15±462.50 283.69±0.72*甲苯磺丁脲AUC0-∞,mg·L-1·h 9.66±8.30 5.81±5.31 2.88±2.11 AUC0-∞,mg·L-1·h 2426.82±1940.72 1835.88±1164.95 399.58±0.69*MRT0-t/h 2.02±0.70 3.43±1.86 3.76±1.20**△MRT0-t/h 9.80±0.90 9.11±2.25 5.9±2.9**△MRT0-∞/h 2.15±0.60 3.61±2.06 4.09±1.20**△MRT0-∞/h 23.75±14.70 22.35±14.25 9.02±2.18**△t1/2β/h 0.99±0.65 1.01±0.74 0.34±0.20 t1/2β/h 0.69±0.20 0.71±0.40 1.55±0.55 tmax/h 0.25±0.09 0.20±0.19 0.14±0.04 tmax/h 0.25±0.09 0.23±0.20 0.30±0.17 Vd/F,L·kg-18.61±0.04 9.27±0.07 14.69±1.19 Vd/F,L·kg-11.49±0.07 76.86±5.70 2.21±0.11奥美拉唑CL/F,L·h-1·kg-16.03±0.04 6.36±0.07 29.95±4.13 CL/F,L·h-1·kg-11.5±0.23 75.02±9.87 0.99±0.14 cmax,mg·L-14.62±2.29 4.33±2.47 3.32±1.32 cmax,mg·L-119.83±12.43 7.06±5.73 8.86±1.48 AUC0-t,mg·L-1·h 8.42±5.44 9.52±4.34 2.14±1.50氯唑沙宗AUC0-t,mg·L-1·h 22.35±17.70 5.36±4.53 18.67±6.36△AUC0-∞,mg·L-1·h 8.45±5.44 9.53±4.34 2.17±1.49 AUC0-∞,mg·L-1·h 22.36±17.70 5.36±4.53 19.66±6.89△MRT0-t/h 1.45±0.48 2.53±1.60 1.91±0.52 MRT0-t/h 1.33±0.53 2.79±1.41 3.09±0.84**MRT0-∞/h 1.51±0.53 2.57±1.61 2.87±1.98 MRT0-∞/h 2.67±2.64 3.41±1.74 4.53±2.59**t1/2β/h 2.36±1.99 5.33±2.76 4.68±2.06 t1/2β/h 3.20±2.03 3.06±1.23 3.50±2.37 tmax/h 1.71±0.67 2.79±1.92 2.36±0.87 tmax/h 1.40±0.88 3.21±2.46 3.31±1.16 Vd/F,L·kg-11.63±0.48 0.50±0.11 0.73±0.23 Vd/F,L·kg-10.75±0.44 0.88±0.02 0.99±0.0007右美沙芬CL/F,L·h-1·kg-113.97±4.21 16.29±5.33 16.49±5.04 CL/F,L·h-1·kg-10.17±0.03 0.44±0.02 0.17±0.02 cmax,mg·L-10.53±0.47 0.90±1.59 0.92±0.27 cmax,mg·L-125.12±8.30 12.08±4.46**22.67±4.71△△AUC0-t,mg·L-1·h 3.96±3.43 2.29±1.83 2.51±2.07茶碱AUC0-t,mg·L-1·h 171.12±87.18 57.26±37.20**232.71±57.72△△AUC0-∞,mg·L-1·h 3.97±3.43 2.30±1.83 2.51±2.06 AUC0-∞,mg·L-1·h 178.57±101.41 60.39±36.14**242.24±66.34△△MRT0-t/h 3.24±1.20 4.38±3.56 5.10±0.44 MRT0-t/h 6.22±0.89 5.52±1.16 7.02±0.99△△MRT0-∞/h 3.33±1.15 4.43±3.62 5.70±2.03 MRT0-∞/h 6.77±1.70 6.55±1.17 7.95±2.23△△
综上分析,毛冬青胶囊连续给予14 d后,甲苯磺丁脲和氯唑沙宗在大鼠体内浓度降低,代谢迅速,实验结果表明,毛冬青胶囊对CYP2C6有强诱导作用,对CYP2E1有中强诱导作用,毛冬青中剂量时对CYP1A2有强诱导作用,而高剂量时对CYP1A2有弱抑制作用。奥美拉唑和右美沙芬的代谢变化不明显,表明对CYP2D1和CYP2D2基本没有影响。咪达唑仑的代谢变化由于统计学结果与DAS1.0分析结果存在差异,需进一步实验验证。此外,和凡等[4]考察了复方毛冬青颗粒(成分毛冬青、大青叶和南板蓝根)对CYP450酶的诱导作用,实验结果表明,该药对CYP1A2和CYP2E1具有诱导作用,且呈剂量依赖性。与本实验对比,相同之处:毛冬青对CYP1A2和CYP2E1酶具有诱导作用;不同之处:本实验毛冬青对CYP1A2和CYP2E1酶的作用不呈剂量依赖性,同时发现毛冬青对CYP2C6也具有诱导作用。由于两个实验一个体内,一个体外,且选用的探针底物及动物性别不完全相同,所以结果可能会有差异。
根据本实验结果,提示临床联合用药中,毛冬青胶囊与CYP2C6、CYP1A2和CYP2E1酶的底物药物合用时需调整剂量,避免产生毒副作用或药效降低。由于人与大鼠存在种族差异,所以在临床用药时还需进一步临床验证。
[1]冯 锋,朱明晓,谢 宁.毛冬青化学成分研究[J].中国药学杂志,2008,43(10):732-6.
[2]Kennedy DA,Seely D.Clinically based evidence of drug-herb interactions:a systematic 215 review[J].Ex-pert Opin Drug Saf,2010,9(1):79-124.
[3]CFDA化学药物临床药代动力学研究技术指导原则[S]. 2005.
[4]韩南银,徐秉玖.生物样品分析中基质效应和准确度的确定[J].中国新药杂志,2012,21(14):1607-10.
[5]Michielan L,Terfloth L,Gasteiger J,et al.Comparison of multilabel and single-label classification applied 220 to the prediction ofthe isoform specificity ofcy-tochrome P450 substrates[J].J Chem Inf Model,2009, 49(11):2588-605.
[6]陈 烨,袁 瑾,王新宏,等.葛根芩连汤及不同配伍对肝细胞色素P450酶的影响[J].中成药,2013,35(8):2593-8.
[7]Orianne V,Sylvain P,Sylvie T,et al.Can a cocktail designed for phenotyping pharmacokinetics and metabolism enzymes in human be used efficiently in rat[J].Xenobiotica,2012,42(4):349-54.
[8]Han YL,Li D,Ren B,et al.Evaluation of impact of Herba Erigerontis injection,a Chinese herbal prescription, on rat hepatic cytochrome P450 enzymes by cocktail probe drugs[J].J Ethnopharmacol,2012,139(1):104-9.
[9]Vec姚er姚a R,Zachar姚ová A,Orolin J,et al.Fenofibrate-in-duced decrease of expression of CYP2C11 and CYP2C6 in rat[J].Biopharm Drug Dispos,2011,32(8):482-7.
[10]和 凡,杨 彤,谢庆君,等.复方毛冬青颗粒对大鼠肝微粒体细胞色素P450酶的诱导作用研究 [J].临床合理用药,2012,5(1C):13-4.
[11]程小桂,居文政,戴国梁,等.Cocktail探针药物法评价威麦宁胶囊对大鼠体内CYP450活性的影响 [J].中国新药与药物临床,2014,33(8):593-8.
[12]Zhu B,Ou-Yang DS,Chen XP,et al.Assessment of cytochrome P450 activity by a five-drug cocktail ap-proach[J].Clin Pharmacol Ther,2001,70(5):455-61.
[13]Brockm觟ller J,Roots I.Assensement of liver metabolic function:clinical implications[J].Clin Pharmacokinet, 1994,27(3):216-48.
[14]王丹,刘萍霞,张振清,等.雷公藤活性成分对大鼠体内 CYP450酶活性的影响 [J].中国药理学通报,2011,27(2):276-80.
[15]Tanaka E,Kurata N,Yasuhara H.How useful is the"cock-tail approach"for evaluating human hepatic drug metabo-lizing capacity using cytochrome P450 phenotyping probes in vivo[J].Clin Pharm Ther,2003,28(3):157-65.
Influence of Maodongqing Capsules on Metabolic Activities of Cytochrome P450 Enzymes in Rats
ZHAO Wen-zhu1,JU Wen-zheng1,2,ZANG Yu-xin1,SUN Bing-ting1,TAN Heng-shan3,JIANG Zhi-tao4
1College of Pharmacy,Nanjing University of Traditional Chinese Medicine,Nanjing 210029;2Department of Clinical Pharmacology,the Affiliated Hospital of Nanjing University of Traditional Chinese Medicine,Nan-jing 210029;3General Hospital of Nanjing Military Command,Nanjing 210002;4Zhangjiagang Hospital of Traditional Chinese Medicine,Zhangjiagang 215600
Objective:To study the influence of Maodongqing Capsules on metabolic activities of CYP1A2,CYP3A2,CYP2C6,CYP2D1,CYP2D2 and CYP2E1 by Cocktail probe drugs in rats.Methods:Theophylline,midazolam,tolbutamide,omeprazole,dextromethorphan and chlorzoxazone were used as the probe drugs of cytochrome P450s.The rats were randomly divided into three groups:control group,low group and high group.Maodongqing capsules were orally given to rats of the low and high groups once a day with the dose of 0.45 g and 0.9 g per rat,respectively.The control group and the low group administered equal volume of saline,each group was once a day,for 14 days.Cocktail probe drugs in each group were given in the 15th day,the plasma samples were taken at different time before and after the probe drugs.The plasma concentrations of probe drugs were determined by LC-MS/MS and their corresponding pharmacokinetic parameters were calculated.Results:The cmaxand AUC0-tof theophylline in the low group were significantly different (P≤0.01);the AUC0-tof tolbutamide in the high group was significantly different (P≤0.01);the AUC0-tof chlorzoxazone in the low group was significantly different (P≤0.05);while no other significantly different activities were found.Conclusion:Maodongqing capsules had a significant induction to CYP2C6 and CYP1A2 in rats,a moderate induction to CYP2E1 in rats, while no significant influence on the other subtypes.
Cocktailprobe drugs;CYP1A2;CYP3A2;CYP2C6;CYP2D1;CYP2D2;CYP2E1; Maodongqing capsule
R965
A
1673-7806(2015)03-217-06
江苏省中医药领军人才项目(No.LJ200906);江苏高校优势学科建设工程资助项目2010;中药新药临床评价研究技术平台(南京)建设(No.2012ZX09303009-002)重大新药创新
赵文珠,女,硕士,研究方向:中药学E-mail:zhaowenzhu0604@126.com
**通讯作者居文政,男,主任药师,博士生导师,研究方向:中药临床药物代谢动力学 E-mail:wzhju333@163.com
2014-12-03
2015-03-05
