硫酸亚铁铵的绿色化制备与表征
2015-02-27钟国清吴治先白进伟西南科技大学材料科学与工程学院四川绵阳621010
钟国清, 吴治先, 白进伟(西南科技大学 材料科学与工程学院,四川 绵阳 621010)
硫酸亚铁铵的绿色化制备与表征
钟国清, 吴治先, 白进伟
(西南科技大学 材料科学与工程学院,四川 绵阳 621010)
硫酸亚铁铵制备实验是一个经典的综合性实验。对传统的硫酸亚铁铵制备实验内容进行了绿色化改造,改进后的实验在常规仪器中完成实验教学,一方面减少环境污染,实现实验教学的绿色化;另一方面降低实验消耗,节省实验经费。同时用滴定分析、X射线粉末衍射、红外光谱、热重差热分析等对硫酸亚铁铵产品进行了表征分析。
综合性实验; 硫酸亚铁铵; 制备; 表征; 绿色化学
0 引 言
硫酸亚铁铵的制备是学习化学课程的大学生常做的一个综合性实验,通过该实验可了解复盐的一般特征与制备方法,氧化还原、杂质去除、提高产率和纯度、防止副反应发生及绿色化学教育等有关化学原理的应用,以及综合训练学生称量、水浴加热、蒸发、浓缩、结晶、干燥、倾析、常压过滤、减压过滤、目视比色、滴定分析等一系列化学基本操作[1-5]。由于常规的制备方法存在着污染严重,试剂用量大,产品质量不高,实验时间长和消耗费用高等问题,我们对该实验进行了绿色化改进,取得了良好的教学效果[6]。为进一步了解所制得硫酸亚铁铵的组成与结构,在对硫酸亚铁铵制备实验进行的减量化与绿色化改造基础上,用滴定分析、X射线粉末衍射、红外光谱、热重差热分析等方法对制得的产品进行了表征分析。
1 实验部分
1.1 仪器与试剂
电热恒温水浴、恒温磁力搅拌器、台秤、量筒(10、50 mL)、烧杯(250 mL)、锥形瓶(50、250 mL)、蒸发皿、表面皿、真空泵、漏斗、吸滤瓶、布氏漏斗、移液管(5、10 mL)、比色管(25 mL)、酸式滴定管(25 mL)等。
BS-124S电子天平(感量0.1 mg,北京塞多利斯仪器系统有限公司),Nicolet 5700型傅里叶变换红外光谱仪(KBr压片法,美国Nicolet仪器公司),D/max-Ⅱ型X射线衍射仪(日本理学公司),SDT Q600同步热分析仪(美国TA仪器公司)。
铁屑、10% Na2CO3、2 mol/L H2SO4、2 mol/L HCl、10%磺基水杨酸、95%乙醇、Fe3+标准溶液(含Fe3+0.100 mg/mL)、0.01 mol/L KMnO4标准溶液、硫酸铵(A.R.)、pH试纸、滤纸等。
1.2 实验原理
硫酸亚铁铵是由等摩尔的硫酸亚铁和硫酸铵形成的复盐,为浅绿色单斜晶体,空气中稳定,不易被氧化,溶于水,不溶于乙醇。其制备方法一般是用铁与稀硫酸按照一定摩尔比在适当温度下反应,先制得硫酸亚铁溶液,再按等摩尔比加入硫酸铵,利用复盐的溶解度比组成它的简单盐溶解度小的性质,经适当温度加热浓缩结晶而制得硫酸亚铁铵产品。反应式为:
FeSO4+(NH4)2SO4+6H2O= (NH4)2SO4·FeSO4·6H2O
1.3 实验步骤
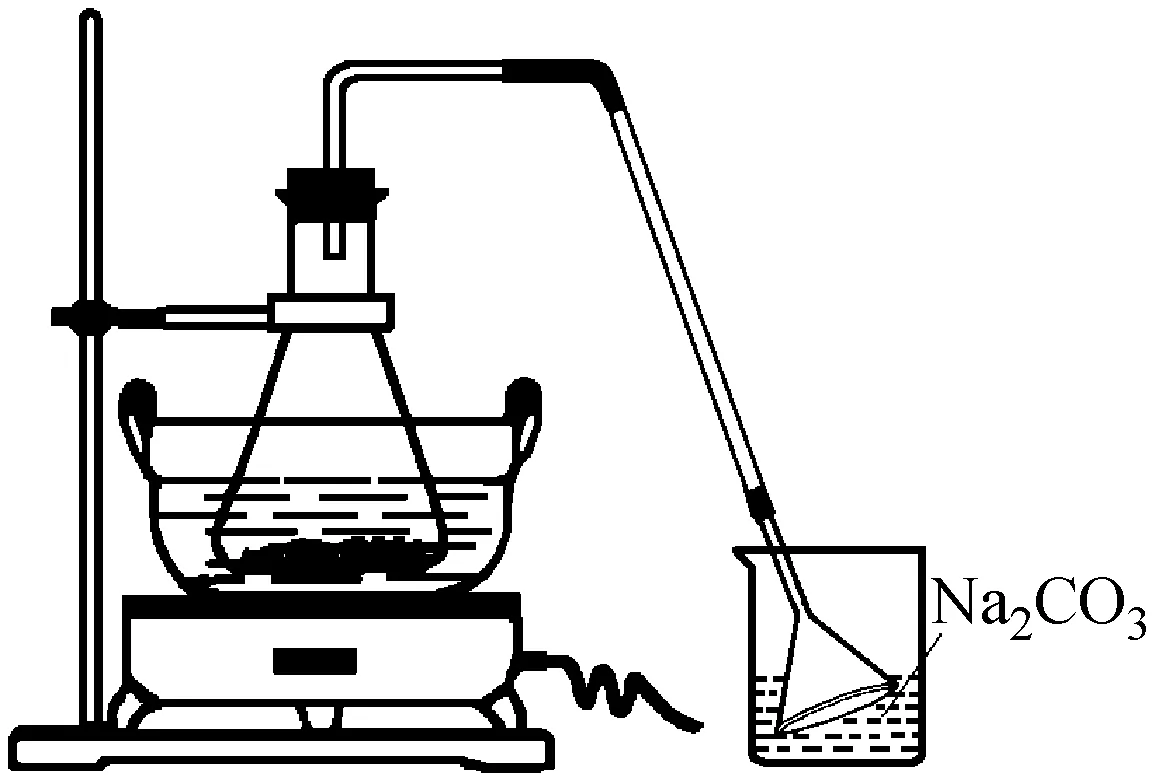
用台秤称取1.0 g铁屑,放入50 mL锥形瓶中,加入10% Na2CO3溶液10 mL。在石棉网上小火加热约10 min,然后倾倒出碳酸钠溶液(用于吸收H2S等有毒气体),用自来水冲洗后,再用蒸馏水将铁屑冲洗洁净。往盛锥形瓶中加入2 mol/L H2SO4溶液11 mL,烧杯中装入废碳酸钠溶液,按图1装好仪器,水浴加热使铁屑与稀硫酸反应至基本不再冒出气泡。趁热过滤,用少量蒸馏水洗涤残渣,滤液承接在干净蒸发皿中。按n[(NH4)2SO4]∶n(Fe)=1∶1称取硫酸铵,并加到硫酸亚铁溶液中。水浴上加热使硫酸铵全部溶解,搅拌下蒸发浓缩至溶液表面刚好出现薄层晶膜为止。取下蒸发皿,静置、冷却、结晶,减压过滤,用少量乙醇洗涤晶体表面的水分。将晶体取出,晾干、称重,计算产率。
硫酸亚铁铵产品中,Fe3+的限量分析和Fe2+含量的测定按照化学试剂六水合硫酸亚铁铵国家标准(GB/T 661—2011)进行。分别测定硫酸亚铁铵产品的XRD、FTIR图谱和TG-DTA曲线,以确定其结构。
2 结果与讨论
2.1 制备反应的绿色化与减量化改造
实验关键步骤是硫酸亚铁的制备,但传统方法采用敞开实验装置,因铁屑含有碳、硫、磷、硅等杂质,与硫酸反应时会生成H2S、PH3等刺鼻、呛人的有毒气体并伴随大量氢气逸出,导致实验室弥漫着强烈的刺激性气味,危害师生的身体健康[7]。硫酸亚铁铵制备实验即便在通风橱中进行,但整个实验室还是能闻到臭味,与绿色化学要求相比,存在着废气有待治理和未达到原料最大限度的合理利用等缺点。选用铁屑为原料,可降低实验成本,实现废物的资源化利用,培养学生的绿色化学理念[8-10]。本实验把铁屑与稀硫酸反应装置封闭起来,反应中产生的H2S、PH3等有毒气体的除油污后的碳酸钠溶液吸收,也可以用氢氧化钠溶液或高锰酸钾的酸性溶液或氢氧化铜溶液吸收[4],在导气管末端连接一个倒扣的漏斗,以便吸收产生的毒气和防止倒吸。实验反应装置是封闭的,反应过程中水分蒸发很少,可不补充蒸馏水,给实验操作带来方便。改进装置后,不在通风橱内进行实验,也闻不到臭味,体现了绿色化学的思想。在保证培养学生基本操作的前提下,采用小剂量实验既可节约药品消耗又可减少对环境的污染。改进后的实验缩短了反应时间,洗涤油污后的碳酸钠溶液用于除去反应中产生的有毒气体,保护了实验环境,实现了化学实验室绿色化[11-12]。
2.2 硫酸亚铁铵的表征
2.2.1 Fe3+的限量分析与Fe2+的测定
取3支25 mL具塞比色管,分别加入Fe3+标准溶液0.50、1.00、2.00 mL,然后加入2 mol/L的HCl溶液2 mL和10%磺基水杨酸溶液2 mL,用不含氧气的蒸馏水稀释至25 mL刻度,摇匀。称取1.0 g硫酸亚铁铵样品于25 mL比色管中,加入2 mol/L的HCl溶液2 mL和10%磺基水杨酸溶液2 mL,用不含氧气的蒸馏水稀释至刻度,进行目视比色,确定产品等级。

表1 硫酸亚铁铵的产率和纯度 %
准确称取0.3~0.4 g硫酸亚铁铵试样于250 mL锥形瓶中,加入2 mol/L的H2SO4溶液5 mL和新煮沸而冷却的蒸馏水20 mL,用0.01 mol/L的KMnO4标准溶液滴定至溶液呈粉红色,30 s不褪色即为终点,平行测定3次,同时作空白实验。从表1可知,产率可达78%以上,Fe3+含量均低于0.005%,产品六水合硫酸亚铁铵的纯度高,制得的产物均为浅绿色晶体。
2.2.2 X射线粉末衍射分析
将硫酸亚铁铵样品磨细,用D/max-Ⅱ型X射线粉末衍射仪分别对其进行扫描,采用Cu Kα射线(λ=0.154 056 nm),工作电压35 kV,工作电流60 mA,扫描速度8 °/min,在室温下收集3°~80°衍射数据,本实验所制得硫酸亚铁铵及分析纯硫酸亚铁铵的X射线粉末衍射图谱见图2。XRD图谱的本底较小,衍射峰高而尖锐,说明制得的产物晶型很好。由图2可知,实验所制得的硫酸亚铁铵在2θ=21.19°、23.43°和29.51°处出现三强峰,同文献[13]报道的XRD图谱完全一致,与分析纯硫酸亚铁铵在21.22°、23.43°、29.48°处的三强峰吻合。同时,本实验制得硫酸亚铁铵的XRD谱图也与六水合硫酸亚铁铵的标准谱图(JCPDS 35-0764)在2θ=21.15°、23.38°和29.47°处的三强峰完全吻合,证明实验制得的产品是单一物相。
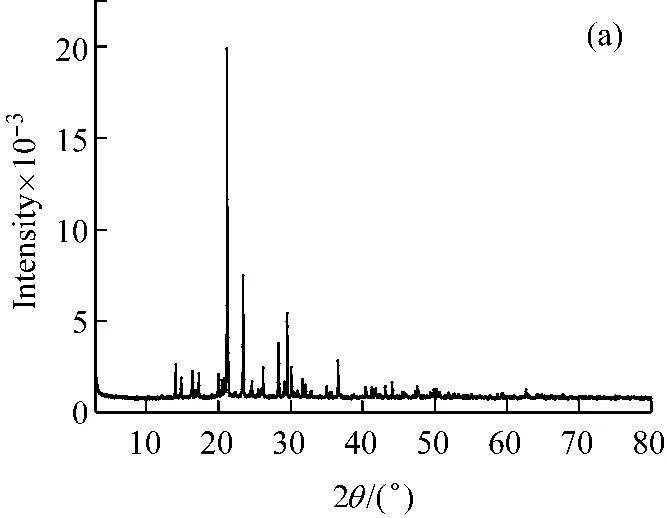
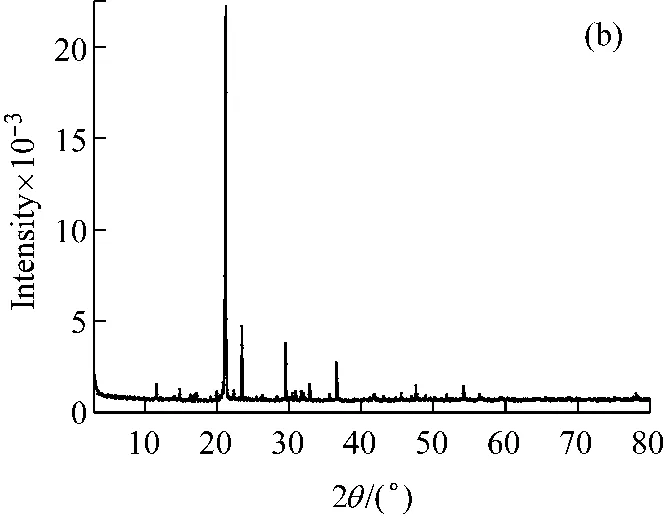
图2 实验所得硫酸亚铁铵(a)及分析纯硫酸亚铁铵(b)的XRD图谱
2.2.3 红外光谱分析
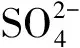
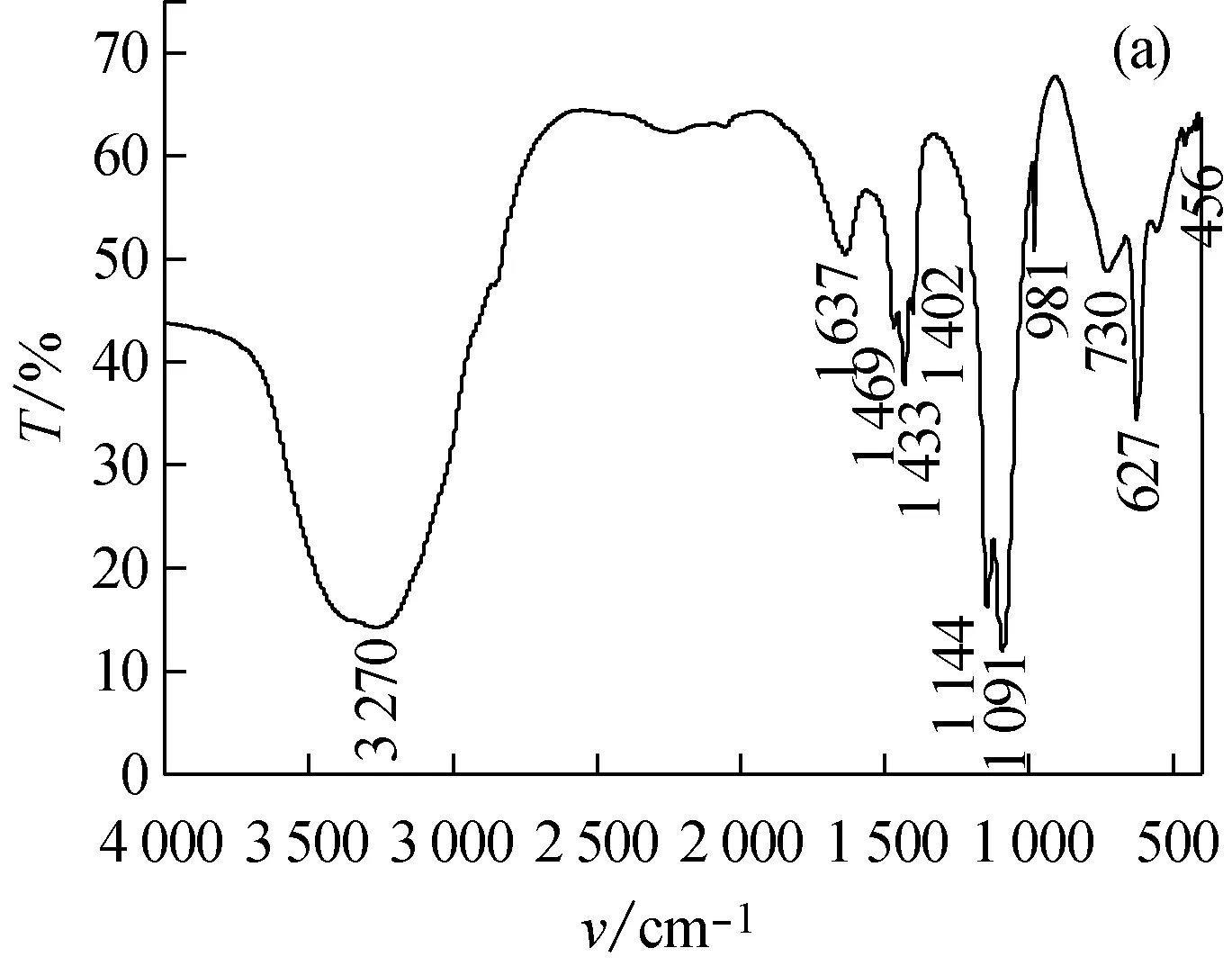
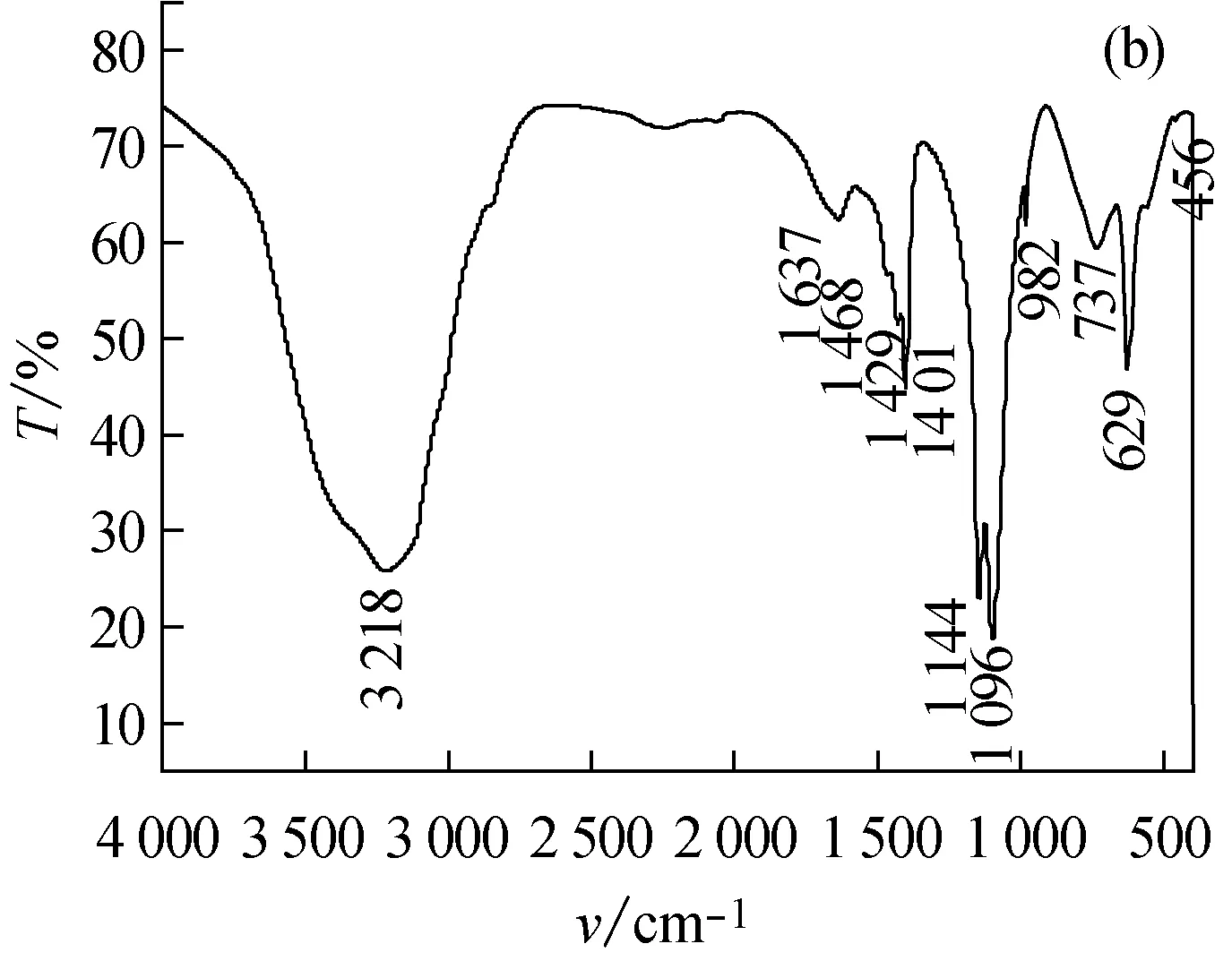
图3 实验所得硫酸亚铁铵(a)及分析纯硫酸亚铁铵(b)的IR图谱
2.2.4 热重差热分析
分别研究了所制备的硫酸亚铁铵和分析纯硫酸亚铁铵在氮气气氛中的热分解行为,升温速率10 ℃/min,其TG-DTA曲线见图4,本实验制得的硫酸亚铁铵和分析纯硫酸亚铁铵的热分解过程的TG曲线和DTA曲线完全相似。由图4(a)可知,通过TG曲线推算出硫酸亚铁铵分子中有6个结晶水,与其化学组成一致,低于180 ℃时硫酸亚铁铵只有结晶水逸出而样品本身并不分解。从TG曲线可以看出,其失水过程是一步完成的,与文献[13,16]报道的分步失水有些差异。DTA曲线在104 ℃处有一个较强的吸热峰,对应TG曲线的失重率为27.81%,与完全失去6个结晶水的理论值27.57%吻合。DTA曲线在180~450 ℃有4个连续的弱吸热峰,而TG曲线对应着4个连续的失重台阶,表明硫酸亚铁铵逐步分解。本实验制得产物和分析纯硫酸亚铁铵的TG曲线与其对应的DTA曲线所得各分解阶段反映出的温度范围一致,这进一步说明制得的硫酸亚铁铵很纯。
3 结 语
对综合性实验硫酸亚铁铵制备的实验内容进行了减量化与绿色化研究,改造后的试剂用量比传统实验减少50%以上,实验时间缩短1/3,降低了实验消耗费用,减少了环境污染。同时,用滴定分析、X射线粉末衍射、红外光谱、热重差热分析等方法对所制得的产品进行了表征分析,有助于学生对相关表征方法和对硫酸亚铁铵组成结构的了解。该实验是一个较好的综合性化学实验,不仅可培养学生有关的基本实验操作技术与技能,同时可培养和训练学生的科学思维方法及绿色环保意识,从而促进学生创新能力、综合实践技能的提高。
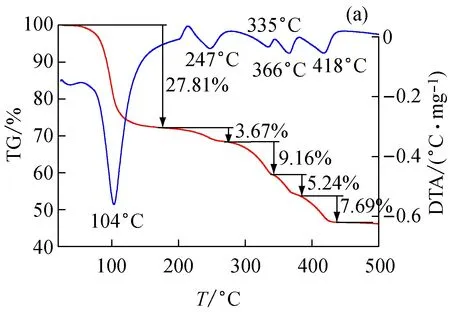
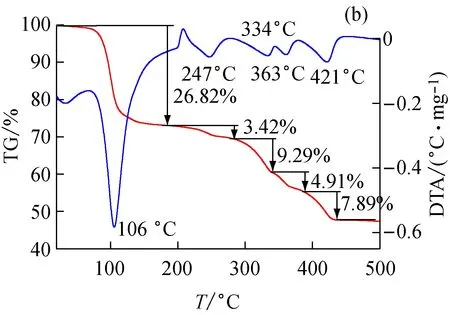
图4 实验所得硫酸亚铁铵(a)及分析纯硫酸亚铁铵(b)的TG-DTA曲线
[1] 南京大学《无机及分析化学实验》编写组. 无机及分析化学实验[M]. 4版. 北京:高等教育出版社, 2006: 70-72.
[2] 崔爱莉. 基础无机化学实验[M]. 北京:高等教育出版社, 2007: 62-64.
[3] 王嗣祖, 韩 莉, 奂东兰, 等. 改进教材中硫酸亚铁铵的制备方法[J]. 阴山学刊, 2011, 25(2): 38-40.
[4] 姜述芹, 马 荔, 梁竹梅, 等. 硫酸亚铁铵制备实验的改进探索[J]. 实验室研究与探索, 2005, 24(7): 18-20.
[5] 刘少华, 田博士. 硫酸亚铁铵制备实验的绿色化改进[J]. 广州化工, 2011, 39(12): 162-163.
[6] 钟国清, 周齐文, 夏 安. 硫酸亚铁铵的制备反应条件与绿色化研究[J]. 实验技术与管理, 2013, 30(5): 14-16、25.
[7] 曾琦斐. 硫酸亚铁铵的制备方法研究[J]. 化学工程与装备, 2011(4): 23-25.
[8] 汪丰云, 王小龙. 硫酸亚铁铵制备的绿色化设计[J]. 大学化学, 2006, 21(1): 51-53.
[9] 钟国清. 化学实验教学的绿色化改革与实践[J]. 实验技术与管理, 2006, 23(12): 18-19.
[10] 刘 萍, 任有良, 孙红丽. 硫酸亚铁铵制备实验研究[J]. 商洛学院学报, 2013, 27(4): 27-30.
[11] 娄军芳, 倪弘昕. 硫酸亚铁铵的绿色制备[J]. 广州化工, 2011, 39(24): 164-165.
[12] 陈彦玲, 徐林林, 林世威. 硫酸亚铁铵制备方法微型化的研究[J]. 长春师范学院学报(自然科学版), 2011, 30(1): 73-75.
[13] 耿金灵, 王 岩, 殷海燕. 硫酸亚铁铵的纯度和组成的测定[J]. 实验技术与管理, 2009, 26(5): 33-36.
[14] 陈文彦, 刘心纯, 刘够生, 等. 网状结构结晶Ⅴ型聚磷酸铵的合成与表征[J]. 高等学校化学学报, 2010, 31(12): 2494-2499.
[15] 陈利娟, 史岽瑛, 王玉龙, 等. 三核铁簇硫酸盐K2(H3O)3[Fe3(H2O)3O(SO4)6]·6H2O的合成与晶体结构[J]. 化学研究, 2010, 21(4): 1-56.
Greening Preparation and Characterization of Ammonium Ferrous Sulfate
ZHONGGuo-qing,WUZhi-xian,BAIJin-wei
(School of Material Science and Engineering, Southwest University of Science and Technology, Mianyang 621010, China)
It is an important part of the chemical education to put the idea of green chemistry in university chemistry teaching, since it can reduce environmental pollution in the chemical experiment, enhance the students' awareness of environmental protection. The green chemistry is also a new topic of chemical experimental teaching reform. Therefore, abandoning the heavily-polluted traditional chemical experiments and exploring of the green transformation of chemical experiment are the direction of the struggle of chemistry experiment educators. The preparation experiment of ammonium ferrous sulfate is a classic comprehensive experiment for learning chemistry curriculum of college students. The conventional experiment content for the preparation of ammonium ferrous sulfate of the miniaturization and greenization transformation were studied. The improved experiment for experimental teaching with normal experiment devices, on one hand, could reduce environmental pollution in laboratory, and could realize greening experiment teaching; On the other hand, it can greatly reduce the experimental reagent wastage, save experimental expenditure. The product of ammonium ferrous sulfate was characterized by titration analysis, X-ray powder diffraction, infrared spectra, and thermogravimetry and differential thermal analysis.
comprehensive experiment; ammonium ferrous sulfate; preparation; characterization; green chemistry
2014-04-02
西南科技大学重点实验技术研究项目(12syjs-24)资助
钟国清(1965-),男,四川内江人,教授,主要从事基础化学教学及功能配位化学研究工作。
Tel.:0816-6088252;E-mail:zgq316@163.com
O 611.6;G 642.423
A
1006-7167(2015)02-0046-04
