纤维素乙醇发酵残渣制备纳米二氧化硅及其表征
2015-02-23周景辉
炊 颖,周景辉
(大连工业大学 轻工与化学工程学院,辽宁 大连 116034)
0 引 言
生物乙醇的生产存在与人类争粮的问题,因此可利用农作物废弃物如秸秆、麦皮等来生产纤维素乙醇[1]。生物化学途径是生产纤维素乙醇的转化途径之一,主要通过水解和酶解发酵使秸秆中的糖转化成纤维素乙醇,但在此转化过程中会产生大量残渣。目前对纤维素乙醇发酵残渣开发利用的研究并不多,主要以燃烧回收热量的方式处理。有研究表明,发酵残渣中含有少量未酶解的纤维素、大量木质素以及灰分等杂质[2],其中灰分的主要成分为二氧化硅。二氧化硅因其具有高活性、强吸附性及好的补强性等特点,广泛用于橡胶工业中作为补强剂[3]。对二氧化硅进行表面修饰改善其分散性能后,可作为一种较好的消光剂用于涂料工业[4]。纳米二氧化硅因其具有硬度高、稳定性好及可屏蔽紫外线等特点,可将其加入高分子材料中达到改善材料的热光稳定性,提高产品的抗老化性及抗紫外线老化性[5]。纤维素乙醇残渣在国内工厂中通常用于直接燃烧或是作为肥料使用[6],由于残渣中灰分含量较高,会影响残渣的热利用率,且燃烧后残余的二氧化硅容易在炉壁上形成结垢,如果将残渣中的硅加以应用,这样不仅能提高资源的利用价值,还能提高生产纤维素乙醇工业的经济效益。
目前制备纳米二氧化硅的成熟工艺[7]有沉淀法、气相沉积法及溶胶-凝胶法等,而用来检测硅含量的方法有重量法、硅钼蓝分光光度法、α-硅钼黄显色测定法、容量法等[8-9]。本论文采用酸沉淀法来提取NaOH 提取液(下文称“提取液”)中溶解的硅,用α-硅钼黄显色测定法来测定提取液中硅的含量,旨在为纤维素乙醇发酵残渣的利用和纳米二氧化硅的制备提供新的途径。
1 实 验
1.1 原 料
玉米秸秆纤维素乙醇发酵残渣,取自中粮集团;氢氧化钠、Na2SiO3·9H2O、乙酸、钼酸铵、乙酸钠、硫酸、盐酸、二氧六环、纳米二氧化硅,均为分析纯。
1.2 原料成分分析
参照国标测得纤维素乙醇发酵残渣中灰分质量分数为18.70%,酸不溶木素和酸溶木素分别为68.39%,2.18%,综纤维素[10]为9.88%。
1.3 原料预处理
将残渣风干、粉碎,过100目筛。由于残渣中含有少量未酶解的纤维素、半纤维素,因此在NaOH 处理残渣前先用1%H2SO4在120℃下处理1h[11],结束后过滤并用去离子水洗至中性,风干备用。
1.4 纤维素乙醇发酵残渣中硅含量的测定
有研究表明,草类原料中的硅只有在碱性介质中才能溶解[7],因此将纤维素乙醇发酵残渣溶于NaOH 溶液中。用紫外分光光度仪测定提取液中硅的吸光度值,回归得到硅标准曲线方程,用式(1)计算提取液中硅的质量浓度[8]。
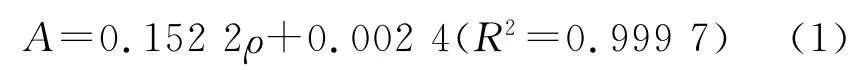
式中:A为吸光度值;ρ为提取液中硅的质量浓度,μg/mL。
1.5 纤维素乙醇发酵残渣制备纳米二氧化硅
取一定量预处理过的纤维素乙醇发酵残渣,加入配制好的NaOH 溶液,然后将其放入一定温度的水浴锅中,在搅拌的情况下反应一定时间,结束后冷却、离心分离收集提取液。
将在优化条件得到的提取液置于一定温度的水浴锅中,缓慢加入体积分数为2%的盐酸,机械搅拌,并将pH 计放入提取液中在线检测,当提取液达到pH=7时停止加酸,静置2h,离心分离并洗涤沉淀物,冷冻干燥,将干燥后的样品放入马弗炉里灼烧,得到的白色粉末即为纳米二氧化硅。
1.6 纳米二氧化硅的表征
采用Spectrum-B 型红外光谱仪、D/Max-3B型X 射线衍射仪、K-Alpha型X 射线光电子能谱、JSM-7800F型扫描电子显微镜分别对纳米二氧化硅进行结构和形貌表征,用Color Touch PC白度仪进行白度检测。
2 结果与讨论
2.1 提取液的制备
2.1.1 NaOH 质量分数对提取液中硅含量的影响
在反应时间1h、反应温度95 ℃、料液比1∶20条件下,考察NaOH 质量分数对提取液中硅含量的影响,结果如图1(a)所示。当NaOH 质量分数小于7%时,提取液中硅含量随NaOH 浓度的增加而提高,NaOH 质量分数7%时提取液中硅含量最大,继续增加NaOH 质量浓度,提取液中硅含量反而下降。这说明,残渣中的硅在一定NaOH 质量浓度溶液中有很好的溶解性。当NaOH 质量分数超过7%时,生成的Na2SiO3会形成胶团,而此胶团可能会与提取液中存在的少量过渡金属离子形成复合物,此复合物可能对紫外法测提取液中硅的含量产生影响,故制备提取液时NaOH 的较优质量分数为7%。

图1 反应条件对提取液中硅含量的影响Fig.1 Reaction conditions on the influence of silicon content in the extract
2.1.2 反应时间对提取液中硅含量的影响
在NaOH 质量分数7%、反应温度95 ℃、料液比1∶20条件下,考察反应时间对提取液中硅含量的影响,如图1(b)所示。当反应时间小于1h时,提取液中硅的含量随着反应时间的延长而增大;当反应时间为1h时,提取液中硅的含量最大;再延长反应时间,提取液中硅含量反而下降,2h后趋于平稳。这可能是由于在反应时间为1h时,从残渣中溶解进入NaOH 溶液中的硅达到饱和,延长时间,溶出的硅可能由于存在其他方式的转化,没有被检测到(实验中检测到的硅是提取液中稳定的硅),故制备提取液比较合适的反应时间为1h。
2.1.3 反应温度对提取液中硅含量的影响
在NaOH 质量分数7%、反应时间1h、料液比1∶20的条件下,考察反应温度对提取液中硅含量的影响,如图1(c)所示。当反应温度小于75 ℃时,提取液中硅含量随反应温度的升高而增大,75 ℃时,提取液中硅含量达到最大,继续升高温度,提取液中硅含量降低并趋于平稳。出现这种现象可能是因为适当地增加温度会使硅的溶出速率提高[12],当温度大于75 ℃时,溶出的硅可能由于存在其他方式的转化,没有被检测到,因此制备提取液的较适合的反应温度为75 ℃。
2.1.4 料液比对提取液中硅含量的影响
在NaOH 质量分数7%、反应时间1h、反应温度75℃条件下,考察料液比对提取液中硅含量的影响,结果如图1(d)所示。从图中可看出,随着料液比的增大,提取液中硅含量呈先增大后降低的趋势,在料液比为1∶25时,提取液中硅含量最大。反应初始,一部分NaOH 溶液与纤维素乙醇发酵残渣中的木素发生反应,另一部分与残渣中的硅反应。随着料液比的增大,当溶出硅量达到最大时,NaOH 的残余碱量会逐渐减少,从而导致较大分子质量的硅酸钠凝胶分子团沉淀出来[12],故使得提取液中能检测到的硅含量减少。因此,制备提取液的较合适的料液比为1∶25。
2.2 纳米二氧化硅的制备及表征
2.2.1 纳米二氧化硅FT-IR 分析
图2为市售分析纯纳米二氧化硅与自制纳米二氧化硅红外谱图。分析比较可知,两者的谱图基本骨架很相似。3 441.79和1 632.77cm-1附近的吸收峰可能是Si—OH 的振动峰[13],1 102.64和806.16cm-1处的吸收峰分别是Si—O—Si的对称伸缩振动和反对称伸缩振动,478.46cm-1处的吸收峰是Si—O 键的弯曲振动峰。由于所购买的分析纯纳米二氧化硅为疏水型,故其在2 900,2 800cm-1附近出现了C—H 键的伸缩振动峰,而自制纳米二氧化硅在2 900,2 800cm-1附近也出现了较小的吸收峰,这是因为制得的纳米二氧化硅中含有一定杂质。

图2 纳米二氧化硅FT-IR 谱图Fig.2 FT-IR spectra of nanosilica
2.2.2 纳米二氧化硅XRD 分析
图3为市售分析纯纳米二氧化硅和自制纳米二氧化硅的X 射线衍射图。从图中可看出,市售分析纯纳米二氧化硅与自制纳米二氧化硅均在2θ=22°左右处出现一个非晶态的衍射峰,由此可知,自制的纳米二氧化硅为无定形纳米二氧化硅。同时,自制纳米二氧化硅在2θ=22°左右处的峰较宽且有小杂峰,这可能是由于杂质的存在引起的。

图3 纳米二氧化硅XRD 谱图Fig.3 XRD patterns of nanosilica
2.2.3 纳米二氧化硅的XPS分析
图4 为自制纳米二氧化硅的XPS 能谱图。从图中可看出,二氧化硅中的特征峰Si 2p、Si 2s以及O 1s的光电子束缚能分别在103,150 和532eV附近出现。同时,在285eV 附近出现的小峰为C 1s的光电子束缚能。由XPS分析数据得,自制纳米二氧化硅中C,Si,O 质量分数分别为3.91%,33.83%和62.26%,纯度为96.09%。
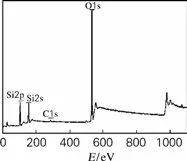
图4 纳米二氧化硅XPS谱图Fig.4 XPS patterns of nanosilica
2.2.4 纳米二氧化硅的外观形态
图5分别为分析纯纳米二氧化硅(a)和经过干燥的自制纳米二氧化硅(b)扫描电镜图。从图中可看出,制得的纳米二氧化硅和分析纯纳米二氧化硅形貌相似,均为球形状颗粒,且颗粒的粒径较均匀,自制的纳米二氧化硅单体颗粒粒径为几十纳米。

图5 纳米二氧化硅SEM图Fig.5 SEM images of nanosilica
2.2.5 纳米二氧化硅的白度
对市售分析纯纳米二氧化硅和自制纳米二氧化硅进行白度检测,测试结果分别为84.96%和82.19%。由此可看出自制的纳米二氧化硅白度和市售的白度接近。
3 结 论
(1)以玉米秸秆发酵生产纤维素乙醇得到的残渣为原料,NaOH 溶液为反应溶剂,通过条件实验得出制备含硅提取液的较适宜条件:NaOH质量分数7%,反应时间1h,反应温度75 ℃,料液比1∶25。
由于检测到的硅可能不是残渣中溶解硅的全部,后续研究可以通过检测碱提取后残渣中残余硅含量加以验证。
(2)红外谱图表明所制样品为二氧化硅;XRD 谱图表明制得的二氧化硅为无定形;XPS分析得所制二氧化硅具有较高纯度;由SEM图可看出,样品颗粒为球形,颗粒粒径分布较均匀。
(3)用玉米秸秆发酵生产纤维素乙醇残渣制备的纳米二氧化硅白度达到82.19%(ISO),与市售纳米二氧化硅白度(84.96%)接近。
[1]赵彩云,王异静,关东明.纤维素乙醇研究进展[J].酿酒科技,2009(10):87-89.
[2]潘奇,陈介南,张新民,等.纤维乙醇发酵残渣中酶解木质素的提取与表征[J].化工进展,2015,34(1):86-90.
[3]彭书传,宋磊,马步春,等.棒状活性二氧化硅补强橡胶[J].硅酸盐学报,2009,37(1):104-106.
[4]赵丽颖,郑伟.沉淀二氧化硅的应用与发展[J].牙膏工业,2001(4):47-49.
[5]李建新,王磊,孙洪巍.纳米二氧化硅的制备、改性和在塑料中的应用[J].安阳工学院学报,2008(2):43-45.
[6]杨辉,王凤奇,黄勇.含木质素的发酵残渣在脲醛树脂中的应用研究[J].中国胶粘剂,2011,20(12):33-37.
[7]刘希良.高纯二氧化硅的制备与应用[J].化工管理,2014(11):87-89.
[8]李海龙,柴欣生,詹怀宇,等.一种快速测定草类原料制浆黑液中硅含量的新方法[J].光谱学与光谱分析,2012,32(6):1681-1684.
[9]徐永建,胡忠宇,张永奇,等.硫酸盐法制浆黑液硅含量测定的新方法[J].中国造纸,20143,33(1):10-14.
[10]崔金龙,李海明,毕佳捷.离子色谱在造纸原料碳水化合物分析中的应用[J].大连工业大学学报,2013,32(6):432-436.(CUI Jinlong,LI Haiming,BI Jiajie.Analysis of carbohydrates in paper-making materials by ion chromatography[J].Journal of Dalian Polytechnic University,2013,32(6):432-436.)
[11]MINU K,JIBY K K,KISHORE V V N.Isolation and purification of lignin and silica from the black liquor generated during the production of bioethanol from rice straw[J].Biomass and Bioenergy,2012,39:210-217.
[12]程志声,刘淑习,华宁熙.芦苇在硫酸盐蒸煮过程中硅的脱除特点[J].中国造纸学报,1988(3):9-19.
[13]王晓英,蔡旭,洪若瑜,等.纳米二氧化硅的制备及应用[J].中国粉体技术,2011,17(3):64-67.
