急性心肌梗死并发首次心力衰竭患者在院 死亡率及临床预后分析
2015-02-23邓伏雪王小娟胡云凤
邓伏雪,王小娟,胡云凤,常 静
(1. 重庆医科大学附属第一医院心内科,重庆 400016;2. 西安交通大学医学院公共卫生学院,陕西西安 710061)
◇经验交流◇
急性心肌梗死并发首次心力衰竭患者在院 死亡率及临床预后分析
邓伏雪1,王小娟2,胡云凤1,常 静1
(1. 重庆医科大学附属第一医院心内科,重庆 400016;2. 西安交通大学医学院公共卫生学院,陕西西安 710061)
目的 旨在探索急性心肌梗死后首次心力衰竭的发生率、在院治疗情况及心血管不良事件和短期死亡率的影响因素。方法 2009年2月至2012年12月入住我院的591例急性心肌梗死的患者,按在院期间是否并发心力衰竭分为2组,比较分析其入院基本信息、在院治疗方案、冠脉造影结果及在院死亡率。结果 591例急性心肌梗死患者中被诊断为首发心力衰竭者222例,未并发心力衰竭者369例。心力衰竭组的患者较少应用冠脉造影(56.3∶73.4)%及再灌注(43.2∶62.9)%作为诊疗手段,而且相比于非心力衰竭患者较少服用美国心脏病学会/美国心脏学会(ACCF/AHA)的推荐药物。心力衰竭患者较非心力衰竭患者有着较高的在院死亡率(15.3∶2.4)%。急性心肌梗死并发心力衰竭(OR=2.97)和心源性休克(OR=7.53)是在院死亡率最强的影响因素。结论 急性心肌梗死后新发的心力衰竭患者短期预后不良。准确快捷的诊断以及及时和全面的治疗可以明显降低短期死亡率。
急性心肌梗死;心力衰竭;在院死亡率;心血管不良事件
急性心肌梗死(acute myocardial infarction, AMI)是全球范围内致死率和致残率的主要原因之一[1]。据估计,每年有约300万人患有急性ST段抬高性心肌梗死(STEMI),约超过400万患急性非ST段抬高性心肌梗死(NSTEMI)[2]。左心室功能的失调在临床上表现为心力衰竭或者心源性休克。许多调查研究表明,心力衰竭不仅1年和5年的死亡率高[3],而且再入院率也居高不下。现有资料显示AMI后的心力衰竭发生率及死亡率分别为32.4%和21.6%[4]。在中国,每年约200万的心血管疾病患者中至少有50万患者被诊断为AMI[5],这是一个不容忽视的社会公共健康问题。然而,有关于AMI后心力衰竭的发生率、临床特点、短期预后研究较少。本研究将针对AMI后心力衰竭的临床特点、在院治疗情况(药物及介入治疗)、在院心血管事件以及短期预后应用统计分析方法进行研究,为制定相应的预防及治疗措施提供依据。
1 对象与方法
1.1 研究对象 连续入选2009年2月至2012年12月以AMI在重庆医科大学附属第一医院心内科住院的患者共591例,包括STEMI和NSTEMI。主要的排除标准是:患者未满18岁;患者在此次AMI前有心力衰竭病史(包括先天性心脏病、瓣膜性心脏病、心肌病、病毒性心肌炎、结节病导致的心脏病以及严重的心律失常);患者仅有稳定或不稳定心绞痛而未发展至心肌梗死。
1.2 方法及观察指标 制定统一表格收集患者住院期间的有关数据,包括人口统计学资料、临床情况、诊断、冠脉造影结果、生化检测结果(第一次结果)、冠脉造影检测结果、在院期间的药物和介入治疗情况以及患者的在院心血管事件(MACEs)和在院死亡率等。将591例AMI患者按在院期间是否并发心力衰竭分为心力衰竭组(222例)与非心力衰竭组(369例)进行比较分析。对于AMI后发生心力衰竭的患者再根据是否同时服用β受体阻滞剂和肾素-血管紧张素-醛固酮系统(RAAS)类药物分为两个亚组进行对比分析。主要在院心血管不良事件包括心房颤动、室性心律失常、术后出血、心源性休克、再缺血和再次心肌梗死。
1.3 诊断标准 根据2012年AMI的国际定义以及综合以前的一些研究[6-7],AMI的诊断标准为:①胸痛持续至少30 min且服用硝酸酯类药物不能完全缓解;②典型的心电图改变;③血清学标志物如肌酸激酶或者肌钙蛋白高于正常2倍以上;④冠脉造影有血管病变的证据。据美国心脏病联合会指南,心力衰竭的诊断主要依据临床表现及体格检查:①新发的心力衰竭典型临床表现(如呼吸困难及疲劳);②三分之一以上肺野可闻及湿罗音;③胸腔X线显示有非心源性的肺水肿或者肺阻塞;④不正常水平的脑钠肽或者B型脑钠肽前体。心源性休克定义为收缩压小于80 mmHg,血容量不足以及与之相关的发绀、四肢厥冷、神智改变和持续性少尿。
1.4 统计学处理 采用SPSS 18.0软件,计数资料以频数(率)表示,计量资料用均值±标准差表示。心力衰竭组与非心力衰竭组两组间的率间比较采用χ2检验,计量资料呈正态分布而且符合方差齐性者行两独立样本t检验,不符合方差齐性的行近似t检验。统计因素中所有与在院死亡率可能相关的影响因素采用Logistic多因素向后逐步去除回归法(Backwald)进行回归分析,回归统计时依次输入31个变量:心力衰竭、年龄、性别、心率、吸烟、饮酒、糖尿病、高血压、COPD、心绞痛病史、中风、慢性肾病、高脂血症、家族冠状动脉病病史、多次心肌梗死病史、院前耽误时间、住院天数、在院心血管事件(心律失常、再缺血或再梗、主要出血、心源性休克)、在院期间用药(抗心律失调药、口服受体阻滞剂、钙通道阻滞剂、RAAS类、受体阻滞剂+ACEI、肝素、阿司匹林)、冠脉造影、PCI以及溶栓治疗,SPSS系统对以上变量进行多个步骤从而筛选出差异有统计学意义的与在院死亡率相关的影响因素。由于纳入回归方程的变量数量较多(包含计数及计量资料),所以我们采用Cox & Snell R2、Nagelkerke R2以及Hosmer-Lemeshow检验来检验回归模型的拟合优度。表1中个别数据采用Mann-Whitney检验。P<0.05为差异有统计学意义。
2 结 果
2.1 一般临床情况的比较 2009年2月1日至2012年12月30日期间收入AMI患者共591例,其中在住院期间被诊断为首发心力衰竭者222例(37.6%),非心力衰竭者369例(62.4%)。两组患者的一般情况及相关AMI危险因素比较结果见表1。在2组患者的既往史和入院资料中,是否有糖尿病、高血压、心肌梗死病史、中风、高脂血症、家族心血管疾病以及入院时是否伴有心律失常,差异均无统计学意义;而且心肌梗死类型(STEMI或者NSTEMI)在2组患者中差异也无统计学意义。
2.2 药物及介入治疗情况 的使用率较高(所有P<0.001)。虽然β受体阻滞剂和血管紧张素转换酶抑制剂(ACEI)被证实在心肌重塑和心力衰竭的预后上起到很大作用,
表1 591例AMI患者心力衰竭组与非心力衰竭组入院基本资料的比较
Tab.1 Comparison of baseline characteristics of 591 hospitalized patients with or without post-AMI HF
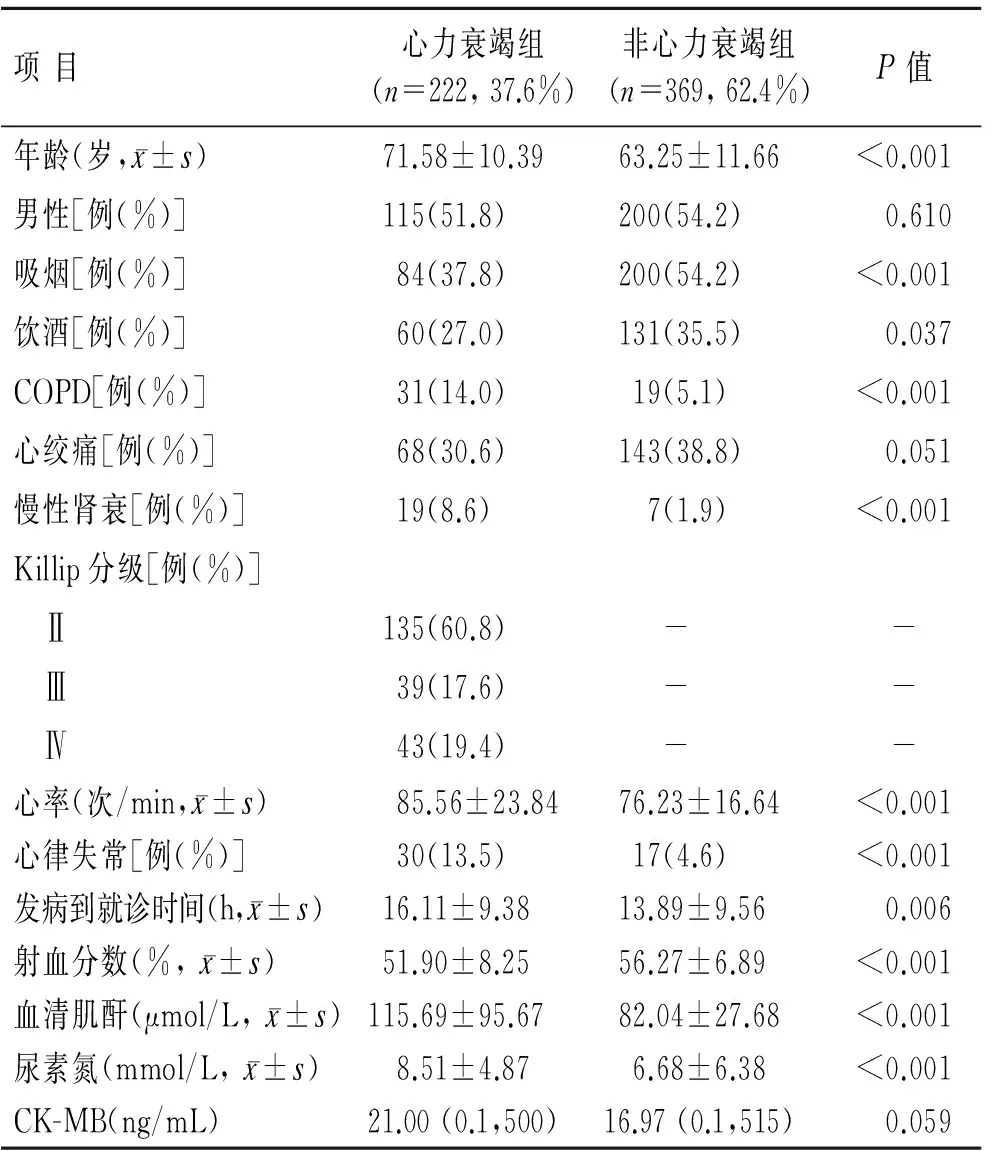
项目心力衰竭组(n=222,37.6%)非心力衰竭组(n=369,62.4%)P值年龄(岁,x±s)71.58±10.3963.25±11.66<0.001男性[例(%)]115(51.8)200(54.2)0.610吸烟[例(%)] 84(37.8)200(54.2)<0.001饮酒[例(%)] 60(27.0)131(35.5)0.037COPD[例(%)] 31(14.0) 19(5.1)<0.001心绞痛[例(%)] 68(30.6)143(38.8)0.051慢性肾衰[例(%)] 19(8.6)7(1.9)<0.001Killip分级[例(%)] Ⅱ135(60.8)-- Ⅲ 39(17.6)-- Ⅳ 43(19.4)--心率(次/min,x±s)85.56±23.8476.23±16.64<0.001心律失常[例(%)] 30(13.5) 17(4.6)<0.001发病到就诊时间(h,x±s)16.11±9.3813.89±9.560.006射血分数(%,x±s)51.90±8.2556.27±6.89<0.001血清肌酐(μmol/L,x±s)115.69±95.6782.04±27.68<0.001尿素氮(mmol/L,x±s) 8.51±4.87 6.68±6.38<0.001CK-MB(ng/mL)21.00(0.1,500)16.97(0.1,515)0.059
CK-MB:肌酸激酶同工酶,应用 Mann-Whitney检验,表示为中位数(最小值,最大值)。
表2 心力衰竭组和非心力衰竭组在院期间治疗的比较
Tab.2 Comparison of in-hospital treatment for patients with or without post-AMI HF
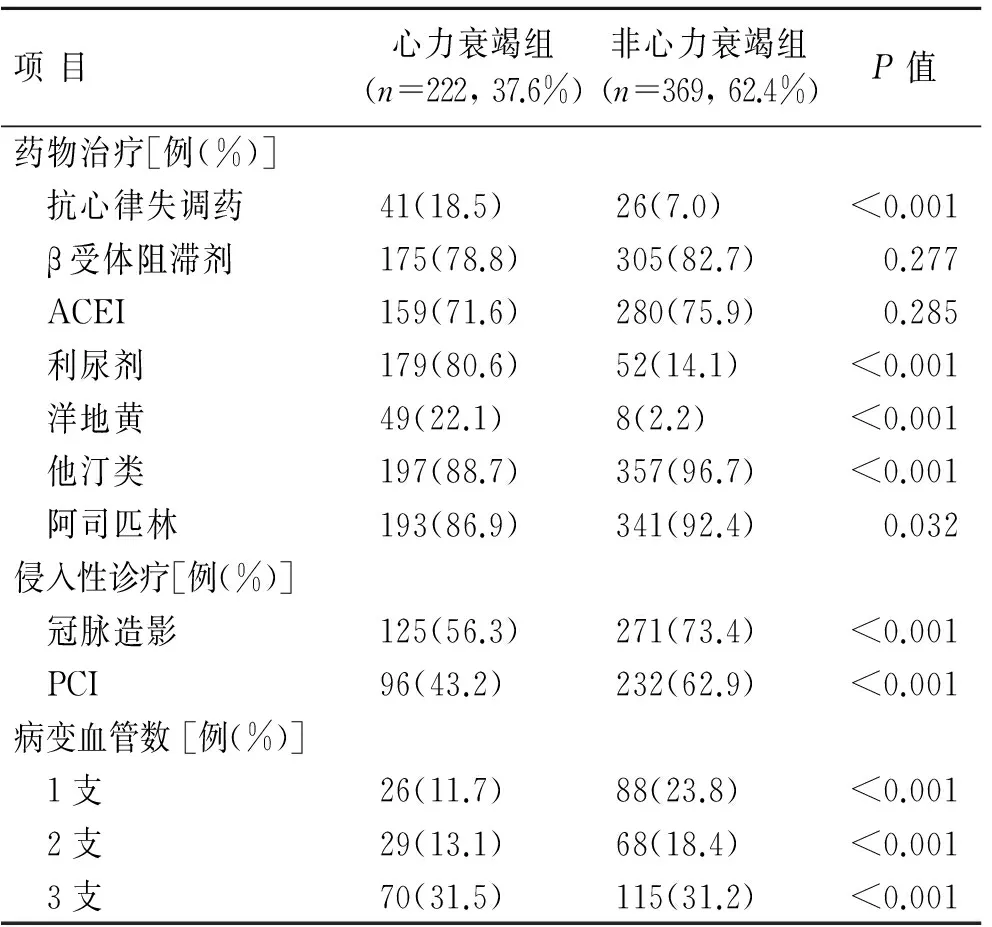
项目心力衰竭组(n=222,37.6%)非心力衰竭组(n=369,62.4%)P值药物治疗[例(%)] 抗心律失调药41(18.5)26(7.0)<0.001 β受体阻滞剂175(78.8)305(82.7)0.277 ACEI159(71.6)280(75.9)0.285 利尿剂179(80.6)52(14.1)<0.001 洋地黄49(22.1)8(2.2)<0.001 他汀类197(88.7)357(96.7)<0.001 阿司匹林193(86.9)341(92.4)0.032侵入性诊疗[例(%)] 冠脉造影125(56.3)271(73.4)<0.001 PCI96(43.2)232(62.9)<0.001病变血管数[例(%)] 1支26(11.7)88(23.8)<0.001 2支29(13.1)68(18.4)<0.001 3支70(31.5)115(31.2)<0.001
PCI:经皮冠状动脉介入治疗;ACEI:血管紧张素转换酶抑制剂。
但在此研究中,心力衰竭组和非心力衰竭组患者间β受体阻滞剂和ACEI的使用差异无统计学意义。而且,钙通道阻滞剂、肝素(包括静脉注射及皮下注射)、氯吡格雷以及药物溶栓的治疗在2组患者中差异均无统计学意义。
关于β受体阻滞剂和RAAS类药物(主要为ACEI类)的进一步分析结果见表3。所有AMI并发心力衰竭的患者中,尽管两组患者间的基本情况差别不大,但是同时服用两种药物的患者(n=142)比只服用其中一种或者两种药物都未服用的患者(n=80)有着较好的在院生存率(94.4∶67.5,P<0.001)%。而两种药物均未服用的心力衰竭患者(n=30)生存率最低。另一方面,尽管在并发心力衰竭患者中同时服用两种推荐药物(β受体阻滞剂和ACEI类)有着较好的生存率,但是远远不如AMI未并发心力衰竭的患者的生存率,差异有统计学意义(P<0.001,图1)。
表3 急性心肌梗死后首发心力衰竭的患者中β受体阻滞剂和ACEI类药物的应用及预后情况的比较
Tab.3 Comparison of post-AMI HF patients with or without use of beta-blockers and ACEIs
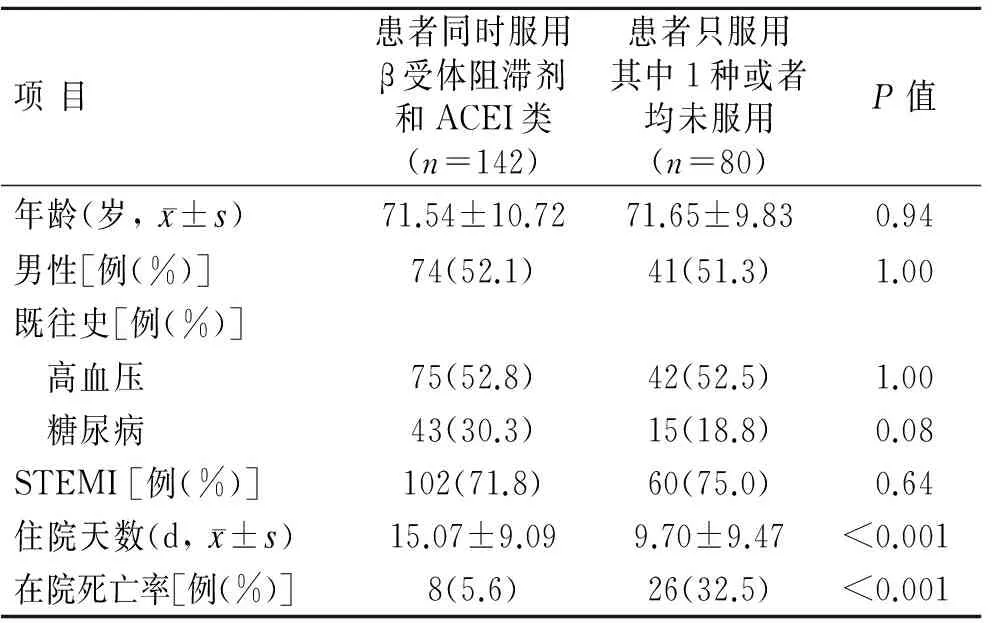
项目患者同时服用β受体阻滞剂和ACEI类(n=142)患者只服用其中1种或者均未服用(n=80)P值年龄(岁,x±s)71.54±10.7271.65±9.830.94男性[例(%)]74(52.1)41(51.3)1.00既往史[例(%)] 高血压75(52.8)42(52.5)1.00 糖尿病43(30.3)15(18.8)0.08STEMI[例(%)]102(71.8)60(75.0)0.64住院天数(d,x±s)15.07±9.099.70±9.47<0.001在院死亡率[例(%)]8(5.6)26(32.5)<0.001

图1 关于与AMI后非心力衰竭患者相比较β受体阻滞剂和ACEI类在心力衰竭组患者中的使用对在院死亡率的影响情况的生存分析
Fig.1 Kaplan-Meier about unadjusted in-hospital survival rate of patients without HF (n=369), HF patients treated with both beta-blockers and ACEIs (n=142), HF patients treated with either one (n=50), and HF patients receiving neither one (n=30) during hospital stay
除此之外,并发心力衰竭的患者较少进行冠脉造影和PCI的诊疗。根据冠脉造影结果分析心力衰竭的发生率在3支血管病变患者中明显高于1支血管病变的患者(31.5∶11.7)%。
2.3 在院心血管事件及死亡率 主要在院心血管不良事件及在院死亡率见表4。心力衰竭组患者在院死亡率明显高于非心力衰竭组的患者(15.3%∶2.4%,P<0.001)(表4)。而且,心力衰竭组患者的心房颤动(12.6%∶3.3%)、室性心律失常(15.8%∶6.2%)、心源性休克的发生率高,住院时间长[(13.14±9.57)d∶(9.38±5.17)d],差异均有统计学意义。虽然心力衰竭组患者主要出血、再缺血、再梗以及高度房室传导阻滞(包括二级和三级阻滞)的发生率高于非心力衰竭组,但差异无统计学意义。心力衰竭组患者中伴发有MACEs的患者,其在院死亡率高于不伴有MACEs的患者,差异有统计学意义(P<0.001,图2)。
表4 心力衰竭组与非心力衰竭组在院死亡率及不良心血管事件的比较
Tab.4 Comparison of in-hospital morality rate and adverse cardiovascular events between patients with or without post-AMI HF
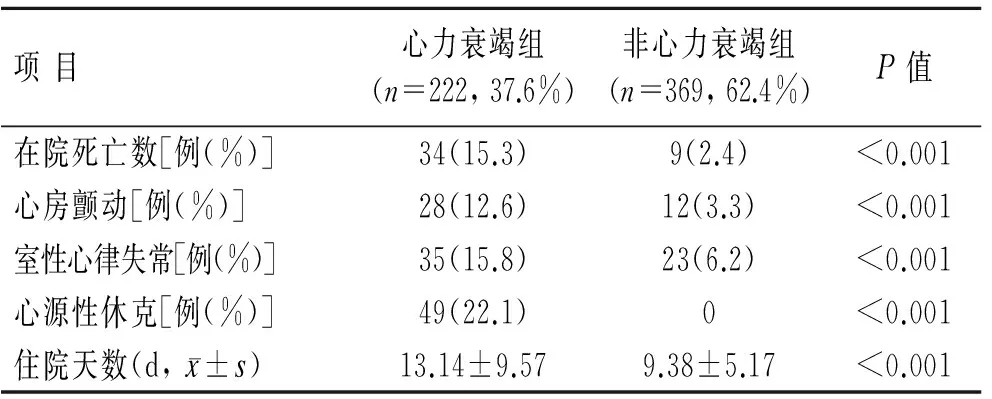
项目心力衰竭组(n=222,37.6%)非心力衰竭组(n=369,62.4%)P值在院死亡数[例(%)]34(15.3)9(2.4)<0.001心房颤动[例(%)]28(12.6)12(3.3)<0.001室性心律失常[例(%)]35(15.8)23(6.2)<0.001心源性休克[例(%)]49(22.1)0<0.001住院天数(d,x±s)13.14±9.579.38±5.17<0.001
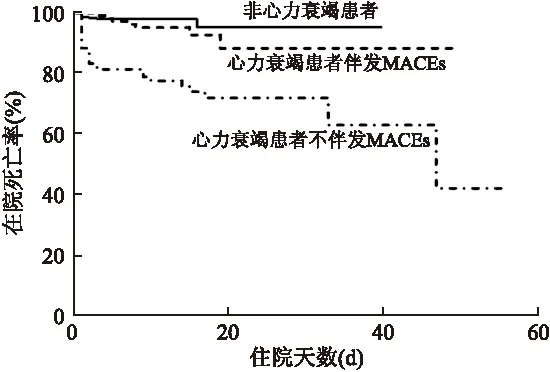
图2 关于AMI是否伴发主要心血管不良事件(MACEs)与在院死亡率关系的生存分析
Fig.2 Kaplan-Meier about in-hospital survival rate of patients without HF (n=369), HF patients with MACEs (n=103) or without MACEs (n=119) during hospital stayMACEs包括房颤、室性心律失常、出血、心源性休克、再缺血、再梗。
2.4 影响在院死亡率的多因素平Logistic逐步回归分析 AMI患者在院死亡率高低的可能影响因素回归分析见表5。Cox & Snell R2、Nagelkerke R2以及Hosmer-Lemeshow检验结果显示,纳入多个变量的回归方程在误差允许范围内该回归方程模型具有较好的拟合度,差异有统计学意义。表中列出经向后逐步去除回归法(Backwald)筛选出的差异有统计学意义的与在院死亡率相关的影响因素。其中,AMI后心源性休克(OR=7.53)为影响患者预后的最重要的独立因素。除此之外,AMI并发心力衰竭(OR=2.97)、年龄(OR=1.06)也是影响患者预后的危险因素。Killip3级和4级患者的在院死亡率比Killip1级和2级的患者高2倍以上(P<0.001,图3),这也提示Killip分级也与患者短期死亡率相关。相反地,服用β受体阻滞剂(OR=0.39)、ACEI类药物(OR=0.35)以及住院天数长短(OR=0.93)与患者的预后呈负相关。尽管溶栓治疗及PCI对在院死亡率的影响差异无统计学意义,但冠脉造影检查(OR=0.13)却是患者预后的独立保护因素。
表5 影响心肌梗死患者在院死亡率的多因素Logistic回归分析
Tab.5Logisticregression analysis of predictors for in-hospital death of patients with AMI
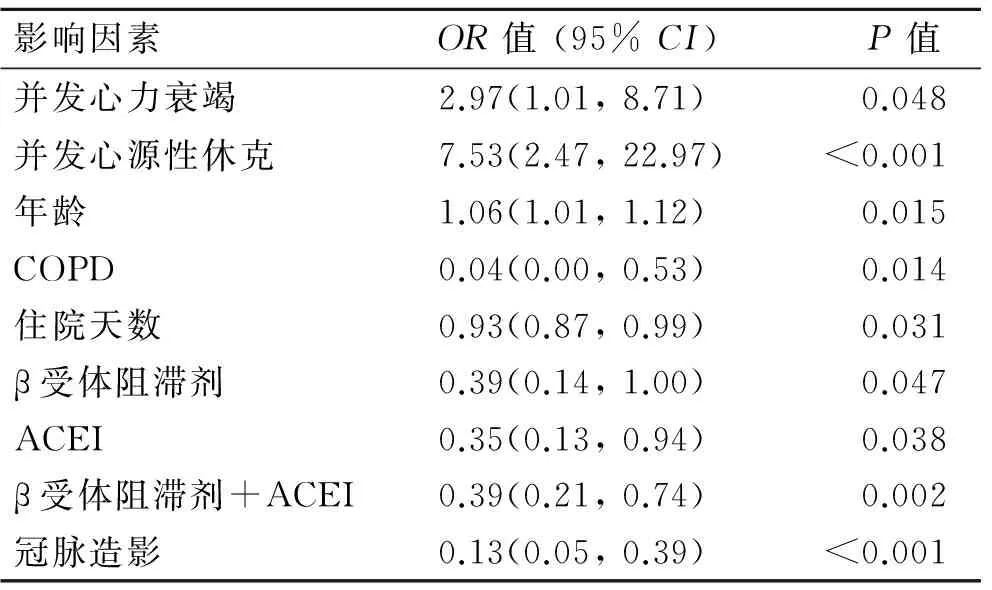
影响因素OR值(95%CI)P值并发心力衰竭2.97(1.01,8.71)0.048并发心源性休克7.53(2.47,22.97)<0.001年龄1.06(1.01,1.12)0.015COPD0.04(0.00,0.53)0.014住院天数0.93(0.87,0.99)0.031β受体阻滞剂0.39(0.14,1.00)0.047ACEI0.35(0.13,0.94)0.038β受体阻滞剂+ACEI0.39(0.21,0.74)0.002冠脉造影0.13(0.05,0.39)<0.001
可能与在院死亡率存在相关性的影响因素均被纳入回归方程式进行统计分析,采用Logistic分析中的Backwald方法对31个变量总共进行了20个分析步骤筛选出差异有统计学意义的变量及建立最佳方程模型。
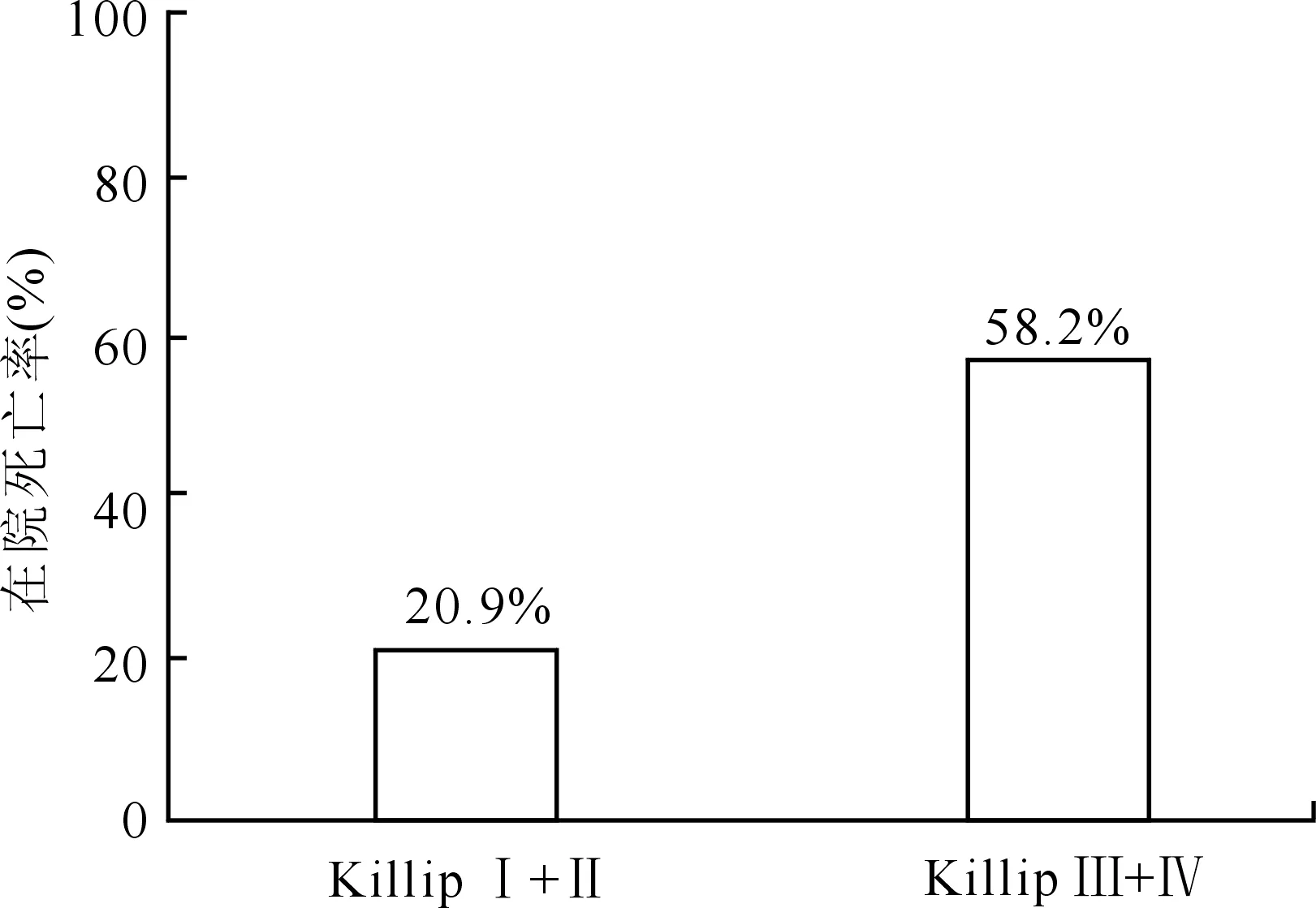
图3 Killip分级与在院死亡率关系的生存分析
Fig.3 Kaplan-Meier about in-hospital death rate of HF patients with different Killip class
3 讨 论
该研究显示AMI伴发心力衰竭的患者预后不良且常伴有严重的心血管不良事件。特别指出的是伴发心力衰竭患者的死亡率大约是非心力衰竭患者的7倍。住院期间发生的心源性休克及心力衰竭与在院死亡率显著相关。尽管在此研究中β受体阻滞剂与ACEI的应用明显优于其他研究[7-8],但2种药物的使用率还是未达到标准。两种药物均未使用的患者有着较高的死亡风险。在591例AMI患者中,有222(37.6%)患者在院期间并发心力衰竭,与近两年有关心力衰竭发生率32.4%和34%相类似[4]。但Killip分级情况却比以往的研究严重[9],其中一个原因可能是AMI发生到就诊时延误时间[(14.72±9.55)h]比西方国家长(平均<6 h)[9],从而不可避免导致再灌注时间窗的延长。多数文献报道称再灌注时间窗越短AMI后心血管不良事件的发生率越低[11-12]。
该研究中,AMI后心力衰竭患者的在院死亡率为15.3%。该结果处于西方国家短期死亡率(21.6%)与中国报道的在院死亡率(12.3%)的一个中间范围[10,13]。与以往多数研究的结果类似。Killip分级的级别越高其在院死亡率也会相应增加[14]。而且,Killip分级标准是对AMI患者在院死亡率进行早期风险评估的一种准确方法[15]。尽管心力衰竭的发病率和生存率近些年有好转趋势[10],但越高级别的Kiliip分级预后越差的趋势却未改变。
在药物使用方面,虽然我们有着较好的药物使用率,但仍有部分并发心力衰竭的患者未及时应用如阿司匹林、β受体阻滞剂及ACEI等药物。在心肌梗死后并发心力衰竭组的患者中,除了β受体阻滞剂,ACEI及阿司匹林其他常用的心血管药物使用率高于非心力衰竭组的患者。根据国际上对AMI后并发心力衰竭一线治疗以及欧洲心血管协会对心力衰竭的诊疗建议[16-17],在没有严重禁忌证的前提下,心力衰竭诊断确立后ACEI应该尽快用于所有射血分数不十分低下的患者而且在不同的心力衰竭阶段都应该维持治疗。而诊断为STEMI的患者排除严重用药禁忌后应在最初的24 h内口服β受体阻滞剂[18]。在我们的回归分析中,β受体阻滞剂和ACEI与在院死亡率负相关,差异有统计学意义(表5)。有Meta分析报道,在有心肌梗死和左室功能收缩障碍的患者中ACEI 的使用可以减少心血管事件的发生率和死亡率。而且国际上也强调β受体阻滞剂在心肌梗死和心力衰竭的收益中起到不可磨灭的作用[19-20]。
同以往许多研究类似,我们的结果也显示AMI后并发心力衰竭的患者较少行PCI治疗[4,9]。早期再灌注治疗不仅可以减小梗死面积或者防止其进一步扩大,而且也能降低心源性休克的发生几率[4]。尽管有一小部分研究表示溶栓及PCI治疗可以使并发心力衰竭的患者生存率提高[21-22],但也有些文献的结论并不支持此观点[23-24],同样在我们的研究中,溶栓及PCI治疗与生存率的提高差异无统计学意义。在该项研究中,溶栓和PCI在降低死亡率方面没有统计学意义的可能原因是病情延误时间较长,整体患者的低灌注率,心脏本身存在较严重的并发症(如二尖瓣反流等)或者是梗死面积过大[25]。2013年美国心脏病学会和美国心脏学会关于心肌梗死的一份联合指南提示,梗死时间小于等于90 min的患者PCI治疗是首选推荐再灌注的方式。但如果医生或者家属根据病情选择了溶栓作为主要治疗手段,最好在入院时或者30 min以内进行[18]。值得注意的是,在院死亡率的高低与是否进行冠脉造影息息相关[24],可能是由于冠脉造影提供了准确的诊断证据从而使得患者得到更及时更适合的治疗方式。然而,对于AMI后并发心力衰竭的患者,PCI与溶栓哪一种治疗手段更能使患者最大程度的受益还需进一步深入的研究。
总之,本研究结果表明AMI后并发心力衰竭患者预后不良且短期死亡率明显高于非心力衰竭的患者。在这些并发心力衰竭的患者中被证实可提高生存率的推荐药物(β受体阻滞剂和ACEI)使用率却较低,同样地侵入性检查如冠脉造影的应用也较少。心力衰竭的早期、准确诊断以及最合适、最优化的治疗在降低在院死亡率和不良预后方面至关重要。
[1] THYGESEN K, ALPERT JS, WHITE HD. Universal definition of myocardial infarction[J]. Eur Heart J, 2007, 28(20):2525-2538.
[2] WHITE HD, CHEW DP. Acute myocardial infarction[J]. Lancet, 2008, 372(9638):570-584.
[3] 尹巧香,赵玉生,候晓平,等. 心力衰竭患者住院病死率15年趋势分析[J]. 中国心血管杂志, 2012, 17(4):276-279.
[4] MCMANUS DD, CHINALI M, SACYNSKI JS, et al. 30-years trends in heart failure in patients hospitalized with acute myocardial infarction[J]. Am J Cardiol, 2011, 107(3):353-359.
[5] XU T, LI W, KOON T, et al. Association of psychological risk factors and acute myocardial infarction in China: the INTER-HEART China study[J]. Chin Med J, 2011, 124(14):2083-2088.
[6] THYGESEN K, ALPERT JS, JAFFE AS, et al. Third universal definition of myocardial infarction: the writing group on behalf of the Joint ESC/ACCF/AHA/WHF Task Force[J]. Circulation, 2012, 126:2020-2035.
[8] YANCY CW, JESSUP M, BOZKURT B, et al. 2013 ACCF/AHA guidelines for the management of heart failure: a report of the American College of Cardiology Foundation/American Heart Association Task Force on practice guideline[J]. J Am Coll Cardilo, 2013, 62(16):e147-e239.
[9] WU AH, PARSONS L, EVERY NR, et al. Hospital outcomes in patients presenting with congestive heart failure complicating acute myocardial infarction: A report from the second national registry of myocardial infarction (NRMI-2)[J]. J Am Coll Cardiol, 2002, 40(8):1389-1394.
[10] KAUL P, EZEKOWITZ JA, ARMSTRONG PW, et al. Incidence of heart failure and mortality after acute coronary syndromes[J]. Am Heart J, 2013, 165(3):379-385.
[11] GOLDBERG RJ, SPENCER FA, GORE JM, et al. Thirty-year trends (1975 to 2005) in the magnitude of, management of, and Hospital death rates associated with cardiogenic shock in patients with acute myocardial infarction: A population-based perspective[J]. Circulation, 2009, 119(9):1211-1219.
[12] ALESSANDRA SB, LUCIA MB, LIGIA MC, et al. Time of arrival of patients with acute myocardial infarction to the emergency department[J]. Rev Bras Cir Cardiovasc, 2012, 27(3):411-418.
[13] NADIA AK, MAJA G, BRENDA H, et al. Outcome after acute myocardial infarction in South Asian, Chinese, and White patients[J]. Circulation, 2010, 122(16):1570-1577.
[14] DEGEARE VS, BOURA JA, GRINES LL, et al. Predictive value of the Killip classification in patients undergoing primary percutaneous coronary intervention for acute myocardial infarction[J]. Am J Cardiol, 2001, 87(9):1035-1038.
[15] FRESCO C, CARINCI F, MAGGIONI AP, et al. Very early assessment of risk for in-hospital death among 11,483 patients with acute myocardial infarction[J]. Am Heart J, 1999, 138(6):1058-1064.
[16] MCDERMOTT MM, FEINGLASS J, LEE P, et al. Heart failure between 1986 and 1994: temporal trends in drug-prescribing practices, hospital readmission, and survival at an academic medical center[J]. Am Heart J, 1997, 134(5):901-909.
[17] MCMURRAY JJ, ADAMOPOULOS S, ANKER SD, et al. ESC guidelines for the diagnosis and treatment of acute and chronic heart failure 2012: The Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2012 of the European Society of Cardiology. Developed in collaboration with the Heart Failure Association (HFA) of the ESC[J].Eur Heart J, 2012, 33(14):1787-1847.
[18] O’GARA PT, KUSHNER FG, ASCHEIM DD, et al. 2013 ACCF/AHA guideline for the management of ST-elevation myocardial infarction: A report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines[J]. Circulation, 2013, 127(4): e362-e425.
[19] SWEDBERG K, CLELAND J, DARGIE H, et al. Guidelines for the diagnosis and treatment of chronic heart failure: executive summary (update 2005): The Task Force for the Diagnosis and Treatment of Chronic Heart Failure of the European Society of Cardiology[J]. Eur Heart J, 2005, 26(11): 1115-1140.
[20] VAN DE WERF F, ARDISSINO D, BETRIU A, et al. Management of acute myocardial infarction in patients presenting with ST-segment elevation[J]. Eur Heart J, 2003, 24(1):28-66.
[21] HUYNH T, PERRON S, O’LOUGHLIN J, et al. Comparison of primary percutaneous coronary intervention and fibrinolytic therapy in ST-segment-elevation myocardial infarction: Bayesian hierarchical meta-analyses of randomized controlled trials and observational studies[J]. Circulation, 2009, 119(24):3101-3109.
[22] BABAEV A, FREDERICK PD, PASTA DJ, et al. Trends in management and outcomes of patients with acute myocardial infarction complicated by cardiogenic shock[J]. JAMA, 2005, 294(4):448-454.
[23] HARJOLA VP, FOLLATH F, NIEMINEN MS, et al. Characteristics, outcomes, and predictors of mortality at 3 months and 1 year in patients hospitalized for acute heart failure[J]. Eur J Heart Fail, 2010, 12(3):239-248.
[24] ELLIS SG, TENDERA M, DE BELDER MA, et al. Facilitated PCI in patients with ST-elevation myocardial infarction[J]. N Engl J Med, 2008, 358(21):2205-2217.
[25] BATES ER, TOPOL EJ. Limitations of thrombolytic therapy for acute myocardial infarction complicated by congestive heart failure and cardiogenic shock[J]. J Am Coll Cardiol, 1991, 18(4):1077-1084.
(编辑 韩维栋)
In-hospital mortality and cardiovascular outcomes in myocardial infarction patients with or without first-time heart failure
DENG Fu-xue1, WANG Xiao-juan2, HU Yun-feng1, CHANG Jing1
(1. Department of Cardiology, the First Affiliated Hospital of Chongqing Medical University, Chongqing 400016; 2. Department of Public Health, Medical School of Xi’an Jiaotong University, Xi’an 710061, China)
Objective To examine factors that affect incidence, in-hospital treatment, major cardiovascular events (MACEs) and short-term mortality in patients hospitalized for acute myocardial infarction (AMI) newly complicated with heart failure (HF). Methods The baseline characteristics, treatment patterns, major cardiovascular events, and in-hospital mortality were examined in 591 AMI patients complicated with first-time HF who were admitted in our hospital between February 2009 and December 2012. Results Among these 591 AMI patients, 222 were complicated with HF and 369 patients were without HF. It was found that patients with HF were less likely to be examined by cardiac angiogram [(56.3∶73.4)%] or treated with reperfusion therapy [(43.2∶62.9)%] and medications recommended by ACCF/AHA for HF. And they had a greater risk for in-hospital mortality [(15.3∶2.4)%] than non-HF patients. In addition, HF (OR=2.97) and cardiogenic shock (OR=7.53) complicating AMI were strongest predictors of in-hospital death. Conclusion Patients with new and first-time HF complicated with AMI are at a higher risk for adverse in-hospital outcomes. Accurate and rapid diagnosis and timely and comprehensive treatment such as reperfusion and recommended medication can significantly lower the short-term mortality rate.
acute myocardial infarction; heart failure; in-hospital mortality; major cardiovascular event
2014-06-12
2014-08-07
国家临床重点专科建设项目经费资助(财社[2011]170号) Supported by the National Key Clinical Specialties Construction Program of China (No.2011k170)
常静. E-mail: chang8753@aliyun.com
R541.4
A
10.7652/jdyxb201501026
优先出版:http://www.cnki.net/kcms/detail/61.1399.R.20141119.0858.006.html(2014-11-19)
