硫酸亚铁还原硫酸浸取软锰矿动力学研究*
2015-02-17崔益顺向云刚
崔益顺,向云刚
(1.四川理工学院材料与化学工程学院,四川自贡643000;2.企业信息化与物联网测控技术四川省高校重点实验室)
硫酸亚铁还原硫酸浸取软锰矿动力学研究*
崔益顺1,2,向云刚1
(1.四川理工学院材料与化学工程学院,四川自贡643000;2.企业信息化与物联网测控技术四川省高校重点实验室)
以硫酸亚铁作为还原剂,研究硫酸浸取软锰矿过程的动力学。考察了搅拌速率、浸出温度、硫酸初始浓度、硫酸亚铁初始浓度、矿粉初始粒度对锰浸出率的影响。结果表明:锰浸出速率随搅拌速率的增大、浸出温度的升高、硫酸浓度的增大、硫酸亚铁浓度的增大、矿粉初始粒径的减小而增大,其中矿粉粒度对锰浸出率的影响最大,硫酸浓度次之,硫酸亚铁浓度影响较小。硫酸亚铁作为还原剂,在硫酸环境下浸出软锰矿的过程受内扩散控制,浸出过程的宏观动力学方程为:1-2/3x-(1-x)2/3=1.95(1/d02)exp[-29 680/(RT)]t,其表观活化能为29.68 kJ/mol。
软锰矿;硫酸亚铁;硫酸;浸取动力学;锰浸出率
中国已经探明的锰矿总储量约为7.46亿t,贫矿多,富矿少,平均品位为22%,远远低于国际商品级富矿含锰量48%(质量分数)的标准,且杂质含量高[1]。贫锰矿占的比重较大,约占全国总储量的93%,而富锰矿仅占7%。中国大部分的锰矿为Mn质量分数为25%~28%的贫锰矿,还未得到有效的开发利用,如何开发贫软锰矿资源并实现其综合利用是亟待解决的问题。目前,中国的贫软锰矿主要用于制备硫酸锰。软锰矿制备硫酸锰的工艺研究很多,总体分为以下几种[2-3]:煤焙烧酸浸法、两矿焙烧酸浸法、硫酸亚铁法、二氧化硫浸出法、有机物还原法等。煤焙烧酸浸法,能耗高,设备投资较大,焙烧过程产生的烟气对环境污染严重,且随着煤的价格逐渐上涨成本越来越高;而两矿高温焙烧酸浸法同样存在能耗高,浸出产物复杂,除杂难度大等问题;硫酸亚铁法比较适合用于处理钛白粉厂的副产硫酸亚铁和废酸,变废为宝,有利于环境保护;有机物还原法虽然浸出杂质较少,但是成本较高。所以研究开发一种低能耗、低成本的硫酸锰的生产工艺具有重要意义。动力学研究是讨论各因素与锰浸出率随着时间变化的关系,其目的是找出反应过程的关键控制步骤,以提高传质和反应速率。S.Gamini[4]研究认为二氧化硫浸出软锰矿过程符合混合控制;任志凌等[5]研究了软锰矿浆烟气脱硫动力学,认为锰的浸出过程符合内扩散控制;梅光贵等[6]研究表明两矿法浸出过程受颗粒表面化学反应控制;Jiang Tao等[7]研究认为双氧水还原浸出软锰矿过程受内扩散控制;F.W.Y.Momade等[8]研究了在硫酸的环境下用甲醇浸出二氧化锰的动力学,反应前期受外扩散控制,反应后期则受产物层扩散控制。F.Beolchini等[9]和F.Veglio等[10]用可变活化能模型,分别研究了用蔗糖和乳糖为还原剂,硫酸浸出软锰矿,浸出过
程符合颗粒表面的化学反应控制。笔者以硫酸亚铁作为还原剂,研究硫酸浸出软锰矿过程的动力学。考察搅拌速率、浸出温度、硫酸的初始浓度、硫酸亚铁的初始浓度、矿粉的初始粒度对锰浸出率的影响,得出宏观动力学模型。
1 实验部分
1.1 实验原料
硫酸亚铁、硫酸均为分析纯;软锰矿来自于广西某地,其组成见表1。

表1 软锰矿组分 %
1.2 实验主要仪器
DK-S22型电热恒温水浴锅;AR1140电子分析天平;SHB-3循环水式真空泵;101-1AB型电热恒温鼓风干燥箱;JHS-1190电子恒速搅拌机;ND6-4L球磨机;S4 Explorer X荧光光谱仪。
1.3 分析方法
四价锰的测定采用碘量法;Mn2+检测采用硫酸亚铁铵滴定法;硫酸锰含量的测定采用高氯酸法。
2 结果与讨论
2.1 搅拌速率的影响
实验固定条件:软锰矿4 g,反应温度为60℃,硫酸亚铁浓度为0.7 mol/L,硫酸浓度为1 mol/L,液固质量比(以下简称液固比)为150∶1,矿粉平均粒径为164 μm。测定不同搅拌速率下不同时间锰的浸出率,结果见图1。由图1可以看出,当搅拌速率低于400 r/min时,锰的浸出率随搅拌速率增大而迅速增大;当搅拌速率高于400 r/min后,锰的浸出率增长缓慢,在500 r/min时锰的浸出率达到最大值,继续增大搅拌速率锰的浸出率几乎不再增大。
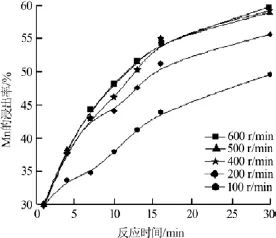
图1 锰浸出率与搅拌强度的关系
2.2 温度的影响
实验固定条件:软锰矿4 g,硫酸亚铁浓度为0.7 mol/L,硫酸浓度为0.8 mol/L,液固比为150∶1,矿粉平均粒径为104 μm,搅拌速率为500 r/min。分别测定不同温度下锰的浸出率,结果如图2所示。

图2 锰浸出率与温度的关系
对图2中实验数据进行处理,分别作t~1-(1-x)1/3和t~1-2x/3-(1-x)2/3图,其中t为反应时间,x为锰浸出率。结果表明t~1-2x/3-(1-x)2/3的线性相关性好,且基本过原点,如图3所示。故硫酸亚铁和硫酸浸出软锰矿的过程受内扩散控制。

图3 不同温度下t~1-2x/3-(1-x)2/3的关系
由阿伦尼乌斯方程ln K=-E/(RT)+B,其中K为图3中各温度下直线的斜率,T为反应温度,由ln K与1/T作图,求得直线斜率为3.57,从而得出活化能E=29.68 kJ/mol。
2.3 硫酸浓度的影响
实验固定条件:软锰矿4 g,硫酸亚铁浓度为0.7 mol/L,反应温度为70℃,液固比为150∶1,矿粉平均粒径为106 μm,搅拌速率为500 r/min。分别测定不同硫酸浓度下锰的浸出率,结果如图4所示。
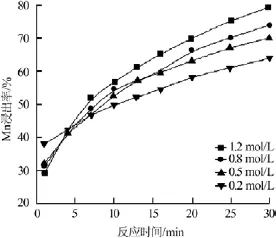
图4 不同硫酸浓度下锰的浸出率
通过数据处理,作不同硫酸浓度下的t~1-2x/3-(1-x)2/3图,结果见图5。由图5可知,t~1-2x/3-(1-x)2/3线性相关性好,每条直线的斜率为其相应硫酸浓度下的反应速率k1。k1=k01c1,式中c1为硫酸浓度,n1为反应级数,k01为待定常数。
两边取对数得:ln k1=ln k01+n1ln c1
对不同硫酸浓度下的反应速率常数作ln k1~ln c1图,可求得直线的斜率(反应级数)n1=0.103。
n1
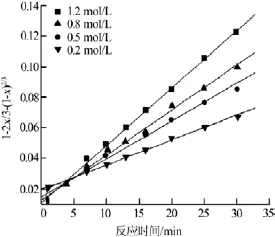
图5 不同硫酸浓度下t~1-2x/3-(1-x)2/3的关系
2.4 硫酸亚铁浓度的影响
实验固定条件:软锰矿 4 g,硫酸浓度为0.8mol/L,反应温度为70℃,液固比为150∶1,矿粉平均粒径为106 μm,搅拌速率为500 r/min。分别测定不同硫酸亚铁浓度下锰的浸出率,结果如图6所示。
通过数据处理,作不同硫酸亚铁浓度下的t~1-2x/3-(1-x)2/3图,结果见图7,图7中每条直线的斜率为相应硫酸亚铁浓度下的反应速率k2。k2=k02c2,式中c2为硫酸亚铁浓度,n2为反应级数,k02为待定常数。
两边取对数得:ln k2=ln k02+n2ln c2
对不同硫酸亚铁浓度下的反应速率常数作ln k2~ln c2图,求得直线的斜率(反应级数)n2=0.19。
n2
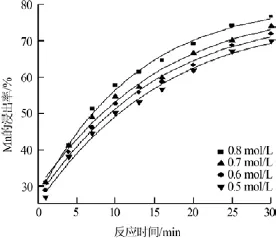
图6 不同硫酸亚铁浓度下锰的浸出率

图7 不同硫酸亚铁浓度下t~1-2x/3-(1-x)2/3关系
2.5 矿粉粒度的影响
实验固定条件:软锰矿4 g,硫酸亚铁浓度为0.7 mol/L,硫酸浓度为0.8 mol/L,反应温度为70℃,液固比为150∶1,搅拌速率为500 r/min。分别测定不同粒度下锰的浸出率,结果如图8所示。作t~1-2x/ 3-(1-x)2/3图,见图9。将图9中不同粒度下的直线斜率与矿粉初始半径平方的倒数作图,满足很好的线性关系,说明浸出过程受内扩散控制。

图8 不同粒度下锰的浸出率
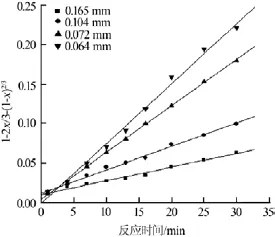
图9 不同粒度下t~1-2x/3-(1-x)2/3的关系
2.6 浸出过程的宏观动力学方程建立
由前面讨论的各因素影响情况可知,本浸出过程的表观反应速率方程可用下式表示:
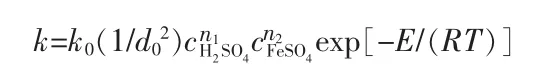
式中:k为表观速率常数;k0为常数;d0为软锰矿的初始半径;c为反应物浓度;E为活化能;T为反应温度;n1,n2为反应级数。
由内扩散控制模型:1-2/3x-(1-x)2/3=kt
将前面得到的n1=0.103,n2=0.19,E=29.68 kJ/mol等数据带入方程,则浸出过程的宏观动力学方程为:
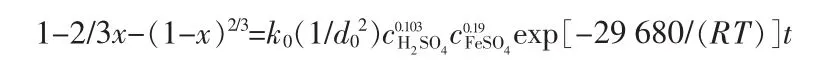
再综合数据,拟合求出k0=1.95,最后得出浸出动力学方程为:
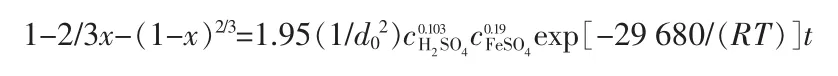
3 结论
1)锰的浸出率随搅拌速率的增大而增大,在搅拌速率为500 r/min时达到最大值,随后搅拌速率增大浸出率不再增大;浸出速率随着粒径的缩小、温度升高、硫酸亚铁浓度增大、硫酸浓度增大而增大,其中矿物粒度对浸出率的影响最大,硫酸浓度次之,硫酸亚铁浓度影响较小。2)通过对锰的浸出率进行数据处理得出:硫酸亚铁作为还原剂,硫酸浸出软锰矿过程受内扩散控制,矿粉粒径是影响其浸出速率的关键因素。同时得出了宏观动力学方程,其表观活化能为29.68 kJ/mol。
[1] 薛友智.中国锰矿地质特征与勘查评价[J].四川地质学报,2012,32(B09):14-19.
[2] 张苑.浅谈软锰矿中制备硫酸锰工艺[J].环境,2011(S1):136-137.
[3] 崔益顺,杨静,赵勇.利用低品位软锰矿制备硫酸锰的工艺进
展[J].四川理工学院学报:自然科学版,2011,24(4):483-485.[4] Gamini S.A mixed surface reaction kinetic model for the reductive
leaching of manganese dioxide with acidic sulfur dioxide[J].Hydrometallurgy,2004,73(3):215-224.
[5] 任志凌,朱晓帆,蒋文举,等.软锰矿浆烟气脱硫动力学研究[J].环境污染治理技术与设备,2006,7(6):89-91.
[6] 梅光贵,钟竹前,周元敏,等.硫铁矿(FeS2)与MnO2浸出的热力学与动力学分析[J].中国锰业,2004,22(1):15-17.
[7] Jiang Tao,Yang Yongbin,Huang Zhucheng,et al.Leaching kinetics of pyrolusite from manganese-silver ores in the presence of hydrogen peroxide[J].Hydrometallurgy,2004,72(1/2):129-138.
[8] Momade F W Y,Momade Z G.A study of the kinetics of reductive leaching of manganese oxide ore in aqueous methanol-sulphuric acid medium[J].Hydrometallurgy,1999,54(1):25-39.
[9] Beolchini F,Papini P M,Toro L,et al.Acid leaching of manganiferous ores by sucrose:kinetic modeling and related statistical analysis[J].Minerals Engineering,2001,14(2):175-184.
[10] Veglio F,Trifoni M,Pagnanelli F,et al.Shrinking core model with variable activation energy:a kinetic model of manganiferous ore leaching with sulphuric acid and lactose[J].Hydrometallurgy,2001,60(2):167-179.
Study on sulfuric acid leaching kinetics of pyrolusite with ferrous sulfate as reducing agent
Cui Yishun1,2,Xiang Yungang1
(1.College of Material and Chemical Engineering,Sichuan University of Sciences&Engineering,Zigong 643000,China;2.Key Laboratory of Higher Education of Sichuan Province for Enterprise Informationalization and Internet of Things)
The leaching kinetics of pyrolusite by sulfuric acid with ferrous sulfate as reducing agent was studied.The effects of stirring intensify,leaching temperature,initial concentration of sulfuric acid,initial concentration of ferrous sulfate,and initial particle size of mineral powder on the leaching rate of manganese were investigated.The results showed that the leaching rate of manganese was increased with the increase of the stirring speed,leaching temperature,sulfuric acid concentration,ferrous sulfate concentration and the decrease of diameter of pyrolusite.The influence order was particle size of mineral powder,concentration of sulfuric acid,and concentration of ferrous sulfate.The pyrolusite leaching process was controlled by the diffusion through the solid film.The macroscopic kinetic equation of the leaching process was:1-2/3x-(1-x)2/3= 1.95(1/d02)exp[-29 680/(RT)]t,and the apparent activation energy was 29.68 kJ/mol.
pyrolusite;ferrous sulfate;sulfuric acid;leaching kinetics;manganese leaching rate
TQ125.14
A
1006-4990(2015)01-0026-04
2014-07-14
崔益顺(1969— ),女,硕士,教授,主要从事矿物加工与无机精细化工研究。
四川省教育厅重点项目(13ZA0127);企业信息化与物联网测控技术四川省高校重点实验室开放基金项目(2013WZJ01)。
联系方式:yishuncui@126.com
