玻璃配合料中铬渣最大允许用量研究*
2015-02-17方久华左明扬齐砚勇
方久华,杨 峰,左明扬,齐砚勇
(1.绵阳职业技术学院,四川绵阳621000;2.西南科技大学)
玻璃配合料中铬渣最大允许用量研究*
方久华1,杨 峰1,左明扬1,齐砚勇2
(1.绵阳职业技术学院,四川绵阳621000;2.西南科技大学)
研究配合料中铬渣最大允许用量,以提高铬渣在玻璃化过程中的处置效率。利用CaO-Al2O3-SiO2相图分析玻璃形成规律及铬渣掺入比例,采用X射线衍射分析仪判断玻璃化程度。研究表明,以铝矾土为成分调节原料时,理论上配合料中铬渣掺入比例可达到89.11%(质量分数);考虑到熔制条件对熔窑寿命的影响,掺入比例为57%(质量分数)左右为宜;如果加入助熔性组分、极化率高的阳离子等,掺入比例可达到65.6%(质量分数)。
玻璃;配合料;铬渣
因铬渣中Al2O3、Fe2O3等的存在,铬渣被用作着色剂加入玻璃早有尝试并得到实际应用。肖汉宁等[1]对以铬渣为主要原料制造微晶玻璃问题进行了有效探索,指出铬渣用量超过40%(质量分数)时玻璃容易析晶。大剂量掺入铬渣可用于制成玻璃马赛克、泡沫玻璃等玻璃产品;如果作为着色剂制作绿色、蓝绿色玻璃,可有效防止铬渣中残留铬铁矿导致玻璃中出现黑点、着色不均匀等缺陷。笔者探索铬渣制作均匀玻璃过程中允许使用的铬渣最高加入比例,以期以尽可能低的原料成本和尽可能高的铬渣加入比例,提高铬渣处置效率。
1 材料与方法
1.1 理论分析
铬渣所含有的 SiO2、Na2O、CaO、MgO、Fe2O3、Al2O3及 Cr2O3都是制造硅酸盐玻璃的有用成分。SiO2是玻璃形成体氧化物,以最基本结构单元[SiO4]构成玻璃网络骨架,Na2O、CaO、MgO等为网络外体氧化物,Fe2O3、Al2O3及Cr2O3是网络中间体氧化物,Na+、Ca2+、Mg2+存在于网络空隙中,Fe3+、Al3+及Cr3+等阳离子配位数为4时,可以进入[SiO4]构成的网络骨架中,否则存在于网络空隙之中。但在逆性玻璃中,骨架则由阳离子与氧的电子云构成,[SiO4]则分散于电子云中[2]。
要利用铬渣制成均匀的玻璃(不分相、不析晶),玻璃组成点应位于图1所示相图各液相线、共熔点处。由于几种晶体结构不同,结晶过程中相互干扰,降低了每种晶相的析晶能力而使晶体不容易产生。
根据各氧化物在玻璃形成过程中的作用分类,将不同的网络形成体氧化物、网络外体氧化物和网络中间体氧化物分别按其摩尔数加合,再分别计入SiO2、CaO、Al2O3的含量。
如果以铬渣为主要原料,以石英砂、粘土等为调整剂,经计算可知组成点的玻璃配合料各原料掺入比例。

图1 CaO-Al2O3-SiO2相图
1.2 实验研究
1.2.1 玻璃化学成分设计
根据图1,实验采用下列玻璃成分:w(SiO2)= 20%~60%;w(CaO)=13%~25%;w(MgO)=6%~12%;w(Fe2O3)=6%~20%;w(Al2O3)=4%~12%;w(Cr2O3)= 1%~2.8%;w(Na2O)=2%~6%;w(B2O3)=0~6%;w(PbO)=0~9%。
1.2.2 玻璃配合料制备
铬渣化学成分很不稳定,一般波动范围为:w(SiO2)=5%~10%;w(Al2O3)=6%~12%;w(Cr2O3)= 1%~6%;w(Na2O)=0.5%~3.5%;w(CaO)=25%~40%;w(MgO)=12%~18%;w(FeO+Fe2O3)=12%~20%。
采用实验用搅拌机对不同来源、批次的铬渣进行预均化,稳定铬渣化学成分,以稳定配料。
实验采用的各原料成分如表1所示。

表1 实验用主要原料化学成分 %
采用制样机对块状原料进行粉碎,使原料粒度小于0.8 mm。
按设计成分用excel进行配料计算[3],计算结果如表2所示。7#、53#、76#成分点分别为图1中A、B、C点。
采用精度为1/1 000 g电子天平进行称量,用研钵混合,配制成100 g/份配合料。

表2 实验用配方 %
1.2.3 玻璃试样制备
将配合料加入100mL刚玉坩埚中,在1390℃保温2 h进行熔制,制成玻璃液;将玻璃液浇注于模型制成试块,采用TD3500 X射线衍射分析仪对玻璃试块表面进行X射线衍射分析,分析玻璃形成情况。
2 结果与分析
2.1 配合料中铬渣掺入比例
按上文阐述方法,图1中共熔(双升)点的化学组成如表3所示;采用不同原料,保持铬渣掺入比例最高,计算出的配合料中铬渣及其他原料掺入比例也如表3所示。
配合料中铬渣掺入比例因所采用的成分调节原料种类不同而有差异。成分调节剂选择应能使配合料制备时铬渣用量大、原料成本低、来源广,还应使玻璃熔制温度低。从表3可见,若确定的组成点SiO2含量高而CaO含量低,宜以石英砂、粘土为成分调节剂;CaO含量高而Al2O3含量低时宜用粘土、石灰石为调节剂;Al2O3含量高而SiO2含量低时宜用铝矾土为调节剂。
虽然配合料中石英砂掺入量小,在硅酸盐形成阶段可以全部参与反应,但铬渣中含有铬铁矿等难熔矿物,采用铝矾土为调节剂时还引入了难熔矿物Al2O3等,实际采用的熔制温度比熔化温度高80~120℃[2]。
为了使原料成本尽量低,同时铬渣掺入比例高,应采用共熔点“15”的玻璃组成,并以铝矾土为成分调节剂,铬渣掺入比例可达到89.11%(质量分数)。
但是,组成点在“15”的玻璃共熔温度高达1 470℃,需要的熔制温度将达到1 600℃左右,对目前所用耐火材料而言熔窑寿命短,因此组成点宜为共熔点“13”,以铝矾土为成分调节剂,铬渣掺入比例为75.28%(质量分数),此时共熔温度为1 335℃,在熔制温度为1 450℃以内即可熔化。
考虑原料来源广与成本低廉问题,组成点宜选用“4”,在该点可采用粘土、石英砂为成分调节剂,在该点铬渣掺入比例为57.06%(质量分数),但如果配合料中引入更多组分,尤其引入助熔性成分Na2O、F-或极化率高的阳离子,铬渣掺入比例会更高,实验表明可达到66%(质量分数)左右。
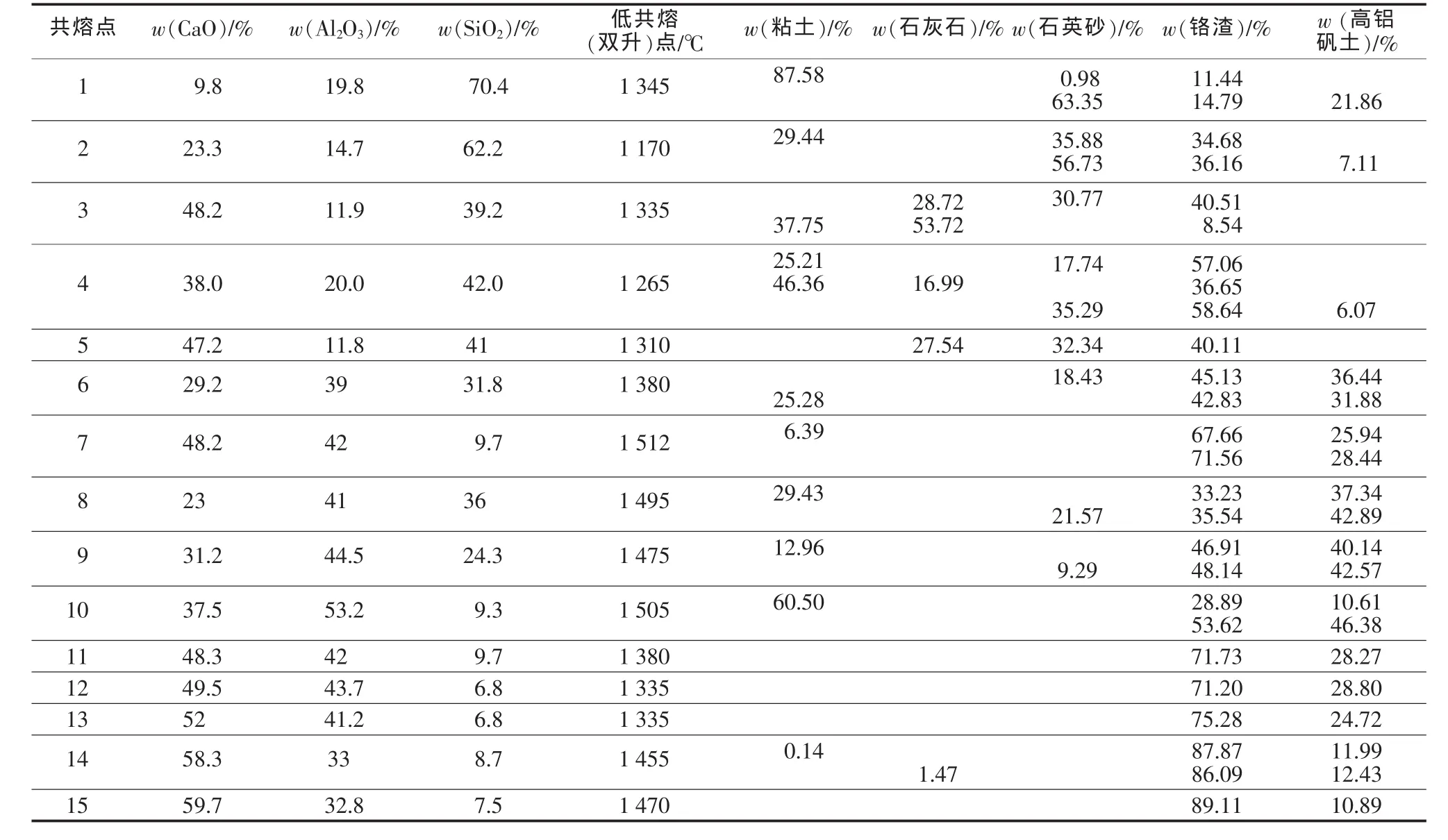
表3 铬渣掺入比例
2.2 配合料熔化
不同用量的铬渣熔制及制得试块情况如表4所示。

表4 不同铬渣用量下配合料熔制情况及制得玻璃试块情况
由于玻璃中SiO2等玻璃形成体氧化物含量低,难以形成链状、网状分子集团,所以熔制的玻璃液黏度小,几种玻璃试样均表现出较好的流动性;高温时B2O3以[BO3]形式存在,不能形成三维网络,玻璃液黏度小;Pb2+极化率高,有利于减小Si—O、Al—O等化学键键强,有利于减小玻璃液黏度,同时对这些高价离子氧化物具有助熔效果[2]。
2.3 玻璃化效果
玻璃试样衍射曲线如图2所示。
铬渣中存在方镁石(MgO)、硅酸钙(2CaO·SiO2)和残余铬铁矿(Fe,Mg)Cr2O4等矿物,硅酸钙及MgO高温下与SiO2反应形成的MgSiO3于1 200℃左右即可熔化成为玻璃液,但铬铁矿熔点高,且在硅酸盐熔体中难以参与反应,即便在远高于共熔(双升)点的1 390℃下也难以熔化而残留于玻璃中,如图2中7#、53#所示。

图2 玻璃试样X射线衍射曲线
图1中,当玻璃中Al2O3含量较低、组成点位于液相线(图1中“2”、“4”连线)附近时,系统趋于产生硅灰石(α-CS)和钙长石(CAS2)两种晶体;当SiO2含
量较低,组成点位于液相线(图1中“4”、“6”连线)及附近时,结构不同的铝方柱石(C2AS)和CAS2两种晶体互相干扰,不容易析晶;同样地,组成点在图1中“6”、“8”、“7”、“1”等共熔点及其连线附近,也不容易析晶。
组成点位于CAS2区域但远离这些共熔点、共熔线时,温度为1 400℃左右,就会出现CAS2晶体,因此7#、53#试样(如图1中A、B两个组成点)出现钙长石晶体,但由于Ca2+、Mg2+具有相似的性能,Mg2+进入晶体之中,而在有足够游离氧时,Al2O3以[AlO4]形式存在,与[SiO4]一样也进入晶体骨架,所以实际出现图2所示的晶体Ca[MgAl][SiAl]2O6。
配合料中MgO、Al2O3、Cr2O3、Fe2O3玻璃熔制时能发生如下反应[4]:

通过上述反应,约在900~1 200℃开始形成尖晶石MgO·Al2O3、MgO·Cr2O3、MgO·Fe2O3,1 400℃反应显著,1 550℃反应基本完成,几种尖晶石能以任意比例混溶。铬渣玻璃的制备,尤其铬渣用量大时,上述反应几乎无可避免,并且一旦产生,难以熔化。实验表明,极化率高的Pb2+等阳离子的存在,对尖晶石的产生具有抑制作用。
76#试样组成点 (图1中C点)位于共熔线附近,图2显示的衍射曲线无明显特征峰,符合玻璃X射线衍射曲线基本特征,表明配合料已经全部熔制成为玻璃。
从实验结果看,铬渣玻璃的形成有下列规律:
1)玻璃能否形成主要取决于组成点在相图中的位置,如果组成点位于相图中的共熔点、线上,即便铬渣加入量大,也能形成玻璃;2)组成玻璃的组分数越多,共熔温度越低,有利于难熔组分的熔化,有利于玻璃的形成;3)铬渣玻璃中网络外体氧化物含量高,玻璃液黏度小,加上Cr2O3能成为晶核而容易析晶,缩短玻璃液在析晶温度范围内停留时间,有利于防止玻璃析晶;4)以B2O3代替部分SiO2,以Na2O、BaO、PbO代替部分CaO,增加了铬渣玻璃组分数,同时破坏了形成晶体的晶格结构,有利于玻璃的形成[5]。
3 结论
1)铬渣中铬铁矿等矿物影响铬渣玻璃的形成;2)玻璃组成点在相图中的位置影响到玻璃的形成,合理的铬渣掺入比例应能使组成点位于CaOAl2O3-SiO2相图的共熔点、线上,否则容易产生晶体;3)如果熔制条件允许,铬渣玻璃配合料中铬渣掺入比例可达到89.11%,在一般熔制条件下以不超过65.6%为宜,B2O3、PbO等有助于配合料的熔化和玻璃的形成;4)确定铬渣掺入比例,需要考虑可提供的熔制温度、耐火材料质量等熔制条件;5)如果原料化学成分变化,文内各原料比例应做相应调整。
[1] 肖汉宁,时海霞,陈钢军.利用铬渣制备微晶玻璃的研究[J].湖南大学学报:自然科学版,2005(4):82-87.
[2] 许超,周世珪.玻璃工艺原理[M].北京:中国建筑工业出版社,2009.
[3] 方久华,左明扬,杨峰.EXCEL平台设计彩釉着色剂配方与可见光谱[J].中国陶瓷工业,2009,16(4):18-20.
[4] 陈树江,田凤仁,李国华,等.相图分析及应用[M].北京:冶金工业出版社,2007:132-139.
[5] 周琦,王枫成,南雪丽,等.碱金属氧化物对镍渣微晶玻璃性能的影响[J].兰州理工大学学报,2010,36(6):17-20.
Research on the biggest allowable level of chrome residue in mixed batch of glass
Fang Jiuhua1,Yang Feng1,Zuo Mingyang1,Qi Yanyong2
(1.Mianyang Vocational and Technical College,Mianyang 621000,China;2.Southwest Science and Technology University)
The biggest allowable level of chrome residue in mixed batch of glass was studied,so as to improve the handling efficiency in the vitrification process of chrome residue.Glass formation regulation and doping ratio of chrome residue were analyzed by making use of CaO-Al2O3-SiO2phase diagram,and X-ray diffraction analyzer was also used to determine the degree of vitrification.Research results showed that the theoretical doping ratio of chrome residue in mixed batch can reach 89.11%(mass fraction),while bauxite as composition-regulating raw material;In consideration of the influence of melting conditions on serving life of glass kiln,about 57%(mass fraction)of the doping ratio was proper;If adding flux and cations with high polarizability in mixed batch,the doping ratio can reach 65.6%(mass fraction).
glass;mixed batch;chrome residue
TQ171.4
A
1006-4990(2015)01-0018-04
2014-07-22
方久华(1965— ),男,副教授,硕士,研究方向为无机材料、环境工程,已发表论文8篇,主编教材、专著2本。
先进建筑材料四川省重点实验室(西南科技大学)开放基金项目(09zxxk12);四川省教育厅重点项目(13ZA0327);绵阳职业技术学院项目。
联系方式:fjh210@163.com
