隐丹参酮单剂量和多剂量给药在大鼠体内药代动力学研究
2015-02-16王猛猛沈淑娇张志荣裘福荣
曾 金,王猛猛,沈淑娇,张志荣,蒋 健*,裘福荣*
(上海中医药大学附属曙光医院临床药理科,上海 201203)
隐丹参酮单剂量和多剂量给药在大鼠体内药代动力学研究
曾 金,王猛猛,沈淑娇,张志荣,蒋 健*,裘福荣*
(上海中医药大学附属曙光医院临床药理科,上海 201203)
目的评价单剂量和多剂量灌胃隐丹参酮(Cryptotanshinone,CTS)的药动学特征。方法将20只SD雄性大鼠随机分为单剂量组(隐丹参酮10 mg/kg,1 d)、多剂量组(隐丹参酮10 mg/kg,每天1次,连续10 d)给予灌胃后,用LC-MS/MS法测定血浆中隐丹参酮的浓度。血药浓度数据用DAS 2.0药代动力学软件处理,按两室模型拟合并求算药代动力学参数。结果隐丹参酮单剂量给药后,Cmax为 (12.16±14.11)ng/mL,Tmax为 (2.88±2.56)h,T1/2为 (3.70±3.50)h,MRT为 (6.69±0.54)h,AUC0~24为 (58.40± 25.73)ng·h/mL;多剂量给药后,Cav为(1.95±0.61)ng/mL,Tmax为(3.20±2.08)h,T1/2为(7.12±5.06)h,AUCss为(46.74±14.51)ng·h/mL,DF为2.42±0.28。单剂量和多剂量的AUC0~24、Tmax、T1/2差异无统计学意义。结论隐丹参酮长期给药后无蓄积风险。
隐丹参酮;单剂量和多剂量;药代动力学;LC-MS/MS
目前临床上许多药物长期使用会产生蓄积或耐药现象,有特殊用途的药物如抗肿瘤药、抗病毒药等出现蓄积现象提高药物在体内的血药浓度,加大临床药物运用的危险性;耐药将会降低患者体内的药物浓度,使药物的治疗作用降低甚至消失。纵观临床上发生耐药现象,究其原因可能是长期服药后造成体内药物代谢酶发生变化,进而影响药物在体内的吸收、代谢、排泄等过程,加速药物排出体外;而蓄积效应的原因则更需要研究,以便更有效的保证临床用药的安全可靠。
隐丹参酮(Cryptotanshinone,CTS)是中药丹参(Salvia miltiorrhiza Bunge)的脂溶性成分之一。丹参味苦,微寒,归心、肝经,具有活血祛瘀、通经止痛、清心除烦、凉血消痈等功效。CTS是二萜醌类化合物,是从丹参中提取出的脂溶性混合物丹参酮成分之一,这类化合物在骨架上大多具有三元或四元碳环的邻醌或对醌结构,其特殊结构使其具有抗肿瘤、抗氧化、抗炎、抗菌等活性。在众多实验及临床研究中发现,CTS单体在抑制细菌生长[1]、改善组织炎症[2-3]、抑制肿瘤增殖[4]、改善脑缺血损伤[5]、治疗多囊卵巢综合征[6]等发面发挥了有效的作用,含有CTS的中成药如丹参酮胶囊、妇炎康片、丹蒌片等在临床中得到广泛的运用。有关CTS的单用以及合并用药等研究已有报道,然而其剂量研究却未见实验报道。本研究通过灌胃SD大鼠CTS,评价单剂量和多剂量给药后CTS在健康SD大鼠的药动学特性,探讨单剂量多剂量给药方式之间是否存在差异,为该药进一步在临床应用提供依据。
1 材料
1.1 仪器
日本岛津LC-20A超高速液相色谱仪 (日本岛津公司):配置二元泵、系统控制器、自动进样器、柱温箱;API 4000-QTRAP型质谱仪(美国ABI/SCIEX公司):配有电喷雾离子化源(ESI)、大气压化学离子化接口、三重四极杆质量分析器以及Analyst 1.5.2数据处理软件;XS-105型十万分之一电子天平 (瑞士 Mettler Toledo公司);AS20500A型超声波清洗器(天津奥特赛恩斯仪器有限公司);Millipore纯水系统 (美国Millipore公司);Thermo超低温冰箱 (美国Thermo公司);WH-3微型旋涡混合仪(上海沪西分析仪器厂有限公司)。
1.2 药品及试剂
CTS,批号 110852-200305,规格 20 mg,纯度98%,购自中国药品生物制品检定所;内标(IS):地西泮 (DZP),批号115-9302,规格20 mg,纯度100%,购自中国药品生物制品检定所。甲醇、乙腈均为色谱纯(美国TEDIA公司);甲酸、吐温-80、乙酸铵、无水乙醇等均为分析纯,购自中国医药集团总公司;水为去离子水;其它试剂均为分析纯。
2 方法
2.1 色谱及质谱条件
液相条件:色谱柱Agilent Eclipse XDB-C18(4.6 mm×150 mm,5μm,美国Agilent Technologies公司);流动相4 mmol/L乙酸铵水溶液-乙腈 (15∶85,v/v),流速1 mL/min;等度洗脱5 min;进样量20μL;柱温30℃;进样器温度4℃。
质谱条件:离子检测方式多重反应监测(MRM);离子极性正离子(Positive);离子化方式电喷雾离子化(ESI);离子对CTS m/z 297.3→251.2;内标m/z 285.2→193.1;传输电压103 V(CTS)、98 V(IS);碰撞能量33 eV(CTS)、43 eV(IS);干燥气温度350℃;干燥气流速10 L/min;雾化室压力50 psi;毛细管电压5 000 V。
2.2 对照品溶液的配置
精密称取CTS对照品5.0 mg,置于10 mL棕色容量瓶内,加乙腈溶解并稀释至刻度,摇匀,即得0.49 mg/mL的CTS储备液,取储备液适量,依次稀释至所需浓度。精密称取内标2.5 mg,加乙腈溶于10 mL棕色容量瓶内,加乙腈溶解并稀释至刻度,摇匀,即得浓度为0.25 mg/mL的内标储备液,取适量储备液用乙酸乙酯配置成0.4 ng/mL的溶液,作为内标溶液备用。
2.3 血浆处理方法
将血浆从-80℃取出,37℃解冻,振荡5 min,用移液枪精密吸取血浆样品100μL加入1.5 mL EP管中,并加入含 0.4 ng/mL内标的乙酸乙酯800μL,涡旋混匀3 min,静置10 min,4℃ 12 000 r/min高速离心10 min,吸700μL上清,于60℃氮气挥干,加100μL乙腈复溶,涡旋混匀,12 000 r/min离心10 min,吸取上清,进行LC-MS/MS分析。
2.4 动物实验方案
2.4.1 实验动物 6~8周龄SPF级SD雄性大鼠20只,体质量(220±20)g,由上海斯莱克实验动物有限责任公司提供,许可证号:SCXK(沪)2014-0002,饲养于上海中医药大学实验动物中心,自由饮水、饮食。
2.4.2 实验用药配制 精密称取CTS标准品适量,吐温-80、超声振荡器超声助溶,用生理盐水溶解并定容至浓度为2 mg/mL的混悬液,置4℃冰箱中保存,备用。
2.4.3 动物分组及给药 将20只SD大鼠随机分为单剂量组、多剂量组两组,每组10只。
单剂量组:前9天每天予生理盐水(含10%吐温-80)灌胃,灌胃剂量为5 mL/kg(剂量换算与灌胃CTS体积相当),第10天以10 mg/kg灌胃含有CTS的生理盐水混悬液,每天每只大鼠给药量不超过2 mL。末次给药前空腹取血后再灌胃,并按如下时间点进行采血取样:0、10、20、30、45 min,1、1.5、2、3、4、8、12、24 h。至大鼠眼底静脉窦取血0.3 mL,肝素钠100μL抗凝,放置片刻后室温下4 000 r/min离心10 min,分离血浆,于-80℃保存待测。
多次给药组:每天按10 mg/kg的剂量连续灌胃含有 CTS的生理盐水混悬液 (含吐温-80)10 d,每天每只大鼠给药量不超过2 mL。末次给药前空腹取血后再灌胃,余下不同时间点采血取样等操作同单剂量组。上述两组动物整个实验过程中不禁水,给药前禁食12 h,给药后2 h给予食物。
3 结果
3.1 分析方法验证
3.1.1 方法专属性 在“2.1”项下的色谱和质谱条件下,分别将空白血浆以及实验大鼠给药后的血浆样品按“2.3”项下方法处理后,进样,记录色谱图。由图1可见,CTS(保留时间3.44 min)和DZP(保留时间2.11 min)峰形良好,血浆中内源性物质对测定干扰不明显。
3.1.2 标准曲线 取1.5 mL的EP管数支,分别精密加入不同量的CTS标准液,加入空白血浆0.1 mL,涡旋混匀,配成含CTS浓度分别为0.1、0.25、0.625、1.5、2.5、7.5、15 ng/mL的标准含药血浆。按“2.3”项下方法处理,进样,记录色谱图。计算以血浆中CTS的浓度C为X轴,CTS峰面积AS和IS的峰面积Ai比值f(AS/Ai)为Y轴,采用加权(1/ x2)最小二乘法分别进行线性回归,CTS的标准曲线回归方程为:f=0.006 03X+0.000 05,r=0.999 6,n= 7,线性范围 0.1~15 ng/mL。最低定量下限为0.1 ng/mL。
3.1.3 精密度和准确度 依“3.1.2”方法精密配制含CTS浓度分别为 0.2 ng/mL(低)、2.5 ng/mL(中)、15 ng/mL(高)的标准含药血浆,每个浓度平行5份,并制备随行标准曲线,按“2.3”项下方法处理,进行检测,并于3 d内重复测定得到日间精密度,将所测定的结果进行t检验(P>0.05),无统计学意义,计算精密度(RSD)和准确度,结果见表1。
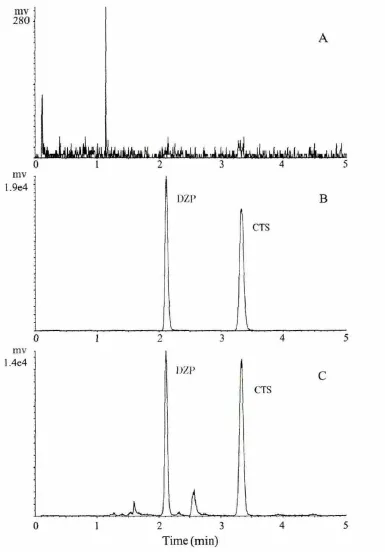
图1 专属性考查的LC-MS/MS色谱图
表1 CTS大鼠血浆浓度测定精密度准确度测定结果 (±s,n=5,%)
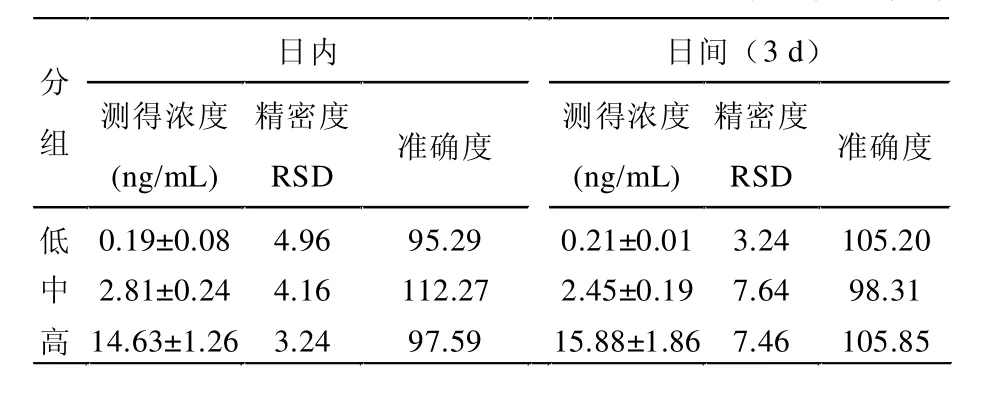
表1 CTS大鼠血浆浓度测定精密度准确度测定结果 (±s,n=5,%)
分组 测得浓度(ng/m L)日内精密度RSD准确度低 0.19–0.08 4.96 95.29 0.21–0.01 3.24 105.20 日间(3 d)测得浓度(ng/m L)精密度RSD准确度中 2.81–0.24 4.16 112.27 2.45–0.19 7.64 98.31高 14.63–1.26 3.24 97.59 15.88–1.86 7.46 105.85 ?
3.1.4 介质效应和提取回收率 以CTS的0.2 ng/mL(低)、2.5 ng/mL(中)、15 ng/mL(高)3种浓度考察CTS的介质效应,结果见表2,其结果表明CTS和IS无明显的介质效应。取含CTS浓度为0.2 ng/mL(低)、2.5 ng/mL(中)、15 ng/mL(高)3种浓度的标准含药血浆,按照绝对回收率方法处理后进样。3种血药浓度的绝对回收率结果见表2。
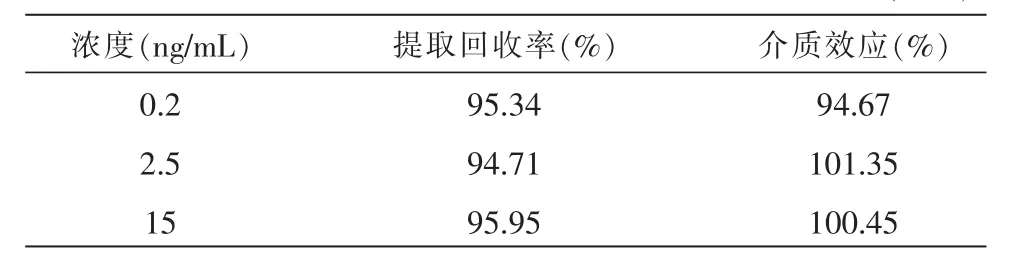
表2 CTS提取回收率和基质效应 (n=5)
3.1.5 稳定性试验 取低(0.2 ng/mL)、中(2.5 ng/mL)、高(15 ng/mL)的CTS标准含药血浆,分别在4、12 h测定以考察CTS的稳定性;反复冻融稳定性:同法配制低中高3种浓度的血浆样品各5份,置于-20℃冰箱冷冻,后拿出融化,反复3次,并按照前法分别加以测定;长期冷冻:将血样放置-80℃保存30 d后按前法配置3种浓度的CTS标准含药血浆后进行检测。
以上稳定性的检测结果无明显改变。
3.2 药代动力学研究
3.2.1 血药浓度-时间曲线 20只SD大鼠随机分组灌胃CTS后,采取血浆经LC-MS/MS分析后,发现CTS呈双峰吸收,与大多数药物在体内的药时曲线模式一致,即经过首过效应后药物的吸收曲线呈双峰现象。单剂量和多剂量组给药后CTS的平均血药浓度-时间曲线见图2。
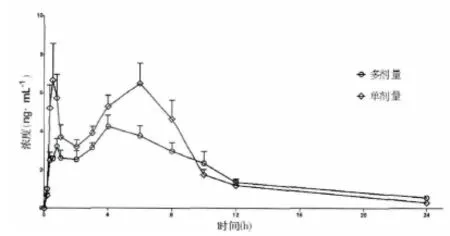
图2 单剂量和多剂量灌胃隐丹参酮的平均血药浓度-时间曲线(±s,n=20)
3.2.2 药代动力学参数 单剂量灌胃CTS后,10只SD大鼠血浆中的CTS的Cmax为(12.16±14.11)ng/mL,AUC0~t为(58.40±25.73)ng·h/mL,Tmax为(2.88±2.56)h,主要药动参数结果见下表3。10只大鼠多剂量灌胃CTS后,平均稳态血药浓度为Cav为 (1.95±0.61)ng/mL,稳态血药浓度-时间曲线下面积 AUCss为 (46.74± 14.51)ng·h/mL,波动度DF为2.42±0.28,多剂量灌胃CTS后的主要药动学参数结果见表3。
利用统计学软件SPSS 18.0对单次和多次给药条件下血浆中CTS的各药动学参数进行统计分析,AUC0~24和Cmax等经剂量矫正和自然对数转换后用独立样本t检验分析,用“独立样本 t检验”对t1/2、“独立样本非参数检验”对Tmax进行检验,分析结果见表4。分析数据表明,单次给药和多次给药各药动学参数血药浓度-时间曲线下面积(AUC0~24)、半衰期(t1/2)、达峰时间(Tmax)等差异无显著统计学意义(P>0.05),CTS在大鼠体内没有发生蓄积现象。
表3 CTS单剂量、多剂量的主要药动学参数(±s,n=20)
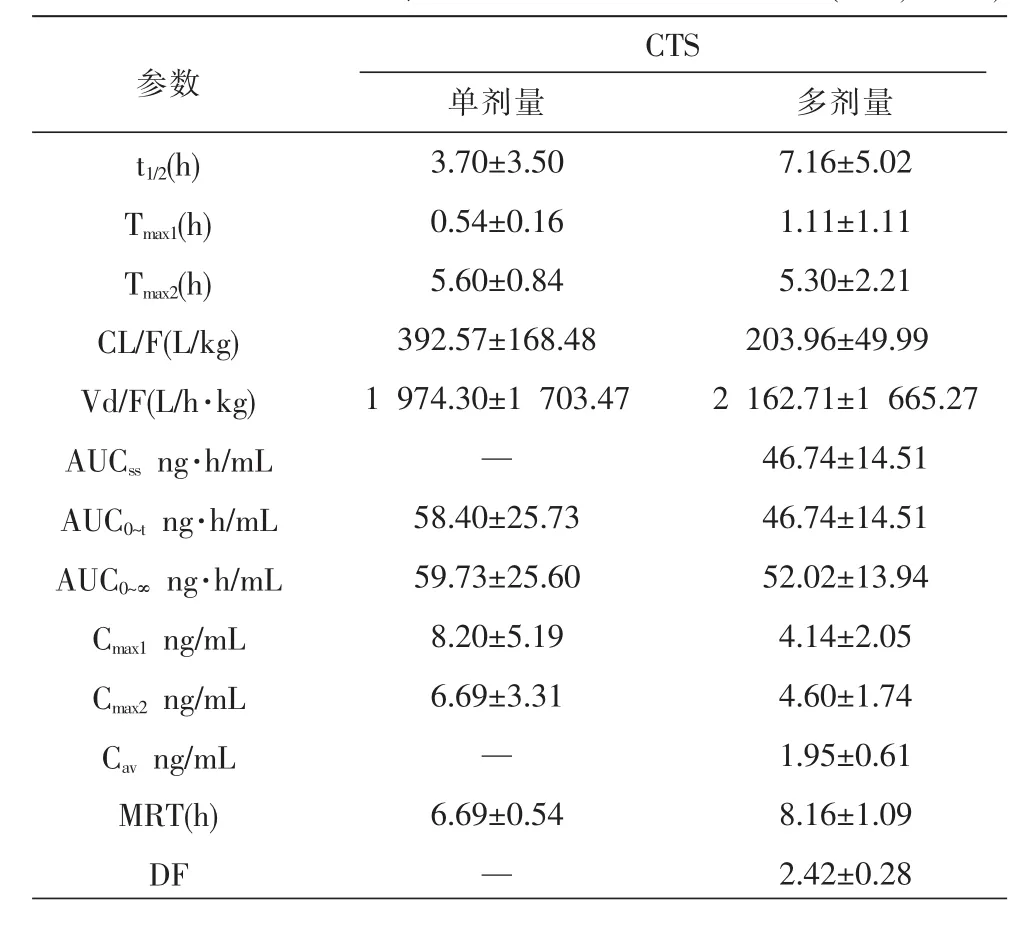
表3 CTS单剂量、多剂量的主要药动学参数(±s,n=20)
CTS参数t1/2(h) Tmax1(h) Tmax2(h) CL/F(L/kg) Vd/F(L/h·kg) AUCssng·h/mL AUC0~tng·h/mL AUC0~∞ng·h/mL Cmax1ng/mL Cmax2ng/mL Cavng/mL MRT(h) DF单剂量3.70±3.50 0.54±0.16 5.60±0.84 392.57±168.48 1 974.30±1 703.47—58.40±25.73 59.73±25.60 8.20±5.19 6.69±3.31—6.69±0.54—多剂量7.16±5.02 1.11±1.11 5.30±2.21 203.96±49.99 2 162.71±1 665.27 46.74±14.51 46.74±14.51 52.02±13.94 4.14±2.05 4.60±1.74 1.95±0.61 8.16±1.09 2.42±0.28
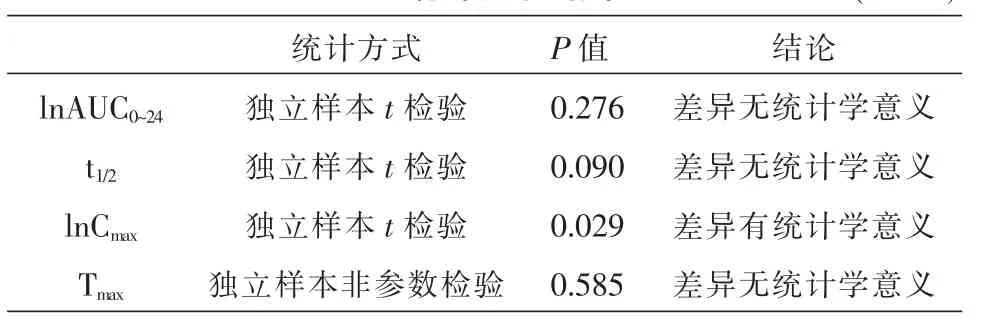
表4 CTS单剂量、多剂量的主要药动学参数统计分析结果 (n=20)
4 讨论
CTS是丹参的脂溶性成分,口服给药的生物利用度很低,长期给药后是否会产生耐药。本研究基于这一问题进行研究,同时LC-MS/MS是实验中检测药物浓度的常用方法,本试验建立了CTS的LCMS/MS测定方法。
关于CTS单次给药[7-9]以及复方给药[10-11]的研究已经很多,都是基于CTS或者丹参酮在大鼠、猪、狗等动物上研究,缺乏CTS多剂量给药后体内药动学的研究,本文将SD大鼠单次、多次灌胃CTS后,采用LC-MS/MS检测CTS血浆中的浓度,考察CTS在单次和多次给药条件下体内药动学行为是否存在差异,为临床运用提供必要的数据支持。研究比较SD大鼠多剂量与单剂量给药CTS,其药动学主要参数经统计分析发现,二者的药代动力学参数基本无差异,其AUC、t1/2统计的P值<0.05。单、多剂量的Tmax统计发现有差异,反应到平均药时曲线上二者显示出差异。从药时曲线图看,单次给药的体内暴露量大于多次给药,实际情况为单剂量组第5只大鼠给药后体内暴露量明显高于其他大鼠,导致单剂量平均药时曲线较多剂量高。第5只大鼠体内超高暴露量提示CTS在大鼠体内的代谢可能存在基因多态性,具体原因有待进一步研究。如果将第5只大鼠的数据剔除后,单多次给药的药时曲线是相似的。灌胃CTS在体内属于二室模型,与之前的研究[11]一致。
对于此次研究药时曲线出现的双峰,原因可能有下面几点:(1)本次实验采取口服灌胃给药,胃按一定时间排空,药物分成两次到达小肠,造成药物两次入血,出现双峰;(2)CTS由于肝肠循环的原因;(3)CTS是脂溶性化合物,其吸收后,迅速分布到组织中,在血液中药物代谢到一定程度后,又出现二次释放入血。如要知晓是何种原因造成药物吸收后出现的双峰现象,需要更进一步的研究。
本文比较SD大鼠单剂量和多剂量给药条件下血浆CTS的浓度,发现单剂量和多剂量的AUC、t1/2等无统计学差异,提示单剂量和多剂量的生物利用度无差异,说明长期给药后CTS在大鼠体内的吸收、分布、代谢和排泄没有显著改变,长期给药后无药物蓄积的风险,同时长期给药后大鼠体内仍然能维持较稳定的血药浓度。有研究[12]发现CTS在人肝脏微粒体内可通过CYP3A4进行代谢,大鼠的代谢酶确证暂时未知。本次研究中单剂量第5只大鼠出现体内超高暴露量则提示在未来研究中需要进行CTS的大鼠代谢酶型进行确证。
本研究对今后临床运用CTS血药浓度、药物蓄积等安全性问题提供必要的数据支持,尽管实验对象为SD大鼠,和人相比有一定的差异,但实验结果提示多次给药后CTS血药浓度的蓄积风险较低。有关CTS在人体内多次给药后的药动学行为仍需进一步研究。
[1]Cha JD,Lee JH,Choi KM,et al.Synergistic Effect between cryptotanshinone and antibiotics against clinic methicillin and vancomycin-resistant staphylococcus aureus[J].Evid Based Complement Alternat Med,2014,3(2):587-594.
[2]Li X,Lian L-H,Bai T,et al.Cryptotanshinone inhibits LPS-induced proinflammatory mediators via TLR4 and TAK1 signaling pathway [J].International immunopharmacology,2011,11(11):1 871-1 876.
[3]Jiang WY,Jeon BH,Kim YC,et al.PF2401-SF,standardized fraction of Salvia miltiorrhiza shows anti-inflammatory activity in macrophages and acute arthritis in vivo[J].Int immunopharmacol,2013,16(2):160-164.
[4]Wu CY,Hsieh CY,Huang KE,et al.Cryptotanshinone downregulates androgen receptor signaling by modulating lysinespecific demethylase 1 function[J].Int J Cancer,2012,131 (6):1 423-1 434.
[5]Mahesh R,Jung HW,Kim GW,et al.Cryptotanshinone from Salviae miltiorrhizae radix inhibits sodium-nitroprusside-induced apoptosis in neuro-2a cells[J].Phytotherapy research:PTR,2012,26(8):1 211-1 219.
[6]Yu J,Wang ZZ,Zhou LH.Study of cryptotanshinone on improving hyperandrogenism of polycystic ovary syndrome via downregulating the expression of gene CYP17 and AR[J].CJTCMP,2014,29(5):1 699-1 705.
[7]谢明智,申竹芳.隐丹参酮的吸收、分布、排泄和代谢[J].药学学报,1983,18(2):90-96.
[8]崔 颖,薛 明,罗永江,等.猪口服隐丹参酮排泄数据分析[J].中国兽医科技,1999,29(12):30-32.
[9]薛 明,崔 颖,张 彬,等.隐丹参酮在猪体内外的代谢转化与抗菌活性[J].中国兽医学报,1999,19(1):49-51.
[10]李晓莉,李晓蓉,王丽娟,等.单用与复方给药后隐丹参酮在家兔体内的药物动力学比较[J].中国药理学通报,2007,23(8):1 102-1 105.
[11]宋 敏,杭太俊,张正行.隐丹参酮及丹参酮提取物在大鼠体内药动学比较研究[J].中国药学杂志,2008,43(1):51-54.
[12]Qiu FR,Zhang R,Wang GJ,et al.Activation of CYP3A-mediated testosterone 6β-hydroxylation by tanshinoneIIA and midazolam 1-hydroxylation by cryptotanshinone in human liver microsomes [J].Xenobiotica,2010,40(12):800-806.
(本文编辑 杨 瑛)
Pharmacokinetics of Cryptotanshinone w ith Single and M ultip le Doses in Rats
ZENG Jin,WANG Mengmeng,SHEN Shujiao,ZHANG Zhirong,JIANG Jian*,QIU Furong*
(Department of Clinical Pharmacology,Shuguang Hospital Affiliated to Shanghai University of Chinese Medicine, Shanghai 2012203,China)
ObjectiveTo evaluate the pharmacokinetic properties of cryptotanshinone(CTS)with single and multiple doses administration in SD rats.MethodsTotally 20 male SD rats were random ly divided into 2 groups:the single-dose group(CTS 10 mg/kg,1 d)and multiple-dose group(CTS 10 mg/kg,once a day,10 consecutive days).The CTS concentration in plasma was detected by LC-MS/MS method.The data of plasma concentration was processed by DAS 2.0 software and the pharmacokinetic parameters were calculated according to a two-compartment open model.ResultsThe pharmacokinetic parameters obtained from the single-dose study were as follows:Cmaxwas(12.16±14.11)ng/mL,Tmaxwas(2.88±2.56)h,T1/2was (3.70±3.50)h,MRT was(6.69±0.54)h and AUC0~24was(58.40±25.73)ng·h/mL;The pharmacokinetic parameters obtained from the multiple-dose study were as follows:Cavwas(1.95±0.61)ng/mL,Tmaxwas(3.20±2.08)h,T1/2was(7.12±5.06)h,AUCsswas (46.74±14.51)ng·h/mL and DF was 2.42±0.28.There was no significant difference in AUC0~24,Tmaxand T1/2of single and multiple doses.ConclusionThere was no risk of accumulation after long-term administration with cryptotanshinone.
cryptotanshinone;single dose and multiple doses;pharmacokinetics;LC-MS/MS
R285.5;R969.1
A
10.3969/j.issn.1674-070X.2015.04.001
2014-12-01
十二五重大新药创新《创新药物研究开发技术平台建设》(2012ZX09303009-001);国家自然科学基金资助项目(81173118);上海市中医临床重点实验室项目(C10dZ2220200)。
曾 金,男,博士研究生,研究方向:中医内科学。
*蒋 健,男,博士,主任医师,博士生导师。*裘福荣,男,博士,主任药师,硕士生导师。
