实时细胞电子分析应用于复方丹参滴丸质量评价的初步研究
2015-01-13雷飞飞王建春张咏梅孙成祥潘金火
雷飞飞, 王建春, 张咏梅, 孙成祥, 潘金火*
(1.南京中医药大学,江苏南京210046;2.张家港市中医医院,江苏苏州215600)
实时细胞电子分析应用于复方丹参滴丸质量评价的初步研究
雷飞飞1, 王建春2, 张咏梅2, 孙成祥1, 潘金火1*
(1.南京中医药大学,江苏南京210046;2.张家港市中医医院,江苏苏州215600)
目的建立复方药物复方丹参滴丸 (CDDP)的生物活性检测方法;将细胞指数值 (CI)与主要活性成分含有量进行相关性分析,为其质量控制提供研究基础。方法采用实时细胞电子分析技术 (RTCA),测定样本对不同细胞株的IC50值,筛选出对复方丹参滴丸有特定依赖性的细胞株,对不同批次复方丹参滴丸建立时间剂量依赖性细胞反应曲线(TCRPs),以细胞指数值 (CI)为考察指标,比较各批次药物的生物活性;测定复方丹参滴丸主要活性成分含有量,并与生物活性进行相关性分析。结果复方丹参滴丸在一定浓度范围内与空白相比对A549细胞株的增殖有明显的抑制作用 (P<0.05),并有明显的量效关系 (r>0.9);由TCRPs反映各批次滴丸质量稳定,但在特定时间点特定的浓度仍有一定差异,今后可用于同种药物不同批次间的稳定性研究;相关性结果表明复方丹参滴丸生物活性与丹参素含有量有显著性相关 (P<0.05)。结论说明本技术能反映复方丹参滴丸生物活性,可与化学成分分析方法结合共同把关中药质量。
复方丹参滴丸;实时细胞电子分析技术;质量评价;相关性
中药质量控制与评价的根本目的和最终目标是要保证其临床使用的安全、有效,而现行中药质量标准只通过鉴别、检查、含量测定等手段控制中药质量,这只是立求保证中药质量在化学层面的均一与稳定,中药质量控制与评价模式基本上是 “惟成分论”,既难以保证中药内在质量的真正稳定、可控,更无法保证其临床使用的切实安全、有效。生物活性 (效价)测定则是一步到位直接考察药物安全性和有效性的质控方法,中药质量生物控制已成为中药质量控制研究发展的趋势[1-4]。
本实验采用了一种新型的生物活性检测方法:实时细胞电子分析技术(RTCA)。RTCA是一种实时、定量检测细胞形态和分化增殖改变的细胞阻抗测试微电子传感器技术,其以细胞电子阻抗为原理,系统的核心是把微电子细胞传感器芯片整合到表面适于细胞贴附与生长的细胞检测板的底部或细胞浸润迁移板的微孔膜上,加入细胞后,黏附在检测板底部的细胞数量决定了细胞指数值的大小,黏附在电极表面的细胞越多,电阻抗越高,细胞指数值越大。通过细胞指数值(CI)间接反映药物对细胞作用 (促进或抑制)的强弱,并可据此评价药物的生物活性。该技术完全有别于传统的细胞检测方法,可以实现无标记、全过程动态跟踪,在药物量效关系指标的测定中具有突出优势。当前已有部分研究者将这种方法应用于中药研究中,Fu等[5]研究表明实时细胞电子分析技术能直观地反应出中药活性成分对细胞产生的影响,该技术可应用于中药分析领域。
目前本课题组主要将此方法应用于活血化瘀类药中的单味药材的质量评价[6]。本研究是运用实时细胞电子分析技术对活血化瘀类复方药物复方丹参滴丸 (CDDP)进行生物检测,并与化学分析结果进行相关性分析,希望为中药质量标准研究提供一种具有良好普适性和实用性,能定量表征中药生物活性的新思路与新方法。
1 仪器和材料
96孔细胞培养板 (美国Costar公司);实时细胞电子分析仪 [艾森生物 (杭州)有限公司];Waters2695高效液相色谱仪 (美国沃特世公司);岛津AUX220分析天平(万分之一)、岛津AUW220D分析天平 (十万分之一)、SCQ-250超声波清洗器 (上海声浦超声波设备厂);胎牛血清、磷酸盐缓冲液 (PBS)、胰酶细胞消化液 (杭州四季青公司);RPMI-1640培养液(美国Gibco公司);二甲亚砜(DMSO)等试剂均为国产分析纯;对照品丹参素钠、丹参素、丹酚酸B、原儿茶醛、三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1均购于中国药品生物制品检定所,纯度均大于98%;肺癌A549等细胞株购于美国模式培养物集存库(ATCC);复方丹参滴丸 (天津天士力制药集团股份有限公司)批次分别为 130121、130420、130315、130301、130105,经鉴定符合 《中国药典》2010年版规定。
2 试验方法
2.1 细胞培养 肺癌A549细胞、HeLa细胞、人乳腺癌MDA-MB-231细胞(雌激素受体阴性,her2阴性)、人乳腺癌MCF-7细胞(雌激素受体阳性,her2阴性)用含10%胎牛血清的RPMI-1640作培养液,置于37℃,含5%CO2的培养箱中培养。
2.2 供试品溶液的制备 取复方丹参滴丸适量,置于研钵内捣碎,取1.35 g,精密称定,置于25 ML量瓶内,加入适量纯净水,超声30 min溶解,再加入纯净水定容至刻度,4℃储存备用。
2.3 特定依赖性细胞株的筛选 RTCA测定样本的TCRPs(时间剂量依赖性细胞反应曲线)。首先在细胞检测板的每个小孔中加入生长介质50μL,再加入密度为2×105个/mL的特定细胞悬液100μL,将此包含一定细胞数量的检测板在室温放置约30min后放入培养箱中培养,并进行连续读数,当细胞数量达到稳定时(约18~24 h),除空白组外,其余给药组将配好的药液加入小孔内,使小孔内的药液终质量浓度分别为 0.015、0.044、0.133、0.4、1.2、3.6、10.8 mg/mL,将加好样的检测板放入实时细胞电子分析仪中,设定好参数,采用实时细胞电子分析技术测出各药液作用于该细胞株后所产生的TCRPs,同时系统计算出IC50,通过IC50数值,筛选出对复方丹参滴丸具有较好依赖性的细胞株。
2.4 复方丹参滴丸主要化学成分定量测定 参照文献[8],采用HPLC法分别同时测定复方丹参滴丸内丹参素、原儿茶醛、丹酚酸B和三七皂苷R1、人参皂苷Rg1、Rb1的含有量。丹参酚酸类3种成分采用C18柱,流动相A为0.02%磷酸-水,B为0.02%磷酸-乙腈梯度洗脱,0 min 8%B,8 min 18%B,15 min 21%B,40 min 34%B,体积流量1 mL/min,检测波长280 nm,柱温30℃。三七皂苷类3种成分采用C18柱,流动相A为0.01%醋酸-乙腈,B为0.01%醋酸-水梯度洗脱,0 min 20%B,40 min 20%B,55 min 35%B,65min 38%B,体积流量1mL/min,检测波长203 nm,柱温30℃。
2.5 不同批号复方丹参滴丸TCRPs的测定 方法同特定依赖性细胞株的筛选。测定不同批号的复方丹参滴丸样品溶液加入细胞培养板小孔内质量浓度分别为0.95、1.18、1.47、1.84、2.3、2.88、3.6 mg/mL的TCRPs。
2.6 统计学处理 采用SPSS 16.0分析生物检测结果与化学成分结果相关性。
3 结果
3.1 特定依赖性细胞株的筛选 采用RTCA测定样本对不同细胞株的TCRPs。同一样本作用于不同细胞株的TCRPs有较大差异,由RTCA测得的IC50见表1。根据结果显示,复方丹参滴丸对这4种细胞的增殖均有明显的抑制作用,但不同细胞对复方丹参滴丸的敏感度存在一定差异,MCF-7及A549细胞的敏感度较MDA-MB-231与HeLa好,但MCF-7较A549过于敏感,经分析比较,选择肺癌A549细胞进行对复方丹参滴丸的研究。样本作用于肺癌 A549细胞株的TCRPs如图1所示。
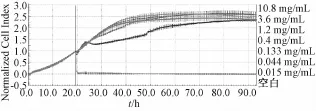
图1 样本作用于A549细胞株的TCRPs
RTCA测定的加药后48 h时的IC50值见表1。

表1 48 h时不同细胞株的IC50
3.2 复方丹参滴丸内主要化学成分定量测定 参考文献,测定了复方丹参滴丸内6种主要成分的含有量,结果见表2。
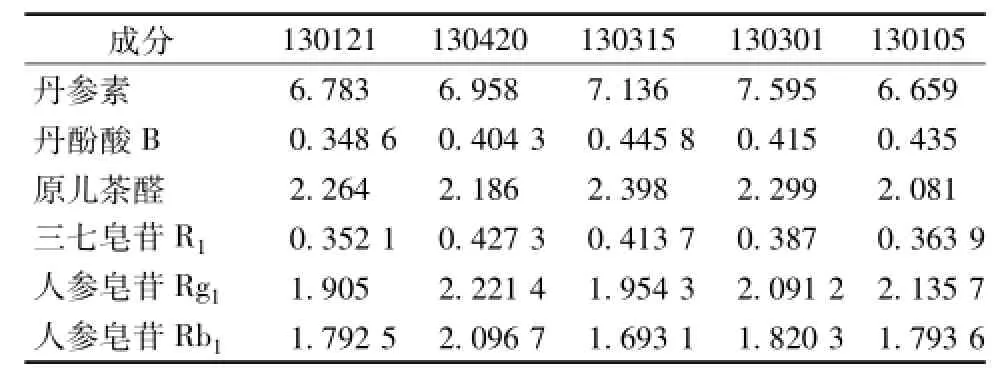
表2 复方丹参滴丸中主要成分测定结果 (Mg·g-1)
3.3 RTCA测得的各样本作用于肺癌A549细胞株的TCRPs
各样本作用于肺癌A549细胞株的TCRPs曲线如图2~7所示,可以由图实时观察出细胞生长动态趋势。从图2~6可以看出TCRPs曲线有高度相似性,表现出各批次复方丹参滴丸质量的稳定性,符合各文献关于研究不同批次复方丹参滴丸稳定性的报道。

图2 样本批号13021作用于肺癌A549细胞株的TCRPs
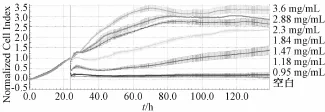
图3 样本批号130420作用于肺癌A549细胞株的TCRPs
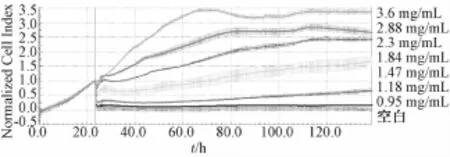
图4 样本批号130315作用于肺癌A549细胞株的TCRPs
经筛选,各批号复方丹参滴丸在特定时间点即60 h时,质量浓度为0.95~2.88 mg/mL时,细胞指数值(CI)与药液浓度的对数值lgC呈现较好的量效关系,r>0.9,且在该时间点,各批次不同质量浓度复方丹参滴丸与空白相比对A549细胞株增殖均有显著的抑制作用 (P<0.05),精密度与稳定性均较好,所以选取60 h为分析的最佳时间点。60 h时的不同样本浓度的指数值lgC与细胞指数值CI结果如表3所示。当样本质量浓度为1.84 mg/mL时,不同批次复方丹参滴丸的CI值均有显著性差异 (P<0.05),可区分出在该质量浓度各批次复方丹参滴丸生物活性有一定差异,从分析结果可得出在1.84mg/mL时各批次生物活性强弱顺序为130301>130315>130420>130121>130105,此法今后可用于复方丹参滴丸质量评价中的稳定性研究中。
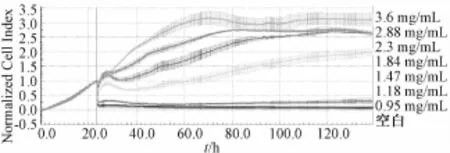
图5 样本批号130301作用于肺癌A549细胞株的TCRPs
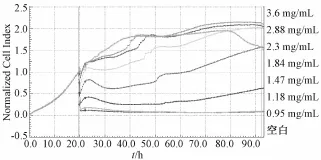
图6 样本批号130105作用于肺癌A549细胞株的TCRPs
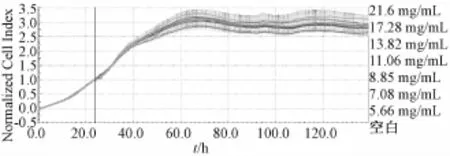
图7 丹参素对照品作用于肺癌A549细胞株的TCRPs
《中国药典》2010年版控制复方丹参滴丸的指标性成分为丹参素,根据本实验所测样品中丹参素的量,配制了与成药含相同质量浓度的丹参素的对照品样本,图7发现,与空白相比,丹参素对A549细胞增殖抑制作用很小,量效关系不明显,说明丹参素的作用不能等同于整个成药的药效,丹参素的量也不能全面代表成药的质量。所以控制单一指标性成分的含有量,并不能保证药物的疗效,也无法控制药物的质量。
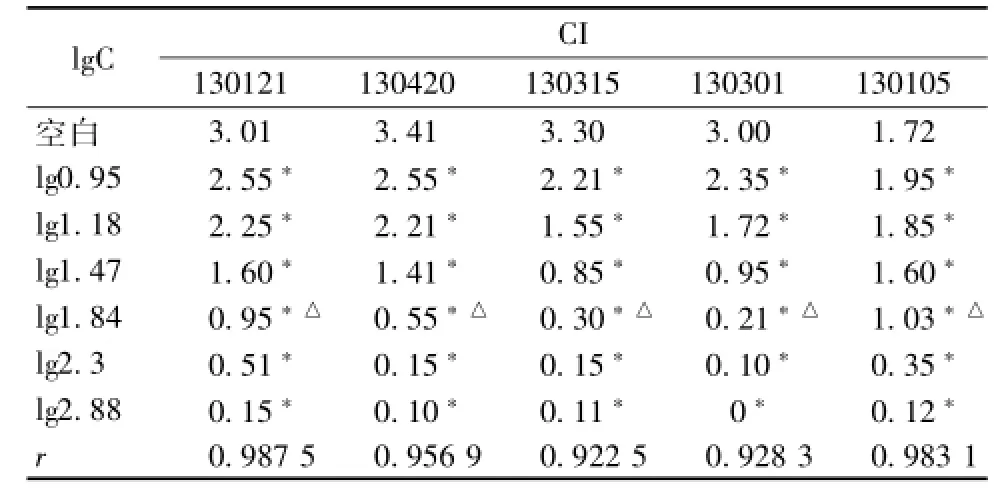
表3 细胞指数值CI与不同样本浓度的指数值lgC关系
3.4 生物活性检测与化学成分分析结果的相关性分析 运用SPSS 16.0将复方丹参滴丸药液质量浓度为1.84 mg/mL时的细胞指数值与各化学成分含有量进行相关性分析,分析结果见表4,结果表明,复方丹参滴丸的生物活性与丹参素的含有量有显著性相关 (P<0.05),与其他成分未见显著性相关 (P>0.05)。细胞指数值与丹参素含有量的Pearson相关系数r=-0.915,P=0.029<0.05,说明丹参素含有量越高,细胞指数值越低,存活的细胞数量越少,其抑制细胞生长的活性越强。一定程度上说明以丹参素含有量作为指标性成分控制整个成药质量有一定依据,但是应结合生物活性测定方法共同把关中药质量。
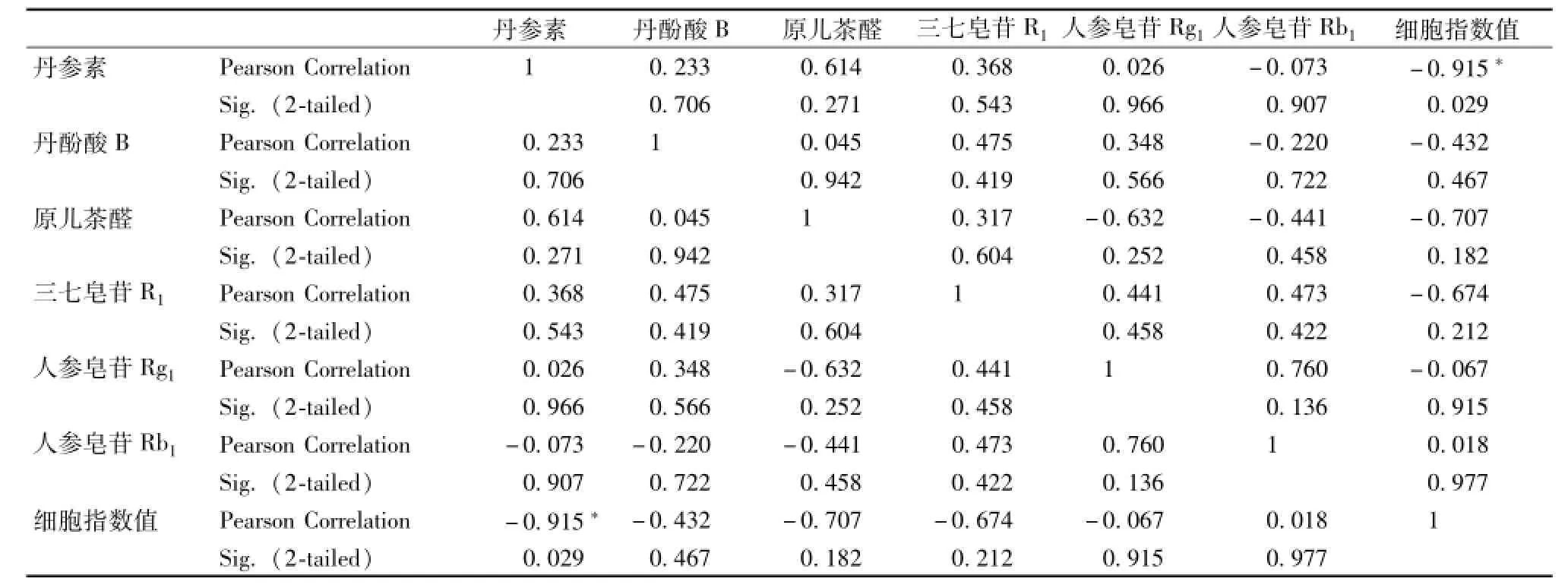
表4 复方丹参滴丸细胞指数值与化学成分相关性分析
4 讨论
实验过程中比较了复方丹参滴丸作用于不同细胞株产生的细胞曲线有很大的差异,而其不同样本作用于某种特定细胞株产生的细胞曲线有高度相似性。说明复方丹参滴丸作用于某种特定依赖的细胞株后可产生独特专属的TCRPs曲线。RTCA普适性好、实时在线、客观灵敏,无需标记,对细胞无创伤,在最接近生理状态下获得检测结果,实验过程中参数少,数据处理快速方便,符合中药药效和质量评价的客观现实和发展方向[8]。
本实验应用实时细胞电子分析技术筛选出对活血化瘀类复方药复方丹参滴丸具有特定依赖性的细胞株,测定不同批次复方丹参滴丸的细胞指数值 (CI),从而评价各批次复方丹参滴丸的质量,并根据不同的细胞指数值 (CI)与该药物的主要化学成分进行相关性分析,得出其与丹参素含有量显著相关,这说明 《中国药典》规定通过测定其中丹参素的含有量控制整体药物质量有一定依据,深入研究化学成分分析和生物活性评价来共同把关中药质量有很大的可行性。
本实验运用的新型技术实时细胞电子分析技术现主要应用于抗肿瘤药物的筛选,对贴壁类肿瘤细胞更具有灵敏度,而将该技术运用于中药复方质量评价方面仍处于初步阶段,经查阅大量文献表明活血化瘀类中药能改善微循环,增加血管通透性,抑制肿瘤血管生成[9-10],本实验所选择的活血化瘀类复方药物复方丹参滴丸属于活血化瘀类药的代表,实验设计时从复方丹参滴丸活血化瘀的整体作用出发,利用其对癌细胞的生长抑制作用,检测出不同的细胞指数值,以期评价药物的生物活性。实验中选取了4种贴壁细胞:肺癌A549细胞、HeLa细胞、人乳腺癌MDA-MB-231细胞 (雌激素受体阴性,her2阴性)、人乳腺癌MCF-7细胞 (雌激素受体阳性,her2阴性)进行试验,从中筛选对复方丹参滴丸有特定依赖性的细胞株。本研究的关键是正确选择对被测中药具有特定依赖和高度灵敏的细胞株,虽然实验前期进行了大量预实验,但细胞筛选方面仍需做很多工作,在今后的实验中仍要加大细胞株的筛选,以期为将此技术应用于中药质量评价方面提供更科学的依据。在后续的研究中,将尝试应用RTCA定量检测中药质量,并结合体内外药效学试验来进一步验证该方法应用于中药质量评价方面的可行性。
[1]肖小河,金 城,赵中振,等.论中药质量控制与评价模式的创新与发展[J].中国中药杂志,2007,32(14):1377-1381.
[2]王 平,钱忠直. 《中国药典》2010年版编制大纲解读[J].药物分析杂志,2008,28(2):337-340.
[3]陈广云,吴启南,王新胜,等.生物效价测定法用于活血化瘀中药三棱品质评价的研究[J].中国中药杂志,2012,37(19):2913-2916.
[4]周丹蕾,鄢 丹,李宝才,等.微量量热法研究天然虫草和人工虫草对大肠杆菌生长代谢的影响[J].药学学报,2009,44(6):640-644.
[5]Fu H,Fu W,Sun M,et al.Kinetic cellular phenotypicprofiling:prediction,identification and analysis of bioactive natural products[J].Anal Chem,2011,83(17):6518-6526.
[6]Yan Guojun,Mei Xin,Yang Jin,et al.A novel real-time cell electronic analysis technology for the authentication and qualitycontrol of natural medicines[J].Chin CheMLett,2013,24(12):1140-1144.
[7]叶正良.复方丹参滴丸质量控制方法学研究[D].杭州:浙江大学,2007:44-50.
[8]肖小河,肖培根,王永炎.基于道地药材和生物效价检测的中药质量控制与评价模式的研究[J].湖南中医药大学学报,2007,27(S1):5-8.
[9]周燕萍,杨 航,关江峰,等.5种不同治法中药对人肺癌A549细胞增殖的影响[J].成都中医药大学学报,2013,36(3):15-30.
[10]王 斌,董 阳,周江云.活血化瘀法在恶性肿瘤治疗中研究 [J].辽宁中医药大学学报,2013,15(12):177-179.
R285.5
:B
:1001-1528(2015)05-1119-05
10.3969/j.issn.1001-1528.2015.05.045
2014-06-05
学校重点培育课题 (10xpy01)
雷飞飞(1988—),女,硕士生,研究方向为中药新剂型新技术。Tel:15105161306,E-mail:leifeifei0831@163.com
*通信作者:潘金火 (1963—),男,教授,研究方向为中药新剂型工艺及中药质量标准。Tel:(025)85811517,E-mail:panjinhuo@ 163.com
